Lemuroidea
| Lémures | ||
|---|---|---|
 Lémur de cola anillada (Lemur catta) | ||
| Estado de conservación | ||
| Apéndice I de la CITES [1][2] | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Chordata | |
| Clase: | Mammalia | |
| Orden: | Primates | |
| Suborden: | Strepsirrhini | |
| Infraorden: |
Lemuriformes * * (ver texto) | |
| Superfamilia: |
Lemuroidea Gray 1821 | |
| Diversidad | ||
| Unas 100 especies (existentes) | ||
| Distribución | ||
 Los lémures son endémicos de Madagascar (en rojo) | ||
| Familias | ||
Los lémures son unos primates estrepsirrinos endémicos de la isla de Madagascar. Reciben su nombre por los lemures, fantasmas o espíritus de la mitología romana, debido a las estrepitosas vocalizaciones que emiten, sus ojos brillantes y los hábitos nocturnos de algunas de sus especies.
Aunque a menudo se los confunda con primates ancestrales, los primates antropoides (monos, hominoides y seres humanos) no evolucionaron de los lémures, sino de los omomíidos, aunque sí comparten algunos rasgos morfológicos y de comportamiento con primates basales.
Su clasificación taxonómica es controvertida y depende de que concepto de especie se utilice. Incluso se discute la taxonomía de nivel más alto, y algunos expertos ubican a la mayor parte de los lémures en el infraorden Lemuriformes, mientras que otros prefieren que Lemuriformes contenga a todos los estrepsirrinos existentes, colocando a todos los lémures en la superfamilia Lemuroidea y a los lorísidos y galágidos en la superfamilia Lorisoidea.
La hipótesis más extendida es que los lémures llegaron a Madagascar hace aproximadamente entre 62 y 65 Ma por rafting (dispersión biológica por balsas de vegetación) en algún momento en que las corrientes oceánicas favorecieron la dispersión hacia la isla. Desde entonces los lémures han evolucionado para enfrentarse a un ambiente sumamente estacional y sus adaptaciones les dan un nivel de diversidad que rivaliza con los demás grupos de primates. Hasta la llegada de los humanos a la isla, hace aproximadamente 2000 años, existían lémures tan grandes como un gorila macho. En la actualidad perviven unas cien especies de lémures, la mayor parte de ellas descubiertas o promovidas al estatus de especie a partir de los años 1990.
Con un peso que va desde los treinta gramos hasta los nueve kilogramos en las especies actuales, los lémures comparten muchos de los rasgos básicos de los primates, como manos y pies con cinco dedos y pulgar oponible, y uñas en lugar de garras (en la mayoría de las especies). Sin embargo, su proporción cerebro-masa corporal es menor que en los primates antropoides, y, al igual que los demás primates estrepsirrinos, tienen la «nariz húmeda» (rinario). Los lémures son generalmente los estrepsirrinos más sociales y se comunican más con olores y vocalizaciones que con señales visuales. Tienen un metabolismo basal relativamente bajo, muchos se reproducen estacionalmente, tienen períodos de dormancia (como hibernación o letargo), y algunos muestran un dominio social de las hembras. La mayoría se alimenta con una amplia variedad de frutas y hojas, mientras que otros son especialistas. Aunque muchas comparten dietas similares, especies distintas comparten los mismos bosques a través de un proceso de diferenciación de nicho.
La investigación sobre estos primates se centró en su taxonomía y en la recogida de especímenes durante los siglos XVIII y XIX. Aunque las observaciones aportadas por los primeros investigadores de campo fueron abundantes, los estudios modernos sobre la ecología y comportamiento de estos animales no se desarrollaron hasta los años 1950 y 1960. Ante las dificultades surgidas por la inestabilidad política y la confusión reinante en Madagascar a mediados de los años 1970, los trabajos de campo se detuvieron, pero se reanudaron en los años 1980 y supusieron un gran avance en el conocimiento de estos primates. Instalaciones de investigación como el Duke Lemur Center de la Universidad Duke han proporcionado la oportunidad de avanzar en su estudio en un ambiente controlado. Los lémures son importantes para la investigación porque su mezcla de características primitivas y rasgos compartidos con los primates antropoides puede arrojar un mayor conocimiento sobre la evolución de los primates y de los humanos. Sin embargo, muchas especies de lémur están en peligro de extinción debido a la pérdida de su hábitat y a la caza. Aunque por lo general las tradiciones locales ayudan a proteger a los lémures y sus bosques, la tala forestal ilegal, la generalización de la pobreza y la inestabilidad política dificultan y menoscaban los esfuerzos por la conservación de estos primates. Debido a estas amenazas y a la disminución constante de sus poblaciones, la Unión Internacional para la Conservación de la Naturaleza (UICN) considera que los lémures son los mamíferos en mayor peligro de extinción, considerando que —hasta 2013— más del 90 % de las especies de lémures están amenazadas.
Etimología[editar]
Linneo, el fundador de la nomenclatura binomial moderna, les dio el nombre de lémures ya en 1758 en la 10.ª edición de su Systema naturae. Linneo situó tres especies bajo el género Lemur: L. tardigradus (el loris esbelto rojo, actualmente Loris tardigradus), L. catta (el lémur de cola anillada) y L. volans (el lémur volador de Filipinas, hoy Cynocephalus volans).[3] Aunque el término «lémur» se aplicara inicialmente a los loris, pronto fue asociado a todos los primates endémicos de Madagascar, que han sido conocidos desde entonces como lémures.[4] El nombre proviene del latín lemŭres,[5][6] espectros o espíritus de la muerte conocidos como larvae o lemures en la Antigua Roma.[7] Linneo conocía los hábitos nocturnos y el aspecto fantasmal de lémures y loris,[8] así como sus movimientos silenciosos por la noche, sus también fantasmales ojos reflectantes y sus gritos. También es posible que los pobladores malgaches le contaran algunas leyendas que hablan de los lémures como las almas de sus antepasados.[9] Estando familiarizado con los trabajos de Virgilio y Ovidio y sus referencias a la Lemuralia o festival de Lemuria y, viendo una analogía que encajaba en su esquema de nomenclatura, Linneo asignó el término lemur a estos primates nocturnos.[10]
Historia evolutiva[editar]
Los lémures son unos primates prosimios que pertenecen al suborden Strepsirrhini. Al igual que otros primates estrepsirrinos, como los loris, potos y gálagos, comparten rasgos basales (plesiomorfia) con los primeros primates, por ello a menudo se les confunde con primates ancestrales, sin embargo, los primates antropoides (monos, hominoides y seres humanos) no evolucionaron de los lémures. El lémur evolucionó de forma independiente en su aislamiento en la isla de Madagascar.[11] Tradicionalmente se consideraba que todos los estrepsirrinos modernos, incluidos los lémures, evolucionaron de unos primates primitivos conocidos como adapiformes durante el Eoceno (hace entre 56 y 34 Ma) o el Paleoceno (entre 65 y 56 Ma),[11][12][13] sin embargo, los adapiformes carecían de una disposición especializada de los dientes, conocida como peine dental, que prácticamente todos los estrepsirrinos vivientes poseen.[14][15][16] Una hipótesis más reciente propone que los lémures descienden de primates lorisiformes (similares a loris). Esta hipótesis está apoyada por estudios comparativos del gen citocromo b y la presencia del peine dental estrepsirrino en ambos grupos.[16][17] En lugar de ser los antepasados directos de los lémures, los adapiformes pueden haber dado lugar tanto a los lémures como a lorisiformes, una escisión que estaría apoyada por estudios de sistemática molecular.[16] De acuerdo con los estudios moleculares se cree que la división posterior entre lémures y loris pudo haber ocurrido hace entre 62 y 65 Ma,[18] aunque otras pruebas genéticas y el registro fósil en África sugieren estimaciones más conservadoras de 50 a 55 Ma para esta divergencia.[19]
Habiendo sido en algún momento parte del supercontinente Gondwana, la isla de Madagascar quedó aislada cuando se separó de África Oriental (~160 Ma), la Antártida (~80-130 Ma) y la India (~80-90 Ma).[20][21] Dado que se cree que los primeros lémures se originaron en África hace aproximadamente entre 62 y 65 Ma, tendrían que haber cruzado el canal de Mozambique, que tiene una anchura mínima de unos 560 km.[16] En 1915, el paleontólogo William Diller Matthew indicó que la biodiversidad mamífera en Madagascar (incluidos los lémures) sólo podía explicarse por acontecimientos de rafting (dispersión biológica a través de balsas de vegetación) esporádicos, donde grupos muy pequeños fueron transportados desde la cercana África en balsas de vegetación enredada que llegaban al mar desde los principales ríos;[22] esta forma de dispersión biológica pudo ocurrir al azar a lo largo de millones de años.[16][23] En los años 1940, el paleontólogo George Gaylord Simpson acuñó el término «sweepstakes hypothesis» (hipótesis de la lotería, del azar) para estos eventos aleatorios.[24] El rafting ha sido desde entonces la explicación más aceptada de la colonización de Madagascar por parte del lémur,[25][26] aunque hasta hace poco se creía que este viaje era muy improbable debido a las fuertes corrientes marinas que discurren cerca de la isla.[27] No obstante, en enero de 2010, un informe demostró que hace aproximadamente 60 Ma tanto Madagascar como África se encontraban 1650 km al sur de sus posiciones actuales, situándolas en un giro oceánico diferente, y con corrientes que fluían al contrario de lo que lo hacen en la actualidad. Además, estas corrientes oceánicas eran más fuertes que hoy en día, lo que habría empujado las balsas de vegetación más rápido y acortando el viaje hasta unos treinta días o incluso menos, tiempo lo suficientemente corto como para que un pequeño mamífero pudiera sobrevivir fácilmente. Cuando las placas continentales derivaron hacia el norte, las corrientes cambiaron de forma gradual, y en 20 Ma la ventana abierta para la dispersión oceánica se había cerrado, aislando con eficacia a los lémures y al resto de la fauna terrestre malgache de la plataforma continental africana.[27] Aislados en Madagascar con un limitado número de competidores mamíferos, los lémures no tuvieron que contender con otros grupos de mamíferos arborícolas evolucionados, como los esciúridos,[28] ni tampoco tuvieron necesidad de competir con los monos, que evolucionaron más tarde, y cuya inteligencia, agresividad y carácter evasivo les daba ventaja sobre otros primates en la explotación del entorno.[6][15] Hallazgos fósiles recientes parecen plantear que estos primates se desplazaron en al menos dos períodos a Madagascar, por lo que pudieron llegar en el Mioceno, momento en el que el espacio físico entre la isla y el continente africano estaba ocupado por grandes placas de hielo.[29]
Distribución y diversidad[editar]

Los lémures se han adaptado para ocupar muchos nichos ecológicos abiertos desde su llegada a Madagascar.[15][28] Su nivel de diversidad tanto en comportamiento como en morfología (aspecto externo) rivaliza con los demás grupos de primates existentes a lo largo de todo el mundo.[6] Su tamaño va desde los 30 g del lémur ratón de Berthe (Microcebus berthae), el primate más pequeño del mundo,[30] a los 160-200 kg del recientemente extinguido Archaeoindris fontoynonti,[31] y han desarrollado diversas formas de locomoción, distintas formas de complejidad social y adaptaciones únicas al clima local.[15][32]
Dado que los lémures carecen de cualquier tipo de rasgo compartido que los distinga de los demás primates, su diversidad ha ayudado a definirlos.[33] Distintos tipos de lémures han desarrollado combinaciones únicas de características atípicas para enfrentarse con el clima riguroso y de fuertes contrastes estacionales de Madagascar, como el almacenaje de grasa estacional, hipometabolismo (como hibernación o letargo), grupos de pequeño tamaño, baja encefalización (tamaño cerebral relativo), comportamiento catemeral (con actividad tanto de día como de noche) y temporadas de cría estrictas.[12][32] Se cree que las limitaciones extremas para obtener recursos y la cría estacional han dado lugar a otros tres comportamientos relativamente comunes en los lémures: el dominio social de las hembras, el monomorfismo sexual y un modelo de competición entre machos para aparearse con bajos niveles de agonismo, como la competencia espermática.[34]
Antes de la llegada de los humanos, hace aproximadamente 1500-2000 años, los lémures podían encontrarse a todo lo largo de la isla.[28] Sin embargo, los primeros pobladores humanos pronto convirtieron los bosques en arrozales y prados por medio de la agricultura de rozas y quema (conocida localmente como tavy), restringiendo a los lémures a la periferia de la isla, aproximadamente el 10 % de la superficie terrestre total de la misma, equivalente a unos 60 000 km².[35] En la actualidad, la diversidad y complejidad de las comunidades de lémur aumenta con la diversidad floral y de precipitaciones, particularmente en las selvas tropicales de la costa oriental, donde esta diversidad floral y precipitaciones son también mayores.[13] A pesar de sus adaptaciones para resistir condiciones extremas, la destrucción de su hábitat y la caza han tenido como consecuencia que las poblaciones de lémures y su diversidad hayan disminuido bruscamente, causando la extinción reciente de al menos diecisiete especies en ocho géneros,[28][31][36] conocidos colectivamente como lémures subfósiles. La mayor parte de las aproximadamente cien especies y subespecies actuales están amenazadas o en peligro de extinción. A menos que se produzca un cambio en la tendencia, probablemente seguirán produciéndose extinciones.[37]
Hasta tiempos recientes existieron lémures de gran tamaño en Madagascar. Ahora representados solo por restos recientes o subfósiles, eran formas modernas que una vez formaron parte de la rica diversidad de estos primates que evolucionaron en su aislamiento insular. Algunas de sus adaptaciones eran distintas a las que se pueden ver en sus parientes vivientes.[28] Diecisiete de las especies extinguidas eran de mayor tamaño que las actuales, algunas con un peso que llegaba hasta los 200 kg,[6] y que se cree que podrían haber sido activas durante el día.[38] No solo eran diferentes de los lémures actuales tanto en tamaño como en aspecto, sino que también ocuparon nichos ecológicos que ya no existen o que ahora están deshabitados.[28] Grandes extensiones de Madagascar que ahora carecen de bosques y de lémures, en un tiempo albergaron comunidades diversas de primates que incluían más de veinte especies de lémur que abarcaban el amplio rango de tamaños de estos animales.[39]
Clasificación taxonómica y filogenia[editar]
| Filogenias en disputa | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Propuesta de Horvath et al.:[40] | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| Propuesta de Orlando et al.:[41] | ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||
| (Nótese que Horvath et al no intentaron ubicar a los lémures subfósiles). |
Desde un punto de vista taxonómico, el género Lemur, que se asoció originalmente al término «lémur», hoy solo contiene al lémur de cola anillada (Lemur catta). En la actualidad, lémur es el nombre común que se utiliza para hacer referencia a todos los primates malgaches.[42]
La taxonomía de los lémures es controvertida, y no todos los expertos están de acuerdo, en buena parte debido al reciente aumento del número de especies reconocidas.[33][43][44] Según Russell Mittermeier, presidente de Conservation International (CI), el taxónomo Colin Groves y otros, hay unas cien especies o subespecies de lémures reconocidas que perviven en la actualidad, divididas en cinco familias y quince géneros.[45] Dado que los datos genéticos indican que los subfósiles de lémures extinguidos recientemente estaban estrechamente relacionados con los actuales,[46] unas tres familias, ocho géneros y diecisiete especies adicionales pueden ser incluidos en el total.[31][36] Sin embargo, otros expertos califican estas afirmaciones como una «inflación taxonómica»,[44] y reducen el número de especies vivientes hasta cincuenta.[33]
También existen discrepancias sobre la clasificación de los lémures dentro del suborden Strepsirrhini, aunque la mayoría de los expertos coincidan en el mismo árbol filogenético. En una taxonomía, Lemuriformes incluye a todos los estrepsirrinos vivientes en dos superfamilias, Lemuroidea para todos los lémures y Lorisoidea para loris y gálagos.[19] A veces a los lorises y los gálagos se les separa de los lémures y los ubican en su propio infraorden, Lorisiformes.[47] En otra taxonomía publicada por Colin Groves, el aye-aye fue situado en su propio infraorden, Chiromyiformes, mientras que los lorises y los gálagos se los ubicó en Lorisiformes y al resto de los lémures en Lemuriformes.[48]
Aunque está generalmente aceptado que el aye-aye es el miembro más basal del clado de los lémures, la relación entre las otras cuatro familias no está tan clara ya que divergieron durante el relativamente estrecho espacio de tiempo de 10 a 12 millones de años entre el Eoceno tardío (42 Ma) y el Oligoceno (30 Ma).[18][25] Aunque todos los estudios sitúen Cheirogaleidae y Lepilemuridae como un clado hermano a Indriidae y Lemuridae, algunos sugieren que Cheirogaleidae y Lepilemuridae divergieron primero,[49][50] mientras otros apuntan a que Indriidae y Lemuridae fueron los primeros en separarse.[25]
| 2 infraordenes[19][51] | 3 infraórdenes[47] | 4 infraórdenes[48] |
|---|---|---|
|
|
|

La taxonomía de los lémures ha cambiado considerablemente desde la primera clasificación taxonómica realizada por Carlos Linneo en 1758. Uno de los mayores desafíos fue la clasificación del aye-aye, que ha sido un tema de debate hasta muy recientemente.[6] Hasta que Richard Owen publicó un estudio anatómico definitivo en 1866, los primeros naturalistas no estaban seguros si el aye-aye (género Daubentonia) era un primate, un roedor o un marsupial,[52][53][54] y su ubicación entre los primates también fue problemática hasta hace muy poco tiempo. Basándose en su anatomía, los investigadores han encontrado un respaldo para clasificar el género Daubentonia como un índrido especializado, un grupo hermano a los estrepsirrinos, y como un taxón indeterminado dentro del orden de Primates.[17] Las pruebas moleculares han mostrado ahora que Daubentoniidae es basal a todos los Lemuriformes,[17][55] y en 2008, Russell Mittermeier, Colin Groves y otros no tuvieron en cuenta su localización en una taxonomía de nivel superior y definieron a los lémures como monofiléticos y conteniendo cinco familias vivas, incluida Daubentoniidae.[45]
Las relaciones entre familias también han sido problemáticas y todavía están pendientes de ser definitivamente resueltas.[17] Para complicar todavía más la cuestión, varios fósiles de primates del Paleógeno de fuera de Madagascar, como Bugtilemur, han sido clasificados como lémures,[56] sin embargo, el consenso científico no acepta estas asignaciones basadas en pruebas genéticas,[17][55] por lo que generalmente se considera que los primates malgaches son monofiléticos.[17][25][49] Otra área controvertida es la relación entre los lepilemúridos y los extintos lémures koala (Megaladapidae), antes agrupados en la misma familia debido a las similitudes en su dentición,[57] pero a la vista de los estudios genéticos ya no se considera que se encuentren estrechamente relacionados.[49][58]
Muchos cambios taxonómicos se han dado a nivel de género, aunque estas revisiones han resultado más concluyentes, a menudo apoyadas por análisis genéticos y moleculares. Una de las revisiones más notables consistió en la división gradual de un amplio género Lemur en géneros separados para el lémur de cola anillada, los lémures rufos y los lémures marrones (también llamados lémures verdaderos), debido a un gran número de diferencias morfológicas.[59][60]
Tras las revisiones taxonómicas realizadas por Mittermeier, Groves y otros, el número de especies reconocidas ha pasado de treinta y tres especies y subespecies en 1994 a aproximadamente cien en 2008.[33][45][61] Si se continúa con las investigaciones citogenéticas y de genética molecular, además de los estudios de campo en curso, en particular con especies crípticas como los lémures ratón, el número de especies reconocidas probablemente seguirá creciendo.[33] Sin embargo, la escalada en el número de especies reconocidas ha tenido también sus críticos entre estudiosos de los lémures y los taxónomos. También hay que considerar que las clasificaciones a fin de cuentas dependen del concepto de especie que se utilice, y algunos especialistas proponen que se realicen análisis más minuciosos.[33][44]
Anatomía y fisiología[editar]
Los lémures son un grupo diverso en términos de morfología y fisiología.[33] Algunos, como los lepilemúridos y los índridos, tienen las extremidades inferiores más largas que las superiores, y son excelentes saltadores.[62][63][64] En su condición de folívoros, los índridos cuentan con un aparato digestivo especializado, con glándulas salivales muy desarrolladas, un estómago espacioso y un ciego alargado que facilita la fermentación.[13][15][65] [66][67] El lémur enano de orejas peludas (Allocebus trichotis) tiene una lengua muy larga, que le permite alimentarse de néctar,[53] y el lémur de vientre rojo (Eulemur rubriventer) tiene una lengua similar a un cepillo, también especialmente adaptada para alimentarse de néctar y polen.[13] El aye-aye ha desarrollado algunas características que son únicas entre los primates y que lo distingue de entre los demás lémures; entre estos rasgos diferenciativos se incluyen unos incisivos que crecen continuamente, de forma similar a los roedores, que le permiten roer la madera y semillas de cáscara dura, un dedo medio filiforme (muy fino, en forma de filamento) para extraer comida de agujeros diminutos, unas grandes orejas, similares a las de los murciélagos, para detectar oquedades en los árboles,[15][28][53][68] o el uso de señales acústicas para buscar alimento.[52]
Varían enormemente en cuanto a tamaño; cuentan con el primate más pequeño del mundo y, hasta tiempos recientes, con algunos de los más grandes. En la actualidad, su tamaño va desde los 30 g de Microcebus berthae hasta los 7-9 kg del indri (Indri indri) y el sifaca diademado (Propithecus diadema),[69][65] pero si se consideran las especies recientemente extinguidas su rango de tamaño se extiende hasta el equivalente al de un gorila macho, con los 160-200 kg de Archaeoindris fontoynonti.[6][31]

Como todos los primates, los lémures tienen cinco dedos divergentes provistos de uñas (en la mayoría de casos) en sus manos y pies. La mayor parte posee una uña alargada y contraída lateralmente, llamada garra de aseo, en el segundo dedo del pie, la cual usan para rascarse y acicalarse.[53][70] Además de esta garra de aseo, los lémures comparten otros rasgos característicos de los primates estrepsirrinos, como son el rinario (o «nariz húmeda», principal diferencia con los haplorrinos), un órgano vomeronasal totalmente funcional que detecta feromonas, una barra ósea postorbitaria y la cavidad ocular carente de cierre postorbital, sínfisis mandibular no fusionada (mandíbulas izquierda y derecha separadas), y una proporción cerebro-masa corporal baja.[16][71]
Entre los rasgos adicionales compartidos con otros primates prosimios se encuentran el útero bicorne (con dos cuernos, en forma de 'Y') y la placentación epitelicorial.[14][71] Como sus pulgares son solo seudooponibles, lo que hace su movimiento menos independiente de los otros dedos,[70] sus manos son menos eficientes para el agarre y la manipulación de objetos.[21] Su hallux (primer dedo del pie) está muy desarrollado, lo que facilita el agarre a las ramas de los árboles.[53] Un error bastante común es la creencia de que los lémures tienen colas prensiles; sin embargo, esta es una característica que entre los primates solo se da en los monos del Nuevo Mundo, y, más concretamente, en los atélidos.[70] Los lémures cuentan con un sentido del olfato muy desarrollado, un rasgo compartido con la mayor parte de los demás mamíferos y primates primitivos, pero no con los primates superiores, que se orientan principalmente con la vista.[21]
Los lémures son atípicos por la gran variedad de sus estructuras sociales, aunque generalmente carecen de dimorfismo sexual en cuanto a su tamaño y a la morfología de sus dientes caninos.[13][42] Sin embargo, algunas especies suelen tener unas hembras de mayor tamaño,[52] y dos especies de lémures marrones (género Eulemur), el lémur de cabeza gris (E. cinereiceps) y el lémur marrón de frente roja (E. rufus), presentan diferencias de tamaño en sus caninos.[72] Entre los lémures marrones se da un cierto dicromatismo sexual (diferencias entre los sexos en la coloración de la piel),[42] aunque esta diferencia varía desde sorprendentemente obvia, como en el lémur negro (E. macaco), a casi imperceptible en el lémur pardo (E. fulvus).[72]
Se ha descubierto recientemente que el complejo críptico de especies, esto es, la dificultad para los humanos de distinguir visualmente entre dos o más especies distintas, se ha dado a la hora de la identificación de los lémures, en particular dentro de los lémures saltadores (Lepilemur) y lémures ratón (Microcebus). Las subespecies de los lémures saltadores se definieron tradicionalmente basándose en pequeñas diferencias morfológicas, aunque nuevas pruebas genéticas han apoyado la consideración como especies plenas otorgada a algunas poblaciones regionales.[58] En el caso de los lémures ratón, el lémur naranja (M. murinus), el lémur ratón dorado marrón (M. ravelobensis) y el lémur de Goodman (M. lehilahytsara) hace poco estaban considerados como la misma especie, hasta que pruebas genéticas los identificaron como especies crípticas.[73]
Dentición[editar]
| Familia | Fórmula dental decidua |
[57][74] Fórmula dental permanente [42][53][75][76] |
|---|---|---|
| Cheirogaleidae, Lemuridae | ||
| Lepilemuridae | ||
| †Archaeolemuridae | ||
| †Megaladapidae | ||
| Indriidae, †Palaeopropithecidae | [N 1] | [N 2] |
| Daubentoniidae |
Su dentición es heterodonta (múltiples morfologías dentales) y deriva de una ancestral dentición permanente primate de . Índridos, lémures saltadores, el aye-aye y los extintos Mesopropithecus, Archaeolemuridae y Megaladapis han reducido su dentición, y perdieron incisivos, caninos o premolares.[78] La dentición decidua (dientes de leche) ancestral es , pero los índridos jóvenes, aye-ayes, Megaladapis, Palaeopropithecidae, y probablemente Archaeolemuridae, tienen menos dientes deciduos.[57][74]
También hay diferencias sensibles en morfología y topografía dental entre los lémures. El indri, por ejemplo, tiene dientes que están perfectamente adaptados para arrancar hojas y aplastar semillas.[65] En el peine dental de la mayor parte de los lémures, los incisivos y caninos inferiores son procumbentes (hacia adelante) y alineados y espaciados con precisión, proporcionando así una herramienta para el acicalado o la alimentación.[16][57][78] Por ejemplo, los indris no utilizan el peine dental solo para el aseo, sino también para extraer las grandes semillas del resistente epicarpio de los frutos de Beilschmiedia,[79] mientras que los lémures de orejas ahorquilladas utilizan su relativamente largo peine dental para rasgar la corteza de los árboles y conseguir que fluya su savia.[53] Mantienen el peine dental limpio utilizando un órgano sublingual delgado, llano y fibroso que cubre gran parte de la base de la lengua, una estructura especializada que actúa de forma similar a un cepillo de dientes para eliminar pelos y otros restos;[N 3] esta «segunda lengua» se extiende por debajo de la punta de la lengua y tiene unos puntos dentados queratinizados que rastrillan entre los dientes incisivos.[80][81]
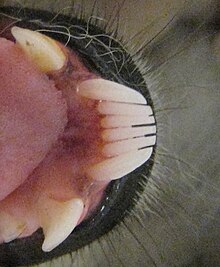
Tan solo el aye-aye, el extinto aye-aye gigante (Daubentonia robusta) y el más grande de los también extintos Mesopropithecus carecen de un peine dental funcional, característico de los estrepsirrinos.[78][76] En el caso del aye-aye, la morfología de sus incisivos deciduos, que pierden poco después de nacer, indica que sus antepasados tenían peine dental. Pierden estos dientes de leche poco después del nacimiento,[82] y son reemplazados por unos incisivos que crecen continuamente y durante toda su vida.[78]
El peine dental de los lémures está formado generalmente por seis dientes (cuatro incisivos y dos caninos), aunque en el caso de los índridos, los lémures babuinos y algunos lémures perezosos la estructura está formada por cuatro dientes.[16][78] Debido a que el colmillo inferior forma parte del peine dental o se ha perdido, la dentición inferior puede ser difícil de interpretar, sobre todo desde el primer premolar (P2) que a menudo tiene forma caniniforme (de un canino) para ocupar el papel del canino.[57] En los lémures folívoros, excepto en los índridos, los incisivos superiores están ausentes o son muy reducidos.[57][78] Usado junto con el peine dental del maxilar inferior, este complejo dental recuerda la almohadilla dental de los ungulados.[78]
Los lémures son atípicos entre los primates por su rápido desarrollo dental, en particular entre las especies más grandes. Los índridos tienen un crecimiento corporal relativamente lento, pero una extremadamente rápida formación dentaria y erupción.[83] Por el contrario, los primates antropoides experimentan un desarrollo dental más lento, y cuentan con mayor tamaño y un desarrollo morfológico también más lento.[78] Los lémures son asimismo dentalmente precoces al nacer, y ya tienen su dentición permanente completa al destete.[32]
Generalmente tienen un esmalte dental fino comparado con los primates antropoides. Esto puede causar un mayor desgaste y la rotura de los dientes anteriores (delanteros) debido a su uso intensivo en el acicalamiento, la alimentación y la lucha. Existe poca información disponible sobre la salud dental de los lémures, salvo que los lémures de cola anillada salvajes de la reserva privada de Berenty (Madagascar) a veces presentan abscesos en los caninos superiores y caries dental, posiblemente debido al consumo de alimentos no nativos.[78]
Sentidos[editar]

El sentido del olfato es muy importante para estos primates y lo utilizan con frecuencia en la comunicación.[13][15][21] Los lémures tienen hocicos largos (a diferencia de los cortos hocicos de los haplorrinos), lo que se considera tradicionalmente que es una evolución motivada para conseguir una mejor posición de la nariz para percibir los olores,[15] aunque un hocico largo no necesariamente se traduce en una alta agudeza olfativa, ya que no es el tamaño relativo de la fosa nasal lo que guarda correlación con el olor, sino la densidad de receptores olfativos.[84][85] En cambio, los hocicos largos pueden facilitar una mejor masticación.[85]
La «nariz húmeda», o rinario, es un rasgo compartido con otros estrepsirrinos y muchos otros mamíferos, pero no con los primates haplorrinos.[53] Aunque se afirme que realza el sentido del olfato,[71] en realidad es un órgano del sentido basado en el tacto que se une con un órgano vomeronasal bien desarrollado. Dado que las feromonas son moléculas por lo general grandes y no volátiles, el rinario se utiliza para tocar un objeto marcado por el olor y transferir las moléculas de las feromonas bajando por el surco nasolabial hasta el órgano vomeronasal vía los conductos nasopalatinos que discurren a través del foramen incisivo del paladar duro.[14]
Para comunicarse mediante el olor, algo muy útil por la noche, los lémures marcan su territorio con orina y con las glándulas odoríferas situadas en las muñecas, la cara interna del codo, las zonas genitales o el cuello.[14][71] La piel escrotal de la mayor parte de los lémures machos tiene glándulas odoríferas.[86] Los lémures rufos y los sifacas machos tienen una glándula en la base del cuello,[14][53] mientras que el lémur grande del bambú (Prolemur simus) y el lémur de cola anillada (Lemur catta) tienen glándulas en las patas anteriores, cerca de la axila.[14] Los machos de los lémures de cola anillada también tienen glándulas odoríferas en la cara interna de sus antebrazos, junto a una espuela similar a una espina, que utilizan para excavar y, al mismo tiempo, marcar ramas de los árboles con señales de olor.[53] También frotan sus colas entre los antebrazos y luego toman parte en «luchas apestosas» agitando su cola ante sus oponentes.[14]
| Lémures | Primates antropoides | |
|---|---|---|
| Ángulo entre ojos | 10-15° | 0° |
| Campo binocular | 114-130° | 140-160° |
| Campo combinado (binocular + periférico) |
250-280° | 180-190° |
Se considera que los lémures (y los estrepsirrinos en general) se orientan visualmente en menor medida que los primates superiores, ya que se apoyan fundamentalmente en su sentido del olfato y en la percepción de feromonas. Tienen poco desarrollada la fóvea de la retina, que confiere una mayor agudeza visual. Se cree que el septo postorbital (cierre óseo detrás del ojo) en los primates haplorrinos estabiliza ligeramente el ojo, permitiendo la evolución de la fóvea; solo con la barra postorbital, los lémures han sido incapaces de desarrollar la fóvea.[88] Por ello, independientemente de su modelo de actividad (nocturno, catemeral o diurno), los lémures muestran una baja agudeza visual y una elevada sumación retiniana.[32] Sin embargo, los lémures tienen un campo visual más amplio que los primates antropoides, debido a una pequeña diferencia en el ángulo entre ojos, como se puede ver en la tabla de la izquierda.[87]
Aunque carezcan de fóvea, algunos lémures diurnos tienen un área central (porción de la retina que rodea a la fóvea y donde se produce la mayor fotorrecepción) rica en conos, aunque menos agrupada.[88] Esta área central tiene una alta proporción de bastones/conos en muchas especies diurnas estudiadas, mientras que los antropoides diurnos no tienen bastones en su fóvea. De nuevo, esto sugiere una menor agudeza visual de los lémures frente a los primates antropoides.[89] Además, la proporción bastones/conos varía incluso entre especies diurnas. Por ejemplo, el sifaca de Verreaux (Propithecus verreauxi) y el indri (Indri indri) tienen solo unos pocos conos grandes dispersos a lo largo de una retina predominantemente dominada por bastones. Los ojos del lémur de cola anillada (Lemur catta) contienen un cono por cada cinco bastones. Por otra parte, los lémures nocturnos, como los lémures ratón y los lémures enanos, tienen retinas compuestas solo por bastones.[14]
Dado que los conos hacen posible la percepción del color, el predominio de los bastones en los ojos de los lémures sugiere que no han desarrollado la visión en color.[14] En el lémur más estudiado, el de cola anillada, se ha comprobado que tiene la visión azul-amarilla, pero carece de la capacidad de distinguir matices rojos y verdes.[90] Debido al polimorfismo en las moléculas de opsinas, que cifran la receptividad en color, la visión tricromática puede darse muy raramente en las hembras de unas pocas especies, como el sifaca de Coquerel (Propithecus coquereli) y el lémur rufo rojo (Varecia rubra). La mayor parte de los lémures son, por tanto, monocromáticos o dicromáticos.[14]

La mayor parte de los lémures cuentan con el tapetum lucidum, una capa reflexiva de tejidos en el ojo de muchos animales vertebrados.[42] Los primates haplorrinos carecen de esta característica, y su presencia favorece la capacidad visual de los lémures.[32][89] El tapetum coroideo de los estrepsirrinos es único entre los mamíferos porque está compuesto de riboflavina cristalina, y la dispersión óptica resultante es lo que limita su agudeza visual.[89] Aunque se considere que el tapetum está presente en todos los lémures, parece haber excepciones entre el género Eulemur, como el lémur negro (Eulemur macaco) y el lémur pardo (Eulemur fulvus), así como en los del género Varecia.[14][32][89] Sin embargo, dado que la riboflavina del tapetum tiene tendencia a disolverse y desaparecer cuando es tratada para la investigación histológica, las excepciones todavía son cuestionables.[14]
Los ojos también cuentan con una membrana nictitante o «tercer párpado», mientras que la mayor parte de los demás primates solamente tienen un pliegue semilunar de la conjuntiva (plica semilunaris) menos desarrollado; la membrana nictitante mantiene la córnea húmeda y limpia deslizándose por la superficie del ojo.[91][92]
Metabolismo[editar]
Los lémures tienen un metabolismo basal bajo, lo que les ayuda a conservar la energía durante la estación seca, cuando escasean el agua y la comida.[13][64] Pueden optimizar su uso de energía bajando su tasa metabólica a un 20 % por debajo de los valores correspondientes a mamíferos con una masa corporal similar.[93] Por ejemplo, hay informes de que el lémur saltador de cola roja (Lepilemur ruficaudatus) tiene uno de los metabolismos basales más bajos entre los mamíferos. Su baja tasa metabólica puede estar relacionada con su dieta generalmente folívora y su relativamente baja masa corporal.[64] Los lémures presentan adaptaciones de comportamiento para complementar esta característica, como tomar el Sol, sentarse encogidos, acurrucarse en grupo y compartir lecho, a fin de reducir la pérdida de calor y conservar la energía.[93] Los lémures enanos y los lémures ratón tienen ciclos estacionales de dormancia para conservar energía.[93] Antes de la estación seca acumulan grasa en el tejido adiposo blanco localizado en la base de la cola y las patas traseras, hasta llegar a doblar su peso.[30][94][95] Al final de la temporada seca, su masa corporal puede bajar hasta la mitad de lo que era antes de la temporada.[30] Los que no experimentan estados de dormancia también son capaces de suspender algunas funciones de su metabolismo para conservar energía.[93]
Comportamiento[editar]
El comportamiento de los lémures es tan variable como su morfología. Las diferencias en dieta, sistemas sociales, modelos de actividad, locomoción, comunicación, tácticas para evitar a los depredadores, sistemas reproductivos y niveles de inteligencia ayudan a definir los taxones de los lémures y a separar a unas especies de las demás. Aunque se tiende con frecuencia a diferenciar a los lémures más pequeños y nocturnos de los lémures más grandes y diurnos, a menudo hay excepciones que ayudan a ejemplificar la naturaleza única y diversa de estos primates malgaches.
Dieta[editar]

Sus dietas son muy variadas y demuestran un alto grado de versatilidad,[96] aunque la tendencia general es que las especies más pequeñas consuman principalmente fruta e insectos (omnívoras), mientras que las especies más grandes son más herbívoras, y consumen sobre todo materia vegetal.[38] Como todos los primates, los lémures hambrientos podrían comer casi cualquier cosa que sea comestible, estuviera o no entre sus alimentos preferidos.[14] Por ejemplo, el lémur de cola anillada come insectos y pequeños vertebrados cuando es necesario,[38][59] por lo que se le considera comúnmente como un omnívoro oportunista.[78] El lémur ratón gigante de Coquerel es sobre todo frugívoro, pero consume secreciones de insecto durante la estación seca.[38]
Una asunción común en mastozoología es que los pequeños mamíferos no pueden subsistir con una alimentación exclusivamente vegetal y deben tener una dieta alta en calorías para sobrevivir. Por ello se consideraba que la dieta de los primates menudos debía tener un alto contenido en insectos (insectívoros), ricos en proteínas. Las investigaciones han mostrado, sin embargo, que los lémures ratón, los primates vivientes más pequeños, consumen más fruta que insectos, contradiciendo la hipótesis general.[14][38]
La materia vegetal compone la parte fundamental de la mayoría de las dietas de las especies de lémur. Miembros de al menos 109 de todas las familias de plantas conocidas en Madagascar (el 55 %) son aprovechadas por lémures. Dado que son fundamentalmente arborícolas, la mayor parte de estas especies vegetales aprovechadas son plantas leñosas, como árboles, arbustos o lianas. Solo se tiene conocimiento de que el lémur de cola anillada (Lemur catta), los lémures del bambú (género Hapalemur) y el lémur rufo blanco y negro (Varecia variegata) consumen hierbas. Aunque Madagascar es rico en una gran variedad de helechos, estas plantas raramente son ingeridas por los lémures; una posible razón podría ser que los helechos carecen de las flores, frutas o semillas comunes en su dieta, y que además se desarrollan en el suelo, mientras que los lémures pasan la mayor parte de su tiempo en los árboles; por otra parte, los helechos tienen un gusto desagradable debido al alto contenido de taninos en sus frondes. De igual manera, los mangles raramente son aprovechados por los lémures, también debido a su alto contenido de tanino.[96] Sin embargo, parece que algunos lémures han desarrollado respuestas contra algunas defensas comunes de las plantas, como taninos y alcaloides.[79] El lémur dorado (Hapalemur aureus), por ejemplo, come el bambú gigante Cathariostachys madagascariensis, que contiene altos niveles de cianuro. Este lémur puede consumir cada día doce veces la dosis habitualmente letal para la mayor parte de los mamíferos; se desconocen los mecanismos fisiológicos que lo protegen del envenenamiento por cianuro.[13] En el Duke Lemur Center de la Universidad Duke en los Estados Unidos, los lémures que vagan por los recintos al aire libre han sido observados comiendo hiedra venenosa (Taxicodendron radicans) sin haber mostrado síntomas de haberles afectado negativamente.[70]

Muchas de las especies de lémur más grandes son folívoras,[96] y en particular los índridos.[62] Sin embargo, algunas especies más pequeñas, como los lémures saltadores (género Lepilemur) y los lémures lanudos (género Avahi) también se alimentan fundamentalmente de hojas, lo que los convierte en los primates más pequeños con este tipo de dieta.[64] Los lémures más pequeños raramente se alimentan de hojas.[96] En conjunto, está documentado que los lémures consumen hojas de al menos 82 familias de plantas nativas y 15 familias de plantas ajenas. Tienden a ser selectivos a la hora de elegir la parte de la hoja o del brote que consumen, así como su edad; a menudo prefieren más hojas jóvenes que maduras.[96]
Muchos lémures que comen hojas suelen hacerlo durante épocas de escasez de fruta, en ocasiones sufriendo una pérdida de peso por ese motivo.[97] La mayor parte de las especies de lémur, incluidos la mayoría de los más pequeños, y excluyendo algunos indris, se alimenta predominantemente de fruta (frugívoros) cuando está disponible. En conjunto, se ha comprobado que los lémures consumen la fruta de al menos 86 familias de planta nativas y 15 familias de planta foráneas. Al igual que en la mayor parte de frugívoros tropicales, en su dieta predomina la fruta de las especies de Ficus (higueras).[96] En muchos primates antropoides, la fruta es una fuente primaria de vitamina C, pero a diferencia de éstos, los lémures (y todos los estrepsirrinos) pueden sintetizar su propia vitamina C.[98] Históricamente se ha considerado que las dietas de lémures cautivos altas en frutas ricas en vitamina C causaban hemosiderosis, un tipo de trastorno provocado por sobrecarga sistémica de hierro, dado que la vitamina C incrementa la absorción de este metal. Aunque se haya comprobado que los lémures en cautividad son propensos a la hemosiderosis, la frecuencia de la enfermedad varía de unas instituciones a otras y puede depender de la dieta, protocolos de mantenimiento o patrimonio genético. Las asunciones sobre este problema tienen que ser probadas por separado para cada especie.[99] Parece que el lémur de cola anillada, por ejemplo, es menos propenso a esta enfermedad que otras especies de lémur.[100]
Solamente ocho especies de lémur se alimentan de semillas (granívoros), aunque este dato podría ser inferior a la realidad, ya que la mayor parte de las observaciones solo muestran el consumo de fruta y no indican si también se consumen semillas. Entre estos lémures granívoros se incluyen algunos índridos, como el sifaca diademado (Propithecus diadema), el sifaca de Tattersall (Propithecus tattersalli), el indri (Indri indri),[13][67] y el aye-aye (Daubentonia madagascariensis). El aye-aye, que se especializa en especies con defensas estructurales, puede masticar semillas de Canarium, que son más duras que las semillas que son capaces de abrir los platirrinos, o monos del Nuevo Mundo.[52] Al menos 36 géneros de 23 familias de plantas forman parte de la dieta de los lémures granívoros.[96]
Las inflorescencias de al menos 60 familias de plantas son ingeridas por lémures con tamaños que van desde los diminutos lémures ratón hasta los relativamente grandes lémures rufos. Si no utilizan las flores, a veces consumen el néctar (nectarívoros) junto con el polen (polinívoros). Al menos 24 especies nativas de 17 familias de plantas forman parte de la dieta de los lémures por su polen o néctar.[96]
La corteza y exudados de las plantas como la savia de árbol son consumidas por unas pocas especies. La ingestión de exudados ha sido reportada respecto a 18 especies de plantas y solo en las regiones secas del sur y oeste de Madagascar. Solo Phaner furcifer y Mirza coquereli consumen con regularidad savia de árboles. La corteza nunca ha sido reportada como un elemento significativo en la dieta de los lémures, pero al menos cuatro especies la consumen: el aye-aye, el lémur saltador de cola roja (Lepilemur ruficaudatus), el lémur pardo (Eulemur fulvus) y el sifaca de Verreaux (Propithecus verreauxi). La alimentación con corteza por lo general está directamente unida a la alimentación con exudados, excepto la alimentación por parte del aye-aye de corteza de Afzelia bijuga en la Reserva de Nosy Mangabe, al nordeste de la isla.[96]
También se ha informado sobre el consumo de tierra (geofagia), probablemente como ayuda a la digestión, proporcionando minerales y sales y ayudando a absorber toxinas. Se ha observado a algunos sifacas comiendo tierra de montículos de termitas, posiblemente para añadir beneficiosa flora intestinal y ayudar a la digestión de la celulosa de su dieta folívora.[70]
Sistemas sociales[editar]
Los lémures son animales sociales y viven en grupos que por lo general cuentan con al menos quince individuos.[13] Entre sus modelos de organización social, podemos hablar de «solitario, pero social», «fisión-fusión»,[N 4] «uniones de pareja» y «grupo multimachos».[102] Los lémures nocturnos son fundamentalmente solitarios, aunque sociales, buscando solos el alimento por la noche, pero por lo general se reúnen en grupos durante el día. El grado de socialización varía en función de las especies, el género, la localización y la estación.[28][38] Por ejemplo, en muchas especies nocturnas las hembras, junto con sus crías, compartirán lugares de crianza con otras hembras y posiblemente un macho, que abarca un amplio territorio y que puede superponerse con uno o varios grupos de hembras. En el caso de Lepilemur y Phaner, una o dos hembras pueden compartir un territorio, posiblemente con un macho. Además del compartir espacios vitales, también se relacionarán vocal o físicamente con su compañero de territorio mientras buscan alimento por la noche.[38] Entre los lémures diurnos se dan muchos de los sistemas sociales vistos en monos y hominoides,[13][38] viviendo en grupos sociales relativamente permanentes y cohesionados. Los grupos multimachos son el sistema más común entre ellos, al igual que en la mayor parte de los primates antropoides.[N 5] Los lémures marrones o verdaderos utilizan este sistema social, y a menudo viven en grupos de diez o menos individuos. Se ha comprobado que los lémures rufos viven en sociedades de fisión-fusión,[38] y los indris forman uniones de pareja.[102]

En algunos lémures se ha observado filopatría (tendencia a permanecer en su territorio natal o a volver tras haberlo abandonado) entre las hembras, que permanecen dentro de su territorio mientras los machos emigran al alcanzar la madurez; en otras especies ambos sexos emigran.[13] En algunos casos, la filopatría femenina puede ayudar a explicar la evolución de grupos multimachos de hembras vinculadas, como en el caso del lémur de cola anillada, el sifaca de Milne-Edwards (Propithecus edwardsi) y el sifaca de Verreaux. Sus antepasados pueden haber sido más solitarios, con hembras que vivían en parejas madre-hijo (díada). Con el tiempo, estas díadas pueden haberse unido con otras parejas madre-hijo vecinas a fin de defender recursos distribuidos en un territorio amplio. Si así fuera, los grupos multimachos de los lémures estarían claramente diferenciados en su estructura interna en comparación con los primates catarrinos (simios del Viejo Mundo).[104]
La presencia de un dominio social de las hembras diferencia a los lémures de la mayor parte de los demás primates e incluso de los demás mamíferos;[13][38][42][105] en la mayor parte de las sociedades de primates, los machos son los dominantes a menos que las hembras se unan para formar coaliciones que los desplacen.[106] Sin embargo, hay especies que no muestran este dominio femenino, como en el caso de muchas especies de Eulemur,[38][72] o del lémur grande del bambú (Prolemur simus).[107] Cuando las hembras son las dominantes dentro de un grupo, la forma en que mantienen ese dominio varía. Los machos del lémur de cola anillada actúan de forma sumisa con o sin señales de agresión por parte de las hembras, en cambio, los machos del lémur coronado (Eulemur coronatus) solo actuarán sumisamente cuando las hembras actúen de forma agresiva contra ellos. La agresión de las hembras a menudo tiene que ver con la alimentación, pero no se limita a ese aspecto.[108]
Existen muchas hipótesis que han intentado explicar por qué los lémures han establecido un dominio social de las hembras, mientras que otros primates con estructuras sociales similares no lo hacen,[13][105] pero no se ha alcanzado ningún consenso tras décadas de investigación. El punto de vista dominante en la literatura apunta a que el dominio femenino es una característica ventajosa dados los altos costes de la reproducción y la escasez de recursos disponibles,[105] pues se ha comprobado que el dominio de las hembras está ligado a un incremento del cuidado y atención maternal.[106] Sin embargo, cuando los costes reproductivos y una extrema estacionalidad de los recursos se compararon con la misma situación entre otros primates, se comprobó la existencia de un dominio masculino en condiciones que eran similares o incluso más difíciles que las afrontadas por los lémures. En 2008 una nueva hipótesis revisó este modelo usando la teoría de juegos. Se sostuvo que cuando dos individuos estaban parejos en cuanto a su capacidad de pelear, el más necesitado ganaría el conflicto ya que tendría más que perder. Por ello la hembra, con más necesidades de recursos debido al embarazo, la lactancia y el cuidado maternal, tendría más probabilidad de vencer en conflictos para obtener recursos con machos del mismo tamaño. Para ello, sin embargo, se asumía un monomorfismo entre sexos.[105] Al año siguiente se propuso una nueva hipótesis para explicar el monomorfismo, afirmando que dado que la mayor parte de las hembras de lémures solo son sexualmente receptivas durante un día o dos cada año, los machos pueden utilizar una forma más pasiva de protección de la pareja: la esfragis copulatoria (secreción gelatinosa utilizada en el acoplamiento de algunas especies animales), que bloquea el tracto reproductivo de la hembra, impidiendo a otros machos un apareamiento exitoso con ella, y así reducir la necesidad de comportamientos agresivos y el camino evolutivo hacia el dimorfismo sexual.[34]

En general, los niveles agonísticos (o agresivos) tienden a guardar relación con la longitud relativa de los caninos. El lémur de cola anillada tiene unos dientes caninos superiores largos y agudos en ambos sexos, y muestra altos niveles de agonismo. En cambio, el indri tiene colmillos más pequeños y muestra niveles inferiores de agresión.[32] Cuando grupos vecinos de la misma especie defienden sus territorios, el conflicto puede tomar la forma de defensa ritualizada; en los sifacas, estos combates ritualizados implican mirar fijamente, gruñir, dejar marcas de olor y saltar para ocupar ciertas secciones del árbol, mientras que el indri defiende su territorio con batallas rituales de «canto».[13]
Como otros primates, los lémures utilizan el acicalado social para aliviar relaciones tensas y consolidar relaciones. Se acicalan al saludarse, cuando despiertan, al prepararse para dormir, entre las madres y sus hijos, en las relaciones juveniles y para fomentar relaciones sexuales.[109] A diferencia de los primates antropoides, que apartan el pelaje con las manos y cogen con los dedos o la boca las partículas como piel muerta o restos de comida, o los insectos y otros ectoparásitos, los lémures se acicalan con la lengua y se cepillan con su peine dental.[13][109] A pesar de estas diferencias en la técnica, los lémures se acicalan con la misma frecuencia y por los mismos motivos que los antropoides.[109]
Patrones de actividad[editar]
Su ritmo biológico puede variar desde un comportamiento nocturno en los lémures más pequeños a diurno en la mayor parte de los más grandes. La diurnalidad no se da en ningún otro prosimio.[28] La catemeralidad (actividad tanto de día como de noche) se da entre algunos lémures más grandes; pocos o casi ningún otro primate expone esta clase de modelo de actividad,[110] con regularidad o irregularmente, ante el cambio de condiciones ambientales.[13] Los lémures catemerales a los que se ha estudiado en mayor profundidad son los lémures marrones o verdaderos (género Eulemur).[42][111] Aunque el lémur mangosta (E. mongoz) sea el mejor documentado, todas las especies estudiadas de este género han mostrado algún grado del comportamiento catemeral,[72] aunque la actividad nocturna a menudo se vea restringida por la disponibilidad de luz y las fases lunares.[14] Este tipo de comportamiento fue documentado por primera vez en los años 1960 en especies de lémures verdaderos así como en otras especies de lemúridos, como los lémures rufos y los lémures del bambú. Inicialmente descrito como «crepuscular» (actividad al amanecer y al anochecer), el antropólogo Ian Tattersall llevó a cabo investigaciones adicionales y acuñó el nuevo término «catemeral»,[110] aunque otros científicos no antropólogos prefieran los términos «circadiano» o «nictimeral».[14]
A fin de conservar la energía y el agua en su ambiente altamente estacional,[93][112] los lémures ratón y los lémures enanos han desarrollado ciclos estacionales de dormancia durante los cuales su ritmo metabólico y su temperatura corporal disminuyen; son los únicos primates conocidos que lo hacen.[93] Acumulan reservas de grasa en sus miembros inferiores y en la base de su cola antes del árido invierno, cuando la comida y el agua escasean,[30][94] y pueden mostrar períodos prolongados de letargo diario durante la estación seca. Este letargo diario constituye menos de 24 horas de dormancia, mientras que el promedio de los letargos prolongados alcanza las dos semanas de duración y señalan la proximidad de la hibernación.[93] Los lémures ratón han sido observados experimentando un letargo que dura varios días consecutivos, pero se sabe que los lémures enanos hibernan durante entre seis y ocho meses cada año,[28][30][95] en particular en la costa oeste de Madagascar.[112]
Los lémures enanos son los únicos primates conocidos que hibernan durante períodos prolongados.[93][113] A diferencia de otros mamíferos hibernantes de regiones templadas, que tienen que despertar con regularidad durante unos días, los lémures enanos tienen un período de hibernación profunda continua (de mayo a septiembre). Antes y después de esta hibernación profunda, hay dos meses de transición (abril y octubre), donde buscarán alimento de forma limitada para reducir las posibles demandas a sus reservas de grasa.[112] A diferencia de cualquier otro mamífero que hiberne, la temperatura corporal de los lémures enanos hibernantes fluctuará con la temperatura ambiente, en lugar de mantenerse baja y estable.[30][95][112]
Otros lémures que no experimentan períodos de dormancia conservan energía seleccionando microhábitats termorregulados (como agujeros en los árboles), compartiendo nido y reduciendo la superficie corporal expuesta, al sentarse encorvados y acurrucarse en grupo. A los lémures de cola anillada, a los lémures rufos y a los sifacas se les ve habitualmente tomando el sol, utilizando la radiación solar para calentarse en lugar del calor corporal generado por el metabolismo.[93]
Locomoción[editar]


El comportamiento locomotor de los lémures, tanto existentes como extintos, es muy variado y su diversidad excede a la de los primates antropoides.[38] Entre las posturas y comportamientos locomotores están el salto y agarre vertical,[N 6] propio de los lémures del bambú y de los indris;[38][62] el desplazamiento cuadrúpedo arbóreo lento (como los loris), que en su día utilizaba Mesopropithecus;[115] el desplazamiento cuadrúpedo arbóreo rápido, como en el caso de los lémures marrones y los lémures rufos;[38][116] la locomoción cuadrúpeda parcialmente terrestre, observada en el lémur de cola anillada; la locomoción cuadrúpeda fundamentalmente terrestre, desarrollada antaño por los lémures mono, como Hadropithecus;[38] y el desplazamiento en suspensión, similar al de los perezosos, que mostraban en su día los lémures perezosos, como Palaeopropithecus.[13][38] Existen informes que indican que el bandro (Hapalemur alaotrensis) es un buen nadador.[13] A veces estos sistemas de locomoción se agrupan en dos tipos, los de agarre y salto vertical y los cuadrúpedos arbóreos (y ocasionalmente terrestres).[70]
El poderoso salto de los índridos está bien documentado y es muy popular entre los ecoturistas que visitan Madagascar.[117] Utilizando sus largas y potentes patas se catapultan hacia arriba y caen al suelo o en un árbol cercano con una postura erguida y se agarran con fuerza al tronco con pies y manos.[15] Los indris pueden desplazarse con rapidez del tronco de un árbol a otro dando saltos de hasta diez metros,[15][66] una capacidad conocida como ricochetal leaping («salto de rebotes»).[79] El sifaca de Verreaux (Propithecus verreauxi) es capaz de realizar este tipo de saltos en los bosques espinosos del sur de Madagascar; se desconoce cómo puede evitar que sus manos queden ensartadas en los troncos cubiertos de espinas de grandes plantas como Alluaudia.[15] Cuando la separación entre los árboles es demasiado grande, el sifaca desciende a tierra y cruza distancias de más de cien metros mientras permanece erguido de pie y saltando de lado agitando de arriba abajo el pecho para ganar altura y manteniendo los brazos abiertos, presumiblemente para mantener el equilibrio.[15][66] Este movimiento se describe en ocasiones como un «salto de baile».[15]
Comunicación[editar]
Los lémures pueden comunicarse mediante sonidos y a través de la visión y el olfato. El lémur de cola anillada, por ejemplo, usa modelos complejos aunque muy estereotipados, como el marcado territorial y las vocalizaciones.[90] Las señales visuales son probablemente las que menos utilizan los lémures, ya que carecen de muchos de los músculos utilizados por otros primates para las expresiones faciales.[87] Debido a su pobre visión, las posturas de cuerpo entero son generalmente más identificables. Sin embargo, se ha comprobado que el lémur de cola anillada utiliza distintas expresiones faciales ante diversas situaciones, como una mirada fija amenazante, echar hacia atrás los labios en señal de sumisión, o girar hacia atrás las orejas y ensanchar las fosas nasales durante el marcado territorial.[90] También se ha visto a esta especie utilizando bostezos como señal de amenaza.[118][119] Su cola anillada también comunica distanciamiento, advierte a grupos vecinos y ayuda a localizar a miembros de su grupo.[90] Se sabe que los sifacas utilizan un gesto de juego con la boca abierta,[120] así como una mueca sumisa enseñando los dientes utilizada en interacciones agonísticas.[67]

El olfato es particularmente importante para los lémures,[13] a excepción del indri, que carece de la mayoría de las glándulas odoríferas comunes en los demás lémures, aparte de que su cerebro tiene una región olfatoria muy reducida.[79] A través del olfato pueden transmitir información sobre edad, sexo o estatus reproductivo, así como demarcar los límites de un territorio. Es el sentido más útil para que se comuniquen animales que raramente se encuentran unos con otros.[52] Los lémures pequeños y nocturnos marcan sus territorios con orina, mientras que las especies más grandes y diurnas usan glándulas odoríferas localizadas en varias partes de su anatomía. El lémur de cola anillada toma parte en «luchas apestosas» frotándose la cola con sus glándulas de olor de las muñecas, para después azotarla hacia los machos oponentes. Algunos lémures defecan en áreas específicas (rasgo conocido a veces como «comportamiento de letrina»); aunque muchos animales muestren este comportamiento, es un rasgo raro entre los primates. Esta conducta a la hora de defecar puede representar un marcado territorial y una ayuda en la señalización interespecies.[14]
Comparados con otros mamíferos, los primates en general son muy vocales, y los lémures no son una excepción.[14] Algunas especies de lémur tienen extensos repertorios vocales, como el lémur de cola anillada y los lémures rufos o de collar.[90][121] Algunas de las llamadas más comunes entre los lémures son las de alarma de depredadores. Los lémures no solo reaccionan ante llamadas de alarma de sus propias especies, sino también ante llamadas de alarma de otras especies o de aves no predadoras. El lémur de cola anillada y algunos otros lémures tienen distintas llamadas y reacciones ante tipos específicos de depredadores.[38] Con las llamadas de apareamiento, se ha comprobado que los lémures ratón que no pueden discernirse visualmente responden con más fuerza a las llamadas de su propia especie, especialmente cuando son las llamadas de otros lémures ratón que se encuentran habitualmente en su territorio.[122] Las llamadas de los lémures pueden ser muy fuertes y alcanzar grandes distancias. Los lémures rufos utilizan algunas llamadas que pueden oírse hasta a un kilómetro de distancia durante un día claro y en calma.[121] El lémur más ruidoso es el indri, cuyas llamadas pueden ser oídas hasta a dos kilómetros de distancia o más,[53][65] para así poder comunicar de una forma más eficaz los límites de sus territorios, que abarcan de 34 a 40 hectáreas de extensión.[79] Tanto los lémures rufos como los indris muestran un comportamiento de llamadas contagiosas, donde un individuo o grupo comienza una llamada fuerte y otros dentro del área se le unen.[65][121] El canto del indri puede durar desde 45 segundos hasta más de 3 minutos y tienden a coordinarse para formar un dúo estable comparable al de los gibones.[65][64]
La comunicación táctil se utiliza fundamentalmente en la forma de acicalado social, aunque los lémures de cola anillada también se reúnen en grupos para dormir juntos (en un orden determinado por el rango), extendiendo la mano y tocando a algunos miembros adyacentes del grupo, o dando manotazos a otros. En esta especie, tender la mano y tocar a otros individuos se ha visto como una posible conducta de sometimiento, realizada por animales más jóvenes o sumisos hacia miembros más viejos y más dominantes del grupo. Sin embargo, el acicalamiento social parece que se da con más frecuencia entre individuos de mayor posición, un rasgo compartido con otras especies de primates.[123] A diferencia de los primates antropoides, parece que el acicalado en los lémures es más íntimo y mutuo, a menudo directamente recíproco. Los antropoides, por otra parte, utilizan el acicalado social para manejar interacciones agonísticas.[124] Se sabe que el lémur de cola anillada es muy táctil, y le dedica entre un 5 y un 11 % de su tiempo al acicalado.[123]
| Muestra de vocalizaciones de lémures | |
|---|---|
Defensa contra depredadores[editar]
Todos los lémures experimentan algún tipo de presión por parte de depredadores.[125] Entre las medidas de defensa comunitaria contra la depredación se encuentra la utilización de llamadas de alarma y el ataque o el hostigamiento colectivo (mobbing) contra el agresor,[126] sobre todo entre lémures diurnos.[38] De acuerdo con un estudio cinemático realizado, las capacidades de salto de los lémures pueden haber evolucionado para la defensa frente a predadores, más que para desplazarse.[127] Los lémures nocturnos son difíciles de ver y rastrear por la noche, y dificulta todavía más su visibilidad que realicen la búsqueda de alimento en solitario. También intentan evitar a los depredadores utilizando posiciones encubiertas para dormir, como nidos, agujeros en los árboles o vegetación densa,[38] y cambiando entre múltiples localizaciones.[30] Incluso el letargo y los estados de hibernación entre los quirogaleidos puede que se deban en parte a que sufren niveles elevados de depredación.[125] Las crías se mantienen protegidas durante la búsqueda de alimento, bien dejándolas en el nido o escondiéndolas en un lugar oculto, donde la cría permanece inmóvil mientras los padres están ausentes.[38]
Los lémures diurnos son visibles durante el día, por lo que viven en grupos, donde un mayor número de ojos y oídos ayuda a descubrir a posibles depredadores. Los lémures diurnos utilizan y responden a las llamadas de alarma, e incluso a las de otras especies de lémur y las de aves no predadoras. El lémur de cola anillada tiene diferentes llamadas y reacciones ante distintos depredadores, como las aves de presa, mamíferos o serpientes.[38] Algunos, como el indri, usan una estrategia de cripsis para camuflarse; se les oye a menudo, pero son difíciles de ver entre los árboles debido a la luz moteada (mezcla de luz y sombra) de los bosques, lo que les ha dado una reputación de ser «fantasmas del bosque».[79]
Reproducción[editar]
Exceptuando al aye-aye y al bandro, los lémures se reproducen estacionalmente,[13][42] con temporadas de apareamiento y nacimiento muy cortas debido a la influencia de la disponibilidad muy estacional de recursos en su entorno. Las épocas de celo por lo general duran menos de tres semanas cada año,[38] y la apertura vaginal de las hembras solo se produce durante unos días u horas de su período más receptivo del estro.[86] Estos estrechos márgenes para la reproducción y la disponibilidad de recursos parecen estar relacionados con sus cortos períodos de gestación, rápida maduración y bajo metabolismo basal, así como un elevado coste energético para las hembras a la hora de reproducirse. También puede estar relacionado con la tasa de mortalidad relativamente alta que se da entre las hembras adultas y una mayor proporción de machos adultos en algunas poblaciones de lémures (ambos rasgos son raros entre los primates). Tanto en el caso del aye-aye como en el del bandro, el nacimiento (parto) se produce a lo largo de un período de seis meses.[13]
Acoplan sus temporadas de apareamiento y nacimiento de modo que los períodos de destete estén sincronizados para coincidir con el momento de mayor disponibilidad de comida.[86][97] El destete se produce un poco antes o después de la erupción de sus primeras muelas permanentes.[32] Los lémures ratón son capaces de ajustar su ciclo de cría completo a la estación húmeda, mientras que los lémures más grandes, como los sifacas, deben lactar durante dos meses durante la temporada seca.[97] Se ha comprobado que la supervivencia infantil en algunas especies, como el sifaca de Milne-Edwards, se ve afectada directamente tanto por las condiciones ambientales como por el rango, la edad y la salud de la madre. La temporada de cría también está afectada por la situación geográfica; por ejemplo, los lémures ratón paren entre septiembre y octubre en su hábitat natal en el hemisferio sur, pero los ejemplares en cautividad en el hemisferio norte lo hacen de mayo a junio.[86]
Los factores odoríferos son de gran importancia en la reproducción de los lémures. La actividad de marcado territorial se intensifica durante la época de celo, y las feromonas pueden coordinar el momento reproductivo para las hembras que entran en el estro.[86] El apareamiento puede ser monógamo o promiscuo tanto en el caso de los machos como de las hembras, y el acoplamiento puede incluir a individuos ajenos al grupo.[13][38] Entre los lémures monógamos se encuentra el lémur de vientre rojo (Eulemur rubriventer) y el lémur mangosta (Eulemur mongoz), aunque se ha visto a este último apareándose fuera de su vínculo de pareja.[38] La monogamia es más común entre las especies nocturnas, aunque se dan algunas muestras de competiciones de lucha, supresión sexual de subordinados o competencia entre machos que evitan enfrentamientos directos.[32] En el caso de los lémures ratón, los machos utilizan la esfragis copulatoria, un aumento del desarrollo de los testículos durante la época de celo, y también desarrollan un incremento en el dimorfismo de tamaño.[128]

El período de gestación varía según la especie, y va desde las nueve semanas en los lémures ratón y entre nueve y diez de los lémures enanos, hasta las dieciocho o veinticuatro semanas en otros lémures.[86] Las especies más pequeñas y nocturnas, como las del género Mirza, los lémures ratón y los lémures enanos, por lo general dan a luz a más de una cría, mientras que los lémures más grandes, nocturnos, como los lémures de orejas ahorquilladas, los lémures saltadores o el aye-aye por lo general tienen un descendiente.[28] Los lémures enanos y los lémures ratón tienen hasta cuatro descendientes, pero en ambas especies la media es de solo dos. Los lémures rufos son los únicos lémures grandes y diurnos que paren de forma habitual dos o tres crías; todas las demás especies tienen partos simples. Los partos múltiples en los lémures son normalmente dicigóticos, y suelen ocurrir en uno de cada cinco o seis nacimientos en especies como el lémur de cola anillada o en algunos del género Eulemur.[86]
Después de dar a luz, mientras buscan alimento suelen llevar sujetas a ellos a las crías, o bien las esconden. Cuando cargan con ellas, las crías se agarran a la piel de la madre o son llevadas con la boca cogidas por el cuello. En algunas especies, como los lémures del bambú, los pequeños son llevados con la boca hasta que son capaces de agarrarse a la piel de su madre.[129] Entre las especies que no cargan con su progenie se incluyen las especies nocturnas (como los lémures ratón, los lémures saltadores y los lémures enanos), los lémures del bambú y los lémures rufos.[28][129] En el caso de los lémures rufos, los pequeños son altriciales y las madres construyen nidos para ellos, al igual que las especies de lémur más pequeñas y nocturnas.[13] Los avahi o lémures lanudos son una excepción entre los lémures nocturnos porque viven en grupos familiares cohesionados y llevan a su única cría con ellos en lugar de dejarla en el área de cría.[62][63] Se ha descrito la crianza o cuidado aloparental (asistencia por parte de individuos distintos de los progenitores en el cuidado de la prole, bien de forma individual o por parte del grupo) en todas las familias de lémures excepto en los lémures saltadores y en el aye-aye. También se sabe que el aloamamantamiento (la cesión de leche a crías diferentes de la propia) se da en varios grupos de lémures.[130] Se ha comprobado que incluso los machos pueden cuidar a las crías en algunas especies como el lémur de vientre rojo, el lémur mangosta,[72] el lémur mano gris (Hapalemur griseus), el sifaca sedoso (Propithecus candidus),[130] el lémur enano de cola gruesa (Cheirogaleus medius)[131] o los lémures rufos.[132]
Otra de las características que diferencia a la mayor parte de los lémures de los primates antropoides es su longevidad y su alta tasa de mortalidad infantil.[97] Muchos lémures, incluido el lémur de cola anillada, se han adaptado a un ambiente altamente estacional, que ha afectado a su índice de natalidad, madurez y tasa de apareamiento (selección r); esto les ayuda a recuperarse rápidamente de una caída demográfica.[90] En cautiverio pueden vivir el doble de lo que lo hacen en la naturaleza, al beneficiarse de una nutrición consistente que satisface sus exigencias alimenticias, de los progresos médicos y de la mejora en la compresión de sus exigencias de alojamiento. En 1960 se creía que los lémures podrían vivir entre 23 y 25 años, pero actualmente se sabe que las especies de mayor tamaño pueden vivir durante más de 30 años sin mostrar señales de envejecimiento (senescencia) y manteniendo su capacidad para reproducirse.[86]
Habilidades cognoscitivas y uso de herramientas[editar]
Tradicionalmente se ha considerado a los lémures menos inteligentes que los primates antropoides,[133] y se ha descrito a monos y hominoides como más astutos, hábiles y embaucadores.[15] Muchas especies de lémur, como los sifacas y el lémur de cola anillada, han dado peores resultados en pruebas diseñadas para monos, mientras que se desempeñaban igual que ellos en otras.[15][109] Estas comparaciones pueden no ser justas ya que los lémures prefieren manipular los objetos con la boca (más que con las manos) y solo se interesan por objetos cuando están en cautividad.[109] De hecho, varios estudios han demostrado que los lémures poseen el mismo nivel de inteligencia técnica que el resto de los primates.[134] No se ha visto a los lémures utilizando herramientas en la naturaleza, aunque en cautividad el lémur pardo y el lémur de cola anillada han demostrado ser capaces de entender y utilizar herramientas.[14]
El cerebro de algunas especies tiene un tamaño relativamente grande. El extinto Hadropithecus tenía el tamaño corporal de un babuino macho grande y poseía un cerebro de un tamaño similar, lo que lo convierte en el cerebro de mayor tamaño con relación a la masa corporal de todos los prosimios.[135] El aye-aye también tiene una proporción cerebro-masa corporal grande, lo que puede indicar un nivel más alto de inteligencia.[42] Sin embargo, a pesar de tener incorporado en su cuerpo un instrumento en la forma de su largo y delgado dedo medio, que utiliza para capturar larvas de insectos, el aye-aye ha ofrecido pobres resultados en las pruebas de utilización de herramientas.[14]
Ecología[editar]
- Ver secciones: dieta, metabolismo, patrones de actividad y locomoción
Madagascar no solo cuenta con dos zonas climáticas radicalmente diferentes, las selvas tropicales del este y las regiones secas del oeste,[13] sino que además sufre desde profundas sequías hasta inundaciones provocadas por ciclones.[136] Estos desafíos climáticos y geográficos, junto con unos suelos pobres, de baja productividad vegetal, una gran variedad y complejidad de sus ecosistemas y una carencia de árboles que den fruta con regularidad (como las higueras), ha llevado a los lémures a evolucionar hacia una enorme diversidad morfológica y de comportamiento.[12][13][32][97] Su supervivencia ha requerido la capacidad de soportar los extremos constantes, en lugar de una estabilidad o regularidad anual.[136]
Los lémures ocupan actualmente, o lo hicieron con anterioridad, los nichos ecológicos generalmente ocupados por monos, ardillas, pájaros carpinteros y ungulados de pasto.[15] Dada su diversidad de adaptaciones a nichos ecológicos específicos, la selección de hábitat entre las familias y algunos géneros de lémures a menudo es muy distinta, minimizando la competencia.[13] Hasta cinco especies de lémures nocturnos de los bosques más estacionales del oeste pueden coexistir durante la estación húmeda gracias a la gran abundancia de comida. Sin embargo, para soportar la extrema estación seca de la isla, tres de estas cinco especies utilizan distintos modelos alimenticios (con sus rasgos fisiológicos subyacentes) para poder coexistir: los lémures de orejas ahorquilladas se alimentan de la goma del árbol, los lémures saltadores de las hojas y los del género Mirza a veces se alimentan de secreciones de insectos. Las otras dos especies, el lémur naranja y el lémur enano de cola gruesa, evitan la competencia reduciendo la actividad; el lémur naranja se vale de temporadas de letargo, mientras que el lémur enano de cola gruesa hiberna completamente.[28] Del mismo modo, en la costa oriental géneros enteros se centran en una comida específica para evitar una excesiva superposición de nichos; los lémures marrones y los lémures rufos son frugívoros, los índridos son folívoros y los lémures del bambú se especializan en el bambú y otras hierbas. Una vez más, las diferencias alimenticias estacionales, así como las sutiles diferencias en las preferencias de sustrato, los estratos forestales utilizados, el ciclo de actividad y la organización social permiten la coexistencia de distintas especies de lémures, aunque en este caso las especies estén más estrechamente relacionadas y tengan nichos similares.[13] Un buen ejemplo es la división de recursos entre tres especies de lémures del bambú que viven muy próximas en pequeñas áreas arboladas: el lémur dorado, el lémur grande del bambú y el lémur mano gris; cada uno utiliza especies diferentes de bambú, partes diferentes de la planta o capas diferentes del bosque.[15][57] El contenido de nutrientes y toxinas (como el cianuro) ayudan a regular la selección de comida,[13] aunque se sabe que las preferencias estacionales de alimento también desempeñan un papel en la selección.[57]
Tienen regímenes alimenticios variados según las especies, y los hay nectarívoros, folívoros, frugívoros u omnívoros, con especies que son muy adaptables mientras que otras tienen una dieta especializada, como exudaciones de plantas o bambú.[73] En algunos casos, los patrones alimenticios de los lémures benefician la vida vegetal local; cuando se alimentan de néctar pueden actuar como polinizadores, mientras que las partes funcionales de la flor no resultan dañadas.[96] De hecho, varias plantas con flor malgaches no relacionadas muestran rasgos de polinización específicos del lémur, y diversos estudios indican que algunas especies diurnas, como el lémur de vientre rojo y los lémures rufos, actúan como polinizadores primarios.[13] Dos ejemplos de especies de planta que se valen de los lémures para la polinización son la palma del viajero (Ravenala madagascariensis)[60] y una especie de liana parecida a una legumbre, Strongylodon cravieniae.[13] La dispersión de semillas es otro de los servicios facilitados por los lémures; después de pasar por el vientre del lémur, las semillas de trepadoras y árboles muestran una mortalidad inferior y germinan más rápido.[97] El comportamiento de defecar en algunas áreas específicas que muestran algunos lémures puede ayudar a mejorar la calidad del suelo y facilitar la dispersión de semillas.[14] Debido a su importancia para el mantenimiento de un bosque sano, los lémures frugívoros pueden calificarse como mutualistas clave.[97]
Todos los lémures, y en particular las especies de menor tamaño, son víctimas de la depredación,[28][125] y constituyen una presa importante para varios predadores.[128] Los humanos son los predadores más significativos para los lémures diurnos, a pesar de que algunos tabús prohíben su caza y alimentarse de ciertas especies de lémur.[13] Entre sus depredadores se encuentran eupléridos nativos como la civeta de Madagascar (Fossa fossana) y el fosa (Cryptoprocta ferox), gatos salvajes, perros domésticos, serpientes, aves de presa diurnas, rapaces nocturnas y cocodrilos. Águilas gigantes extinguidas, como el águila coronada de Madagascar (Stephanoaetus mahery), y una o dos especies del género Aquila, así como el fosa gigante (Cryptoprocta spelea), antaño también se alimentaron de lémures, quizás incluso de los recientemente extintos lémures gigantes o sus crías subadultas.[28][125] La existencia de estos gigantes extintos sugiere que las interacciones entre presa y predador que implicaban a los lémures fueron más complejas de lo que son en la actualidad.[13] Hoy en día, el tamaño de los depredadores solo limita a los búhos a los lémures más pequeños, por lo general de unos 100 g o menos, mientras que los lémures de mayor tamaño caen víctimas de las aves de presa diurnas más grandes, como el aguilucho malgache (Polyboroides radiatus) y el buitre de Madagascar (Buteo brachypterus).[125]
Investigación[editar]
Las semejanzas que los lémures comparten con los primates antropoides, como la dieta y la organización social, junto con sus propios rasgos distintivos, ha hecho que los lémures hayan sido los más estudiados de todos los grupos de mamíferos de Madagascar.[13][69] Las investigaciones a menudo se centran en la relación entre su ecología y organización social, pero también en su comportamiento y morfofisiología (estudio de la anatomía con relación a su función).[13] Los estudios sobre las características de su ciclo vital, comportamiento y ecología ayudan a la compresión de la evolución de los primates, ya que se cree que comparten semejanzas con los primates ancestrales. Por otra parte, por su cercanía filogenética al hombre, al igual que otros primates los lémures son sujetos de experimentación y estudio de enfermedades de gran incidencia y mortalidad entre los humanos como el mal de Alzheimer[137][138] o el sida.[139]
Han sido el eje central de series monográficas, planes de acción, guías de campo y obras clásicas en etología.[69] Sin embargo, pocas especies han sido estudiadas a fondo hasta la fecha, y la mayor parte de la investigación ha sido preliminar y se ha restringido a una localización única.[13] Solo recientemente se han publicado numerosos artículos científicos que explican aspectos básicos de comportamiento y ecología de especies poco conocidas. Los estudios de campo han dado una nueva percepción de estos primates en campos como la dinámica de poblaciones y ecología evolutiva de la mayor parte de sus géneros y de muchas especies.[69] Las investigaciones a largo plazo centradas en individuos identificados están en su infancia y solo han comenzado para unas pocas poblaciones. Sin embargo, las oportunidades de aprendizaje disminuyen debido a la destrucción de su hábitat y otros factores que amenazan la existencia de las poblaciones de lémures a lo largo de la isla.[13]

Los lémures son mencionados por los marinos en los cuadernos de bitácora de sus viajes ya en 1608 y en 1658, y al menos siete especies fueron descritas con detalle por el gobernador francés de Madagascar Étienne de Flacourt, que también puede que haya sido el único occidental que vio e hizo una crónica sobre la existencia de un lémur gigante (actualmente extinguido) al que llamó tretretretre.[140][N 7] Aproximadamente en 1703 comerciantes y marinos comenzaron a llevar lémures a Europa, y en ese tiempo James Petiver, un boticario de Londres, describió e ilustró al lémur mangosta. A partir de 1751 el naturalista londinense George Edwards comenzó a describir e ilustrar diversas especies de lémur, algunas de las cuales fueron incluidas por Linneo en varias ediciones de su Systema naturae. En los años 1760 y 1770, los naturalistas franceses Georges Louis Leclerc y Louis Jean Marie Daubenton comenzaron a describir la anatomía de varias especies de lémur. El primer naturalista de campo en confeccionar informes sobre los lémures fue Philibert Commerson en 1771, aunque fue Pierre Sonnerat quien registró una mayor variedad de especies durante sus viajes.[136][142]
Durante el siglo XIX hubo una explosión de nuevos nombres y descripciones de lémures, que posteriormente llevó décadas clasificar. Durante este tiempo, los colectores profesionales recogieron especímenes para museos, menagerías o «casas de fieras» y cuartos de maravillas. Algunos de los principales colectores fueron Johann Maria Hildebrandt y Charles Immanuel Forsyth Major. A partir de estas colecciones, así como de las crecientes observaciones de lémures en sus hábitats naturales, sistemáticos de museos como Albert Günther y John Edward Gray continuaron aportando nuevos nombres para las especies de lémur. Pero quizás las contribuciones más notables de este siglo fueron los trabajos de Alfred Grandidier, un naturalista y explorador que se dedicó al estudio de la historia natural de Madagascar y de la población local. Con la ayuda de Alphonse Milne-Edwards, la mayor parte de los lémures diurnos fueron ilustrados en esos tiempos. Sin embargo, la nomenclatura taxonómica de los lémures alcanzó su forma moderna en los años 1920 y 1930, y fue estandarizada por el zoólogo germano Ernst Schwarz en 1931.[136][142]
Aunque su taxonomía había experimentado un importante desarrollo, no fue sino hasta los años 1950 y 1960 cuando el estudio in situ de su comportamiento y ecología comenzó a florecer. Jean-Jacques Petter y Arlette Petter-Rousseaux recorrieron Madagascar en 1956 y 1957, haciendo un reconocimiento de un gran número de especies de lémur y haciendo importantes observaciones sobre sus grupos sociales y su reproducción. En 1960, año de la independencia de Madagascar, David Attenborough presentó a los lémures a Occidente a través de una película comercial. Bajo la dirección de John Buettner-Janusch, fundador del Duke Lemur Center en 1966, Alison Jolly viajó a Madagascar en 1962 para estudiar la dieta y el comportamiento social del lémur de cola anillada y el sifaca de Verreaux en la Reserva Privada Berenty. Jolly y los Petter sentaron las bases de una nueva era de interés hacia la ecología y el comportamiento de los lémures, y pronto fueron secundados por antropólogos como Alison Richard, Robert Sussman, Ian Tattersall y muchos otros. Tras la pausa debida a la confusión política de mediados de los años 1970 y la revolución de Madagascar, los estudios de campo continuaron en los años 1980, gracias en parte a la renovada participación del Duke Lemur Center bajo la dirección de Elwyn Simons y los esfuerzos conservacionistas de Patricia Wright.[13][136][142] En las décadas posteriores se ha dado un gran salto en el estudio de los lémures y se ha descubierto un gran número de nuevas especies.[6]
Los estudios fuera de Madagascar también resultan atractivos para los investigadores que buscan respuesta a cuestiones que son difíciles de poner a prueba en la naturaleza. Por ejemplo, los estudios para la secuenciación completa del genoma del lémur naranja ayudarán a los investigadores a entender qué rasgos genéticos diferencian a los primates de otros mamíferos y finalmente ayudarán a comprender qué factores genómicos diferencian a los humanos de otros primates.[33] Una de las principales instalaciones de investigación de lémures es el Duke Lemur Center (DLC), en Durham, Carolina del Norte. Este centro, dependiente de la Universidad Duke, cuenta con la población de lémures en cautividad más numerosa existente hoy en día fuera de Madagascar, para desarrollar una investigación no invasiva y para la reproducción en cautividad. [143] En el centro se han llevado a cabo importantes proyectos de investigación, como estudios de sus vocalizaciones,[144] comportamiento locomotor,[145] la cinemática del bipedalismo,[146] los efectos de su complejidad social sobre el razonamiento transitivo,[N 8][147] y estudios sobre cognición que implican la capacidad de un lémur de organizar y recuperar secuencias de la memoria.[148] Otras instalaciones, como la Lemur Conservation Foundation, localizada cerca de la ciudad de Myakka, Florida, también han desarrollado diversos proyectos de investigación, como un estudio sobre la capacidad de los lémures de seleccionar herramientas basándose preferentemente en sus cualidades funcionales.[149]
Estado de conservación[editar]
Los lémures están amenazados por un gran número de problemas ambientales, como la deforestación, la caza para el consumo de su carne, la captura de especímenes vivos para el comercio de mascotas exóticas y el cambio climático.[150][97] Todas las especies de lémur están incluidas en el Apéndice I de la CITES, que prohíbe el comercio de especímenes o de sus partes, excepto cuando van destinados a investigaciones científicas.[1] Desde 2005, la Unión Internacional para la Conservación de la Naturaleza (UICN) incluyó en su Lista Roja de Especies Amenazadas al 16 % de los lémures como especies en peligro crítico, al 23 % en peligro, al 25 % como vulnerable, del 28 % consideró que había datos insuficientes y solo el 8 % tenía la consideración de especie bajo preocupación menor.[143] Durante los siguientes cinco años, se identificaron al menos veintiocho nuevas especies, pero todavía no se ha establecido el estatus de conservación de ninguna de ellas.[45] Muchas probablemente serán consideradas como amenazadas, ya que las nuevas especies descritas recientemente están por lo general concentradas en pequeñas regiones.[151] Considerando el progreso continuo de la destrucción de su hábitat, algunas especies todavía no descubiertas podrían extinguirse antes de ser identificadas.[69] Desde la llegada de los humanos a la isla hace aproximadamente 2000 años, todos los vertebrados endémicos de Madagascar de más de diez kilogramos de peso han desaparecido,[37] incluidas diecisiete especies, ocho géneros y tres familias de lémures.[36][39] La Comisión de Supervivencia de Especies de la UICN (IUCN/SSC, en inglés), la Sociedad Primatológica Internacional (IPS, en inglés) y Conservation International (CI) han incluido al menos a cinco lémures en su publicación bienal Los 25 primates en mayor peligro del mundo; el informe correspondiente a los años 2012-2014 incluye a seis: Eulemur flavifrons, Lepilemur septentrionalis, Propithecus candidus, Microcebus berthae, Indri indri y Varecia rubra.[152] En 2012, una evaluación hecha por el Grupo de Expertos en Primates de la Unión Internacional para la Conservación de la Naturaleza (UICN) concluyó que el 91 % de las 103 especies de lémures conocidas por entonces estaban amenazadas, lo que los convierte en el grupo de mámiferos en mayor peligro de extinción.[153][154] En 2013, la UICN reiteró su preocupación y afirmó que el 90 % de las especies de lémures podrían extinguirse dentro de los próximos 20 a 25 años, a menos que se implemente en plan de conservación de tres años para ayudar a las comunidades locales, el cual costaría siete millones de dólares estadounidenses.[155][156]
Madagascar es uno de los países más pobres del mundo,[157][158] con una elevada tasa de crecimiento poblacional del 2,5 % anual y con casi el 70 % de su población viviendo en la pobreza.[38][157] El país también soporta un elevado nivel de deuda externa y cuenta con recursos limitados.[158] Estas cuestiones socioeconómicas hacen que resulte complicado aportar recursos dedicados a la conservación de la naturaleza, aunque la isla de Madagascar ha sido declarada por la Comisión de Supervivencia de Especies de la UICN como una región de primates crítica durante más de veinte años.[151] Debido a su relativamente pequeña superficie terrestre (587 045 km²) comparada con otras regiones de biodiversidad prioritaria, y su elevado nivel de endemismo, el país está considerado como uno de los denominados puntos calientes de biodiversidad (biodiversity hotspot, en inglés) más importantes del mundo, con la conservación de los lémures calificada como de alta prioridad.[143][151] A pesar del énfasis en los esfuerzos orientados hacia la conservación, no hay ningún indicio que muestre que las extinciones que comenzaron con la llegada de los humanos hayan llegado a su fin.[37]
Amenazas en la naturaleza[editar]
La mayor amenaza a la que se enfrentan las poblaciones de lémures es la destrucción y degradación de su hábitat.[38][1] A menudo la deforestación es provocada por las necesidades de subsistencia local, como la agricultura de rozas y quema (conocida como tavy en malgache), la creación de zonas de pasto para el ganado por medio de la incineración, el acopio legal e ilegal de madera para leña o producción de carbón vegetal, la minería comercial y la tala ilegal de maderas nobles para mercados exteriores.[38][150] Después de siglos de uso no sostenible, así como la rápida y progresiva intensificación de la destrucción forestal desde 1950,[143] menos de 60 000 km² (el 10 % de la superficie terrestre) de Madagascar permanecen arbolados. Solo 17 000 km² del área terrestre (el 3 %) de la isla están bajo protección y, debido a unas condiciones económicas extremas e inestabilidad política, la mayor parte de las áreas protegidas son administradas y defendidas de forma ineficaz.[150][151] Algunas áreas protegidas fueron dejadas de lado porque estaban salvaguardadas de forma natural por su situación aislada y remota, y a menudo escarpada; otras áreas, como los bosques secos y los bosques espinosos del oeste y sur de la isla, reciben poca protección y están en serio peligro de ser destruidas.[38]
Algunas especies pueden estar en riesgo de extinción incluso sin una deforestación completa, como los lémures rufos, que son muy sensibles a la perturbación de su hábitat.[69] Si se eliminan los grandes árboles frutales, el bosque puede mantener a menos individuos de una especie y su éxito reproductivo puede verse afectado durante años.[97] Las poblaciones pequeñas pueden ser capaces de persistir en fragmentos forestales aislados durante 20 o 40 años gracias a sus prolongados periodos generacionales, pero a largo plazo estas poblaciones pueden no ser viables.[159] Las poblaciones pequeñas y aisladas también se arriesgan a su extinción a causa de catástrofes o epidemias (epizootia). Dos enfermedades que son letales para los lémures y que podrían afectar con severidad a poblaciones aisladas son la toxoplasmosis, propagada por gatos salvajes, y el virus del herpes simple, transmitido por los humanos.[160]

El cambio climático y las catástrofes naturales relacionadas con el clima también amenazan su supervivencia. Durante los últimos 1000 años, las regiones occidentales y montañosas se han vuelto considerablemente más secas, pero en las últimas décadas las sequías severas se han tornado mucho más frecuentes. Hay indicaciones de que la deforestación y la fragmentación forestal aceleran esta desecación gradual.[97] Los efectos de la sequía se aprecian incluso en las selvas tropicales; como consecuencia de la disminución de las precipitaciones anuales, los árboles más grandes que forman la canopea superior de las zonas boscosas sufren un aumento en su mortalidad, que no prosperen sus frutos y una disminución en la producción de nuevas hojas, las que prefieren los lémures folívoros. Los ciclones pueden deshojar algunas áreas, derribar árboles de la canopea y provocar desprendimientos de tierra e inundaciones. Esto puede dejar a algunas poblaciones de lémures sin fruta u hojas hasta la primavera siguiente, obligándoles a subsistir a base de alimentos de crisis, como las epifitas.[161]
Los lémures son cazados como comida por la población nativa, tanto como caza de subsistencia como con fines comerciales, para abastecer de carne de lujo a los mercados de las ciudades más grandes.[6][150][162] La mayor parte de la población local del entorno rural no entiende el significado o las connotaciones de «especie en peligro de extinción», ni que la caza de lémures es ilegal o que los lémures solo pueden encontrarse en Madagascar. [141] Muchos malgaches consideran fady comerlos o cazarlos, pero este hecho no impide su caza en muchas regiones.[13] Aunque la caza siempre ha sido una amenaza para las poblaciones de lémures en el pasado, recientemente se ha convertido en una amenaza mucho más seria debido al deterioro de las condiciones socioeconómicas.[150] Las privaciones económicas han hecho que la población se traslade a lo largo del país en busca de empleo, provocando una pérdida o deterioro de las tradiciones locales;[69][1][141] la sequía y el hambre también pueden causar una pérdida de eficacia en los fady que protegen a los lémures.[69] Las especies más grandes, como los sifacas y los lémures rufos, son el objetivo habitual, pero las especies más pequeñas también son cazadas o atrapadas casualmente en trampas colocadas para presas de mayor tamaño.[6][1] Partidas de caza de cazadores con experiencia, organizados y que usan armas de fuego, hondas y cerbatanas pueden matar no menos de entre ocho a veinte lémures en una jornada. Partidas de caza organizadas y tramperos pueden verse tanto en zonas no protegidas como en rincones remotos de áreas protegidas.[69] Los parques nacionales y otras áreas protegidas no cuentan con una protección suficiente por parte de las agencias encargadas de velar por el cumplimiento de la ley;[141] a menudo hay demasiado pocos guardias para cubrir grandes áreas, y a veces el terreno del parque es demasiado accidentado para poder controlarlo con regularidad.[163]
Algunos lémures, como el lémur coronado y otras especies que han sido mantenidas con éxito en cautividad, son capturados en ocasiones como mascotas exóticas por la población de Madagascar.[53][143] Los lémures del bambú también son utilizados como animales domésticos,[143] aunque solo pueden sobrevivir en esa situación durante unos dos meses.[164] La captura de ejemplares vivos para el comercio de mascotas exóticas con países más ricos no se considera normalmente una amenaza debido a las estrictas regulaciones que controlan su exportación.[143][1]
Esfuerzos para su conservación[editar]

Los lémures han llamado en gran medida la atención hacia Madagascar y hacia sus especies en peligro. Por ello, estos primates actúan como especies estandarte,[N 9][69][143] y de forma más notable lo hace el lémur de cola anillada, que se considera un icono del país.[60] La presencia de lémures en los parques nacionales atrae al turismo ecológico,[143] que ayuda especialmente a comunidades rurales que viven en los alrededores de los parques nacionales, ya que les ofrece oportunidades de empleo y económicas, pues la comunidad recibe la mitad de las cuotas del parque. En el caso del parque nacional de Ranomafana, las oportunidades de trabajo y otros ingresos generados por la investigación a largo plazo pueden rivalizar con las del ecoturismo.[165]
Desde el año 1927 el gobierno de Madagascar ha declarado a todos los lémures como «protegidos»,[68] estableciendo áreas bajo protección clasificadas actualmente bajo tres categorías: Parques Nacionales (Parcs Nationaux), Reservas Naturales Integrales (Réserves Naturelles Intégrales) y Reservas Especiales (Réserves Spéciales). A principios de 2011 había veintiún parques nacionales (19 terrestres y 2 marítimos), cinco reservas naturales integrales y veintiún reservas especiales,[166] así como algunas otras pequeñas reservas privadas, como la Reserva Berenty y la Reserva Privada de Sainte Luce, ambas cerca de Tôlanaro (antes Fort-Dauphin).[143] Todas las áreas protegidas, excluyendo las reservas privadas, ocupan aproximadamente el 3 % de la superficie terrestre de Madagascar y son administradas por el organismo Parques Nacionales de Madagascar (Madagascar National Parks), antes conocido como Association Nationale pour la Gestion des Aires Protégées (ANGAP), así como otras organizaciones no gubernamentales (ONG), como Conservation International (CI), Wildlife Conservation Society (WCS) y el Fondo Mundial para la Naturaleza (WWF).[143][151] La mayor parte de las especies de lémures están cubiertas por esta red de áreas protegidas, y algunas de ellas pueden encontrarse en varios parques o reservas.[151]
La Madagascar Fauna Group (MFG), una asociación formada por cerca de cuarenta zoológicos y organizaciones relacionadas, es otra de las entidades que vela por la conservación de la fauna malgache. Esta organización internacional no gubernamental colabora en el mantenimiento del Parque Zoológico de Ivoloina en Madagascar, ayuda a proteger la Reserva natural integral de Betampona y otras áreas protegidas, y promueve la investigación de campo, desarrollando programas de actuación, planes de conservación y programas educativos en los zoos.[167] Uno de sus principales proyectos supuso la liberación de lémures rufo blancos y negros cautivos, un proyecto diseñado para ayudar a reabastecer la menguante población de la Reserva de Betampona.[167][168]

Los corredores ecológicos son necesarios para unir estas áreas protegidas de modo que las poblaciones pequeñas no se vean aisladas.[151] En septiembre de 2003 en Durban, Sudáfrica, el ex presidente de Madagascar Marc Ravalomanana prometió triplicar el tamaño de las áreas protegidas de la isla en cinco años.[150] Esta declaración se conoce como la «Visión de Durban» (Durban Vision).[143] En el año 1990 las pluviselvas de Atsinanana, que incluyen seis parques nacionales localizados en la costa oriental de la isla, y en junio de 2007 la Reserva natural integral de Tsingy de Bemaraha, que comprende una parte importante de las selvas tropicales del este de Madagascar, fueron catalogadas como un bien natural Patrimonio de la Humanidad de la Unesco.[33][169]
La condonación de deuda exterior puede ayudar a Madagascar a proteger su biodiversidad.[158] Con la crisis política de 2009, la tala ilegal ha proliferado y amenaza las selvas tropicales del nordeste, poniendo en peligro a los lémures que las habitan y también al turismo ecológico del que las comunidades locales dependen.[157]
Se mantienen algunas poblaciones en cautividad en muchos zoológicos fuera de Madagascar, aunque la diversidad de especies es limitada. Los sifacas (género Propithecus), por ejemplo, no sobreviven bien en cautiverio, por lo que pocas instalaciones cuentan con ejemplares de este género.[13][65] La población en cautividad más numerosa se encuentra en el Duke Lemur Center, cuya misión incluye la investigación no invasiva, la conservación y reproducción en cautividad y la educación orientada hacia el público en general.[143]
Referencias culturales[editar]
En la cultura malgache, los lémures, y los animales en general, tienen alma (ambiroa), y su alma puede buscar venganza si se burlan de ella mientras el animal está vivo o si lo matan de una forma cruel. Por ello los lémures, como muchos otros elementos de la vida cotidiana, han sido fuente de tabúes, conocidos localmente como fady, que se basan en historias que giran alrededor de cuatro principios básicos: un pueblo o una región pueden creer que un cierto tipo de lémur puede ser el antepasado del clan, también pueden creer que el espíritu de un lémur puede buscar venganza, igualmente, que el animal pueda resultar un benefactor, o bien se cree que los lémures transmiten sus cualidades, buenas o malas, a los bebés humanos.[170] En general, los fady se extienden más allá de un sentido de lo prohibido, pero pueden abarcar acontecimientos que traen la mala suerte.[82]

Los tabúes puede ayudar a proteger a los lémures y sus bosques bajo situaciones socioeconómicas estables, pero también pueden conducir a su discriminación y persecución si se cree que un lémur trae mala fortuna, por ejemplo, si anda por la ciudad.[69][170] Por otra parte, los fady no protegen a todos los lémures por igual; así, por ejemplo, aunque cazar y comer ciertas especies pueda ser tabú, otras especies no comparten la misma protección y se convierten por tanto en objetivo de los cazadores.[170][13] Los tabúes pueden variar de un pueblo a otro dentro de la misma región.[68] Si la gente se traslada a un nuevo pueblo o región, su fady puede no aplicarse a las especies de lémur presentes en la localidad, poniéndolos en disposición para su consumo. Las restricciones de los tabúes respecto a la carne de lémur pueden relajarse en tiempos de hambre y sequía.[69]
El aye-aye es considerado de forma generalizada como un animal no favorable a lo largo de todo Madagascar, aunque las historias varían de pueblo en pueblo y de región en región.[82] Si la gente ve un aye-aye, puede matarlo y colgar su cadáver en un poste cerca de un camino fuera de la población (y así ser otros los que puedan llevarse la mala fortuna) o quemar su pueblo y mudarse.[68][54] Entre las supersticiones relativas al aye-aye está la creencia de que matan y se comen a los pollos o incluso a personas, que matan seres humanos mientras duermen,[69] que encarnan espíritus de ancestros,[68] o que advierten de enfermedades, muerte o mala suerte en la familia.[53][54] En torno a 1970, la población del distrito de Marolambo en la provincia de Toamasina temía a los aye-aye porque creían que tenía poderes sobrenaturales, por lo que no permitían a nadie burlarse, matar o comerse a estos animales.[170]
También hay un gran número de tabús relacionados con el indri y los sifacas. A menudo son protegidos de la caza y consumo a causa de su parecido con los humanos y sus antepasados, sobre todo debido a su gran talla y su postura erguida u ortógrada; el parecido es aún más notable en el caso del indri, que carece de la larga cola de la mayor parte de los lémures actuales.[65][83] Conocido localmente como babakoto («antepasado del hombre»), el indri es visto a veces como el progenitor de la familia o clan. También hay historias de un indri que ayudó a un humano a bajar de un árbol, y a menudo se les ve como benefactores.[170] Otro fady se refiere a la creencia de que una esposa tendrá niños feos si su marido mata a un indri lanudo, o que si una mujer embarazada se come a un lémur enano, su bebé adquirirá sus redondos y hermosos ojos.[170]
Los lémures también se han hecho populares en la cultura occidental en años recientes. La película de animación del año 2005 Madagascar fue vista por aproximadamente 100 millones de personas en los cines y 200-300 millones de personas en DVD en todo el mundo,[61] Antes de esta película, Zoboomafoo, una serie infantil de televisión de la PBS estadounidense emitida entre 1999 y 2001,[171] ayudó a popularizar a los sifacas mostrando a un sifaca de Coquerel del Duke Lemur Center.[172] Una serie de veinte episodios titulada Lemur Street se emitió en 2008 en el canal Animal Planet; esta serie combinó el típico documental sobre animales con la narración dramática para contar la historia de dos grupos de lémures de cola anillada en la Reserva Privada Berenty.[173][174][175][176]
Véase también[editar]
- Fauna de Madagascar
- Geografía de Madagascar
- Matorral de Madagascar
- Selva y brezal de Madagascar
- Patrimonio de la Humanidad en Madagascar
- Lemurs of Madagascar
Notas[editar]
- ↑ No se han encontrado restos fósiles de ningún joven de Mesopropithecus, Babakotia o Archaeoindris, y se sabe poco sobre la dentición decidua de Palaeopropithecus. Los modelos de desarrollo se deducen de los de sus parientes más cercanos, los índridos.[77]
- ↑ En los índridos un incisivo o canino inferiores no son sustituidos en la dentición permanente. Existen interpretaciones discrepantes sobre esta producción de distintas fórmulas dentales. Así, una fórmula dental alternativa para esta familia es .[57]
- ↑ También cuentan con esta sublingua o lengua secundaria situada bajo la lengua primaria, mamíferos primitivos como los escandentios y los marsupiales, pero que está mucho más desarrollada en los primates prosimios, como los lémures, lórises, gálagos y tarsios. Esta «segunda lengua» carece de papilas gustativas.
- ↑ En primatología, una organización de fisión-fusión es aquella en que la composición cambia día a día, separándose durante periodos de tiempo más o menos prolongados; por ejemplo, los individuos duermen juntos en un lugar, pero buscan alimento en pequeños grupos que se desplazan en diferentes direcciones durante el día.[101]
- ↑ Los grupos multimachos, también llamados multimachos/multihembras, son un tipo de organización social donde el grupo está formado por más de un macho adulto, más de una hembra adulta y crías y jóvenes de todas las edades. Es el grupo social más común entre los primates, y está formado por entre 10 y 100 individuos.[103]
- ↑ El salto y agarre vertical es el tipo de locomoción arbórea más común entre los primates estrepsirrinos, sobre todo entre los miembros de la familia Indriidae. En reposo, el animal se agarra a un soporte vertical, como el lateral de un árbol o un tallo de bambú, y para desplazarse de una planta a otra salta apoyándose en sus miembros inferiores y se agarra a otro soporte vertical.[114]
- ↑ La criatura que describió Flacourt se consideró tradicionalmente como una especie de Megaladapis, sin embargo, estudios más recientes apuntan a que probablemente sea una especie de Palaeopropithecus.[141]
- ↑ El razonamiento transitivo es la capacidad que tiene un individuo de inferir una relación entre dos o más elementos que no han sido presentados juntos. Es una forma del razonamiento deductivo que se ha apuntado como un mecanismo cognoscitivo por el que los animales podrían aprender las múltiples relaciones dentro de la jerarquía de dominio de su grupo.
- ↑ Especies estandarte (flagship species) o totémicas, son especies que se eligen para representar una causa ambiental, como un ecosistema que necesita conservación, y que son escogidas por su vulnerabilidad, atractivo o peculiaridad con el fin de generar apoyo y reconocimiento del público en general y así, con el apoyo a estas especies, conseguir la conservación de un ecosistema completo y de todos los animales que viven en él.[101]
Referencias[editar]
- ↑ a b c d e f Harcourt, 1990, pp. 7-13
- ↑ «UNEP-WCMC Species Database: CITES-Listed Species». UNEP-WCMC. Consultado el 13 de marzo de 2011.
- ↑ Linneo, Carlos (1758). Systema Naturae (en latín) 1. Holmiae: Impensis Direct. Laurentii Salvii. pp. 29-30.
- ↑ Tattersall, 1982, pp. 43-44
- ↑ Real Academia Española. «lémur». Diccionario de la lengua española (23.ª edición). Consultado el 29 de diciembre de 2010.
- ↑ a b c d e f g h i Garbutt, 2007, pp. 85-86
- ↑ Lux, J. (2008). «What are lemures?». Humanitas 32 (1): 7-14.
- ↑ Flower y Lydekker, 1891, p. 682
- ↑ Nield, 2007, p. 41
- ↑ Blunt y Stearn, 2002, p. 252
- ↑ a b Kay, R.F.; Ross, C.; Williams, B.A. (1997). «Anthropoid origins». Science 275 (5301): 797-804. PMID 9012340. doi:10.1126/science.275.5301.797.
- ↑ a b c Gould y Sauther, 2006, pp. vii-xiii
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an Sussman, 2003, pp. 149-229
- ↑ a b c d e f g h i j k l m n ñ o p q r s t Ankel-Simons, 2007, pp. 392-514
- ↑ a b c d e f g h i j k l m n ñ o p Preston-Mafham, 1991, pp. 141-188
- ↑ a b c d e f g h Tattersall, 2006, pp. 3-18
- ↑ a b c d e f Yoder, 2003, pp. 1242-1247
- ↑ a b Yoder, A.D.; Yang, Z. (2004). «Divergence dates for Malagasy lemurs estimated from multiple gene loci: geological and evolutionary context». Molecular Ecology 13 (4): 757-773. PMID 15012754. doi:10.1046/j.1365-294X.2004.02106.x.
- ↑ a b c Godinot, M. (2006). «Lemuriform origins as viewed from the fossil record». Folia Primatologica 77 (6): 446-464. PMID 17053330. doi:10.1159/000095391.
- ↑ Flynn y Wyss, 2003, pp. 34-40
- ↑ a b c d Mittermeier et al., 2006, pp. 23-26
- ↑ Matthew, W.D. (1915). «Climate and evolution». Annals of the New York Academy of Sciences 24: 171-318. doi:10.1111/j.1749-6632.1914.tb55346.x.
- ↑ Garbutt, 2007, pp. 14-15
- ↑ Kline, G. (20 de enero de 2010). «Study: Animals populated Madagascar by rafting there». Purdue Newsroom. Consultado el 31 de diciembre de 2010.
- ↑ a b c d Horvath, J.E. et al (2008). «Development and application of a phylogenomic toolkit: Resolving the evolutionary history of Madagascar's lemurs». Genome Research 18 (3): 490. PMC 2259113. PMID 18245770. doi:10.1101/gr.7265208.
- ↑ Krause, 2003, pp. 40-47
- ↑ a b Ali, J.R.; Huber, M. (2010). «Mammalian biodiversity on Madagascar controlled by ocean currents». Nature 463 (7281): 653-656. PMID 20090678. doi:10.1038/nature08706. Resumen divulgativo – ScienceDaily (21 de enero de 2010).
- ↑ a b c d e f g h i j k l m n ñ Sussman, 2003, pp. 107-148
- ↑ Gunnell, Gregg F.; Boyer, Doug M.; Friscia, Anthony R.; Heritage, Steven; Manthi, Fredrick Kyalo; Miller, Ellen R.; Sallam, Hesham M.; Simmons, Nancy B. et al. (2018). «Fossil lemurs from Egypt and Kenya suggest an African origin for Madagascar’s aye-aye». Nature Communications 9 (3193). ISSN 2041-1723. doi:10.1038/s41467-018-05648-w.
- ↑ a b c d e f g Mittermeier et al., 2006, pp. 89-182
- ↑ a b c d Mittermeier et al., 2006, pp. 37-51
- ↑ a b c d e f g h i j Godfrey, Jungers y Schwartz, 2006, pp. 41-64
- ↑ a b c d e f g h i Yoder, A.D. (2007). «Lemurs: a quick guide». Current Biology 17 (20): 866-868.
- ↑ a b Dunham, A.E.; Rudolf, V.H.W. (2009). «Evolution of sexual size monomorphism: the influence of passive mate guarding». Journal of Evolutionary Biology 22 (7): 1376-1386. PMID 19486235. doi:10.1111/j.1420-9101.2009.01768.x. Resumen divulgativo – ScienceDaily (1/8/2009).
- ↑ Preston-Mafham, 1991, pp. 10-21
- ↑ a b c Gommery, D.; Ramanivosoa, B.; Tombomiadana-Raveloson, S.; Randrianantenaina, H.; Kerloc’h, P. (2009). «A new species of giant subfossil lemur from the North-West of Madagascar (Palaeopropithecus kelyus, Primates)». Comptes Rendus Palevol 3 (5): 471-480. doi:10.1016/j.crpv.2009.02.001. Resumen divulgativo – ScienceDaily (27 de mayo de 2009).
- ↑ a b c Burney, 2003, pp. 47-51
- ↑ a b c d e f g h i j k l m n ñ o p q r s t u v w x y z aa ab Sussman, 2003, pp. 257-269
- ↑ a b Godfrey y Jungers, 2003, pp. 1247-1252
- ↑ Horvath et al., 2008, fig. 1.
- ↑ Orlando et al., 2008, fig. 1.
- ↑ a b c d e f g h i Rowe, 1996, p. 27
- ↑ Groeneveld, L.F.; Weisrock, D.W.; Rasoloarison, R.M.; Yoder, A.D.; Kappeler, P.M. (2009). «Species delimitation in lemurs: multiple genetic loci reveal low levels of species diversity in the genus Cheirogaleus». BMC Evolutionary Biology 9 (30). PMC 2652444. PMID 19193227. doi:10.1186/1471-2148-9-30.
- ↑ a b c Tattersall, I. (2007). «Madagascar's lemurs: Cryptic diversity or taxonomic inflation?». Evolutionary Anthropology 16: 12-23. doi:10.1002/evan.20126.
- ↑ a b c d Mittermeier, R.; Ganzhorn, J.; Konstant, W.; Glander, K.; Tattersall, I.; Groves, C.; Rylands, A.; Hapke, A. et al. (2008). «Lemur diversity in Madagascar». International Journal of Primatology 29 (6): 1607-1656. doi:10.1007/s10764-008-9317-y.
- ↑ Karanth, P.; Rakotosamimanana, B.; Parsons, T.J.; Yoder, A.D.; Yoder, AD (2005). «Ancient DNA from giant extinct lemurs verifies single origin of Malagasy primates». Proceedings of the National Academy of Sciences 102 (14): 5090-5095. PMC 555979. PMID 15784742. doi:10.1073/pnas.0408354102.
- ↑ a b Hartwig, 2011, pp. 20-21
- ↑ a b Groves (2005)
- ↑ a b c Orlando et al., 2008.
- ↑ McLain, A. T.; Meyer, T. J.; Faulk, C.; Herke, S. W.; Oldenburg, J. M.; Bourgeois, M. G.; Abshire, C. F.; Roos, C. et al. (2012). «An Alu-based phylogeny of lemurs (Infraorder: Lemuriformes)» (PDF). En Murphy, W. J, ed. PLoS ONE (en inglés) 7 (8): e44035. PMID 22937148. doi:10.1371/journal.pone.0044035.
- ↑ Cartmill, 2010, pp. 10-30
- ↑ a b c d e Sterling y McCreless, 2006, pp. 159-184
- ↑ a b c d e f g h i j k l m Ankel-Simons, 2007, pp. 48-161
- ↑ a b c Garbutt, 2007, pp. 205-207
- ↑ a b Yoder, A.D.; Vilgalys, R.; Ruvolo, M. (1996). «Molecular evolutionary dynamics of cytochrome b in strepsirrhine primates: The phylogenetic significance of third-position transversions». Molecular Biology and Evolution 13 (10): 1339-1350. ISSN 0737-4038. PMID 8952078.
- ↑ Marivaux, L.; Welcomme, J.-L.; Antoine, P.-O.; Métais, G.; Baloch, I. M.; Benammi, M.; Chaimanee, Y.; Ducrocq, S. et al. (2001). «A fossil lemur from the Oligocene of Pakistan». Science 294 (5542): 587-591. PMID 11641497. doi:10.1126/science.1065257.
- ↑ a b c d e f g h i Ankel-Simons, 2007, pp. 224-283
- ↑ a b Garbutt, 2007, pp. 115-136
- ↑ a b c Mittermeier et al., 2006, pp. 209-323
- ↑ a b c Garbutt, 2007, pp. 137-175
- ↑ a b Mittermeier et al., 2006, pp. 85-88
- ↑ a b c d Garbutt, 2007, pp. 176-204
- ↑ a b Thalmann, 2003, pp. 1340-1342
- ↑ a b c d e Thalmann y Ganzhorn, 2003, pp. 1336-1340
- ↑ a b c d e f g h Thalmann y Powzyk, 2003, pp. 1342-1345
- ↑ a b c Nowak, 1999, pp. 84-89
- ↑ a b c Richard, 2003, pp. 1345-1348
- ↑ a b c d e Sterling, 2003, pp. 1348-1351
- ↑ a b c d e f g h i j k l m Goodman, Ganzhorn y Rakotondravony, 2003, pp. 1159-1186
- ↑ a b c d e f Ankel-Simons, 2007, pp. 284-391
- ↑ a b c d Rowe, 1996, p. 13
- ↑ a b c d e Overdorff y Johnson, 2003, pp. 1320-1324
- ↑ a b Thalmann, U. (2006). «Lemurs - ambassadors for Madagascar». Madagascar Conservation & Development 1: 4-8. ISSN 1662-2510. Archivado desde el original el 22 de septiembre de 2013.
- ↑ a b Lamberton, C. (1938). «Dentition de lait de quelques le´muriens subfossiles malgaches». Mammalia 2: 57-80.
- ↑ Mittermeier et al., 1994, pp. 33-48
- ↑ a b Godfrey y Jungers, 2002, pp. 108-110
- ↑ Godfrey, Petto y Sutherland, 2001, pp. 113-157
- ↑ a b c d e f g h i j Cuozzo y Yamashita, 2006, pp. 67-96
- ↑ a b c d e f Powzyk y Mowry, 2006, pp. 353-368
- ↑ Osman Hill, 1953, p. 73
- ↑ Ankel-Simons, 2007, pp. 421-423
- ↑ a b c Simons, E.L.; Meyers, D.M. (2001). «Folklore and beliefs about the Aye aye (Daubentonia madagascariensis)». Lemur News 6: 11-16. ISSN 0343-3528. Archivado desde el original el 23 de julio de 2011.
- ↑ a b Irwin, 2006, pp. 305-326
- ↑ Ankel-Simons, 2007, pp. 206-223
- ↑ a b Ankel-Simons, 2007, pp. 162-205
- ↑ a b c d e f g h Ankel-Simons, 2007, pp. 521-532
- ↑ a b c Bolwig, N. (1959). «Observations and thoughts on the evolution of facial mimic». Koedoe - African Protected Area Conservation and Science 2 (1): 60-69. doi:10.4102/koedoe.v2i1.854.
- ↑ a b Ross y Kay, 2004, pp. 3-41
- ↑ a b c d Kirk y Kay, 2004, pp. 539-602
- ↑ a b c d e f Jolly, 2003, pp. 1329-1331
- ↑ Osman Hill, 1953, p. 13
- ↑ Ankel-Simons, 2007, pp. 470-471
- ↑ a b c d e f g h i Schmid y Stephenson, 2003, pp. 1198-1203
- ↑ a b Nowak, 1999, pp. 65-71
- ↑ a b c Fietz, 2003, pp. 1307-1309
- ↑ a b c d e f g h i j Birkinshaw y Colquhoun, 2003, pp. 1207-1220
- ↑ a b c d e f g h i j Wright, 2006, pp. 385-402
- ↑ Nakajima, Y.; Shantha, T.R.; Bourne, G.H. (1969). «Histochemical detection of l-gulonolactone: phenazine methosulfate oxidoreductase activity in several mammals with special reference to synthesis of vitamin C in primates». Histochemistry and Cell Biology 18 (4): 293-301. doi:10.1007/BF00279880.
- ↑ Williams, C. V.; Campbell, J. L.; Glenn, K. M. (2006). «Comparison of serum iron, total iron binding capacity, ferritin, and percent transferrin saturation in nine species of apparently healthy captive lemurs». American Journal of Primatology 68 (5): 1-13. PMID 16550526. doi:10.1002/ajp.20237.
- ↑ Glenn, K. M.; Campbell, J. L.; Botstein, D.; Williams, C. V. (2006). «Retrospective evaluation of the incidence and severity of hemosiderosis in a large captive lemur population». American Journal of Primatology 68 (4): 369-381. PMID 16534809. doi:10.1002/ajp.20231.
- ↑ a b Sarmiento, F. O.; Vera, F. y Juncosa, J. (2000). Diccionario de ecología: paisajes, conservación y desarrollo sustentable para Latinoamérica. Editorial Abya Yala. p. 88. ISBN 9978046771.
- ↑ a b Sussman, 2003, pp. 3-37
- ↑ Sussman, 2003, p. 29
- ↑ Jolly, A. (1998). «Pair-bonding, female aggression and the evolution of lemur societies». Folia Primatologica 69: 1-13. doi:10.1159/000052693.
- ↑ a b c d Dunham, A.E. (2008). «Battle of the sexes: Cost asymmetry explains female dominance in lemurs». Animal Behavior 76: 1435-1439. doi:10.1016/j.anbehav.2008.06.018. Archivado desde el original el 21 de junio de 2015. Consultado el 9 de febrero de 2011.
- ↑ a b Young, A.L.; Richard, A.F.; Aiello, L.C. (1990). «Female dominance and maternal investment in strepsirhine primates». The American Naturalist 135: 473-488. doi:10.1086/285057.
- ↑ Tan, 2006, pp. 369-382
- ↑ Digby, L.I.; Kahlenberg, S.M. (2002). «Female dominance in blue-eyed black lemurs». Primates 43: 191-199. PMID 12145400. doi:10.1007/BF02629647.
- ↑ a b c d e Jolly, A. (1966). «Lemur social behavior and primate intelligence». Science 153 (3735): 501-506. doi:10.1126/science.153.3735.501.
- ↑ a b Curtis, 2006, pp. 133-158
- ↑ Johnson, 2006, pp. 187-210
- ↑ a b c d Fietz y Dausmann, 2006, pp. 97-110
- ↑ Garbutt, 2007, pp. 86-114
- ↑ Sussman, 2003, p. 78
- ↑ Godfrey, L.R.; Jungers, W.L. (2003). «The extinct sloth lemurs of Madagascar». Evolutionary Anthropology 12: 252-263. doi:10.1002/evan.10123.
- ↑ Nowak, 1999, pp. 71-81
- ↑ Mittermeier et al., 2006, pp. 324-403
- ↑ Sauther, M. L. (1989). «Antipredator behavior in troops of free-ranging Lemur catta at Beza Mahafaly special reserve, Madagascar». International Journal of Primatology 10 (6): 595-606. doi:10.1007/BF02739366.
- ↑ Jolly, 1966, p. 135
- ↑ Grieser, B. (1992). «Infant development and parental care in two species of sifakas». Primates 33 (3): 305-314. doi:10.1007/BF02381192.
- ↑ a b c Vasey, 2003, pp. 1332-1336
- ↑ Braune, P.; Schmidt, S.; Zimmermann, E. (2008). «Acoustic divergence in the communication of cryptic species of nocturnal primates (Microcebus ssp.)». BMC Biology 6 (19). PMC 2390514. PMID 18462484. doi:10.1186/1741-7007-6-19. Resumen divulgativo – ScienceDaily (14 de mayo de 2010).
- ↑ a b G.R., Hosey; Thompson, R.J. (1985). «Grooming and touching behaviour in captive ring-tailed lemurs (Lemur catta L.)». Primates 26 (1): 95-98. doi:10.1007/BF02389051.
- ↑ Barton, R.A. (1987). «Allogrooming as mutualism in diurnal lemurs». Primates 28 (4): 539-542. doi:10.1007/BF02380868.
- ↑ a b c d e f Goodman, 2003, pp. 1221-1228
- ↑ Eberle, M.; Kappele, P.M. (2008). «Mutualism, reciprocity, or kin selection? Cooperative rescue of a conspecific from a boa in a nocturnal solitary forager the Gray Mouse Lemur». American Journal of Primatology 70 (4): 410-414. PMID 17972271. doi:10.1002/ajp.20496. Archivado desde el original el 19 de julio de 2011.
- ↑ Crompton y Sellers, 2007, pp. 127-145
- ↑ a b Kappeler y Rasoloarison, 2003, pp. 1310-1315
- ↑ a b Mutschler y Tan, 2003, pp. 1324-1329
- ↑ a b Patel, E.R. (2007). «Non-maternal infant care in wild Silky Sifakas (Propithecus candidus)». Lemur News 12: 39-42. ISSN 1608-1439. Archivado desde el original el 23 de julio de 2011.
- ↑ J., Fietz; Dausmanna, K. H. (2003). «Costs and Potential Benefits of Parental Care in the Nocturnal Fat-Tailed Dwarf Lemur (Cheirogaleus medius)». Folia Primatologica 74 (5-6): 246-258. PMID 14605471. doi:10.1159/000073312.
- ↑ Vasey, N. (2007). «The breeding system of wild red ruffed lemurs (Varecia rubra): a preliminary report». Primates 48 (1): 41-54. PMID 17024514. doi:10.1007/s10329-006-0010-5.
- ↑ Ehrlich, A.; Fobes, J. y King, J. (1976). «Prosimian learning capacities». Journal of Human Evolution 5 (6): 599-617. doi:10.1016/0047-2484(76)90005-1.
- ↑ Fichtel y Kappeler, 2010, pp. 413
- ↑ Penn State (29 de julio de 2008). «Piecing together an extinct lemur, large as a big baboon». ScienceDaily. Consultado el 30 de diciembre de 2010.
- ↑ a b c d e Jolly y Sussman, 2006, pp. 19-40
- ↑ Bons, N.; Rieger, F.; Prudhomme, D.; Fisher, A. y Krause, K. H. (2006). «Microcebus murinus: a useful primate model for human cerebral aging and Alzheimer's disease?». Genes, Brain and Behavior 5 (2): 120-130. PMID 16507003. doi:10.1111/j.1601-183X.2005.00149.x.
- ↑ Marchal, S.; Givalois, L.; Verdier, J. M. y Mestre-Francés, N. (2011). «Distribution of lithostathine in the mouse lemur brain with aging and Alzheimer's-like pathology». Neurobiology of Aging. PMID 21371784. doi:10.1016/j.neurobiolaging.2011.01.002.
- ↑ Gifford, R. J. et al (2008). «A transitional endogenous lentivirus from the genome of a basal primate and implications for lentivirus evolution». Proceedings of the National Academy of Sciences 105 (51): 20362-7. PMC 2603253. PMID 19075221. doi:10.1073/pnas.0807873105. Resumen divulgativo – El Mundo (2/12/2008).
- ↑ Mittermeier et al., 2006, p. 29
- ↑ a b c d Simons, 1997, pp. 142-166
- ↑ a b c Mittermeier et al., 2006, pp. 27-36
- ↑ a b c d e f g h i j k l m Mittermeier et al., 2006, pp. 52-84
- ↑ Macedonia, J.M. (1993). «The vocal repertoire of the Ring-tailed Lemur (Lemur catta)». Folia Primatologica 61: 186-217. doi:10.1159/000156749.
- ↑ Tilden, C. D. (1990). «A study of locomotor behavior in a captive colony of red-bellied lemurs (Eulemur rubriventer)». American Journal of Primatology 22 (2): 87-100. doi:10.1002/ajp.1350220203.
- ↑ Wunderlich, R. E.; Schaum, J. C. (2007). «Kinematics of bipedalism in Propithecus verreauxi». Journal of Zoology 272 (2): 165-175. doi:10.1111/j.1469-7998.2006.00253.x.
- ↑ MacLean, E.L.; Merritt, D.J.; Brannon, E.M. (2008). «Social complexity predicts transitive reasoning in prosimian primates». Animal Behaviour 76 (2): 479-486. PMC 2598410. PMID 19649139. doi:10.1016/j.anbehav.2008.01.025. Archivado desde el original el 20 de abril de 2010.
- ↑ Merritt, D.; MacLean, E.L.; Jaffe, S.; Brannon, E.M. (2007). «A comparative analysis of serial ordering in Ring-Tailed Lemurs (Lemur catta)». Journal of Comparative Psychology 121 (4): 363-371. PMC 2953466. PMID 18085919. doi:10.1037/0735-7036.121.4.363. Archivado desde el original el 8 de junio de 2011.
- ↑ Santos, Laurie R.; Mahajan, N.; Barens, J. L. (2005). «How prosimian primates represent tools: Experiments with two lemur species (Eulemur fulvus and Lemur catta)». Journal of Comparative Psychology 119 (4): 394-403. PMID 16366773. doi:10.1037/0735-7036.119.4.394.
- ↑ a b c d e f Mittermeier et al., 2006, pp. 15-17
- ↑ a b c d e f g Mittermeier, Konstant y Rylands, 2003, pp. 1538-1543
- ↑ Schwitzer, C., Mittermeier, R.A., Rylands, A.B., Taylor, L.A., Chiozza, F., Williamson, E.A., Wallis, J. and Clark, F.E. (eds.) (2012). Primates in Peril: The World's 25 Most Endangered Primates 2012-2014 (PDF) (en inglés). IUCN/SSC Primate Specialist Group (PSG), International Primatological Society (IPS), Conservation International (CI) y Bristol Zoological Society (BZS). pp. 1-91.
- ↑ Black, Richard (13 de julio de 2012). «Lemurs sliding towards extinction». BBC News. Consultado el 18 de agosto de 2013.
- ↑ «El 91 % de los lémures de Madagascar están amenazados de extinción». Mongabay. 26 de septiembre de 2012. Consultado el 18 de agosto de 2013.
- ↑ Samuel, H. (19 de agosto de 2012). «Furry lemurs 'could be wiped out within 20 years'». The Telegraph. Consultado el 18 de agosto de 2013.
- ↑ Mintz, Z. (21 de agosto de 2013). «Lemurs Face Extinction In 20 Years, Risk Of Losing Species For ‘First Time In Two Centuries’». International Business Times. Consultado el 18 de agosto de 2013.
- ↑ a b c «Country brief: Madagascar». eStandardsForum. 1 de diciembre de 2009. Archivado desde el original el 26 de julio de 2011. Consultado el 14 de enero de 2011.
- ↑ a b c «Monumental debt-for-nature swap provides $20 million to protect biodiversity in Madagascar». World Wildlife Fund. 11 de junio de 2008. Consultado el 5 de noviembre de 2017.
- ↑ Ganzhorn, Goodman y Dehgan, 2003, pp. 1228-1234
- ↑ Junge y Sauther, 2006, pp. 423-440
- ↑ Ratsimbazafy, 2006, pp. 403-422
- ↑ Butler, Rhett (4 de enero de 2010). «Madagascar’s Political Chaos Threatens Conservation Gains». Yale Environment 360. Yale School of Forestry & Environmental Studies. Consultado el 5 de noviembre de 2017.
- ↑ Schuurman, Derek (2009). «Illegal logging in Madagascar». Traffic Bulletin 22 (2): 49.
- ↑ Rowe, 1996, p. 46
- ↑ Wright y Andriamihaja, 2003, pp. 1485-1488
- ↑ «Madagascar National Parks. Une structure, une mission» (en francés). Madagascar National Parks. Archivado desde el original el 24 de mayo de 2011. Consultado el 28 de abril de 2011.
- ↑ a b Sargent y Anderson, 2003, pp. 1543-1545
- ↑ Britt et al., 2003, pp. 1545-1551
- ↑ «Madagascar». World Heritage List (en inglés). Unesco. Consultado el 22 de marzo de 2011.
- ↑ a b c d e f Ruud, 1970, pp. 97-101
- ↑ Barnes, D. (21 de octubre de 2001). «Fun in the sun with lemurs». The Washington Times.
- ↑ Jacobson, Louis (30 de marzo de 2004). «Looking for lemurs». USA Today. Consultado el 19 de marzo de 2011.
- ↑ Huff, R. (8 de febrero de 2008). «Tonight». New York Daily News. p. 122.
- ↑ «Highlights». The Washington Post. 8 de febrero de 2008. p. C04.
- ↑ «Madagascar; country's unknown creatures on DSTV». Africa News. 28 de diciembre de 2007.
- ↑ Walmark, H (8 de febrero de 2008). «Critic's choice: Lemur Street». The Globe and Mail. p. R37.
Bibliografía[editar]
- Ankel-Simons, F. (2007). Primate Anatomy (3.ª edición). Academic Press. ISBN 0-12-372576-3.
- Blunt, W.; Stearn, W.T. (2002). Linnaeus: the compleat naturalist. Princeton University Press. ISBN 978-0691096360.
- Hartwig, W. (2011). «Capítulo 6: Primate evolution». En Campbell, C. J.; Fuentes, A.; MacKinnon, K. C.; Bearder, S. K.; Stumpf, R. M., eds. Primates in Perspective (2.ª edición). Oxford University Press. pp. 19-31. ISBN 978-0-19-539043-8.
- Fichtel, C.; Kappeler, P. M. (2010). «Capítulo 11: Human universals and primate symplesiomorphies: Establishing the lemur baseline». En Kappeler, P. M.; Silk, J. B., eds. Mind the Gap: Tracing the Origins of Human Universals. Springer. ISBN 978-3-642-02724-6.
- Flower, W.H.; Lydekker, R. (1891). An introduction to the study of mammals living and extinct. Londres: A. and C. Black. ISBN 978-1110768578.
- Garbutt, N. (2007). Mammals of Madagascar, A Complete Guide. A&C Black Publishers. ISBN 978-0-300-12550-4.
- Goodman, S.M.; Benstead, J.P., eds. (2003). The Natural History of Madagascar. University of Chicago Press. ISBN 0-226-30306-3.
- Capítulo 2 - Geology and Soils
- Flynn, J.J.; Wyss, A.R. (2003). «Mesozoic Terrestrial Vertebrate Faunas: The Early History of Madagascar's Vertebrate Diversity». pp. 34-40.
- Krause, D.W. (2003). «Late Cretaceous Vertebrates of Madagascar: A Window into Gondwanan Biogeography at the End of the Age of Dinosaurs». pp. 40-47.
- Burney, D.A. (2003). «Madagascar's Prehistoric Ecosystems». pp. 47-51.
- Capítulo 13 - Mammals
- Goodman, S.M.; Ganzhorn, J.U.; Rakotondravony, D. (2003). «Introduction to the Mammals». pp. 1159-1186.
- Schmid, J.; Stephenson, P.J. (2003). «Physiological Adaptations of Malagasy Mammals: Lemurs and Tenrecs Compared». pp. 1198-1203.
- Birkinshaw, C.R.; Colquhoun, I.C. (2003). «Lemur Food Plants». pp. 1207-1220.
- Goodman, S.M. (2003). «Predation on Lemurs». pp. 1221-1228.
- Ganzhorn, J. U.; Goodman, S. M.; Dehgan, A. (2003). «Effects of Forest Fragmentation on Small Mammals and Lemurs». pp. 1228-1234.
- Yoder, A.D. (2003). «Phylogeny of the Lemurs». pp. 1242-1247.
- Godfrey, L.R.; Jungers, W.L. (2003). «Subfossil Lemurs». pp. 1247-1252.
- Fietz, J. (2003). «Primates: Cheirogaleus, Dwarf Lemurs or Fat-tailed Lemurs». pp. 1307-1309.
- Kappeler, P.M.; Rasoloarison, R.M. (2003). «Microcebus, Mouse Lemurs, Tsidy». pp. 1310-1315.
- Overdorff, D.J.; Johnson, S. (2003). «Eulemur, True Lemurs». pp. 1320-1324.
- Mutschler, T.; Tan, C.L. (2003). «Hapalemur, Bamboo or Gentle Lemur». pp. 1324-1329.
- Jolly, A. (2003). «Lemur catta, Ring-tailed Lemur». pp. 1329-1331.
- Vasey, N. (2003). «Varecia, Ruffed Lemurs». pp. 1332-1336.
- Thalmann, U.; Ganzhorn, J.U. (2003). «Lepilemur, Sportive Lemur». pp. 1336-1340.
- Thalmann, U. (2003). «Avahi, Woolly Lemurs». pp. 1340-1342.
- Thalmann, U.; Powzyk, J. (2003). «Indri indri, Indri». pp. 1342-1345.
- Richard, A. (2003). «Propithecus, Sifakas». pp. 1345-1348.
- Sterling, E. (2003). «Daubentonia madagascariensis, Aye-aye». pp. 1348-1351.
- Capítulo 14 - Conservation
- Wright, P.C.; Andriamihaja, B. (2003). «The conservation value of long-term research: a case study from the Parc National de Ranomafana». pp. 1485-1488.
- Mittermeier, R.A.; Konstant, W.R.; Rylands, A.B. (2003). «Lemur Conservation». pp. 1538-1543.
- Sargent, E.L.; Anderson, D. (2003). «The Madagascar Fauna Group». pp. 1543-1545.
- Britt, A.; Iambana, B.R.; Welch, C.R.; Katz, A.S. (2003). «Restocking of Varecia variegata variegata in the Réserve Naturelle Intégrale de Betampona». pp. 1545-1551.
- Simons, E. L. (1997). «Capítulo 6: Lemurs: Old and New». En Goodman, S. M.; Patterson, B. D., eds. Natural Change and Human Impact in Madagascar. Smithsonian Institution Press. pp. 142-166. ISBN 978-1560986829.
- Gould, L.; Sauther, M. L., eds. (2006). Lemurs: Ecology and Adaptation. Springer. ISBN 978-0387-34585-7.
- Gould, L.; Sauther, M. L. (2006). «Prefacio». Lemurs: Ecology and Adaptation. pp. vii-xiii.
- Tattersall, I. (2006). «Capítulo 1: Origin of the Malagasy Strepsirhine Primates». Lemurs: Ecology and Adaptation. pp. 3-18.
- Jolly, A.; Sussman, R. W. (2006). «Capítulo 2: Notes on the History of Ecological Studies of Malagasy Lemurs». pp. 19-40.
- Godfrey, L. R.; Jungers, W. L.; Schwartz, G. T. (2006). «Capítulo 3: Ecology and Extinction of Madagascar's Subfossil Lemurs». pp. 41-64.
- Cuozzo, F. P.; Yamashita, N. (2006). «Capítulo 4: Impact of Ecology on the Teeth of Extant Lemurs: A Review of Dental Adaptations, Function, and Life History». pp. 67-96.
- Fietz, J.; Dausmann, K.H. (2006). «Capítulo 5: Big Is Beautiful: Fat Storage and Hibernation as a Strategy to Cope with Marked Seasonality in the Fat-Tailed Dwarf Lemur (Cheirogaleus medius)». pp. 97-110.
- Curtis, D. J. (2006). «Capítulo 7: Cathemerality in Lemurs». pp. 133-158.
- Sterling, E. J.; McCreless, E. E. (2006). «Capítulo 8: Adaptations in the Aye-aye: A Review». Lemurs: Ecology and Adaptation. pp. 159-184.
- Johnson, S. E. (2006). «Capítulo 9: Evolutionary Divergence in the Brown Lemur Species Complex». pp. 187-210.
- Irwin, M. T. (2006). «Capítulo 14: Ecologically Enigmatic Lemurs: The Sifakas of the Eastern Forests (Propithecus candidus, P. diadema, P. edwardsi, P. perrieri, and P. tattersalli)». pp. 305-326.
- Powzyk, J. A.; Mowry, C.B. (2006). «Capítulo 16: The Feeding Ecology and Related Adaptations of Indri indri». pp. 353-368.
- Tan, C. L. (2006). «Capítulo 17: Behavior and Ecology of Gentle Lemurs (Genus Hapalemur)». pp. 369-382.
- Wright, P. C. (2006). «Capítulo 18: Considering Climate Change Effects in Lemur Ecology». pp. 385-402.
- Ratsimbazafy, J. (2006). «Capítulo 19: Diet Composition, Foraging, and Feeding Behavior in Relation to Habitat Disturbance: Implications for the Adaptability of Ruffed Lemurs (Varecia variegata editorium) in Manombo Forest, Madagascar». pp. 403-422.
- Junge, R. E.; Sauther, M. (2006). «Capítulo 20: Overview on the Health and Disease Ecology of Wild Lemurs: Conservation Implications». pp. 423-440.
- Groves, Colin (2005). «Strepsirrhini». En Wilson, D. E.; Reeder, D. M., eds. Mammal Species of the World (3ª edición). Baltimore: Johns Hopkins University Press. ISBN 0-8018-8221-4.
- Crompton, R. H.; Sellers, W. I. (2007). «A consideration of leaping locomotion as a means of predator avoidance in prosimian primates». En Gursky, K. A. I.; Nekaris, S. L., eds. Primate Anti-Predator Strategies. Springer. pp. 127-145. ISBN 978-1-4419-4190-9. doi:10.1007/978-0-387-34810-0_6.
- Harcourt, C. (1990). «Introducción». En Thornback, J, ed. Lemurs of Madagascar and the Comoros: The IUCN Red Data Book. World Conservation Union. ISBN 978-2880329570.
- Godfrey, L. R.; Jungers, W. L. (2002). «Capítulo 7: Quaternary fossil lemurs». En Hartwig, W. C., ed. The primate fossil record. Cambridge University Press. pp. 97-121. ISBN 978-0521663151.
- Horvath, J. E.; Weisrock, D. W.; Embry, S. L.; Fiorentino, I.; Balhoff, J. P.; Kappeler, P.; Wray, G. A.; Willard, H. F. et al. (2008). «Development and application of a phylogenomic toolkit: Resolving the evolutionary history of Madagascar's lemurs» (PDF). Genome Research (en inglés) 18 (3): 489-499. PMC 2259113. PMID 18245770. doi:10.1101/gr.7265208.
- Jolly, A. (1966). Lemur Behavior. Chicago: University of Chicago Press. ISBN 978-0226405520.
- Mittermeier, R. A.; Tattersall, I.; Konstant, W. R.; Meyers, D. M.; Mast, R. B. (1994). Lemurs of Madagascar. Ilustrado por S. D. Nash (1.ª edición). Conservation International. ISBN 1-881173-08-9.
- Mittermeier, R. A.; Konstant, W. R.; Hawkins, F.; Louis, E. E.; Langrand, O.; Ratsimbazafy, J.; Rasoloarison, R.; Ganzhorn, J. U., et al (2006). Lemurs of Madagascar. Ilustrado por S. D. Nash (2ª edición). Conservation International. ISBN 1-881173-88-7.
- Nield, T. (2007). Supercontinent: Ten Billion Years in the Life of Our Planet. Harvard University Press. ISBN 978-0674026599.
- Nowak, R. M. (1999). Walker's Mammals of the World (6ª edición). Johns Hopkins University Press. ISBN 0801857899.
- Orlando, L.; Calvignac, S.; Schnebelen, C.; Douady, C. J.; Godfrey, L. R.; Hänni, C. (2008). «DNA from extinct giant lemurs links archaeolemurids to extant indriids» (PDF). BMC Evolutionary Biology (en inglés) 8 (121). PMC 2386821. PMID 18442367. doi:10.1186/1471-2148-8-121.
- Osman Hill, W. C. (1953). Primates Comparative Anatomy and Taxonomy I—Strepsirhini. Edinburgh Univ Pubs Science & Maths, No 3 (en inglés). Edinburgh University Press. OCLC 500576914.
- Cartmill, M. (2010). «Capítulo 2: Primate Classification and Diversity». En Platt, M.; Ghazanfar, A., eds. Primate Neuroethology. Oxford University Press. pp. 10-30. ISBN 978-0195-32659-8.
- Godfrey, L. R.; Petto, A. J.; Sutherland, M. R. (2001). «Capítulo 4: Dental ontogeny and life history strategies: The case of the giant extinct indroids of Madagascar». En Plavcan, J. M.; Kay, R.; Jungers, W.L. et al., eds. Reconstructing behavior in the primate fossil record. Springer. pp. 113-157. ISBN 978-0306466045.
- Preston-Mafham, K. (1991). Madagascar: A Natural History. Facts on File. ISBN 978-0816024032.
- Ross, C. F.; Kay, R. F., eds. (2004). Anthropoid Origins: New Visions (2.ª edición). Springer. ISBN 978-0306481208.
- Ross, C. F.; Kay, R.F. (2004). «Capítulo 1: Evolving Perspectives on Anthropoidea». pp. 3-41.
- Kirk, C. E.; Kay, R.F. (2004). «Capítulo 22: The Evolution of High Visual Acuity in the Anthropoidea». pp. 539-602.
- Rowe, N. (1996). The Pictorial Guide to the Living Primates. Pogonias Press. ISBN 978-0964882515.
- Ruud, J. (1970). Taboo: A Study of Malagasy Customs and Beliefs (2ª edición). Oslo University Press.
- Sussman, R. W. (2003). Primate Ecology and Social Structure. Pearson Custom Publishing. ISBN 978-0-536-74363-3.
- Tattersall, I. (1982). «The Living Species of Malagasy Primates». The Primates of Madagascar. Columbia University Press. ISBN 0-231-04704-5.
Bibliografía adicional[editar]
- Medina, Rafael (2012). «En busca de los Lémures». Journal of Feelsynapsis (JoF) (5): 58-83. ISSN 2254-3651. Archivado desde el original el 16 de junio de 2013.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre lémures.
Wikimedia Commons alberga una categoría multimedia sobre lémures. Wikispecies tiene un artículo sobre Lemuroidea.
Wikispecies tiene un artículo sobre Lemuroidea.- Lemur BBC Nature (en inglés)
- Lemurs of Madagascar (en inglés)


















