Artritis reumatoide
| Artritis reumatoide | ||
|---|---|---|
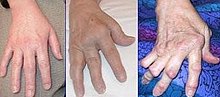
 Mano afectada por la artritis reumatoide | ||
| Especialidad | Reumatología | |
| Síntomas | Dolor musculoesquelético secundario crónico | |
| Tratamiento | Medicamentos para el dolor , esteroides , medicamentos antiinflamatorios no esteroideos , medicamentos antirreumáticos modificadores de la enfermedad | |
| Sinónimos | ||
| ||
La artritis reumatoide (AR) es una enfermedad inflamatoria sistémica autoinmune, caracterizada por una inflamación persistente de las articulaciones, que típicamente afecta a las pequeñas articulaciones de manos y pies, produciendo su destrucción progresiva y generando distintos grados de deformidad e incapacidad funcional. Aunque el trastorno es de causa desconocida, la autoinmunidad juega un papel primordial en su origen, en su cronicidad y en la progresión de la enfermedad. La enfermedad se asocia con la presencia de autoanticuerpos (particularmente el factor reumatoide y los anticuerpos antipéptidos cíclicos citrulinados).[1] En ocasiones, también se presenta con manifestaciones extra articulares, pudiendo afectar a diversos órganos y sistemas, como los ojos, pulmones, corazón, piel o vasos sanguíneos.[2]
La artritis reumatoide se diagnostica fundamentalmente por los síntomas clínicos y la exploración física, con la ayuda de ciertos análisis clínicos y las radiografías. Tanto el diagnóstico como el manejo de la artritis reumatoide corresponde a los especialistas en reumatología.[3]
La artritis reumatoide sin tratamiento habitualmente sigue un curso progresivo, deformante e invalidante. Sin embargo, aunque no existe propiamente una cura de la enfermedad, los tratamientos existentes en la actualidad logran controlar la enfermedad en la mayoría de los pacientes, consiguiéndose un buen control del dolor y la rigidez articular, frenando el daño estructural articular y la aparición de deformidades, evitando el deterioro funcional y mejorando la calidad de vida de los pacientes.[2][4]
Historia
[editar]Terminología
[editar]
El término artritis procede de la raíz griega artr-, –articulación– y el sufijo -itis –inflamación– que designa la inflamación de una articulación. Por su parte el término reumatoide procede del griego rheuma/rheumatos –flujo, algo que fluye– y del sufijo -oid —semejante—. Lo que en conjunto se correspondería con inflamación articular parecida al reumatismo o a la fiebre reumática.
El término artritis reumatoide fue acuñado en 1859 por Alfred Baring Garrod, aunque hay que matizar que en esta denominación incluía entonces no solo las poliartritis inflamatorias, sino también la artrosis poliarticular.[5] En 1922 el término artritis reumatoide pasó a designar solo a las poliartritis inflamatorias, adoptando este nombre el Ministerio de Sanidad británico como la denominación oficial, pasando a adoptarlo la American Rheumatism Association en 1941.[6] Aunque se han usado otras terminologías para referirse a la enfermedad —ver sinónimos—, el término artritis reumatoide es el que aparece recogido en el nomenclátor de las enfermedades reumáticas en castellano,[7] y que deriva de la terminología usada en la literatura inglesa —rheumatoid arthritis—, frente a la terminología usada en la literatura francesa —polyarthrite rhumatoïde—. La AR es mucho más frecuente en el sexo femenino que en el masculino y suele aparecer en personas adultas mayores, pero puede iniciarse en cualquier etapa de la vida y afectar a cualquier persona, con independencia de la raza, el sexo y la ocupación.
La artritis reumatoide en la literatura médica
[editar]Algunos autores piensan que Hipócrates y otros autores de la antigüedad como Galeno, Areteo de Capadocia, Escribonio Largo, Sorano de Éfeso o Miguel Psellos pudieron hacer descripciones de enfermedades semejantes a la artritis reumatoide,[8] aunque más bien sus descripciones parecen compatibles con la gota crónica poliarticular.[5]
Es posible que la artritis reumatoide fuera observada en 1676 por Thomas Sydenham, que mencionó una enfermedad articular caracterizada por cronicidad y deformidades en las manos. En 1703 William Musgrave, en el libro "De Arthritide Symptomatica", describió una poliartritis crónica que él consideraba distinta de la gota y de la fiebre reumática. También, es posible que William Heberden pudiera haber reconocido la enfermedad a finales del siglo XVIII.[5] Sin embargo, para la mayoría de investigadores, la primera descripción convincente de la enfermedad fue hecha en 1800 por Augustin Jacob Landré-Beauvais (1772–1840), médico del Hospital de la Pitié-Salpêtrière en París. Tenía bajo estudio y tratamiento a un grupo de pacientes con dolor articular intenso que no podía explicarse por otras enfermedades conocidas entonces. Al contrario que la gota afectaba a la gente pobre y mayoritariamente mujeres, cuyo estudio había sido ignorado por otros médicos puesto que en vistas de recibir compensación y reconocimiento por su trabajo preferían atender a pacientes más acomodados. La hipótesis de Landré-Beauvais fue que sufrían de una enfermedad no descrita que denominó "la goutte asthenique primitive” —gota asténica primaria—. De acuerdo a la descripción de Landré-Beauvais la nueva enfermedad causaba inflamación permanente de las articulaciones y deformidades, originando tras varios años una discapacidad grave en algunos afectados.[5][6] Aunque la relación con la gota estaba equivocada, su trabajo motivó a otros investigadores a profundizar en el estudio de esta enfermedad.
La artritis reumatoide fue descrita unos años más tarde con claridad por Benjamín C Brodie en 1819, que puso énfasis en su típica lenta progresión y señaló que no solo afectaba a las articulaciones, sino también a bolsas y vainas de tendones.[6] Los estudios clínicos y anatómicos de Jean-Martin Charcot en 1855 separaron definitivamente la gota de otros reumatismos, que Charcot englobó bajo el nombre de “reumatismo crónico deformante”. Las ilustraciones de la obra de Charcot “Les Rhumatismes du Veillard” (1872) ya mostraban claramente las diferencias entre las manos de la artritis reumatoide, los nódulos artrósicos y los tofos gotosos.[9]
El siguiente paso en el descubrimiento de la AR fue el trabajo de Alfred Baring Garrod (1819-1907), médico inglés, en la mitad y postrimerías del siglo XIX. En su obra de 1859 “Treatise on nature and treatment of gout and rheumatic gout”, distinguió la gota de otras condiciones artríticas a partir de la determinación de los niveles de ácido úrico en la sangre de los pacientes, elevados en la gota, pero normales en estas otras artritis, y denominó a la enfermedad “rheumatoid arthritis” —artritis reumatoide—, ya como una enfermedad de distinta naturaleza que la gota.[10]
El test para el factor reumatoide fue desarrollado por primera vez por Eric Waaler en Oslo en 1940 y posteriormente por HM Rose en 1947 en Nueva York, al observar que ciertos sueros reumatoides aglutinaban hematíes de carnero, por lo que la prueba se denominaba con frecuencia "test de Waaler-Rose" y posteriormente “test de látex”, al utilizarse para la aglutinación partículas de látex revestidas con gammaglobulina humana.[6]
En el último medio siglo se han usado diversos criterios para el diagnóstico y clasificación de la artritis, siendo los más aceptados y utilizados los de la American Rheumatism Association de 1958[11] y posteriormente los de 1987[12] para la diferenciación y separación de la artritis reumatoide de otros cuadros articulares inflamatorios, como por ejemplo la artritis psoriásica.[5] Así, fue cambiando el concepto de la enfermedad con los avances en el conocimiento diferenciador de las diversas entidades articulares. Por último, en 2010 se publicaron unos nuevos criterios conjuntos del American College of Rheumatology (ACR) y la European League Against Rheumatism (EULAR) para permitir un diagnóstico más precoz de la enfermedad.[13] Se puede, por tanto, decir que el concepto y nombre de la artritis reumatoide es relativamente nuevo y que el contenido de esta denominación ha cambiado mucho durante su corta existencia. Además, se agrega el concepto de artritis reumatoide temprana si tiene menos de un año de evolución desde la aparición de los síntomas y artritis reumatoide muy temprana cuando el diagnóstico se realiza dentro de los primeros 3 meses de evolución. Los nuevos términos hacen hincapié en la utilización precoz de medicamentos modificadores de la enfermedad para prevenir las secuelas osteoarticulares dejadas por la artritis reumatoide.
La artritis reumatoide en las artes plásticas
[editar]

Uno de los primeros ejemplos compatibles con artritis reumatoide en la pintura es un cuadro de Justus van Gent mostrando a Federico de Montefeltro que murió en 1482. En su mano izquierda se aprecia tumefacción de las articulaciones metacarpofalángicas. Otras pinturas con imágenes sugerentes de esta enfermedad son La Tentación de San Antonio —anónimo—, el retrato de Erasmo de Róterdam por Quinten Metsys, la Sagrada Familia de Giuseppe Maria Crespi, la Familia del Artista, de Jacob Jordaens y algunos retratos de Rembrandt. Notable es el caso de la obra de Rubens, las tres Gracias, en la cual se aprecia la característica deformación que la artritis reumatoide produce en la mano de la "Gracia" situada más a la izquierda,[8] aunque otros autores piensan que se deben observar con cautela estas representaciones que están sujetas a las convenciones artísticas y a interpretaciones individuales.[5] Mención especial merece el gran pintor francés Augusto Renoir que padeció la enfermedad, lo que no le impidió realizar su labor artística.[14]
Paleopatología
[editar]Existe cierta controversia sobre si la artritis reumatoide es una enfermedad nueva, de aparición en los últimos siglos —ya que no hay descripciones convincentes de ella anteriores a 1800—, o si ya era una enfermedad existente en la antigüedad.[8] La paleopatología ha estudiado en restos óseos de diversos asentamientos antiguos la existencia de evidencias de artritis reumatoide. Los restos esqueléticos de indios de hace 3000-5000 años, encontrados en Alabama, indican la presencia de una poliartritis simétrica erosiva, afectando articulaciones pequeñas y grandes, en 6 de 84 esqueletos bien conservados. Hallazgos similares se encontraron en otra población de Kentucky, afectando a 7 de 129 esqueletos.[5][8] Las lesiones óseas observadas son semejantes a las de los esqueletos contemporáneos con artritis reumatoide, observándose osteoporosis periarticular y erosiones indistinguibles de las que se observan en la práctica reumatológica rutinaria.[8] También se han encontrado cambios óseos compatibles con artritis reumatoide en dos esqueletos neolíticos de Gotland, Suecia, aunque la afectación era asimétrica y había anquilosis articular y periostitis. Por otra parte, un estudio inglés sobre 800 esqueletos de una excavación arqueológica, encontró lesiones erosivas compatibles con artritis reumatoide solo en un esqueleto.[8] Existe controversia entre los expertos sobre el diagnóstico de artritis reumatoide basado en el estudio de restos esqueléticos antiguos, en especial en cuanto a la interpretación de los defectos corticales —erosiones—, por lo que faltan evidencias claras de la existencia de la enfermedades anteriores a 1800. Aunque es posible que la enfermedad fuera menos frecuente que en la actualidad —entre otras cosas, debido a la baja expectativa de vida, que haría que muy pocos individuos alcanzase la edad de comienzo habitual de la enfermedad—, sin duda la enfermedad existió en la antigüedad y se diagnosticó erróneamente como una variante de reumatismo, no diferenciándola de otros cuadros articulares hasta este último medio siglo.[6]
Epidemiología
[editar]La prevalencia estimada de la artritis reumatoide es alrededor del 1% en las poblaciones de Europa y Norteamérica.[15][16][17] La enfermedad tiene una distribución universal, pero los estudios señalan unas tasas algo inferiores en las poblaciones asiáticas, incluyendo China y Japón, así como en la población rural africana; por el contrario, algunas poblaciones nativas norteamericanas tienen prevalencias superiores al 5%.[15][18] La incidencia es de aproximadamente 40 casos nuevos cada año por cada 100.000 habitantes.[15]
Las mujeres son afectadas de dos a tres veces más que los hombres,[19] probablemente debido a las influencias hormonales.[18] El pico de comienzo de la enfermedad es entre los 50 y 75 años, por lo que en las mujeres de más de 65 años la prevalencia puede llegar al 5%.[15] El riesgo de desarrollar una artritis reumatoide a lo largo de la vida en los adultos es de 3,6% para las mujeres y de 1,7% para los varones.[15]
Factores de riesgo
[editar]La artritis reumatoide es una enfermedad autoinmune sistémica —puede afectar a todo el cuerpo—, aunque tiene una especial predilección por las articulaciones, cuyas causas no son de todo conocidas, aunque se han identificado algunos posibles factores causales. Probablemente, diversos factores interactúan en la persona predispuesta genéticamente para iniciar la inflamación de las articulaciones. Una vez iniciado, el proceso se autoperpetúa en el tiempo.[20]
Factores genéticos
[editar]Se estima que aproximadamente el 50-60% del riesgo de presentar artritis reumatoide es de origen genético,[18][21] basándose fundamentalmente en los siguientes datos:
- Los estudios epidemiológicos muestran que el riesgo de presentar la enfermedad en familiares de primer grado de un paciente afecto de artritis reumatoide es 1,5 veces más alto que el de la población general.[18]
- La tasa de concordancia es notablemente mayor entre gemelos monocigóticos comparada con gemelos dicigóticos (12-15% frente a 3,5% respectivamente), lo que confirma un papel importante de los genes además de las fundamentales influencias ambientales entre hermanos genéticamente iguales.[18]
- El factor de riesgo genético más potente en la artritis reumatoide proviene de ciertos alelos del complejo mayor de histocompatibilidad, estando asociada la enfermedad fundamentalmente con ciertos alelos del HLA-DR4 (70% frente al 30% del grupo control), DR14 y algunas cadenas beta DR1. Los pacientes con artritis reumatoide presentan en exceso una secuencia de aminoácidos, en concreto glutamina-leucina-arginina-alanina-alanina en la tercera región hipervariable de las cadenas beta HLA-DR en los residuos 67, 70, 71, 72 y 74, llamado el epítopo compartido. La presencia del epítopo compartido se asocia a un incremento de la susceptibilidad a la artritis reumatoide y a una mayor gravedad de la enfermedad.[18] Aunque este hallazgo se ha observado en múltiples poblaciones, no es aplicable a otros grupos como los afroamericanos.[15] Algunos autores sugieren que el epítopo compartido podría ser más un marcador de la presencia de anticuerpos antipéptidos cíclicos citrulinados que un factor de riesgo por sí mismo.[22][18]
- Los polimorfismos de otros genes también pueden contribuir a un incremento del riesgo de artritis reumatoide, mencionándose a variantes de la proteína tirosina fosfatasa intracelular N22 (PTPN22) y su alelo funcional R620W, que regulan la actividad de los linfocitos T, así como polimorfismos de los genes que regulan las diversas citocinas, como polimorfismos del receptor del factor de necrosis tumoral (TNF) alfa, o del STAT4 que codifica un factor de transcripción que transmite señales inducidas por varias citocinas.[18][15]
Factores de riesgo no genéticos
[editar]- Factores relacionados con el género: como ya se ha mencionado las mujeres tienen de dos a tres veces más probabilidades de desarrollar una artritis reumatoide que los hombres, quizás debido en parte al efecto estimulador de los estrógenos sobre el sistema inmune. Los estrógenos inhiben la función celular de los linfocitos T inhibidores y aumentan la función celular de los linfocitos T colaboradores o facilitadores.[23] El riesgo de artritis reumatoide está aumentado en las nulíparas —mujeres que no han tenido hijos— y, por otra parte, el embarazo se asocia con frecuencia a remisión de la enfermedad, aunque los brotes en el postparto son habituales. Los varones con artritis reumatoide tienen niveles más bajos de testosterona que aquellos sin la enfermedad, observándose hipogonadismo en una mayor proporción de pacientes que de controles —32% en varones con artritis reumatoide, frente al 7% en los controles—.[24]

- Tabaquismo: De los factores ambientales que contribuyen a la aparición de la enfermedad el mejor definido es el tabaquismo. Fumar cigarrillos es un fuerte factor de riesgo para el desarrollo de artritis reumatoide, en particular en los individuos con el epítopo compartido, en los que multiplica la susceptibilidad entre 20 y 40 veces.[25][26] Parece que interviene más en el riesgo la duración del hábito de fumar que el número de cigarrillos fumados al día. Además de aumentar la susceptibilidad a la enfermedad, fumar es un factor tanto de una evolución más rápida de la enfermedad hacia etapas invalidantes, como de una peor respuesta a tratamientos.[15][27]
- Infecciones: Se ha pensado que las infecciones pudieran ser un factor desencadenante o iniciador de la artritis reumatoide, pero ningún agente individual se ha demostrado que sea responsable de la enfermedad. Se han descrito varios mecanismos celulares por los que los agentes infecciosos podrían activar o amplificar la inflamación, como por ejemplo mediante los receptores de tipo Toll, el inflamasoma y las respuestas a superantígenos y proteínas de choque térmico, que por un mecanismo de mimetismo molecular o reactividad cruzada podrían inducir la respuesta inmune.[15] Entre las bacterias se han involucrado principalmente a Proteus mirabilis, diversas especies de Mycoplasmas, Porphyromona gingivalis[28][29][27]—el principal agente etiológico de la enfermedad periodontal— y bacterias intestinales como especies de Bacteroides y Prevotella copri.[15] Los estudios evaluando a virus como posibles factores etiológicos de la artritis reumatoide han sido más productivos que los estudios similares con bacterias, habiéndose encontrado antígenos del virus de la rubeola y de adenovirus en la membrana sinovial de pacientes con artritis reumatoide.[15] Los virus más estudiados han sido el virus de Epstein-Barr, herpes virus, retrovirus y parvovirus B19.[15] Una revisión sistemática de 2015 concluye que no existe relación entre la infección por el virus de Epstein-Barr y el desarrollo de la artritis reumatoide.[30]
- Autoanticuerpos: Desde el descubrimiento del factor reumatoide en 1940, muchos investigadores han asociado a este autoanticuerpo con la fisiopatología de la artritis reumatoide. Aunque es claro que la presencia del factor reumatoide solo no causa la enfermedad, no hay duda de que los pacientes con títulos altos de anticuerpos tienen mayor probabilidad de enfermedad extraarticular que los pacientes seronegativos. El factor reumatoide y los anticuerpos antipéptidos cíclicos citrulinados pueden estar presentes en la sangre antes del desarrollo de la artritis y pueden ser vistos como un posible factor de riesgo para el desarrollo posterior de la enfermedad. La combinación de estos autoanticuerpos con marcadores genéticos como el epítopo compartido o el PTPN22 incrementan notablemente el riesgo de desarrollar la enfermedad.[15]
- Permeabilidad intestinal aumentada: Los pacientes con artritis reumatoide presentan una permeabilidad intestinal aumentada.[31][32][33] Esta pérdida crónica de la barrera protectora intestinal permite el paso de antígenos microbianos y dietéticos, lo cual puede desencadenar una respuesta inmunitaria que puede afectar a cualquier órgano o tejido corporal, dependiendo de la predisposición genética de cada persona.[31][32][33] Los dos factores más potentes que provocan aumento de la permeabilidad intestinal son ciertas bacterias intestinales y la gliadina (proteína que forma parte del gluten), tanto en celíacos como en no celíacos.[33][34][35]
- Otros factores de riesgo: La exposición al polvo de sílice, al amianto y los trabajos eléctricos y en la madera parecen aumentar el riesgo de artritis reumatoide. El consumo moderado de alcohol podría reducir el riesgo.[15] Algunos estudios han observado que la suplementación con vitamina D podría disminuir el riesgo, pero otros estudios no lo confirman,[36] lo mismo que el papel de los anticonceptivos orales que es equívoco.[15][27]
Patogenia
[editar]
La patogenia de la artritis reumatoide puede caracterizarse en tres etapas.[37]
Primera etapa o etapa preclínica: activación o cebado inmune
[editar]En la primera etapa, individuos sanos presentan una respuesta inmune frente a factores ambientales, tales como fumar o alteraciones de la flora intestinal, los cuales, mediante mecanismos de inmunidad adquirida propician la producción de autoanticuerpos.[37][38]
El proceso de producción de autoanticuerpos tarda en promedio de tres a cinco años, y en algunos casos hasta diez años, antes de manifestarse la inflamación articular. Estos auto anticuerpos son: factor reumatoide, anticuerpos antipéptidos cíclicos citrulinados, anticuerpos contra peptidil arginina deaminasa, anticuerpos contra proteínas carbamiladas y anticuerpos contra vimentina citrulinada. Los títulos y avidez de estos auto anticuerpos van aumentando gradualmente hasta que se produce un umbral sobre el cual se manifiesta clínicamente la enfermedad.[39]
Un elemento clave en esta fase es la producción de la enzima peptidil arginina deaminasa, que convierte la arginina en citrulina. El aumento de la citrulinización no es específico de la artritis reumatoide y ocurre ante cualquier estrés ambiental, como en los macrófagos de los alvéolos pulmonares en los fumadores.[40] Lo que es único en la artritis reumatoide es su propensión a la respuesta inmune hacia los neoepítopos creados por la citrulinización proteica, con la producción de anticuerpos antipéptidos cíclicos citrulinados, lo que podría iniciar el proceso inflamatorio.[41] Es poco probable que exista un único antígeno reumatoideo; probablemente, un amplio espectro de antígenos específicos articulares, como el colágeno tipo II o antígenos citrulinados inespecíficos, como la vimentina, enolasa o fibrinógeno sean los responsables de desencadenar la respuesta inmune. Como los anticuerpos, los niveles de diversas citocinas aumentan gradualmente en los años anteriores al desarrollo de los síntomas de la artritis reumatoide.[26]


Segunda etapa: inicio del ataque inflamatorio sobre las articulaciones
[editar]En segundo lugar, se produce ya una reacción inflamatoria específica. Esta reacción inflamatoria puede ser ya diagnosticada clínicamente con los primeros signos de la enfermedad. Una de las respuestas histopatológicas más precoces en la artritis reumatoide es la generación de nuevos vasos sanguíneos sinoviales, que se acompaña de la aparición de líquido sinovial en la articulación y de la migración de ambos tipos de linfocitos dentro de la membrana sinovial y de leucocitos polimorfonucleares en el líquido sinovial. A medida que los nuevos vasos se desarrollan, las citocinas producidas en la membrana sinovial en respuesta al factor de necrosis tumoral (TNF) activan las células endoteliales para producir moléculas de adhesión, facilitando así la diapedesis y extravasación de leucocitos en la membrana sinovial. La aparición de una cascada de citocinas proinflamatorias juega un papel clave en el inicio y perpetuación de la artritis reumatoide, originándose una proliferación de líneas celulares sinoviales, pasando de 1-3 capas de células de espesor a 6 o 7 y la formación del pannus. Las células inflamatorias son reclutadas en la sinovial por la acción de la interleuquina (IL)-17A, TNF, IL-1, IL-6, IL-18, factor de crecimiento endotelial vascular, IL-33, HMGB1 y quimiocinas.[42] Otras citocinas intervienen en su retención en la membrana sinovial por inhibición de la apoptosis y de otros mecanismos de la inmunidad innata; y otras intervienen en el proceso proliferativo/destructivo de la sinovitis, que se correspondería con el tercer paso en que la inflamación se convierte en un proceso crónico que conduce a la destrucción y remodelación de los tejidos articulares.[26]
No hay dudas de que tanto los linfocitos B como los T son esenciales en la enfermedad.[43] Las células T constituyen más del 50% de las células en la sinovial reumatoide, siendo la mayoría de ellos linfocitos T CD4+. Solo el 5% de las células de la sinovial son linfocitos B o células plasmáticas.[26] Los componentes celulares del líquido sinovial difieren de los de la sinovial; así los neutrófilos no se suelen observar en la membrana sinovial pero son abundantes en el líquido articular, y hay un predominio de células T CD4+ en la membrana sinovial, mientras que los linfocitos CD8+ son las que predominan en el líquido. Aunque se consideraba a la artritis reumatoide como una enfermedad del tipo celular Th1, caracterizada por aumento de la actividad de TNF, IL-2, INF gamma y IL-12, hoy se piensa que el tipo dominante de células T es Th17, siendo sus factores proinflamatorios más importantes las IL-17A y F.[44] El papel preciso de los linfocitos B y de los autoanticuerpos —como el factor reumatoide y los anticuerpos antipéptidos citrulinados— es incierto, aunque complejos de autoanticuerpos pueden iniciar o aumentar la inflamación articular. El papel de los linfocitos B está apoyado por el efecto terapéutico de los fármacos biológicos dirigidos contra las células B, que no es tan evidente con los fármacos que causan depleción de las células T.[45]
Tercera etapa: inflamación crónica
[editar]Una vez el proceso inflamatorio autoinmune está establecido, la sinovial reumatoide prolifera con la aparición del pannus, produciéndose enzimas que degradan el cartílago y hueso subyacente, originando la destrucción articular. El pannus reumatoide es un tejido de granulación formado por células sinoviales proliferadas, pequeños vasos sanguíneos, células inflamatorias y proteínas estructurales, que causa destrucción del tejido articular y la aparición de erosiones en la unión del cartílago con la sinovial. La sinovial reumatoide activada se convierte así en un tejido invasivo que puede degradar el cartílago y el hueso por invasión directa. La destrucción del cartílago, hueso y tendones en la artritis reumatoide es iniciada principalmente por metaloproteinasas. Igualmente, productos liberados por los neutrófilos en el líquido sinovial pueden causar considerable daño y potenciar la inflamación en la sinovial adyacente. La activación del sistema del complemento y sus interacciones con los inmunocomplejos son importantes en el líquido sinovial y en la interfase del cartílago. Otros factores adicionales, incluyendo óxido nítrico, neuropéptidos y metabolitos del ácido araquidónico también pueden contribuir a la patogénesis de la artritis reumatoide.[26]
Cuadro clínico
[editar]
La artritis reumatoide afecta primariamente las articulaciones, sin embargo también puede afectar a otros órganos o sistemas hasta en un 25% de pacientes.[46] En ocasiones puede ser difícil determinar si estos trastornos son una manifestación más de la enfermedad causada por el propio proceso reumatoide, una enfermedad asociada —comorbilidad— o si son efectos adversos de la medicación usada para tratarla —por ejemplo, la fibrosis pulmonar por el metotrexate o la osteoporosis por los corticoides—.[47]
Articulaciones
[editar]La artritis o inflamación de las articulaciones es la manifestación fundamental de la artritis reumatoide. Las articulaciones afectadas están hinchadas, calientes, dolorosas y rígidas, en especial al levantarse por la mañana o tras el reposo prolongado. Al principio pueden estar afectadas solo una o varias articulaciones, pero progresivamente se van sumando más articulaciones inflamadas —poliartritis—, siendo las que con más frecuencia se afectan las pequeñas articulaciones de las manos y los pies, aunque también es frecuente la afectación de otras articulaciones más grandes como los codos, los hombros, las rodillas o los tobillos.[48] La rigidez matinal es, con frecuencia, un dato destacado de la enfermedad y suele durar más de una hora. Estos datos ayudan a distinguir a la artritis reumatoide de otros problemas no inflamatorios de las articulaciones, como la artrosis u otros tipos de artritis. Las articulaciones se afectan habitualmente de un modo simétrico —afectando articulaciones semejantes en ambos lados del cuerpo—.[49] A medida que la enfermedad progresa, la inflamación articular causa erosiones y destrucción de las superficies articulares y daños tendinosos. Los dedos de las manos pueden sufrir diversas deformidades dependiendo de qué articulaciones y estructuras son las más lesionadas. Son deformidades típicas de la artritis reumatoide evolucionada los dedos en cuello de cisne, la deformidad en ráfaga cubital, la deformidad en boutonniere y el pulgar en Z.[48] La inflamación articular mantenida puede originar daños estructurales en las articulaciones, causando deformidad y pérdida funcional de la articulación afectada.[50][51]
Afectación de otros órganos o sistemas
[editar]- Piel
- Los nódulos reumatoideos se observan hasta en un 25% de los pacientes.[49] El nódulo reumatoideo típico es un nódulo subcutáneo, que puede medir desde unos pocos milímetros a unos centímetros y que aparece habitualmente sobre las prominencias óseas, como el olécranon –codos–, calcáneos, articulaciones metacarpofalángicas o sobre otras zonas sometidas a sobrecargas mecánicas repetidas.[2] Los nódulos se asocian con factor reumatoide positivo y artritis erosiva. Más raro es que se observen en órganos internos, en especial en los pulmones. Además de los nódulos subcutáneos, se pueden observar algunas formas de vasculitis cutáneas, como microinfartos alrededor del lecho ungueal, livedo reticularis —una coloración violácea o eritematosa de la piel en forma reticular, visible sobre todo en extremidades inferiores y que es debida a obstrucciones en los capilares cutáneos, pioderma gangrenoso, síndrome de Sweet, eritema nodoso, así como eritema palmar y fragilidad cutánea con equimosis —a menudo empeorada por el uso de corticoides—.
- Alteraciones hematológicas
- La anemia es, con mucho, la anomalía hematológica más común y es causada por diversos mecanismos.[52] La anemia típica de la artritis reumatoide tiene las características de una anemia de trastorno crónico,[49] donde le hierro es escasamente absorbido y también es secuestrado en los macrófagos.[53] Los hematíes son de tamaño y color normal —normocítica y normocrómica— y su presencia se relaciona con la actividad de la enfermedad y se asocia a un mayor daño estructural.[54] También son comunes las anemias por déficit de hierro, y no son raras las anemias megalobásticas en pacientes tratados con metotrexate o inmunosupresores.[49][52] De modo más excepcional la artritis reumatoide también puede causar una anemia hemolítica autoinmune.[55] En el síndrome de Felty se observa un descenso de los niveles de leucocitos —neutropenia—, junto con un aumento del tamaño del hígado y del bazo. Un aumento del número de plaquetas —trombocitosis— es frecuente encontrarlo cuando la inflamación no está controlada.[49]

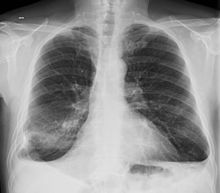
- Pulmón
- La fibrosis pulmonar es una complicación reconocida de la artritis reumatoide[56][57][58] y también puede ser una consecuencia de algunos tratamientos —por ejemplo del metotrexate y leflunomida—.[59] El síndrome de Caplan describe la presencia de nódulos reumatoideos pulmonares en pacientes con artritis reumatoide y exposición al polvo de sílice o carbón. Los derrames pleurales no son raros en el contexto de la artritis reumatoide y obligan a descartar otras posibles causas. Estas alteraciones pulmonares, además de la bronquiolitis obliterante se denominan globalmente enfermedad pulmonar reumatoide, estimándose que al menos una cuarta parte de los pacientes con artritis reumatoide desarrollan afectación pulmonar.[60][61]
- Corazón y vasos sanguíneos
- Los pacientes con artritis reumatoide pueden presentar algunas complicaciones cardiacas asociadas a la propia enfermedad incluyendo pericarditis, afectación valvular, nódulos en las válvulas cardíacas y fallo ventricular por miocarditis.[49] Una complicación grave es la vasculitis reumatoide, caracterizada lesiones cutáneas, lesiones de nervios periféricos –mononeuritis múltiple–, isquemia intestinal y otras posibles lesiones sistémicas.[62][49]
- Ojos
- El ojo se ve afectado directamente por la enfermedad en forma de epiescleritis, que puede ser avanzada y progresar a una escleromalacia perforante. Más común es el daño indirecto por una queratoconjuntivitis seca en el contexto de un síndrome de Sjögren secundario, que es sequedad de los ojos y de la boca causada por la infiltración linfocitaria de las glándulas lagrimales y salivares. Cuando es grave, la sequedad de la córnea puede originar queratitis y pérdida de visión.[63]
- Riñón
- La enfermedad renal en la artritis reumatoide es poco frecuente y puede ser debida a la propia enfermedad o al tratamiento. Una glomerulonefritis mesangial de origen incierto se puede observar en 5-10% de los pacientes.[64] Puede ocurrir amiloidosis renal secundaria (AA) como consecuencia de la inflamación crónica.[49] Los tratamientos con sales de oro y D-Penicilamina, ambos en desuso en la actualidad, eran hace unas décadas una causa relativamente frecuente de nefropatía membranosa. Más frecuente es la nefrotoxicidad por AINEs, incluyendo nefritis intersticial aguda, que a menudo ocurre en unión con síndrome nefrótico. La terapia crónica con AINEs también puede causar infrecuentemente necrosis papilar.[64]
- Hígado
- La afectación hepática en la artritis reumatoide es esencialmente asintomática. La artritis reumatoide activa se asocia con alteraciones en las pruebas de función hepática, que se normalizan con el control de la actividad inflamatoria.[65] En el síndrome de Felty se puede observar un aumento del tamaño del hígado (hepatomegalia) en un elevado porcentaje de pacientes.[65]
- Alteraciones neurológicas
- El problema más habitual es un síndrome del túnel carpiano causado por la compresión del nervio mediano por la inflamación a nivel de la muñeca.[65] También se puede observar una luxación atlas-axis, debido a la erosión de la odontoides y/o de los ligamentos transversos en la unión de la columna cervical con el cráneo. Si el desplazamiento es superior a 3 mm puede originarse un desplazamiento vertebral y compresión de la médula espinal. La aparición de una marcha torpe y trastornos de esfínteres son las manifestaciones iniciales, pero sin los cuidados apropiados puede progresar a tetraplejia.[65] También pueden ocurrir neuropatías periféricas y mononeuritis múltiple en el contexto de la vasculitis reumatoide.[65]
- Síntomas constitucionales
- Algunos síntomas constitucionales como cansancio, fiebre de bajo grado, malestar, pérdida de apetito y pérdida de peso son manifestaciones sistémicas comunes que se pueden observar en los pacientes con artritis reumatoide activa.
Comorbilidad
[editar]Las comorbilidades en el seno de la artritis reumatoide predicen, independientemente de otros factores, la incapacidad asociada a la enfermedad y la mortalidad, por lo que es necesario un abordaje completo de la enfermedad que incluya la evaluación y el tratamiento específico de estas enfermedades asociadas. Una mejor identificación, comprensión y manejo de las comorbilidades en la artritis reumatoide tiene un gran potencial para mejorar la calidad de vida y la supervivencia de los pacientes.[66]
La artritis reumatoide es una enfermedad proaterogénica asociada con un incremento de la mortalidad cardiovascular.[67] Las personas con artritis reumatoide están más predispuestas al desarrollo de arteriosclerosis y a un mayor riesgo de enfermedad cardiovascular —infartos de miocardio e ictus—.[68] La enfermedad cardiovascular es considerada como la causa principal de mortalidad en la artritis reumatoide, siendo responsable de aproximadamente la mitad de todas las muertes.[69][70] Aunque la incidencia global de enfermedad cardiovascular en la artritis reumatoide no parece estar desproporcionadamente elevada, sí parece que puede ocasionar una muerte más temprana en los pacientes con artritis reumatoide, un efecto que podría ser más pronunciado en los varones.[69] La patogénesis de la enfermedad cardiovascular en la artritis reumatoide es multifactorial, estando implicados los factores de riesgo tradicionales y la inflamación crónica.[67][71][72]
Aunque diversos estudios sugieren un riego aumentado de ciertos tipos de neoplasias en los pacientes con artritis reumatoide, algunos investigadores no han encontrado diferencias significativas en la incidencia global de cáncer en los pacientes con artritis reumatoide frente a los controles. A pesar de estos datos conflictivos acerca del riesgo de cáncer global, existe evidencia acumulada de que los pacientes con artritis reumatoide tienen sustancialmente más posibilidades de desarrollar neoplasias linfoproliferativas, en especial linfomas, aunque son poco frecuentes.[73] A su vez, los pacientes con artritis reumatoide consistentemente parecen presentar un menor riesgo de neoplasias gastrointestinales, específicamente cáncer colorrectal.[69]
Las complicaciones infecciosas, en especial infecciones pulmonares y sepsis generalizadas, se encuentran claramente incrementadas en la artritis reumatoide, siendo una causa principal de mortalidad y morbilidad.[70] La inmunosupresión desempeña un papel fundamental en el desarrollo de infecciones, aunque como en el caso de otras comorbilidades es difícil distinguir entre los efectos intrínsecos de la propia enfermedad y los efectos de los fármacos usados para tratarla, probablemente contribuyendo ambos a incrementar el riesgo.[69]
La patogénesis de la osteoporosis asociada a la artrtis reumatoide es multifactorial. Incluso en ausencia de terapia con corticoides, la artritis reumatoide incrementa el riesgo global de osteoporosis y fracturas, influyendo otros factores como la menor realización de ejercicio, la época postmenopáusica y la propia actividad de la enfermedad, siendo más frecuente en la enfermedad más grave y de larga evolución.[69]
La enfermedad celíaca no es una enfermedad únicamente digestiva, sino autoinmune sistémica que puede afectar a diversos órganos y tejidos corporales. La artritis reumatoide y la enfermedad celíaca comparten los mismos mecanismos inmunológicos, por lo que suelen aparecer asociadas.[74][75][76][77] De hecho, las personas con artritis reumatoide pertenecen a los denominados "grupos de riesgo" de desarrollar enfermedad celíaca, por lo que se recomienda que sean evaluadas.[78]
- Enfermedades gastrointestinales
La morbilidad y mortalidad gastrointestinal del tracto superior —estómago y duodeno— debida al uso de AINEs está incrementada en los pacientes con artritis reumatoide.[69] Asimismo, presentan un riesgo aumentado de desarrollar ciertas enfermedades gastrointestinales, como las enfermedades inflamatorias intestinales.[75]
- Otras comorbilidades
Además de las referidas son frecuentes otras enfermedades asociadas que influyen de modo notable en la calidad de vida y funcional de los pacientes con artritis reumatoide, como una mayor prevalencia de otras enfermedades autoinmunes, ansiedad, depresión y fibromialgia. En un estudio frecuente se observaron diferencias de género en las enfermedades asociadas, siendo más frecuentes en las mujeres la depresión, fibromialgia e hipotiroidismo; y en los varones la enfermedad cardiovascular y la diabetes.[79]
Diagnóstico
[editar]El diagnóstico definitivo de la artritis reumatoide depende básicamente de la presencia de las alteraciones clínicas características y de la exclusión de otros procesos inflamatorios que pueden cursar con manifestaciones semejantes.[80] Un cuadro clínico típico de poliartritis inflamatoria simétrica, con afectación de las articulaciones pequeñas de manos y pies, respetando el esqueleto axial con la excepción de la columna cervical, sugiere el diagnóstico.[81] La presencia de rigidez matutina o la ocasional observación de nódulos subcutáneos apoyan el diagnóstico. De forma adicional, la presencia de factor reumatoide, un líquido sinovial inflamatorio y las alteraciones radiológicas de desmineralización ósea y erosiones en las articulaciones afectadas, ayudarán al reumatólogo a confirmar el diagnóstico.[81] La observación aislada de una prueba positiva para el factor reumatoide o de una velocidad de sedimentación elevada, sobre todo en personas de edad avanzada, sin presencia de inflamación en las articulaciones no debe utilizarse como diagnóstico de la artritis reumatoide.[81] En estos datos se basan los criterios de 1987 de la American Rheumatism Association (ARA) que han sido utilizados hasta estos últimos años, constituyendo una guía útil para establecer el diagnóstico.[80]
| Criterios de 1987 para la clasificación de la artritis reumatoide |
|---|
| 1. Rigidez matutina de más de 1 hora de duración. |
| 2. Artritis de 3 o más articulaciones observada por un médico. |
| 3. Artritis de las articulaciones de la mano. |
| 4. Artritis simétrica. |
| 5. Nódulos reumatoides. |
| 6. Factor reumatoide positivo. |
| 7. Alteraciones Rx que incluyan osteoporosis yuxtaarticular o erosiones. |
| Se necesitan 4 de los 7 criterios para clasificar a un paciente como afectado por artritis reumatoide. Los criterios del 1 al 4 deben estar presentes al menos durante 6 semanas. |
Estos criterios tienen una sensibilidad del 91-94% y una especificidad del 89% cuando se utilizan para clasificar a los pacientes con artritis reumatoide en comparación con los enfermos que presentan otros procesos reumáticos. No obstante, el hecho de no cumplir estos criterios, sobre todo durante las primeras fases de la enfermedad, no excluye el diagnóstico. Por otra parte, otras enfermedades reumatológicas como el lupus eritematoso sistémico o la artritis psoriásica pueden cumplir estos criterios si adoptan un patrón de afectación articular semejante a la artritis reumatoide.[81]
En los pacientes que presentan un cuadro típico ya establecido el diagnóstico de artritis reumatoide es fácilmente realizado por el reumatólogo. Sin embargo, en ocasiones el diagnóstico es más difícil de establecer, sobre todo en las fases iniciales de la enfermedad, cuando el paciente puede presentar solo síntomas generales o bien artralgias o artritis intermitente, pudiendo ser necesario un período de observación antes de establecer el diagnóstico definitivo.[82] En la mayoría de los individuos, la enfermedad adquiere sus alteraciones clínicas características al cabo de uno o dos años tras su inicio.[81] El retraso medio desde el inicio de la enfermedad hasta que se estable el diagnóstico es de nueve meses,[81] debido a que con frecuencia los síntomas iniciales son inespecíficos.
Los criterios de 1987 fueron formulados para distinguir a los pacientes con artritis reumatoide establecida de aquellos pacientes con otras enfermedades reumáticas; sin embargo, no permiten distinguir a los pacientes con artritis reumatoide de nueva aparición de los que padecen alguna otra forma de artritis inflamatoria.[80] Además, en los pacientes con artritis inicial, estos criterios no permiten diferenciar de manera fiable a aquellos pacientes que van a padecer más adelante un enfermedad persistente, incapacitante o erosiva, de aquellos que no la van a presentar.[81][80] Por estos motivos en 2010 se desarrollaron unos nuevos criterios conjuntos del ACR (American College of Rheumatology) y EULAR (European League Against Rheumatism).[13] Los criterios ACR/EULAR de 2010 permiten la clasificación como artritis reumatoide con la presencia de sinovitis de al menos una articulación, la ausencia de un diagnóstico alternativo que explique mejor la artritis, y la obtención de una puntuación de al menos 6 de los 10 posibles puntos. Son articulaciones pequeñas: muñecas, metacarpofalángicas (MCFs), interfalángicas proximales (IFPs), interfalángica del pulgar y de 2 a 5.ª metatarsofalángicas (MTFs). Son articulaciones grandes: hombros, codos, caderas, rodillas y tobillos.
| Criterios ACR/EULAR 2010 para la clasificación de artritis reumatoide | ||
|---|---|---|
| Criterio | Variables | Puntos |
| Número de articulaciones afectadas | 2 a 10 articulaciones grandes 1 a 3 articulaciones pequeñas 4 a 10 articulaciones pequeñas más de 10 articulaciones (al menos 1 pequeña) |
1 2 3 5 |
| Serología (FR o PCC) | positiva débil positiva fuerte (más de tres veces valor normal) |
2 3 |
| Reactantes de fase aguda (VSG o PCR) | VSG o PCR elevadas | 1 |
| Duración de la artritis | más de 6 semanas | 1 |
| Para la clasificación como artritis reumatoide se exige la presencia de sinovitis de al menos una articulación, la ausencia de un diagnóstico alternativo que explique mejor la artritis y una puntuación de al menos 6 de los 10 puntos posibles. | ||
Pruebas de laboratorio
[editar]Ninguna prueba de laboratorio es diagnóstica de artritis reumatoide; sin embargo, algunas ayudan a confirmar el diagnóstico y a anticipar el pronóstico de la enfermedad.
- Factor reumatoide
- Son anticuerpos dirigidos contra la fracción Fc de la IgG. Se encuentra en el 70-80% de los pacientes con artritis reumatoide. Los títulos más elevados se asocian en general con enfermedades más graves, con nódulos reumatoideos y peor evolución. Se puede encontrar hasta en un 5% de la población sana mayor de 60 años y también está presentes en otras enfermedades reumáticas autoinmunes, como el síndrome de Sjögren, el lupus eritematoso sistémico o la esclerodermia, así como en infecciones bacterianas crónicas, infecciones virales, hepatopatías crónicas y enfermedades pulmonares crónicas.[2][49]
- Anticuerpos antipéptidos cíclicos citrulinados
- Su sensibilidad para el diagnóstico de la artritis reumatoide es semejante a la del factor reumatoide pero tienen una mayor especificidad.[83] Tienen utilidad en la confirmación del diagnóstico de la enfermedad en pacientes con artritis inicial y en la identificación de pacientes con peor pronóstico.[49]
- Velocidad de sedimentación globular (VSG) y Proteína C reactiva (PCR)
- Son indicadores inespecíficos de la actividad inflamatoria y, además de elevarse en la artritis reumatoide y otros cuadros inflamatorios articulares, también se elevan en otros procesos inflamatorios, en las infecciones y neoplasias. Tienen utilidad en la detección del proceso inflamatorio, en el seguimiento de la actividad de la enfermedad y en la valoración de la respuesta al tratamiento.[84][85]
Técnicas de imagen
[editar]
La radiografía convencional es la técnica de imagen estándar de la artritis reumatoide. Los primeros signos radiológicos son la osteoporosis yuxtaarticular y el aumento de partes blandas. Estos cambios se siguen de la disminución del espacio articular, que corresponde a la pérdida de cartílago articular, y la aparición de erosiones óseas en las zonas adyacentes al cartílago articular. El tiempo mínimo para la detección de cambios estructurales en las radiografías está entre 6 y 12 meses, detectándose erosiones radiológicamente en el 50% de los pacientes en el primer año de la enfermedad.[49] En la práctica clínica se utilizan las radiografías para el diagnóstico de la enfermedad, para valorar la gravedad del daño articular y para evaluar su progresión. El ultrasonido y la resonancia magnética son técnicas más sensibles que la radiología convencional.
Diagnóstico diferencial
[editar]Una evaluación global inicial por el reumatólogo, valorando las características de las quejas articulares y extraarticulares, junto con los posteriores exámenes complementarios analíticos y radiológicos, llevarán al especialista a realizar el diagnóstico de artritis reumatoide. Otras causas de poliartritis inflamatoria simétrica pueden confundirse con una artritis reumatoide —en especial en las fases iniciales— como son otros trastornos del tejido conectivo, las espondiloartritis, en especial la artritis psoriásica, y las artritis de origen vírico (especialmente, las artritis asociadas a parvovirus B19 y virus de la hepatitis C).[80] Es importante establecer el diagnóstico de la artritis reumatoide al inicio de la enfermedad para que pueda iniciarse un tratamiento eficaz de modo temprano.
- Otros trastornos del tejido conjuntivo
- El lupus eritematoso sistémico, la esclerosis sistémica, la polimiositis, la enfermedad mixta del tejido conectivo y el síndrome de Sjögren pueden causar una poliartritis con una distribución como la observada en la artritis reumatoide. Además, el factor reumatoide puede estar presente en todas de estas enfermedades y con una frecuencia especialmente alta en el síndrome de Sjögren. Por otra parte, ocasionalmente los pacientes con una enfermedad del tejido conjuntivo definida, pueden manifestar características y criterios de otra conectivopatía, lo que se llama un síndrome de solapamiento (p.e: un paciente con un lupus desarrolla una artritis erosiva y nódulos reumatoideos, haciendo reconsiderar el diagnóstico hacia un síndrome “rupus” o solapamiento de artritis reumatoide y lupus eritematoso sistémico).[80]
- Espondiloartropatías inflamatorias
- Entre las que se incluyen la espondilitis anquilosante, la artropatía psoriásica, la artritis reactiva y la artritis asociada a enfermedad inflamatoria intestinal. Todos estos cuadros se pueden confundir con una artritis reumatoide cuando se manifiestan fundamentalmente con artritis periférica, aunque su modo de presentación más habitual es una oligoartritis asimétrica. Puede dar más lugar a confusión la artritis psoriásica –en especial en los casos en que la artritis precede a las lesiones cutáneas– si adopta un patrón de afectación articular similar a la artritis reumatoide, aunque habitualmente la psoriasis cutánea aparece antes que la artritis, proporcionando la clave para el diagnóstico. Cuando la artritis precede a la psoriasis, sugiere este origen una historia familiar de psoriasis, la afectación de las articulaciones interfalángicas distales (IFDs), la presencia de dactilitis —tumefacción difusa de un dedo—, una menor simetría o la ausencia de factor reumatoide.[82]
- Reumatismo palindrómico
- El reumatismo palindrómico se caracteriza por episodios de inflamación articular, afectando a una o varias articulaciones, durando entre horas y días, con períodos libres de síntomas de días a meses. Algunos pacientes acabarán desarrollando una enfermedad reumatológica bien definida, la mayor parte de estos (entre 30-60 %) una artritis reumatoide, y algunos otros un lupus eritematoso sistémico u otras enfermedades sistémicas. Los pacientes con anticuerpos antipéptidos cíclicos citrulinados positivos es más probable que evolucionen hacia una artritis reumatoide. El seguimiento y la evaluación serológica específica pueden ayudar a diferenciar estos cuadros.
- Artritis víricas
- La distribución de la afectación articular en pacientes con poliartritis asociada al parvovirus B19 puede ser muy parecida a la de la artritis reumatoide, pero la intensidad de la inflamación suele ser considerablemente menor, y se resuelve espontáneamente en unas semanas o meses en la mayoría de individuos, sin tratamiento. La presencia de anticuerpos IgM específicos antiparvovirus B19 confirmará el diagnóstico. La poliartritis asociada a la hepatitis C con crioglobulinemia puede suponer un dilema diagnóstico, que suele cursar con factor reumatoide positivo. También es frecuente la aparición de artritis en las infecciones por los virus de la rubeola y la hepatitis B que se podría confundir con una artritis reumatoide en sus fases iniciales.[80]
- Artritis microcristalina
- En algún caso de presentación poco usual puede presentarse de modo parecido a la artritis reumatoide la enfermedad por depósito de PPCD o pseudogota y menos probablemente con una gota tofácea crónica.[82]
- Polimialgia reumática
- Puedes ser motivo de confusión en los pacientes de más edad, ayudando a diferenciarlas el dolor y la rigidez fundamentalmente en la raíz de las extremidades (hombros y caderas) con escasa o nula sinovitis que se observa en la polimialgia.[80]
- Otros cuadros articulares
- Otras causas de artritis inflamatoria crónica suelen ser menos simétricas y típicamente de presentación monoarticular u oligoarticular, como las artritis de origen séptico, que habitualmente se manifiestan como una monoartritis aguda en las infecciones bacterianas y más crónica en las infecciones por micobacterias y hongos. La artritis brucelar y la enfermedad de Lyme ocasionalmente se han manifestado como un poliartritis crónica y habría que considerarlas en las zonas donde son endémicas. Otros trastornos como el hipotiroidismo o hipertiroidismo, el hiperparatiroidismo, o el mieloma múltiple pueden causar poliartralgias y en el caso del hipotiroidismo es posible observar artritis de poca intensidad. Las neoplasias ocasionalmente pueden manifestarse como una poliartritis paraneoplásica o como una osteoartropatía hipertrófica, que habitualmente se diferencian bien de la artritis reumatoide por la presencia de otras alteraciones asociadas.[82] La enfermedad del suero-like, la enfermedad de Still del adulto o la sarcoidosis, pueden manifestarse con características articulares semejantes a la artritis reumatoide, pero ayuda a diferenciarlas la presencia de otras alteraciones clínicas o analíticas. Otros cuadros no inflamatorios difícilmente pueden ser confundidos con la artritis reumatoide, como la artrosis o los dolores difusos de la fibromialgia.[80][82]
Evolución y pronóstico
[editar]La evolución de la artritis reumatoide es variable. Aproximadamente un 15-20% de los pacientes tiene un curso intermitente, con periodos de exacerbación y remisión de los síntomas, y relativamente un buen pronóstico. Sin embargo la mayoría tienen una enfermedad progresiva, siguiendo unos pacientes un curso más lento y otros un curso más rápido. El pronóstico de la enfermedad dependerá del grado de daño articular, del estado físico funcional del paciente, de la salud psicológica y de la presencia de comorbilidades.[64]
La artritis reumatoide es la enfermedad musculoesquelética que produce mayor grado de incapacidad. Esta incapacidad funcional aparece pronto en el curso de la enfermedad y progresa de forma lineal, de modo que a los 10 años de evolución el 50% de los pacientes son incapaces de desarrollar un trabajo a tiempo completo; aunque datos más recientes encuentran tasas similares de empleo entre los pacientes con o sin artritis reumatoide.[86] A lo largo de la evolución, un 10% de los pacientes serán incapaces de realizar por sí mismos actividades cotidianas como lavarse, vestirse o comer. Los pacientes con un comienzo de la enfermedad antes de los 40 años tienen un peor pronóstico funcional que los que empiezan después de los 70 años.[49] Es probable que estos datos, generados en épocas con estrategias de tratamiento menos eficaces que las actuales, sean mejores en la actualidad.[87]
La artritis reumatoide es una enfermedad potencialmente fatal.[64] La expectativa de vida para un paciente con artritis reumatoide puede verse reducida entre 3 y 10 años,[87] o incluso más en aquellos pacientes con enfermedad más grave,[49] aunque la mortalidad debida directamente a la artritis reumatoide es baja —9.8% de las muertes—.[64] Los mecanismos por los que puede ocurrir una muerte prematura en la artritis reumatoide incluyen enfermedad cardiaca, amiloidosis, lesión medular por inestabilidad de columna cervical e insuficiencia respiratoria por fibrosis pulmonar; sin embargo, las causas de exceso de mortalidad son las mismas que en la población general, fundamentalmente la mortalidad de origen cardiovascular, las infecciones y los tumores.[64]
Individualmente, los pacientes con artritis reumatoide pueden tener un curso diferente dependiendo de diversas variables clínicas, analíticas o epidemiológicas. Son factores predictores de un mal pronóstico general de la enfermedad:[49]
- La afectación de múltiples articulaciones.
- La afectación temprana de grandes articulaciones.
- Manifestaciones extra-articulares (incluyendo nódulos subcutáneos).
- Factor reumatoide positivo o anticuerpos antipéptidos cíclicos citrulinados positivos.
- La elevación de la VSG (>60 mm) y PCR (>2 veces el valor normal).
- La presencia de HLA DR4 y el epítopo compartido.
- La presencia de cambios radiológicos tempranos.
- Una capacidad funcional disminuida al inicio.
- El retraso en el inicio de un tratamiento eficaz.
Tratamiento
[editar]
No hay cura para la artritis reumatoide, pero los tratamientos actuales pueden mejorar los síntomas y retrasar el progreso de la enfermedad. Los objetivos del tratamiento son reducir al mínimo los síntomas —como el dolor y la inflamación—, prevenir los daños estructurales de las articulaciones —por ejemplo, las erosiones óseas visibles en rayos X—, y mantener la capacidad funcional del paciente.[4][88] Los estudios en conjunto indican que el tratamiento precoz de la enfermedad con fármacos modificadores de la enfermedad (FAMEs) mejora la evolución a largo plazo, minimiza la progresión del daño estructural y mejora la calidad de vida de los pacientes.[49][89]
Medidas generales
[editar]Ejercicio y reposo: El ejercicio físico regular ayuda a mantener el tono y la fuerza muscular, así como un buen estado físico en general. En los períodos de poca inflamación es muy recomendable practicar algún ejercicio físico que no sobrecargue las articulaciones afectadas y que no implique saltos o choques. En las fases de mayor actividad de la enfermedad es mejor el reposo.[90] El tratamiento con un fisioterapeuta puede ocasionalmente ser necesario.
Dieta: La obesidad supone una carga adicional para las articulaciones de las caderas, de las rodillas y de los pies; por este motivo es recomendable adelgazar o evitar el sobrepeso según los casos. La dieta mediterránea típica, rica en legumbres, ensaladas, aceite de oliva y pescado, puede ser beneficiosa para la salud general y para disminuir el riesgo cardiovascular.[90]
No fumar: el tabaco aumenta el riesgo de artritis reumatoide y de artritis reumatoide más grave. Es, por tanto, importante dejar de fumar para mejorar el pronóstico articular y para reducir el riesgo cardiovascular y otras comorbilidades.[91]
Cuidado regular de la dentadura: la enfermedad periodontal es un factor de riesgo emergente para el desarrollo de la artritis reumatoide.[28][29] Por otra parte, la frecuente existencia de un síndrome de Sjögren asociado, con sequedad bucal y el consiguiente deterioro dental, hacen aconsejables las visitas regulares al odontólogo.
Calzado: el uso de un calzado adecuado y/o de plantillas de descarga puede ser necesario cuando exista afectación de los pies —tobillos, tarsos o metatatarsofalángicas—.
Dispositivos de ayuda: En ortopedias y tiendas específicas se pueden encontrar utensilios que pueden ser de gran ayuda para las tareas domésticas y para mejorar la capacidad funcional cuando existen deformidades articulares y/o dificultades para la realización de algunas tareas concretas.[90]
Fármacos para el alivio de los síntomas
[editar]- Fármacos antiinflamatorios no esteroideos (AINEs)
- Los AINEs reducen los síntomas y signos de la enfermedad, pero no tienen efecto sobre su evolución, ni evitan la progresión radiográfica. Los AINEs deben ser utilizados con precaución en las personas con problemas gastrointestinales, cardiovasculares, o renales.[92][93][94] Los inhibidores selectivos de la COX-2, como celecoxib y etoricoxib, son igual de eficaces que los no selectivos pero tienen un perfil de seguridad gastrointestinal superior.[95] No obstante, unos y otros tienen cuestionada su seguridad cardiovascular.[92][96] Los medicamentos para la prevención de la úlcera gastroduodenal no se recomiendan de forma rutinaria, sino solo en aquellos pacientes con alto riesgo —edad superior a 65 años, dosis altas de AINEs, uso concomitante de corticoides, historia previa de úlcera gástrica o duodenal, o de sangrado gastrointestinal, consumo elevado de alcohol o tabaco, tratamiento antiagregante o anticoagulante, o tratamiento con antidepresivos inhibidores de la recaptación de serotonina—.[92][97]
- Corticoides
- Los corticoides mejoran los síntomas y signos de la artritis reumatoide y disminuyen la progresión del daño radiológico. La dosis óptima y la duración del tratamiento no están totalmente definidas, aunque es habitual usarlos en las fases iniciales de la enfermedad y en los períodos de reactivación.[98] No se recomienda el uso mantenido de dosis medias y altas de corticoides, por sus notables efectos adversos; sin embargo, muchos pacientes se mantienen con dosis bajas —por debajo de 7,5 mg/día de prednisona— durante años,[99] aunque su utilización es motivo de controversia.[100][101][102] Ocasionalmente, puede ser muy eficaz la infiltración —inyección intraarticular— de una articulación especialmente inflamada con un corticoide de depósito.[103][104]
Fármacos modificadores de la enfermedad (FAMEs)
[editar]Los FAMEs son el tratamiento básico y fundamental de la artritis reumatoide.[4] Se trata de un grupo de fármacos, poco relacionados entre sí, salvo por su capacidad para enlentecer la progresión de la enfermedad o producir un efecto modificador de la misma.[4] Deben iniciarse precozmente en la enfermedad, pues en las fases iniciales pueden conseguir la remisión de la enfermedad en aproximadamente la mitad de las personas y son mejores los resultados en general.[4] Estos fármacos pueden ser utilizados de modo aislado o en combinación de varios. Se pueden distinguir los FAMEs convencionales y los FAMEs biológicos.
- FAMEs convencionales
- Metotrexato: Es el FAME más eficaz y el de primera elección en el tratamiento de la artritis reumatoide. Se toma en una dosis única semanal, habitualmente entre 10-25 mg. Se usa asociado al ácido fólico para evitar algunos de sus efectos secundarios.[105] Se puede administrar por vía oral y por vía subcutánea, siendo mayor la biodisponibilidad cuando se usa esta última vía y menores los efectos adversos gastrointestinales.[106][107] Varios metaanálisis han demostrado que el metotrexato tiene el mejor balance eficacia/toxicidad de todos los FAMEs.[108] El tratamiento requiere controles periódicos para evitar la posible toxicidad hepática, hematológica, gastrointestinal y pulmonar. El metotrexato es teratógeno, por lo que en las mujeres en edad fértil se recomienda el uso anticonceptivos para evitar el embarazo, así como suprimirlo si se planea el embarazo.[2][4]
- Leflunomida: Su eficacia es similar al metotrexato y se puede considerar como una alternativa al mismo. Sus efectos adversos también son muy semejantes al metotrexato.[109]
- Antipalúdicos de síntesis (cloroquina e hidroxicloroquina): Son eficaces disminuyendo los síntomas y signos de la enfermedad, pero no tienen un efecto demostrable sobre la progresión radiológica. Su rara toxicidad retiniana obliga a controles oftalmológicos periódicos.[2]
- Sulfasalazina: Es eficaz controlando los síntomas y signos de la enfermedad y disminuyendo la progresión radiológica.[4] Es eficaz en asociación con otros FAMEs.
- Otros: sales de oro, D-penicilamina, ciclosporina, azatioprina, ciclofosfamida o doxiciclina son medicamentos en desuso en la actualidad para el tratamiento de la artritis reumatoide, debido al número importante de acontecimientos adversos que ocurren durante su administración y a su efecto terapéutico modesto.[4]
- FAMEs biológicos
Los fármacos biológicos son versiones de moléculas naturales elaboradas mediante biotecnología —por ejemplo, anticuerpos monoclonales— y diseñadas para actuar específicamente sobre mediadores patogénicos de la inflamación y la lesión articular.[4] En general, los fármacos biológicos son considerados como FAMEs si han demostrado en ensayos clínicos amplios que inhiben significativamente la progresión de la lesión articular.[4] Los fármacos biológicos habitualmente se utilizan en pacientes con artritis reumatoide moderada o avanzada que no responde al metotrexato y otros FAMEs convencionales.[110] A menudo se utilizan en combinación con metotrexato o leflunomida, lo que mejora su eficacia —salvo el tocilizumab que es igual de eficaz en monoterapia—.[111]
El fármaco biológico de inicio suele ser un antagonista del factor de necrosis tumoral alfa (TNFα). En los pacientes que no responden a los antagonistas del TNFα, se suelen probar otros biológicos, consiguiéndose buenas respuestas en un buen porcentaje de pacientes.[112] Los problemas fundamentales de los fármacos biológicos son su elevado precio[113] y su potencial asociación con efectos adversos graves, en especial tuberculosis y otras infecciones.[114] Estos fármacos incluyen:
- Infliximab, adalimumab, golimumab, certolizumab pegol y etanercept: antagonistas del factor de necrosis tumoral alfa (TNFα).[115][116]
- Rituximab: anticuerpo monoclonal contra las células B.[117][118]
- Tocilizumab: inhibidor de la interleuquina-6.[119][120]
- Anakinra: bloqueador de la interleuquina-1.[121]
- Abatacept: modulador de la coestimulación de células T.[122][123]
- Tofacitinib: inhibidor de la quinasa Janus —JAK— de administración oral. Propiamente no es un biológico, sino un FAME sintético. Autotizado por la FDA americana.[124][110]
Tratamiento quirúrgico
[editar]Cuando la artritis reumatoide no se puede controlar adecuadamente mediante el tratamiento, la inflamación puede acabar originando lesiones graves e irreversibles en la membrana sinovial, el cartílago articular y el hueso. Es en estos casos cuando se suele recurrir a la cirugía ortopédica o reparadora, con el fin de reducir el dolor, mejorar la movilidad de las articulaciones afectadas y dotar de una mayor autonomía al paciente con esta enfermedad.[125]
Las articulaciones gravemente afectadas, en especial la cadera y la rodilla pueden requerir una prótesis articular. Menos frecuentes son las operaciones en manos y pies, que eran más frecuentes hace unas décadas.[126]
Los procedimientos quirúrgicos más habituales incluyen la sinovectomía (extirpar la membrana sinovial que recubre la articulación, para evitar la deformación), la tenosinovectomia (extirpar la membrana inflamada que recubre al tendón), la transposición tendinosa (trasladar la función de un tendón dañado a otro tendón menos importante), la artroplastia (reconstruir la articulación, reemplazando las partes dañadas con prótesis de metal y plástico) o la artrodesis (fijar o fusionar definitivamente la articulación para evitar el dolor de moverla).[127]
Tratamientos alternativos
[editar]Aunque algunos estudios muestran efectos beneficiosos de una amplia variedad de modalidades terapias complementarias, estos estudios son a menudo de escasa calidad y, en general, faltan ensayos clínicos aleatorizados y controlados que permitan sacar conclusiones definitivas. La artritis reumatoide es una enfermedad grave y en ningún caso se aconseja cambiar el tratamiento médico convencional, de eficacia probada, por un producto o una práctica de utilidad no demostrada.[128] No existe una base científica para sugerir que los suplementos a base de hierbas que se anuncian como "naturales" sean más seguros que el uso de medicamentos convencionales, ya que ambos son productos químicos, y algunos productos con la etiqueta de "natural", pueden ser tóxicos o mortales si se consumen.[128]
Algunas evidencias apoyan el consumo de los ácidos grasos omega-3 y ácido gamma-linolénico en la artritis reumatoide.[128] El beneficio de los omega-3 parece modesto pero consistente,[129] y otro tanto ocurre con la administración del ácido gamma-linolénico, que puede reducir el dolor, el número de articulaciones dolorosas y la rigidez.[130]
El tratamiento con Tripterygium wilfordii —"hierba del trueno del dios de la vid"—, parece en algún estudio ser de eficacia semejante al metotrexato usados ambos en monoterapia y con mejores respuestas con la asociación de ambos.[131] Sin embargo, esta hierba no parece estar exenta de posibles efectos adversos graves.[128]
La suplementación con cápsulas de Lactobacillus casei, como terapia adjunta, puede ayudar a mejorar los síntomas y los datos de actividad inflamatoria de la enfermedad.[132]
El yoga parece ejercer efectos beneficiosos sobre los pacientes con artritis.[133] Algunas investigaciones encuentran beneficioso un programa de poses tradicionales de yoga modificadas y adaptadas de acuerdo a las limitaciones derivadas de la AR, técnicas de respiración profunda y técnicas de relajación, así como de meditación; ya que ayudan a disminuir el dolor e inflamación en las articulaciones.[134]
La dieta sin gluten es beneficiosa en algunos pacientes con artritis reumatoide, aunque las evidencias no son concluyentes. Se ha demostrado que una dieta sin gluten vegana es eficaz en el control de la inflamación y los síntomas de la artritis reumatoide.[74] Asimismo, tiene un efecto beneficioso sobre la dislipidemia, cuyo riesgo de desarrollo es mayor en estos pacientes en comparación con la población general, reduciendo los niveles de colesterol total, de colesterol LDL (colesterol "malo") y la relación LDL/HDL.[135]
Véase también
[editar]Referencias
[editar]- ↑ Scott DL, Wolfe F, Huizinga TWJ. Rheumatoid arthritis. Lancet 2010;376(9746):1094-1108. doi: 10.1016/S0140-6736(10)60826-4. PMID 20870100
- ↑ a b c d e f Alvarez Lario Bonifacio. El libro de la artritis reumatoide (2003). Ediciones Díaz de Santos (2003). ISBN 8479785810
- ↑ Majithia V, Geraci SA. Rheumatoid arthritis: diagnosis and management. Am J Med. 2007;120(11):936-9. doi: 10.1016/j.amjmed.2007.04.005. PMID 17976416
- ↑ a b c d e f g h i j Oliver AM, St Clair EW. Artritis Reumatoide. Tratamiento. En: Primer on the Rheumatic Diseases (13.ª edition) Jhon H Klippel et al ed. Medical Trends, S.L. (2010). ISBN 978-0387356648
- ↑ a b c d e f g Halberg P. Rheumatoid arthritis. History. En: Rheumatology. Klippel JH, Dieppe PA, (eds). Mosby-Doyma Libros S.A. (1994). ISBN 0 397 44731 0
- ↑ a b c d e Benedeck TG. Historia de las enfermedades reumáticas. En: Compendio de las enfermedades reumáticas (10.ª ed). Schumacher RS ed. Arthritis Foundation. Marketing Trends S.L. (1993). ISBN 84-88313-61-6
- ↑ Olivé A, JL Fernández-Sueiro JL, Díaz-Jouanen E. Nomenclátor. Reumatol Clin. 2005;1:59-75. doi: 10.1016/S1699-258X(05)72716-9. http://www.reumatologiaclinica.org/es/nomenclator/articulo/13075521/ Archivado el 14 de agosto de 2014 en Wayback Machine.
- ↑ a b c d e f Entezami P, Fox DA, Clapham PJ, Chung KC. Historical perspective on the etiology of rheumatoid arthritis. Hand Clin. 2011;27(1):1-10. doi: 10.1016/j.hcl.2010.09.006. PMID 21176794
- ↑ Castillo-Ojugas. Hitos históricos de la reumatología. La reumatología en el arte. En: Manual de enfermedades reumáticas de la Sociedad Española de Reumatología (1992). ISBN 84-604-2809-5
- ↑ Alfred Baring Garrod. http://rheumatology.oxfordjournals.org/content/40/10/1189.long
- ↑ Ropes MW, Bennett GA, Cobb S, Jacox R, Jessar RA.1958 Revision of diagnostic criteria for rheumatoid arthritis. Bull Rheum Dis. 1958;9(4):175-6. PMID 13596783
- ↑ Arnett FC, Edworthy SM, Bloch DA, et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum. 1988;31(3):315-24. PMID 3358796
- ↑ a b Aletaha D, Neogi T, Silman AJ, et al. 2010 rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum 2010; 62:2569–81. PMID 20872595
- ↑ Auguste Renoir: artritis en las manos del pintor. El Mundo. Medicina e Historia (2004). Elmundo.es/salud, 16 de septiembre de 2004. http://www.elmundo.es/elmundosalud/2004/09/16/dolor/1095344810.html
- ↑ a b c d e f g h i j k l m n ñ Schur PH, Gabriel SE, Crowson CS. Epidemiology of, risk factors for, and posible causes of rheumatoid arthritis. UpToDate 2014. http://www.uptodate.com
- ↑ Rodés J, Carne X, Trilla García A, Albanell Mestres J. Manual de terapéutica médica. Elsevier España. 2002. ISBN 8445811487
- ↑ Kurkó J, Besenyei T, Laki J, Glant TT, Mikecz K, Szekanecz Z. Genetics of Rheumatoid Arthritis - A Comprehensive Review. Clinic Rev Allerg Immunol. 2013;45(2):170-179. doi: 10.1007/s12016-012-8346-7. PMID 23288628.
- ↑ a b c d e f g h Waldburger JM, Firestein GS. Artritis Reumatoide. Epidemiología, patología y patogénesis. En: Primer on the Rheumatic Diseases (13.ª edition) Jhon H Klippel et al ed. Medical Trends, S.L. (2010). ISBN 978-0387356648
- ↑ «Enfermedades articulares. Artritis reumatoide. Definición.». Archivado desde el original el 11 de agosto de 2014. Consultado el 18 de agosto de 2007.
- ↑ Edwards JC, Cambridge G, Abrahams VM. Do self-perpetuating B lymphocytes drive human autoimmune disease? Immunology. 1999; 97(2): 188–96. doi: 10.1046/j.1365-2567.1999.00772. PMID 10447731 x
- ↑ Scott DL, Wolfe F, Huizinga TW. Rheumatoid arthritis. Lancet. 2010; 376(9746):1094-108. doi = 10.1016/S0140-6736(10)60826-4. PMID 20870100
- ↑ Klareskog L, Stolt P, Lundberg K, et al. A new model for an etiology of rheumatoid arthritis: smoking may trigger HLA-DR (shared epitope)-restricted immune reactions to autoantigens modified by citrullination. Arthritis Rheum. 2006;54(1):38-46. PMID 16385494
- ↑ Takagi H, Ishiguro N, Iwata H, Kanamono T. Genetic association between rheumatoid arthritis and estrogen receptor microsatellite polymorphism. J Rheumatol. 2000;27(7):1638-42. PMID 10914844
- ↑ Tengstrand B, Carlström K, Hafström I. Bioavailable testosterone in men with rheumatoid arthritis-high frequency of hypogonadism. heumatology (Oxford). 2002;41(3):285-9. PMID 11934965
- ↑ Liao KP, Alfredsson L, Karlson EW. Environmental influences on risk for rheumatoid arthritis. Curr Opin Rheumatol. 2009;21(3):279-83. doi: 10.1097/BOR.0b013e32832a2e16. PMID 19318947
- ↑ a b c d e Schur PH, Firenstein GS. Pathogenesis of rheumatoid arthritis. UpToDate 2014. http://www.uptodate.com
- ↑ a b c Ruiz-Esquide V, Sanmartí R. Tabaco y otros factores ambientales en la artritis reumatoide. Reumatol Clin. 2012;8(6):342-50. doi: 10.1016/j.reuma.2012.02.011. PMID 22609003
- ↑ a b Mikuls TR. Help stop tooth decay...and prevent RA? J Rheumatol. 2010;37(6):1083-5. doi: 10.3899/jrheum.100173. PMID 20516033
- ↑ a b Scher JU, Bretz WA, Abramson SB. Periodontal disease and subgingival microbiota as contributors for rheumatoid arthritis pathogenesis: modifiable risk factors? Curr Opin Rheumatol. 2014;26(4):424-9. doi: 10.1097/BOR.0000000000000076. PMID 24807405
- ↑ Ball RJ, Avenell A, Aucott L, Hanlon P, Vickers MA (29 de septiembre de 2015). «Systematic review and meta-analysis of the sero-epidemiological association between Epstein-Barr virus and rheumatoid arthritis». Arthritis Res Ther (Revisión Sistemática) (17): 274. PMC 4587583. PMID 26416719. doi:10.1186/s13075-015-0755-6.
- ↑ a b de Punder K1, Pruimboom L (12 de marzo de 2013). «The dietary intake of wheat and other cereal grains and their role in inflammation». Nutrients (Revisión) 5 (3): 771-87. PMC 3705319. PMID 23482055. doi:10.3390/nu5030771.
- ↑ a b Fasano A (febrero de 2012). «Leaky gut and autoimmune diseases». Clin Rev Allergy Immunol (Revisión) 42 (1): 71-8. PMID 22109896. doi:10.1007/s12016-011-8291-x. «Besides celiac disease, several other autoimmune diseases, including type 1 diabetes [13, 14], multiple sclerosis [15, 16], and rheumatoid arthritis [17], are characterized by increased intestinal permeability secondary to noncompetent TJs that allow the passage of antigens from the intestinal flora, challenging the immune system to produce an immune response that can target any organ or tissue in genetically predisposed individuals [18–21]. Además de la enfermedad celíaca, varias otras enfermedades autoinmunes, incluyendo la diabetes tipo 1 [13, 14], la esclerosis múltiple [15, 16], y la artritis reumatoide [17], se caracterizan por aumento de la permeabilidad intestinal secundaria a uniones estrecha no competentes que permiten el paso de antígenos de la flora intestinal, desafiando el sistema inmune para producir una respuesta inmune que puede dirigirse a cualquier órgano o tejido en individuos genéticamente predispuestos [18-21].».
- ↑ a b c Fasano, A (2011 Jan). «Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer». Physiol Rev (Revisión) 91 (1): 151-75. PMID 21248165. doi:10.1152/physrev.00003.2008.
- ↑ Bressan P, Kramer P (29 de marzo de 2016). «Bread and Other Edible Agents of Mental Disease». Front Hum Neurosci (Revisión) 10: 130. PMC 4809873. PMID 27065833. doi:10.3389/fnhum.2016.00130.
- ↑ Fasano, A (2012 Oct). «Intestinal permeability and its regulation by zonulin: diagnostic and therapeutic implications». Clin Gastroenterol Hepatol (Revisión) 10 (10): 1096-100. PMC 3458511. PMID 22902773. doi:10.1016/j.cgh.2012.08.012.
- ↑ Wen H, Baker JF.Vitamin D, immunoregulation, and rheumatoid arthritis. J Clin Rheumatol. 2011;17(2):102-7. doi: 10.1097/RHU.0b013e31820edd18. PMID 21364350
- ↑ a b Holmdahl, Rikard; Malmström, Vivianne; Burkhardt, Harald (junio de 2014). «Autoimmune priming, tissue attack and chronic inflammation — The three stages of rheumatoid arthritis» [Preparación autoinmune, ataque tisular e inflamación crónica: las tres etapas de la artritis reumatoide]. Eur J Immunol (en inglés) (Weinheim, Alemania: WILEY-VCH Verlag GmbH & Co) 44 (66): 1593-1599. PMID 24737176. doi:10.1002/eji.201444486. Consultado el 5 de septiembre de 2017.
- ↑ Angelotti, F.; Parma, A.; Cafaro, G.; Capecchi, R.; Alunno, A.; Puxeddu, I. (mayo de 2017). «One year in review 2017: pathogenesis of rheumatoid arthritis» [Un año en revisión 2017: patogenia de la artritis reumatoide]. Clinical and Experimental Rheumatology (en inglés) (Italia) 35: 368-378. Consultado el 5 de septiembre de 2017.
- ↑ Demoruelle, M. Kristen; Deane, Kevin D.; Holers, V. Michael (enero de 2014). «When and Where Does Inflammation Begin in Rheumatoid Arthritis?» [¿Cuándo y dónde comienza la inflamación en la artritis reumatoide?]. Curr Opin Rheumatol (en inglés) 26 (1): 64-71. PMID 24247116. doi:10.1097/BOR.0000000000000017. Consultado el 5 de septiembre de 2017.
- ↑ Perry E, Kelly C, Eggleton P, De Soyza A, Hutchinson D. The lung in ACPA-positive rheumatoid arthritis: an initiating site of injury? Rheumatology (Oxford). 2014 May 15. pii: keu195. [Epub ahead of print] PMID 24831057
- ↑ Klareskog L, Amara K, Malmström V. Adaptive immunity in rheumatoid arthritis: anticitrulline and other antibodies in the pathogenesis of rheumatoid arthritis. Curr Opin Rheumatol. 2014;26(1):72-9. doi: 10.1097/BOR.0000000000000016. PMID 24257366
- ↑ Paula FS, Alves JD. Non-tumor necrosis factor-based biologic therapies for rheumatoid arthritis: present, future, and insights into pathogenesis. Biologics. 2014;8:1-12. doi: 10.2147/BTT.S35475. PMID 24353404
- ↑ Pablos Álvarez JL. Participación de los linfocitos T en el desarrollo y perpetuación de la artritis reumatoide. Reumatol Clin. 2011;7(6):352-3. doi: 10.1016/j.reuma.2010.12.010. PMID 22078692
- ↑ Benedetti G, Miossec P. Interleukin 17 contributes to the chronicity of inflammatory diseases such as rheumatoid arthritis. Eur J Immunol. 2014;44(2):339-47. doi: 10.1002/eji.201344184. PMID 24310226
- ↑ Gizinski AM, Fox DA. T cell subsets and their role in the pathogenesis of rheumatic disease. Curr Opin Rheumatol. 2014;26(2):204-10. doi: 10.1097/BOR.0000000000000036. PMID 24445478
- ↑ Turesson C, O'Fallon WM, Crowson CS, Gabriel SE, Matteson EL (2003)."Extra-articular disease manifestations in rheumatoid arthritis: incidence trends and risk factors over 46 years". Ann Rheum Dis. 62 (8): 722-7.doi:10.1136/ard.62.8.722. PMID 12860726
- ↑ Prete M, Racanelli V, Digiglio L, et al. Extra-articular manifestations of rheumatoid arthritis: An update. Autoimmun Rev. 2011;11(2):123-31. doi: 10.1016/j.autrev.2011.09.001. PMID 21939785
- ↑ a b Brasington RD. Clinical features of rheumatoid arthritis. En: Rheumatology. Hochberg MC, Silman AJ, Smolen JS, Weinblatt ME, Weisman MH (ed). Mosby Elsevier (2011). ISBN 978-0-323-06551-1
- ↑ a b c d e f g h i j k l m n ñ Gómez-Reino Carnota JJ. Artritis Reumatoide. En: Manual SER de las enfermedades reumáticas (5.ª ed). Sociedad Española de Reumatología. Editorial médica Panamericana (2008). ISBN 978-84-9835-105-7
- ↑ Majithia V, Geraci SA. Rheumatoid arthritis: diagnosis and management. Am J Med. 2007;120(11):936-9. PMID 17976416
- ↑ Harris ED. Manifestaciones clínicas de la artritis reumatoide. En: Kelley Tratado de Reumatología (7.ª edición). Harris ED ed. Elsevier España (2006) ISBN 978-84-8174-840-6
- ↑ a b Bloxham E, Vagadia V, Scott K, et al. Anaemia in rheumatoid arthritis: can we afford to ignore it? Postgrad Med J. 2011;87(1031):596-600. doi: 10.1136/pgmj.2011.117507. PMID 21659451
- ↑ Stein BL.The anemia of inflammation. J Clin Rheumatol. 2012;18(8):437-42. doi: 10.1097/RHU.0b013e318278f553. PMID 23211586
- ↑ Möller B, Scherer A, Förger F, et al. Anaemia may add information to standardised disease activity assessment to predict radiographic damage in rheumatoid arthritis: a prospective cohort study. Ann Rheum Dis. 2014 Apr;73(4):691-6. doi: 10.1136/annrheumdis-2012-202709. PMID 23505235
- ↑ Estrada CA, Lyons S, Terebelo H. Autoimmune hemolytic anemia and rheumatoid arthritis. South Med J. 1990;83(5):599-600. PMID 2343338
- ↑ Pérez-Dórame R, Mejía M, Mateos-Toledo H, Rojas-Serrano J. Rheumatoid arthritis-associated interstitial lung disease: Lung inflammation evaluated with high resolution computed tomography scan is correlated to rheumatoid arthritis disease activity.Reumatol Clin. 2014 Jun 6. pii: S1699-258X(14)00054-0. doi: 10.1016/j.reuma.2014.02.007. PMID 24913966
- ↑ Fischer A, Cosgrove GP. Interstitial lung abnormalities in rheumatoid arthritis are common and important. Chest. 2014;146(1):8-10. doi: 10.1378/chest.14-0030. PMID 25010956
- ↑ Conway R, Low C, Coughlan RJ, et al. Methotrexate and lung disease in rheumatoid arthritis: a meta-analysis of randomized controlled trials. Arthritis Rheumatol. 2014;66(4):803-12. doi: 10.1002/art.38322. PMID 24757133
- ↑ Hallowell RW, Horton MR. Interstitial lung disease in patients with rheumatoid arthritis: spontaneous and drug induced. Drugs. 2014;74(4):443-50. doi: 10.1007/s40265-014-0190-z. PMID 24570384
- ↑ Abud-Mendoza C, Cuevas-Orta E. Interstitial lung disease (ILD) in rheumatoid arthritis (RA). Rev Invest Clin. 2013;65(5):455-6. PMID 24687345
- ↑ Lake F, Proudman S. Rheumatoid arthritis and lung disease: from mechanisms to a practical approach. Semin Respir Crit Care Med. 2014;35(2):222-38. doi: 10.1055/s-0034-1371542. PMID 24668537.
- ↑ Bartels CM, Bridges AJ. Rheumatoid vasculitis: vanishing menace or target for new treatments? Curr Rheumatol Rep. 2010;12(6):414-9. doi: 10.1007/s11926-010-0130-1. PMID 20842467
- ↑ He J, Ding Y, Feng M, et al. Characteristics of Sjögren's syndrome in rheumatoid arthritis. Rheumatology (Oxford). 2013;52(6):1084-9. doi: 10.1093/rheumatology/kes374. PMID 23382356
- ↑ a b c d e f Venables PJW, Maini RN. Disease outcome and functional capacity in rheumatoid arthritis. UpToDate 2014. http://www.uptodate.com
- ↑ a b c d e Turesson C, Matteson EL. Extra-articular features of rheumatoid arthritis and systemic involvement. En: Rheumatology. Hochberg MC, Silman AJ, Smolen JS, Weinblatt ME, Weisman MH (ed). Mosby Elsevier (2011). ISBN 978-0-323-06551-1
- ↑ Young A, Koduri G. Extra-articular manifestations and complications of rheumatoid arthritis. Best Pract Res Clin Rheumatol. 2007;21(5):907-27. PMID 17870035
- ↑ a b González-Gay MA, González-Juanatey C. Inflammation and lipid profil in rheumatoid arthritis: bridging an apparent paradox. Ann Rheum Dis 2014;73(7):1281-3. doi: 10.1136/annrheumdis-2013-204933. PMID 24907362
- ↑ Aviña-Zubieta JA, Choi HK, Sadatsafavi M, Etminan M, Esdaile JM, Lacaille D. Risk of cardiovascular mortality in patients with rheumatoid arthritis: a meta-analysis of observational studies. Arthritis Rheum. 2008:59 (12):1690-1697. doi:10.1002/art.24092. PMID 19035419
- ↑ a b c d e f Mikuls TR, Saag KG. Comorbidity in rheumatoid arthritis. Rheum Dis Clin North Am. 2001;27(2):283-303. PMID 11396093
- ↑ a b Carmona L, Cross M, Williams B, et al. Rheumatoid arthritis. Best Pract Res Clin Rheumatol. 2010;24(6):733-45. doi: 10.1016/j.berh.2010.10.001. PMID 21665122
- ↑ Radic M, Martinovic Kaliterna D, Radic J. Overview of vasculitis and vasculopathy in rheumatoid arthritis--something to think about. Clin Rheumatol. 2013;32(7):937-42. doi: 10.1007/s10067-013-2273-8. PMID 23649484
- ↑ Choy E, Ganeshalingam K, Semb AG, Szekanecz Z, Nurmohamed M. Cardiovascular risk in rheumatoid arthritis: recent advances in the understanding of the pivotal role of inflammation, risk predictors and the impact of treatment. Rheumatology (Oxford). 2014 Jun 6. pii: keu224. [Epub ahead of print] PMID 24907149
- ↑ Kaiser R. Incidence of lymphoma in patients with rheumatoid arthritis: a systematic review of the literature. Clin Lymphoma Myeloma. 2008;8(2):87-93. doi: 10.3816/CLM.2008.n.009. PMID 18501101
- ↑ a b Badsha H (8 de febrero de 2018). «Role of Diet in Influencing Rheumatoid Arthritis Disease Activity». Open Rheumatol J (Revisión) 12: 19-28. PMC 5827298. PMID 29515679. doi:10.2174/1874312901812010019.
- ↑ a b Craig E, Cappelli LC (febrero de 2018). «Gastrointestinal and Hepatic Disease in Rheumatoid Arthritis.». Rheum Dis Clin North Am (Revisión) 44 (1): 89-111. PMC 5726432. PMID 29149929. doi:10.1016/j.rdc.2017.09.005.
- ↑ Lerner A, Matthias T (noviembre de 2015). «Rheumatoid arthritis-celiac disease relationship: joints get that gut feeling.». Autoimmun Rev (Revisión) 14 (11): 1038-47. PMID 26190704. doi:10.1016/j.autrev.2015.07.007.
- ↑ Dos Santos S, Lioté F (mayo de 2017). «Osteoarticular manifestations of celiac disease and non-celiac gluten hypersensitivity.». Joint Bone Spine (Revisión) 84 (3): 263-266. PMID 27825568. doi:10.1016/j.jbspin.2016.09.007. «Celiac disease and rheumatoid arthritis (RA). RA and celiac disease share similar pathophysiological mechanisms. Features common to both diseases include epidemiological trends, autoantibodies and genes, associated environmental inducers, and a gut microbiota imbalance with increased gut permeability. Gastrointestinal manifestations occur in patients with RA and rheumatic manifestations in those with celiac disease.»
- ↑ Polanco Allué, Isabel (2008). Ministerio de Sanidad y Consumo, ed. «Diagnóstico precoz de la enfermedad celíaca». Madrid, España. Archivado desde el original el 5 de octubre de 2018. Consultado el 11 de marzo de 2018.
- ↑ Albrecht K. Gender-specific differences in comorbidities of rheumatoid arthritis. Z Rheumatol. 2014 Jun 19. [Epub ahead of print]. PMID 24939007
- ↑ a b c d e f g h i Venables PJW, Maini RN. Diagnosis and differential diagnosis of rheumatoid arthritis. UpToDate 2014. http://www.uptodate.com
- ↑ a b c d e f g Lipsky PE. Artritis Reumatoide. Harrison. Reumatología. Fauci AS, Langford CA (eds). Ed. MCGraw Hill-Interamericana (2007). ISBN 978-84-481-5576-6
- ↑ a b c d e Tehlirian CV, Bathon JM. Artritis reumatoide. Manifestaciones clínicas y analíticas. En: Primer on the Rheumatic Diseases (13.ª edition) Jhon H Klippel et al ed. Medical Trends, S.L. (2010). ISBN 978-0387356648
- ↑ Avouac J, Gossec L, Dougados M. Diagnostic and predictive value of anti-cyclic citrullinated protein antibodies in rheumatoid arthritis: a systematic literature review. Ann Rheum Dis. 2006;65(7):845–51. doi:10.1136/ard.2006.051391. PMID 16606649
- ↑ Chandrashekara S, Sachin S. Measures in rheumatoid arthritis: are we measuring too many parameters. Int J Rheum Dis. 2012;15(3):239-48. doi: 10.1111/j.1756-185X.2012.01754.x. PMID 22709486
- ↑ Anderson J, Caplan L, Yazdany J, et al. Rheumatoid arthritis disease activity measures: American College of Rheumatology recommendations for use in clinical practice. Arthritis Care Res (Hoboken). 2012;64(5):640-7. doi: 10.1002/acr.21649. PMID 22473918
- ↑ Chorus AM, Miedema HS, Wevers CJ, van Der Linden S. Labour force participation among patients with rheumatoid arthritis. Ann Rheum Dis. 2000;59(7):549-54. PMID 10873966
- ↑ a b Myasoedova E, Davis JM 3rd, Crowson CS, Gabriel SE. Epidemiology of rheumatoid arthritis: rheumatoid arthritis and mortality. Curr Rheumatol Rep. 2010;12(5):379-85. doi: 10.1007/s11926-010-0117-y. PMID 20645137
- ↑ Singh JA, Furst DE, Bharat A, et al. 2012 update of the 2008 American College of Rheumatology recommendations for the use of disease-modifying antirheumatic drugs and biologic agents in the treatment of rheumatoid arthritis. Arthritis Care Res (Hoboken). 2012;64(5):625-39. doi: 10.1002/acr.21641. PMID 22473917
- ↑ Genovese MC, Harris ED. Tratamiento de la artritis reumatoide. En: Kelley Tratado de Reumatología (7.ª edición). Harris ED ed. Elsevier España (2006) ISBN 978-84-8174-840-6
- ↑ a b c WikiSER. Artritis Reumatoide. Tratamiento. http://www.ser.es/wp-content/uploads/2015/09/artritis_reumatoide.pdf Archivado el 30 de enero de 2016 en Wayback Machine.
- ↑ Saevarsdottir S, Rezaei H, Geborek P, et al. Current smoking status is a strong predictor of radiographic progression in early rheumatoid arthritis: results from the SWEFOT trial. Ann Rheum Dis. 2014 Apr 4. doi: 10.1136/annrheumdis-2013-204601. [Epub ahead of print] PMID 24706006.
- ↑ a b c Lanas A, Benito P, Alonso J, et al. Safe prescription recommendations for nonsteroidal anti-inflammatory drugs: consensus document ellaborated by nominated experts of three scientific associations (SER-SEC-AEG). Reumatol Clin. 2014;10(2):68-84. doi: 10.1016/j.reuma.2013.10.004. PMID 24462644.
- ↑ Radner H, Ramiro S, Buchbinder R, Landewé RB, van der Heijde D, Aletaha D. Pain management for inflammatory arthritis (rheumatoid arthritis, psoriatic arthritis, ankylosing spondylitis and other spondylarthritis) and gastrointestinal or liver comorbidity. Cochrane Database Syst Rev. 2012;1:CD008951. doi: 10.1002/14651858.CD008951.pub2. PMID 22258995
- ↑ Marks JL, Colebatch AN, Buchbinder R, Edwards CJ. Pain management for rheumatoid arthritis and cardiovascular or renal comorbidity. Cochrane Database Syst Rev. 2011 Oct 5;(10):CD008952. doi: 10.1002/14651858.CD008952.pub2. PMID 21975789
- ↑ Chen YF, Jobanputra P, Barton P, et al. Cyclooxygenase-2 selective non-steroidal anti-inflammatory drugs (etodolac, meloxicam, celecoxib, rofecoxib, etoricoxib, valdecoxib and lumiracoxib) for osteoarthritis and rheumatoid arthritis: a systematic review and economic evaluation. Health Technol Assess. 2008;12(11):1-278, iii. PMID 18405470
- ↑ Crofford LJ. Use of NSAIDs in treating patients with arthritis. Arthritis Res Ther. 2013;15 Suppl 3:S2. doi: 10.1186/ar4174. PMID 24267197
- ↑ No figuran autores. Nonsteroidal anti-inflammatory drugs: add an anti-ulcer drug for patients at high risk only. Always limit the dose and duration of treatment with NSAIDs. Prescrire Int. 2011;20(119):216-9. PMID 21954519
- ↑ Gaujoux-Viala C, Gossec L. When and for how long should glucocorticoids be used in rheumatoid arthritis? International guidelines and recommendations.Ann N Y Acad Sci. 2014;1318:32-40. doi: 10.1111/nyas.12452. PMID 24827544
- ↑ Makol A, Davis JM 3rd, Crowson CS, Therneau TM, Gabriel SE, Matteson EL. Time trends in glucocorticoid use in rheumatoid arthritis: Results from a population based inception cohort 1980-1994 vs. 1995-2007. Arthritis Care Res (Hoboken). 2014 May 12. doi: 10.1002/acr.22365. [Epub ahead of print] PMID 24821680
- ↑ Blanco-Morales EA, Bravo-Ferrer JM, Rubio Romero E, Gil González E, Gantes Pedraza MÁ. Glucocorticoides en artritis reumatoide: ¿casi siempre o casi nunca? Reumatol Clin. 2011;7(6):407-11. doi: 10.1016/j.reuma.2011.01.008. PMID 22078702
- ↑ Rau R. Glucocorticoid treatment in rheumatoid arthritis. Expert Opin Pharmacother. 2014;15(11):1575-83. doi: 10.1517/14656566.2014.922955. PMID 24856989.
- ↑ Kissin EY. The "Dirty Little Secret" Exposed in the 2013 EULAR Recommendations for rheumatoid arthritis therapy. Clin Ther. 2014. pii: S0149-2918(14)00375-0. doi: 10.1016/j.clinthera.2014.06.012. PMID 24996488
- ↑ Hetland ML, Hørslev-Petersen K. The CIMESTRA study: intra-articular glucocorticosteroids and synthetic DMARDs in a treat-to-target strategy in early rheumatoid arhtritis. Clin Exp Rheumatol. 2012;30(4 Suppl 73):S44-9. PMID 23079125.
- ↑ Gvozdenović E, Dirven L, van den Broek M, et al. Intra articular injection with corticosteroids in patients with recent onset rheumatoid arthritis: subanalyses from the BeSt study. Clin Rheumatol. 2014;33(2):263-7. doi: 10.1007/s10067-013-2465-2. PMID 24384824.
- ↑ Shea B, Swinden MV, Ghogomu ET, et al. Folic acid and folinic acid for reducing side effects in patients receiving methotrexate for rheumatoid arthritis.J Rheumatol. 2014;41(6):1049-60. doi: 10.3899/jrheum.130738. PMID 24737913
- ↑ Pichlmeier U, Heuer KU. Subcutaneous administration of methotrexate with a prefilled autoinjector pen results in a higher relative bioavailability compared with oral administration of methotrexate. Clin Exp Rheumatol. 2014 Jul 1. [Epub ahead of print] PMID 24983446
- ↑ Tornero Molina J, Ballina García FJ, Calvo Alén J, et al. Recomendaciones para el uso de metotrexato en artritis reumatoide: incremento y reducción de dosis y vías de administración. Reumatol Clin. 2014 Apr 16. pii: S1699-258X(14)00059-X. doi: 10.1016/j.reuma.2014.02.012. [Epub ahead of print]. PMID 24746914
- ↑ Lopez-Olivo MA, Siddhanamatha HR, Shea B, et al. Methotrexate for treating rheumatoid arthritis. Cochrane Database Syst Rev. 2014 Jun 10;6:CD000957. doi: 10.1002/14651858.CD000957.pub2. PMID 24916606.
- ↑ Cohen S, Cannon GW, Schiff M, et al. Two-year, blinded, randomized, controlled trial of treatment of active rheumatoid arthritis with leflunomide compared with methotrexate. Utilization of leflunomide in the treatment of rheumatoid arthritis Trial Investigator Group. Arthritis Rheum. 2001;44(9):1984-92. PMID 11592358
- ↑ a b Smolen JS, Landewé R, Breedveld FC, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update. Ann Rheum Dis. 2014;73(3):492-509. doi: 10.1136/annrheumdis-2013-204573. PMID 24161836
- ↑ Jansen JP, Buckley F, Dejonckheere F, Ogale S. Comparative efficacy of biologics as monotherapy and in combination with methotrexate on patient reported outcomes (PROs) in rheumatoid arthritis patients with an inadequate response to conventional DMARDs - a systematic review and network meta-analysis. Health Qual Life Outcomes. 2014;12(1):102. PMID 24988902
- ↑ Hirabara S, Takahashi N, Fukaya N, et al. Clinical efficacy of abatacept, tocilizumab, and etanercept in Japanese rheumatoid arthritis patients with inadequate response to anti-TNF monoclonal antibodies. Clin Rheumatol. 2014 Jun 28. [Epub ahead of print] PMID 24970596.
- ↑ Curtis JR, Schabert VF, Harrison DJ, et al. Estimating Effectiveness and Cost of Biologics for Rheumatoid Arthritis: Application of a Validated Algorithm to Commercial Insurance Claims. Clin Ther. 2014 Jul 7. pii: S0149-2918(14)00352-X. doi: 10.1016/j.clinthera.2014.05.062. PMID 25012729.
- ↑ Michaud TL, Rho YH, Shamliyan T, Kuntz KM, Choi HK. The Comparative Safety of TNF Inhibitors in Rheumatoid Arthritis - A Meta-Analysis Update of 44 Randomized Controlled Trials. Am J Med. 2014 Jun 17. pii: S0002-9343(14)00488-4. doi: 10.1016/j.amjmed.2014.06.012. PMID 24950486.
- ↑ Tkacz J, Ellis L, Bolge SC, Meyer R, Brady BL, Ruetsch C. Utilization and adherence patterns of subcutaneously administered anti-tumor necrosis factor treatment among rheumatoid arthritis patients. Clin Ther. 2014;36(5):737-47. doi: 10.1016/j.clinthera.2014.02.019. PMID 24661783.
- ↑ Ma X, Xu S. TNF inhibitor therapy for rheumatoid arthritis. Biomed Rep. 2013;1(2):177-184. PMID 24648915
- ↑ Wendler J, Burmester GR, Sörensen H, et al. Rituximab in patients with rheumatoid arthritis in routine practice (GERINIS): 6-year results from a prospective, multicentre, non-interventional study in 2,484 patients. Arthritis Res Ther. 2014 Mar 26;16(2):R80. [Epub ahead of print] PMID 24670196
- ↑ Richter A, Strangfeld A, Herzer P, et al. Sustainability of rituximab therapy in different treatment strategies - results of a 3-year follow-up of the German biologics register RABBIT. Arthritis Care Res (Hoboken). 2014 Mar 24. doi: 10.1002/acr.22327. PMID 24664818
- ↑ Nakashima Y, Kondo M, Fukuda T, et al. Remission in patients with active rheumatoid arthritis by tocilizumab treatment in routine clinical practice: results from 3 years of prospectively registered data. Mod Rheumatol. 2014;24(2):258-64. doi: 10.3109/14397595.2013.854069. PMID 24593201
- ↑ Álvaro-Gracia JM, Fernández-Nebro A, García-López A, et al. Tocilizumab en pacientes con artritis reumatoide activa y respuesta inadecuada a fármacos antirreumáticos modificadores de la enfermedad o antagonistas del factor de necrosis tumoral: subanálisis de los datos españoles de un estudio abierto cercano a la práctica clínica habitual. Reumatol Clin. 2014;10(2):94-100. doi: 10.1016/j.reuma.2013.07.002. PMID 24099961
- ↑ Thaler K, Chandiramani DV, Hansen RA, Gartlehner G. Efficacy and safety of anakinra for the treatment of rheumatoid arthritis: an update of the Oregon Drug Effectiveness Review Project. Biologics. 2009;3:485-98. PMID 20054439
- ↑ Wells AF, Jodat N, Schiff M. A critical evaluation of the role of subcutaneous abatacept in the treatment of rheumatoid arthritis: patient considerations. Biologics. 2014;8:41-55. doi: 10.2147/BTT.S55783. PMID 24600202
- ↑ Genovese MC, Tena CP, Covarrubias A, et al. Subcutaneous abatacept for the treatment of rheumatoid arthritis: longterm data from the ACQUIRE trial. J Rheumatol. 2014;41(4):629-39. doi: 10.3899/jrheum.130112. PMID 24584926
- ↑ Wollenhaupt J, Silverfield J, Lee EB, et al. Safety and efficacy of tofacitinib, an oral janus kinase inhibitor, for the treatment of rheumatoid arthritis in open-label, longterm extension studies. J Rheumatol. 2014;41(5):837-52. doi 10.3899/jrheum.130683. PMID 24692527
- ↑ «6. Tratamiento | Asociación Coordinadora Nacional de Artritis». Consultado el 21 de abril de 2021.
- ↑ Nikiphorou E, Carpenter L, Morris S, et al. "Hand and foot surgery rates in rheumatoid arthritis have declined from 1986 to 2011, but large-joint replacement rates remain unchanged: results from two UK inception cohorts." Arthritis Rheumatol. 2014;66(5):1081-9. doi 10.1002/art.38344. PMID 24782174
- ↑ «Artritis Reumatoide - UMA Unidad de la Mano». www.umacirugia.com. Consultado el 21 de abril de 2021.
- ↑ a b c d Rheumatoid arthritis and Complementary Health Approaches. National Center for Complementary and Alternative Medicine (NCCAM). http://nccam.nih.gov/health/RA/getthefacts.htm Archivado el 19 de octubre de 2013 en Wayback Machine.
- ↑ Miles EA, Calder PC. Influence of marine n-3 polyunsaturated fatty acids on immune function and a systematic review of their effects on clinical outcomes in rheumatoid arthritis. Br J Nutr. 2012;107 Suppl 2:S171-84. doi: 10.1017/S0007114512001560. PMID 22591891
- ↑ Soeken K L, Miller S A, Ernst E. Herbal medicines for the treatment of rheumatoid arthritis: a systematic review. Rheumatology (Oxford). 2003;42(5):652-9. PMID 12709541.
- ↑ Lv QW, Zhang W, Shi Q, et al. Comparison of Tripterygium wilfordii Hook F with methotrexate in the treatment of active rheumatoid arthritis (TRIFRA): a randomised, controlled clinical trial. Ann Rheum Dis. 2014 Apr 14. doi: 10.1136/annrheumdis-2013-204807. [Epub ahead of print] PMID 24733191
- ↑ Alipour B, Homayouni-Rad A, Vaghef-Mehrabany E, el al. Effects of Lactobacillus casei supplementation on disease activity and inflammatory cytokines inrheumatoid arthritis patients: a randomized double-blind clinical trial. Int J Rheum Dis. 2014 Mar 27. doi: 10.1111/1756-185X.12333. [Epub ahead of print] PMID 24673738
- ↑ Sharma M. Yoga as an alternative and complementary approach for arthritis: a systematic review. J Evid Based Complementary Altern Med. 2014; 19: 51-8. doi=10.1177/2156587213499918 PMID= 24647379
- ↑ «Ahora en Investigación». espanol.arthritis.org. Archivado desde el original el 8 de abril de 2016. Consultado el 24 de enero de 2016.
- ↑ El-Chammas K, Danner E (2011 Jun). «Gluten-free diet in nonceliac disease». Nutr Clin Pract 26 (3): 294-9. PMID 21586414. doi:10.1177/0884533611405538.
Enlaces externos
[editar]- Tabaco y otros factores de riesgo en la artritis reumatoide
- Artritis reumatoide. Sociedad Española de Reumatología (SER)
- Artritis Reumatoide. WikiSER. Sociedad Española de Reumatología (SER).
- Artritis reumatoide. ACR (American College of Rheumatology)
- Artritis reumatoidea. MedlinePlus
- Artritis reumatoide. Coordinadora Nacional de Artritis (ConArtritis)
- Artritis Reumatoide. Tutorial interactivo de MedlinePlus
- Actualización de la guía de práctica clínica para el manejo de la artritis reumatoide en España (2019).
- Recomendaciones para una prescripción segura de antiinflamatorios no esteroideos (2014). SER, SEC, AEG
- Actualización del Documento de Consenso de la Sociedad Española de Reumatología sobre el uso de terapias biológicas en la artritis reumatoide (2009)
- Evaluación y manejo del riesgo cardiovascular en los pacientes con artritis reumatoide (en inglés). Sociedad Española de Reumatología
- The effect of yoga on clinical parameters in patients with rheumatoid arthritis. Arthritis Foundation [1] Archivado el 8 de abril de 2016 en Wayback Machine.
