Diferencia entre revisiones de «Materia»
| Línea 679: | Línea 679: | ||
La [[espectroscopia infrarroja]] explota el hecho de que las moléculas absorben las frecuencias que son características de su [[Estructura química|estructura]]. Estas absorciones ocurren en [[Resonancia (mecánica)|frecuencias de resonancia]] , es decir, la frecuencia de la radiación absorbida coincide con la frecuencia de vibración. Las energías se ven afectadas por la forma de las [[Superficie de energía potencial|superficies de energía potencial]] molecular, las masas de los átomos y el [[acoplamiento vibrónico]] asociado. |
La [[espectroscopia infrarroja]] explota el hecho de que las moléculas absorben las frecuencias que son características de su [[Estructura química|estructura]]. Estas absorciones ocurren en [[Resonancia (mecánica)|frecuencias de resonancia]] , es decir, la frecuencia de la radiación absorbida coincide con la frecuencia de vibración. Las energías se ven afectadas por la forma de las [[Superficie de energía potencial|superficies de energía potencial]] molecular, las masas de los átomos y el [[acoplamiento vibrónico]] asociado. |
||
En particular, en las aproximaciones de [[Aproximación de Born-Oppenheimer|Born-Oppenheimer]] y las armónicas, es decir, cuando el [[hamiltoniano molecular]] correspondiente al [[Estado fundamental (física)|estado fundamental]] electrónico se puede aproximar mediante un [[Oscilador armónico cuántico|oscilador armónico]] en la vecindad de la [[Geometría molecular|geometría molecular de]] equilibrio, las frecuencias resonantes se asocian con los [[Modo normal|modos normales]] correspondientes a La superficie de energía potencial del estado fundamental de la electrónica molecular. Las frecuencias de resonancia también están relacionadas con la fuerza del enlace y la [[Masa atómica|masa de los átomos]] en cada extremo del mismo. Por lo tanto, la frecuencia de las vibraciones está asociada con un modo de movimiento normal particular y un tipo de enlace particular. |
En particular, en las aproximaciones de [[Aproximación de Born-Oppenheimer|Born-Oppenheimer]] y las armónicas, es decir, cuando el [[hamiltoniano molecular]] correspondiente al [[Estado fundamental (física)|estado fundamental]] electrónico se puede aproximar mediante un [[Oscilador armónico cuántico|oscilador armónico]] en la vecindad de la [[Geometría molecular|geometría molecular de]] equilibrio, las frecuencias resonantes se asocian con los [[Modo normal|modos normales]] correspondientes a La superficie de energía potencial del estado fundamental de la electrónica molecular. Las frecuencias de resonancia también están relacionadas con la fuerza del enlace y la [[Masa atómica|masa de los átomos]] en cada extremo del mismo. Por lo tanto, la frecuencia de las vibraciones está asociada con un modo de movimiento normal particular y un tipo de enlace particular. |
||
===Física de la materia condensada=== |
|||
La '''[[física de la materia condensada]]''' es el campo de la [[física]] que se ocupa de las características físicas macroscópicas de la [[materia]]. En particular, se refiere a las [[estado de agregación de la materia|fases]] “condensadas” que aparecen siempre en que el número de constituyentes en un sistema sea extremadamente grande y que las interacciones entre los componentes sean fuertes. Los ejemplos más familiares de fases condensadas son los [[sólido]]s y los [[líquido]]s, que surgen a partir de los enlaces y uniones causados por interacciones [[electromagnetismo|electromagnéticas]] entre los [[átomo]]s. |
|||
Los cuerpos [[sólido]]s están formados por átomos densamente empaquetados con intensas fuerzas de interacción entre ellos. Los efectos de interacción son responsables de las propiedades mecánicas, térmicas, eléctricas,magnéticas y ópticas de los sólidos. |
|||
Excepto el vidrio y las sustancias amorfas, cuya estructura no aparece ordenada sino desorganizada, toda la materia sólida se encuentra en estado cristalino. En general, se presenta en forma de agregado de pequeños cristales (o policristalinos) como en el hielo, las rocas muy duras, los ladrillos, el hormigón, los plásticos, los metales muy proporcionales, los huesos, etc. |
|||
También pueden constituir cristales únicos de dimensiones minúsculas como el [[azúcar]] o la [[sal]], las [[Gema|piedras preciosas]] y la mayoría de los [[mineral]]es, de los cuales algunos se utilizan en la tecnología moderna por sus sofisticadas aplicaciones, como el [[cuarzo]] de los [[oscilador]]es o los [[semiconductor]]es de los dispositivos electrónicos. |
|||
Los [[sólido]]s pueden ser clasificados de acuerdo a la naturaleza del [[enlace químico|enlace]] entre sus componentes atómicos o moleculares. La clasificación tradicional distingue cuatro tipos de enlace:<ref>{{cita libro |
|||
| apellidos = Maksic |
|||
| nombre = Zvonimir |
|||
| título = Theoretical Models of Chemical Bonding |
|||
| capítulo = The Concept of the Chemical Bond in Solids |
|||
| editorial = Springer-Verlag. |
|||
| fecha = 1990 |
|||
| ubicación = New York |
|||
| páginas = 417–452 |
|||
| isbn = 0-387-51553-4 }}</ref> |
|||
* [[Enlace covalente]], que forma '''[[#Sólidos de red covalente|sólidos de red covalente]]''' (algunas veces simplemente denominados "sólidos covalentes"). |
|||
* [[Enlace iónico]], que forma '''[[#Sólidos iónicos|sólidos iónicos]]'''. |
|||
* [[Enlace metálico]], que forma '''[[#Sólidos metálicos|sólidos metálicos]]'''. |
|||
* [[Fuerzas intermoleculares|Enlace intermolecular débil]], que forma '''[[#Sólidos moleculares|sólidos moleculares]]'''. |
|||
==Sistemas supramoleculares== |
|||
La '''química supramolecular''' es la rama de la [[química]] que estudia las interacciones supramoleculares, esto quiere decir entre [[moléculas]]. Su estudio está inspirado por la biología y está basada en los mecanismos de la química orgánica e inorgánica sintética. |
|||
La [[química]] supramolecular estudia el [[Fuerza intermolecular|reconocimiento molecular]] y la formación de '''[[Montaje supramolecular|agregados supramoleculares]]''' lo que nos da paso para comprender e interfasear el mundo biológico, los sistemas complejos y la nanotecnología.La química Supramolecular se define como: |
|||
''"La química supramolecular es la química de los enlaces intermoleculares, cubriendo las estructuras y funciones de las entidades formadas por asociación de dos o más especies químicas"'' J-M- Lehn<ref>{{cita publicación|apellidos1 = Lehn|nombre1 = J.-M|título = Toward complex matter: Supramolecular chemistry|fecha = 2002|pmid = 11929970|doi=10.1073/pnas.072065599|fechaacceso = 10 de noviembre de 2015}}</ref> |
|||
''"La química supramolecular se define como la química más allá de la molecular, una química de interacciones intermoleculares diseñadas" F. Vögtle''<ref>{{Cita libro|título = Dendrimers II: Architecture, Nanostructure and Supramolecular Chemistry|url = https://books.google.com/books?id=AwvY3gQwJqIC|editorial = Springer Science & Business Media|fecha = 15 de junio de 2000|fechaacceso = 30 de noviembre de 2015|isbn = 9783540670971|idioma = en|nombre = Fritz|apellidos = Vögtle}}</ref> |
|||
Los agregados supramoleculares que son objeto de estudio por la química supramolecular son muy diversos, pudiendo abarcar desde sistemas biológicos donde intervienen un número elevado de moléculas que se organizan espontáneamente formando estructuras más grandes,<ref>[http://books.google.es/books?id=UXBx_u2luyEC&pg=PA7 Arquitecturas supramoleculares generadas por nuevos derivados de ciclodextrinas y ácidos biliares]. Antelo Queijo, Álvaro |
|||
Editor Universidad de Santiago de Compostela. Pág. 7</ref> como monocapas, [[Bicapa lipídica|bicapa]]s, [[micela]]s,<ref>[http://books.google.es/books?id=Wx-KvSohCE0C&pg=PA46 Estudio estructural y dinámico de sistemas organizados mediante sondas fluorescentes]. Reija Otero, Belén. [[Universidad de Santiago de Compostela]]. Pág. 46</ref> [[complejo enzimático|complejos enzimáticos]] y [[lipoproteína]]s, hasta conjuntos de pocas moléculas que sufren un fenómeno de [[autoensamblaje molecular]],<ref>[http://books.google.es/books?id=CQtP26vtwL0C&pg=PA4 Estudios sobre el comportamiento de complejos metálicos con bases de Schiff compartimentales en la obtención de compuestos polinucleares]. Ocampo Prado, Noelia. Universidad de Santiago de Compostela. Pág. 4</ref> como los [[catenano]]s, [[rotaxano]]s, poliedros moleculares y otras arquitecturas afines. |
|||
== Propiedades de la materia ordinaria == |
== Propiedades de la materia ordinaria == |
||
Revisión del 10:52 23 mar 2019
En física, materia es todo aquello que se extiende en cierta región del espacio-tiempo, posee una cierta cantidad de energía y por ende está sujeto a cambios en el tiempo y a interacciones con aparatos de medida. Se considera que es lo que forma la parte sensible de los objetos perceptibles o detectables por medios físicos.
Etimológicamente, proviene del latín materia, que significa «sustancia de la que están hechas las cosas» y que también alude a la «madera dura del interior de un árbol»;[1] la palabra está relacionada con māter («origen, fuente, madre»)[2] y se corresponde con el griego hyle[3] (de hylos: «bosque, madera, leña, material»)[4][5] que es un concepto aristotélico de la teoría filosófica del hilemorfismo.[6]
El uso moderno del término va más allá de la noción clásica de sustancia, y los físicos denominan materia a cualquier entidad cuya presencia en una cierta región del espacio-tiempo conlleva que el tensor energía-impulso para dicha región es diferente de cero. Así tanto la materia fermiónica, como los electrones y otras formas como la materia bosónica son consideradas materia.
Concepto de la materia
La definición común de materia es “algo que posee masa y volumen” (ocupa un espacio). [7][8]
Por ejemplo, un coche, como se diría, que está hecho de materia, ya que ocupa espacio, y tiene masa.
La observación de que la materia ocupa espacio viene desde la antigüedad. Sin embargo, una explicación sobre por qué la materia ocupa un espacio es reciente, y se argumenta como un resultado del Principio de exclusión de Pauli. [9] [10]
En física, se llama materia a cualquier tipo de entidad que es parte del universo, tiene energía asociada, es capaz de interaccionar, es decir, es medible y tiene una localización espaciotemporal compatible con las leyes de la naturaleza.
Clásicamente se considera que la materia tiene tres propiedades que juntas la caracterizan: ocupa un lugar en el espacio, tiene masa y perdura en el tiempo.
En el contexto de la física moderna se entiende por materia cualquier campo, entidad, o discontinuidad traducible a fenómeno perceptible que se propaga a través del espacio-tiempo a una velocidad igual o inferior a la de la luz y a la que se pueda asociar energía. Así todas las formas de materia tienen asociadas una cierta energía pero solo algunas formas de materia tienen masa.
Dos ejemplos particulares donde el principio de exclusión relaciona claramente la materia con la ocupación de espacio son las estrellas del tipo enana blanca y estrella de neutrones, discutidas más adelante.
Concepto filosófico de la materia
Desde el comienzo de la filosofía, y en casi todas las culturas, se encuentra este concepto vagamente formulado como lo que permanece por debajo de las apariencias cambiantes de las cosas de la naturaleza. Según esa idea, todo lo observable está dado en sus diversas y cambiantes apariencias en un soporte o entidad en la que radica el movimiento y cambio de las cosas: la materia.
Principio único o diversos de la materia
Una cuestión filosófica importante fue si toda la materia o sustrato material tenía un principio único o tenía diversas fuentes. Que dicho sustrato sea uno sólo, o varios principios materiales, (aire, fuego, tierra y agua), fue cuestión planteada por los filósofos milesios; los eleatas, en cambio, cuestionaron la realidad del movimiento y, junto con los pitagóricos, fundamentaron el ser en un principio formal del pensamiento, dejando a la materia meramente como algo indeterminado e inconsistente, un no-ser.
El atomismo de la materia de la materia
Mayor trascendencia histórica ha tenido la teoría atomista de la antigüedad, puesta de nuevo en vigor por el mecanicismo racionalista en el siglo XVII y XVIII, que supuso el soporte teórico básico para el nacimiento de la ciencia física moderna.
Hilemorfismo
Platón y sobre todo Aristóteles elaboraron el concepto de forma, correlativo y en contraposición a la materia, dándole a ésta el carácter metafísico y problemático que ha tenido a lo largo de la historia del pensamiento, al mismo tiempo que ha servido como concepto que se aplica en otros contextos.
Es Aristóteles quien elaboró el concepto de materia de manera más completa, si bien el aspecto metafísico quedó relegado a la escolástica.
Para Aristóteles, siguiendo la tradición de los milesios y de Platón, la característica fundamental de la materia es la receptividad de la forma. La materia puede ser todo aquello capaz de recibir una forma. Por eso ante todo la materia es potencia de ser algo, siendo el algo lo determinado por la forma.
En función de este concepto hay tantas clases de materias como clases de formas capaces de determinar a un ser. Puesto que el movimiento consiste en un cambio de forma de la sustancia, el movimiento se explica en función de la materia como potencia y el acto como forma de determinación de la sustancia.
La materia, en tanto que sustancia y sujeto, es la posibilidad misma del movimiento. Hay tantas clases de materia cuantas posibles determinaciones de la sustancia en sus predicados.
Cuando las determinaciones son accidentales la materia viene dada por la situación de la sustancia en potencia respecto a recepción de una nueva forma. Así el estar sentado en acto es materia en potencia para estar de pie; el movimiento consiste en pasar de estar de pie en potencia, a estar de pie en acto.
El problema es la explicación del cambio sustancial que se produce en la generación y corrupción de la sustancia. Aparece aquí el concepto metafísico de materia prima, pura potencia de ser que no es nada, puesto que no tiene ninguna forma de determinación.
La tradicional fórmula escolástica por la que se suele definir la materia prima da idea de que realmente es difícil concebir una realidad que se corresponda con dicho concepto: No es un qué (sustancia), ni una cualidad, ni una cantidad ni ninguna otra cosa por las cuales se determina el ser. Una definición meramente negativa que incumple las leyes mismas de la definición.
Materialismo
El materialismo es la idea que postula que la materia es lo primario y que la conciencia existe como consecuencia de un estado altamente organizado de ésta, lo que produce un cambio cualitativo.
En cuanto a la relación del pensamiento humano y el mundo que nos rodea y la cognoscibilidad de ese mundo, el materialismo afirma que el mundo es material y que existe objetivamente, independientemente de la conciencia. Según esta concepción, la conciencia y el pensamiento se desarrollan a partir de un nivel superior de organización de la materia, en un proceso de reflejo de la realidad objetiva.
El materialismo también sostiene que la materia no ha sido creada de la nada, sino que existe en la eternidad y que el mundo y sus regularidades son cognoscibles por el humano, ya que es posible demostrar la exactitud de ese modo de concebir un proceso natural, reproduciéndolo nosotros mismos, creándolo como resultado de sus mismas condiciones y además poniéndolo al servicio de nuestros propios fines, dando al traste con la “cosa en sí, inasequible”.
Ley de la conservación de la materia
Como hecho científico la idea de que la masa se conserva se remonta al químico Lavoisier, el científico francés considerado padre de la Química moderna que midió cuidadosamente la masa de las sustancias antes y después de intervenir en una reacción química, y llegó a la conclusión de que la materia, medida por la masa, no se crea ni destruye, sino que sólo se transforma en el curso de las reacciones. Sus conclusiones se resumen en el siguiente enunciado: En una reacción química, la materia no se crea ni se destruye, solo se transforma. El mismo principio fue descubierto antes por Mijaíl Lomonosov, de manera que es a veces citado como ley de Lomonosov-Lavoisier, más o menos en los siguientes términos: La masa de un sistema de sustancias es constante, con independencia de los procesos internos que puedan afectarle, es decir, "La suma de los productos, es igual a la suma de los reactivos, manteniéndose constante la masa". Sin embargo, tanto las técnicas modernas como el mejoramiento de la precisión de las medidas han permitido establecer que la ley de Lomonosov-Lavoisier, se cumple sólo aproximadamente.
La equivalencia entre masa y energía descubierta por Einstein obliga a rechazar la afirmación de que la masa convencional se conserva, porque masa y energía son mutuamente convertibles. De esta manera se puede afirmar que la masa relativista equivalente (el total de masa material y energía) se conserva, pero la masa en reposo puede cambiar, como ocurre en aquellos procesos relativísticos en que una parte de la materia se convierte en fotones. La conversión en reacciones nucleares de una parte de la materia en energía radiante, con disminución de la masa en reposo; se observa por ejemplo en procesos de fisión como la explosión de una bomba atómica, o en procesos de fusión como la emisión constante de energía que realizan las estrellas.
Distribución de materia en el universo
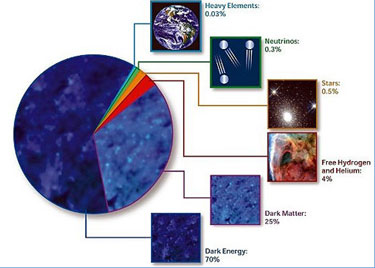
Según los modelos físicos actuales, sólo aproximadamente el 5% de nuestro universo está formado por materia másica ordinaria. Se supone que una parte importante de esta masa sería materia bariónica formada por bariones y electrones, que sólo supondrían alrededor de 1/1850 de la masa de la materia bariónica. El resto de nuestro universo se compondría de materia oscura (23%) y energía oscura (72%).
A pesar que la materia bariónica representa un porcentaje tan pequeño, la mitad de ella todavía no se ha encontrado. Todas las estrellas, galaxias y gas observable forman menos de la mitad de los bariones que debería haber. La hipótesis principal sobre el resto de materia bariónica no encontrada es que, como consecuencia del proceso de formación de estructuras posterior al big bang, está distribuida en filamentos gaseosos de baja densidad que forman una red por todo el universo y en cuyos nodos se encuentran los diversos cúmulos de galaxias. Recientemente (mayo de 2008) el telescopio XMM-Newton de la agencia espacial europea ha encontrado pruebas de la existencia de dicha red de filamentos.[11]
Propiedades intrínsecas de la materia
Masa
En física, masa (del latín massa) es una magnitud que expresa la cantidad de materia de un cuerpo, medida por la inercia de este, que determina la aceleración producida por una fuerza que actúa sobre él.[12] Es una propiedad intrínseca de los cuerpos que determina la medida de la masa inercial y de la masa gravitacional. La unidad utilizada para medir la masa en el Sistema Internacional de Unidades es el kilogramo (kg).[13]
Materia no-másica
Una gran parte de la energía del universo corresponde a formas de materia formada por partículas o campos que no presentan masa, como la luz y la radiación electromagnética, las dos formada por fotones. Junto con estas partículas no másicas, se postula la existencia de otras partículas como el gravitón, el fotino y el gravitino, que serían todas ellas partículas sin masa aunque contribuyen a la energía total del universo.
Materia másica
La materia másica está organizada en varios niveles y subniveles. La materia másica puede ser estudiada desde los puntos de vista macroscópico y microscópico. Según el nivel de descripción adoptado debemos adoptar descripciones clásicas o descripciones cuánticas. Una parte de la materia másica, concretamente la que compone los astros subenfriados y las estrellas, está constituida por moléculas, átomos, e iones. Cuando las condiciones de temperatura lo permite la materia se encuentra condensada.
Carga eléctrica
La carga eléctrica es una propiedad física intrínseca de algunas partículas subatómicas que se manifiesta mediante fuerzas de atracción y repulsión entre ellas a través de campos electromagnéticos. La materia cargada eléctricamente es influida por los campos electromagnéticos, siendo, a su vez, generadora de ellos. La denominada interacción electromagnética entre carga y campo eléctrico es una de las cuatro interacciones fundamentales de la física. Desde el punto de vista del modelo estándar la carga eléctrica es una medida de la capacidad que posee una partícula para intercambiar fotones.
Una de las principales características de la carga eléctrica es que, en cualquier proceso físico, la carga total de un sistema aislado siempre se conserva. Es decir, la suma algebraica de las cargas positivas y negativas no varía en el tiempo.
La carga eléctrica es de naturaleza discreta, fenómeno demostrado experimentalmente por Robert Millikan. Por razones históricas, a los electrones se les asignó carga negativa: –1, también expresada –e. Los protones tienen carga positiva: +1 o +e. A los quarks se les asigna carga fraccionaria: ±1/3 o ±2/3, aunque no se los ha podido observar libres en la naturaleza.[14]
Las investigaciones actuales de la física apuntan a que la carga eléctrica es una propiedad cuantizada. La unidad más elemental de carga se encontró que es la carga que tiene el electrón, es decir alrededor de 1,602 176 487(40) × 10-19 culombios (C) y es conocida como carga elemental.[15] El valor de la carga eléctrica de un cuerpo, representada como q o Q, se mide según el número de electrones que posea en exceso o en defecto.[16]
Impenetrabilidad
En física, la impenetrabilidad (de impenetrable) es la resistencia que opone una porción de materia que otra ocupe su mismo lugar en el espacio. Ningún cuerpo puede ocupar al mismo tiempo el lugar de otro. Así mismo, la impenetrabilidad es la resistencia que opone un cuerpo a ser traspasado. Se encuentra en la categoría de propiedad general. Debe notarse que la impenetrabilidad se refiere a la capacidad de la materia ordinaria para no ser penetrada por fragmentos de materia ordinaria. Esto es importante ya que por ejemplo la materia ordinaria puede ser fácilmente traspasada por partículas de materia no-ordinaria como los neutrinos, que pueden atravesar grandes capas de materia sin interaccionar con ella.
Volviendo al caso de la materia ordinaria, la impenetrabilidad depende del principio de exclusión de Pauli por el cual los electrones, como partículas fermiónicas que son, se ven obligados a ocupar diferentes capas, con lo cual hacen que un átomo estable sea una estructura con amplia extensión en el espacio. Cuando dos fragmentos de materia ordinaria se aproximan entre sí, los respectivos átomos se acercan, pero debido a la restricción impuesta por el principio de Pauli, sus nubes electrónicas no pueden interpenetrarse de lo que resulta una repulsión efectiva. Esta es en último término la causa de la impenetrabilidad de la materia ordinaria.
Dualidad onda-partícula
De acuerdo con la física clásica existen diferencias claras entre onda y partícula. Una partícula tiene una posición definida en el espacio y tiene masa mientras que una onda se extiende en el espacio caracterizándose por tener una velocidad definida y masa nula. La dualidad onda-corpúsculo, también llamada dualidad onda-partícula es un fenómeno cuántico, bien comprobado empíricamente, por el cual muchas partículas pueden exhibir comportamientos típicos de ondas en unos experimentos mientras aparecen como partículas compactas y localizadas en otros experimentos. Dado ese comportamiento dual, es típico de los objetos mecanocúanticos, donde algunas partículas pueden presentar interacciones muy localizadas y como ondas exhiben el fenómeno de la interferencia.
Actualmente se considera que la dualidad onda-partícula es un “concepto de la mecánica cuántica según el cual no hay diferencias fundamentales entre partículas y ondas: las partículas pueden comportarse como ondas y viceversa”. (Stephen Hawking, 2001)
Este es un hecho comprobado experimentalmente en múltiples ocasiones. Fue introducido por Louis-Victor de Broglie, físico francés de principios del siglo XX. En 1924 en su tesis doctoral, inspirada en experimentos sobre la difracción de electrones, propuso la existencia de ondas de materia, es decir que toda materia tenía una onda asociada a ella. Esta idea revolucionaria, fundada en la analogía con que la radiación tenía una partícula asociada, propiedad ya demostrada entonces, no despertó gran interés, pese a lo acertado de sus planteamientos, ya que no tenía evidencias de producirse. Sin embargo, Einstein reconoció su importancia a raíz de sus resultados de los experimentos del efecto fotoeléctrico. En 1905, el mismo año que formuló su teoría de la relatividad especial, Albert Einstein propuso una descripción matemática de este fenómeno que parecía funcionar correctamente y en la que la emisión de electrones era producida por la absorción de cuantos de luz que más tarde serían llamados fotones. En un artículo titulado "Un punto de vista heurístico sobre la producción y transformación de la luz" mostró cómo la idea de partículas discretas de luz podía explicar el efecto fotoeléctrico y la presencia de una frecuencia característica para cada material por debajo de la cual no se producía ningún efecto. Por esta explicación del efecto fotoeléctrico Einstein recibiría el Premio Nobel de Física en 1921. En 1929, De Broglie recibió el Nobel en Física por su trabajo.
Antimateria
A la mayor parte de las partículas de la naturaleza le corresponde una antipartícula que posee la misma masa, el mismo espín, pero contraria carga eléctrica. Algunas partículas son idénticas a su antipartícula, como por ejemplo el fotón, que no tiene carga. Pero no todas las partículas de carga neutra son idénticas a su antipartícula. Siempre hemos tenido la impresión de que las leyes de la naturaleza parecían haber sido diseñadas para que todo fuese simétrico entre partículas y antipartículas hasta que los experimentos de la llamada violación CP (violación carga-paridad) encontraron que la simetría temporal se violaba en ciertos sucesos de la naturaleza. El exceso observado de bariones con respecto a los anti-bariones, en el universo, es uno de los principales problemas sin respuesta de la cosmología.
Los pares partícula-antipartícula pueden aniquilarse entre ellos si se encuentran en el estado cuántico apropiado. Estos estados pueden producirse en varios procesos. Estos procesos se usan en los aceleradores de partículas para crear nuevas partículas y probar las teorías de la física de partículas. Los procesos de altas energías en la naturaleza pueden crear antipartículas, y éstos son visibles debido a los rayos cósmicos y en ciertas reacciones nucleares. La palabra antimateria se refiere a las antipartículas elementales, los compuestos de antipartículas hechos con estas (como el antihidrógeno) y formaciones mayores que pueden hacerse con ellos.
La antimateria es la extensión del concepto de antipartícula a la materia. Así, la antimateria es una forma de materia menos frecuente que está constituida por antipartículas, en contraposición a la materia común, que está compuesta de partículas.[17][18][19] Por ejemplo, un antielectrón (un electrón con carga positiva, también llamado positrón) y un antiprotón (un protón con carga negativa) podrían formar un átomo de antimateria, de la misma manera que un electrón y un protón forman un átomo de hidrógeno. El contacto entre materia y antimateria ocasiona su aniquilación mutua; esto no significa su destrucción, sino una transformación que da lugar a fotones de alta energía, que producen rayos gamma, y otros pares partícula-antipartícula.
Espín
El espín (del inglés spin 'giro, girar') es una propiedad física de las partículas elementales por el cual tienen un momento angular intrínseco de valor fijo. El espín fue introducido en 1925 por Ralph Kronig e, independientemente, por George Uhlenbeck y Samuel Goudsmit. La otra propiedad intrínseca de las partículas elementales es la carga eléctrica. El espín proporciona una medida del momento angular intrínseco de toda partícula. En contraste con la mecánica clásica, donde el momento angular se asocia a la rotación de un objeto extenso, el espín es un fenómeno exclusivamente cuántico, que no se puede relacionar de forma directa con una rotación en el espacio. La intuición de que el espín corresponde al momento angular debido a la rotación de la partícula en torno a su propio eje solo debe tenerse como una imagen mental útil, puesto que, tal como se deduce de la teoría cuántica relativista, el espín no tiene una representación en términos de coordenadas espaciales, de modo que no se puede referir ningún tipo de movimiento. Eso implica que cualquier observador al hacer una medida del momento angular detectará inevitablemente que la partícula posee un momento angular intrínseco total, difiriendo observadores diferentes solo sobre la dirección de dicho momento, y no sobre su valor (este último hecho no tiene análogo en mecánica clásica)[20] .
Niveles de organización de la materia
Partículas subatómicas
Una partícula subatómica es aquella que es más pequeña que el átomo. Puede ser una partícula elemental o una compuesta, a su vez, por otras partículas subatómicas.

Las partículas elementales son los constituyentes elementales de la materia; más precisamente son partículas que no están constituidas por partículas más pequeñas ni se conoce que tengan estructura interna.[21]
En física de partículas, los fermiones son partículas que obedecen la estadística de Fermi-Dirac. Los fermiones pueden ser elementales, como el electrón, o compuestos, como el protón y el neutrón. En el Modelo estándar hay dos tipos de fermiones elementales: los leptones y los quarks, que se exponen a continuación[22]
Estos quarks y leptones interactúan mediante cuatro interacciones fundamentales: gravedad, electromagnetismo, interacciones débiles, e interacciones fuertes. El Modelo estándar es actualmente la mejor explicación de toda la física, pero a pesar de las décadas de esfuerzos, la gravedad aún no puede ser considerada en el nivel cuántico; sólo es descrito por la física clásica (véase gravedad cuántica y gravitón). [23] Las interacciones entre quarks y leptones son el resultado de un intercambio de partículas que transportan fuerza (como fotones) entre los quarks y los leptones. [24] Las partículas que transportan fuerza no son componentes básicos de la materia. En consecuencia, masa y energía no siempre pueden relacionarse a materia. Por ejemplo, los portadores de la fuerza eléctrica (fotones) poseen la energía (según la constante de Planck) y los portadores de la fuerza débil (los bosones W y Z) son masivos, pero ninguno es considerado tampoco como materia. [25] Sin embargo, aunque estas partículas no son consideradas como materia, contribuyen realmente a la masa total de los átomos o de las partículas subatómicas. [26] [27].
Los leptones son partículas de spin-{{}}, lo que significa que son fermiones. Transportan una carga eléctrica de −1 e (leptones como los electrones) o 0 e (neutrinos). A diferencia de los quarks, los leptones no transportan carga de color, lo que significa que no experimentan la interacción fuerte. Los leptones también sufren la desintegración radiactivo, por lo que están sujetos a la interacción débil. Los leptones son partículas masivas, por lo que están sujetas a la gravedad.
| Nombre | Símbolo | Espin | Carga eléctrica (e) |
Masa (MeV/c2) |
Masa comparable a | Antiparticula | Antipartícula símbolo |
|---|---|---|---|---|---|---|---|
| Leptones cargados[28] | |||||||
| Electrón | e- | −1 | 0.5110 | 1 electrón | Antielectrón (positrón) |
e+ | |
| Muon | m- | −1 | 105.7 | ~ 200 electrones | Antimuón | m+ | |
| Tauón | t- | −1 | 1,777 | ~ 2 protones | Antitauón | t+ | |
| Neutrinos[29] | |||||||
| Neutrino del electrón | v e | 0 | < 0.000460 | Menos de una milésima de un electrón | Antineutrino del electrón | ve | |
| Neutrino del muon | v m | 0 | < 0.19 | Menos de la mitad de un electrón | Antineutrino del muon | me | |
| Neutrino del Tauón (o neutrino tau) |
v t | 0 | < 18.2 | Menor que ~ 40 electrones | Antineutrino del tauón (o antineutrino tau) |
te | |
Los quarks son partículas de spin 1/2, lo que implica que son fermiones. Transportan una carga eléctrica de −1/3|3 e (quarks tipo “abajo”) o +2/3 e (quarks tipo “arriba”). Por comparación, un electrón tiene una carga de -1 e. También transportan carga de color, que es el equivalente de la carga eléctrica para la interacción fuerte. Los quarks también sufren decaimiento radiactivo, lo que significa que están sujetas a la interacción débil. Los quarks son partículas masivas, y por lo tanto también están sujetos a la gravedad.
| Nombre | Símbolo | Espin | Carga eléctrica (e) |
Masa ( MeV/ c2) |
Masa comparable a | Antipartícula | Símbolo de la antipartícula |
|---|---|---|---|---|---|---|---|
| Quarks tipo arriba | |||||||
| Arriba (up) | u | + | 1.5 to 3.3 | ~ 5 electrones | Antiarriba | u | |
| Encanto (charme) | c | + | 1160 to 1340 | ~ 1 protón | Antiencanto | c | |
| Cima (Top) | t | + | 169.100 to 173.300 | ~ 180 protones o ~ 1 átomo de wolframio |
Anticima | t | |
| Quarks tipo Abajo | |||||||
| Abajo (down) | d | − | 3.5 to 6.0 | ~ 10 electrones | Antiabajo | d | |
| Extraño (strange) | s | − | 70 to 130 | ~ 200 electrones | Antiextraño | s | |
| Fondo (Bottom) | b | − | 4.130 to 4.370 | ~ 5 protones | Antifondo | b | |

.
Materia bariónica
Una partícula compuesta es una partícula subatómica que está formada por un conjunto de partículas más elementales que forman juntas un estado ligado estable.
Un hadrón (del griego ἁδρός, hadrós, "denso") es una partícula subatómica formada por quarks que permanecen unidos debido a la interacción nuclear fuerte entre ellos. Antes de la postulación del modelo de quarks se definía a los hadrones como aquellas partículas que eran sensibles a la interacción fuerte. Como todas las partículas subatómicas, los hadrones tienen números cuánticos correspondientes a las representaciones del grupo de Poincaré: JPC(m), donde J es el espín, P la paridad, C la paridad C, y m la masa. Además, pueden llevar números cuánticos de sabor como el isoespín, extrañeza, etc.
Tanto el modelo de quarks, como la evidencia empírica sugieren que los hadrones son partículas compuestas por quarks y/o antiquarks. Hay dos tipos de hadrones (sin contar los casos "exóticos"):
- Los bariones están compuestos por tres quarks con cargas de color diferente, se dice que su carga de color global es "neutra" o "blanca", al tener las tres cargas de color compensadas entre sí. Los neutrones y protones también llamados conjuntamente nucleones son ejemplos de bariones. Los bariones aislados se comportan como fermiones.
Estas partículas tienen un número bariónico (B) diferente de cero, que es igual a +1 para los nucleones e igual a -1 para sus antipartículas.
- Los mesones están formados por un quark y un antiquark. Los piones son ejemplos de mesones, su presencia ha sido usada para explicar cómo permanecen unidos neutrones y protones en el núcleo atómico. Los mesones se comportan como bosones.

La mayoría de las partículas elementales que se han descubierto y estudiado no pueden encontrarse en condiciones normales en la Tierra, generalmente porque son inestables (se descomponen en partículas ya conocidas), o bien, son difíciles de producir de todas maneras. Estas partículas, tanto estables como inestables, se producen al azar por la acción de los rayos cósmicos al chocar con átomos de la atmósfera, y en los procesos que se dan en los aceleradores de partículas, los cuales imitan un proceso similar al primero, pero en condiciones controladas. De esta manera, se han descubierto docenas de partículas subatómicas, y se teorizan cientos de otras más. Ejemplos de partícula teórica es el gravitón; sin embargo, esta y muchas otras no han sido observadas en aceleradores de partículas modernos, ni en condiciones naturales en la atmósfera (por la acción de rayos cósmicos).
Como partículas subatómicas, se clasifican también las partículas virtuales, que son partículas que representan un paso intermedio en la desintegración de una partícula inestable, y por tanto, duran muy poco tiempo.
Los bariones son fermiones de interacción fuerte, y así están sujetos a la estadística de Fermi-Dirac. Entre los bariones están los protones y los neutrones, que se producen en el núcleo atómico, pero existen también otros muchos bariones inestables. El término barión se utiliza generalmente para referirse a triquarks (partículas compuestas de tres quarks). Se conocen bariones "exóticos" formados por cuatro quarks y un antiquark denominados pentaquarks, pero su existencia no es generalmente aceptada.
La materia bariónica es la parte del universo que está hecha de bariones (incluidos todos los átomos). Esta parte del universo no incluye la energía oscura, la materia oscura, los agujeros negros o las diversas formas de materia degenerada, como las estrellas enanas blancas y estrellas de neutrones. La radiación de microondas observada por el Wilkinson Microwave Anisotropy Probe (WMAP), sugiere que sólo un 4,6% de la parte del universo dentro de la gama de los mejores telescopios (es decir, la materia que puede ser visible porque la luz puede llegar a nosotros de ella), está hecho de materia bariónica. Alrededor de un 23% es materia oscura, y alrededor de un 72% es energía oscura [31]

Materia degenerada
En física, “materia degenerada” se refiere al estado fundamental de un gas de fermiones a una temperatura próxima al cero absoluto. [32] El principio de exclusión de Pauli, exige que sólo dos fermiones puedan ocupar un estado cuántico, uno con spín arriba y otro con spín abajo. Por lo tanto, a temperatura cero, los fermiones llenan los niveles suficientes para dar cabida a todos los fermiones disponibles, y para el caso de muchos fermiones la máxima energía cinética, llamada Energía de Fermi, y la presión del gas se hacen muy grandes y dependen del número de fermiones en lugar del valor de la temperatura, a diferencia de los estados normales de la materia.
La materia degenerada se cree que ocurre durante la evolución de estrellas pesadas. [33]
La demostración por Chandrasekhar de que las estrellas enana blanca tienen una masa máxima permitida por el principio de exclusión provocó una revolución en la teoría de la evolución de las estrellas. [34] La materia degenerada incluye la parte del universo que está compuesto por estrellas de neutrones y enanas blancas.
Materia extraña
La “materia extraña” es una forma particular de materia de quarks, generalmente considerado como un "líquido" de quarks quark arriba, quark abajo y quark extraño. Esto debe compararse con la materia nuclear, que es un líquido de neutrones y protones (que sí están compuestos de quarks arriba y abajo), y con la materia no extraña de quarks, que es un líquido de quarks que contiene solo los quarks arriba y abajo. A una densidad suficientemente alta, la materia extraña se espera que sea superconductor de color. Se ha sugerido que la materia extraña se ha sugerido se produce en el núcleo de las estrellas de neutrones, o, más especulativamente, en forma de gotas aisladas, que pueden variar en tamaño desde femtometros (Strangelets) a kilómetros (estrellas de quarks).
Dos significados del término "materia extraña"
En física de partículas y astrofísica, el término se utiliza de dos maneras, una más amplia y la otra más específica.
- El significado más amplio es sólo materia de quarks que contiene tres sabores de quarks: arriba, abajo, y extraño. En esta definición, hay una presión crítica y una densidad crítica asociada, y cuando la materia nuclear (hecha de protones y neutrones) se comprime más allá de esta densidad, los protones y neutrones se disocian en los quarks, obteniéndose materia de quarks (probablemente materia extraña).
- El sentido más restringido es materia de quarks que es más estable que la materia nuclear. La idea de que esto podría ocurrir es la "hipótesis de la materia extraña" de Bodmer[35] y Witten.[36]
En esta definición, la presión crítica es cero: el verdadero estado fundamental de la materia es siempre materia de quarks. Los núcleos que se ven en la materia que nos rodea, que son gotitas de la materia nuclear, son en realidad metaestable, y dado el tiempo suficiente (o el estímulo externo a la derecha) se desintegraría en gotas de materia extraña, p.ej. strangelets ".
Átomos
Un átomo es la unidad fundamental estructural de la materia que tiene las propiedades de un elemento químico.[37]. Una sustancia química[38] es una clase particular de materia homogénea constituida por átomos ya sean libres o enlazados entre sí en proporciones definidas [39].[40][41]
La estructura fundamental de un átomo se encuentra constituida por un núcleo bariónico de protones y neutrones, y una nube orbital de electrones atraídos debido a la fuerza electromagnética.
Generalidades del núcleo atómico
Los protones y los neutrones en el núcleo son atraídos el uno al otro por una fuerza diferente, la fuerza nuclear, que es generalmente más fuerte que la fuerza electromagnética que repele los protones cargados positivamente entre sí. Bajo ciertas circunstancias, más acentuado cuanto mayor número de protones tenga el átomo, la fuerza electromagnética repelente se vuelve más fuerte que la fuerza nuclear y los nucleones pueden ser expulsados o desechados del núcleo, dejando tras de sí un elemento diferente: desintegración nuclear que resulta en transmutación nuclear.
El número de protones en el núcleo define a qué elemento químico pertenece el átomo: por ejemplo, todos los átomos de cobre contienen 29 protones. El número de neutrones define el isótopo del elemento.[42]
Los núcleos atómicos tienen algún tipo de estructura interna, por ejemplo los neutrones y protones parecen estar orbitando unos alrededor de los otros, hecho que se manifiesta en la existencia del momento magnético nuclear. Sin embargo, los experimentos revelan que el núcleo se parece mucho a una esfera o elipsoide compacto de 10-15 m (= 1 fm), en el que la densidad parece prácticamente constante. Naturalmente el radio varía según el número de protones y neutrones, siendo los núcleos más pesados y con más partículas algo más grandes.
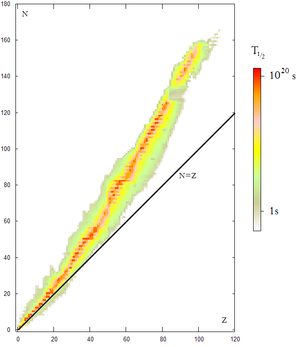
Los núcleos atómicos se comportan como partículas compuestas a energías suficientemente bajas. Además, la mayoría de núcleos atómicos por debajo de un cierto peso atómico y que además presentan un equilibrio entre el número de neutrones y el número de protones (número atómico) son estables. Sin embargo, sabemos que los neutrones aislados y los núcleos con demasiados neutrones (o demasiados protones) son inestables o radiactivos.
La explicación de esta estabilidad de los núcleos reside en la existencia de los piones. Aisladamente los neutrones pueden sufrir vía interacción débil la siguiente desintegración:
(1)
Sin embargo, dentro del núcleo atómico la cercanía entre neutrones y protones hace que sean mucho más rápidas, vía interacción fuerte las reacciones:
(2)
Generalidades de la nube electrónica
Una capa electrónica,[43] capa de electrones o cubierta de electrones designa a la distribución de un órbital alrededor del núcleo de un átomo. Cada capa puede contener un cierto número máximo de electrones y está asociada con un particular rango de energía en función de su distancia al núcleo. En un átomo estable, para que una cierta capa pueda contener electrones, es necesario que todas las interiores a ella estén completamente ocupadas. Los electrones en la capa poblada más externa, llamada capa de valencia y que es la única que puede encontrarse parcialmente vacía, determinan las propiedades químicas del átomo.
El modelo atómico de Schrödinger concebía originalmente los electrones como ondas de materia. Así la ecuación se interpretaba como la ecuación ondulatoria que describía la evolución en el tiempo y el espacio de dicha onda material. Más tarde Max Born propuso una interpretación probabilística de la función de onda de los electrones. Esa nueva interpretación es compatible con los electrones concebidos como partículas cuasipuntuales cuya probabilidad de presencia en una determinada región viene dada por la integral del cuadrado de la función de onda en una región. Es decir, en la interpretación posterior del modelo, este era modelo probabilista que permitía hacer predicciones empíricas, pero en el que la posición y la cantidad de movimiento no pueden conocerse simultáneamente, por el principio de incertidumbre. Así mismo el resultado de ciertas mediciones no están determinadas por el modelo, sino solo el conjunto de resultados posibles y su distribución de probabilidad.
Un orbital atómico es la región del espacio definido por una determinada solución particular, espacial e independiente del tiempo, a la ecuación de Schrödinger para el caso de un electrón sometido a un potencial coulombiano. La elección de tres números cuánticos en la solución general señalan unívocamente a un estado monoelectrónico posible.
Estos tres números cuánticos hacen referencia a la energía total del electrón, el momento angular orbital y la proyección del mismo sobre el eje z del sistema del laboratorio y se denotan por
Un orbital también puede representar la posición independiente del tiempo de un electrón en una molécula, en cuyo caso se denomina orbital molecular.
La combinación de todos los orbitales atómicos dan lugar a la corteza electrónica, representada por el modelo de capas, el cual se ajusta a cada elemento químico según la configuración electrónica correspondiente. Por simplicidad, se recogen las formas de la parte angular de los orbitales, obviando los nodos radiales, que siempre tienen forma esférica.
El orbital s tiene simetría esférica alrededor del núcleo atómico. En la figura siguiente se muestran dos formas alternativas para representar la nube electrónica de un orbital s: en la primera, la probabilidad de encontrar al electrón (representada por la densidad de puntos) disminuye a medida que nos alejamos del centro; en la segunda, se representa el volumen esférico en que el electrón pasa la mayor parte del tiempo y por último se observa el electrón.

La forma geométrica de los orbitales p es la de dos esferas achatadas hacia el punto de contacto (el núcleo atómico) y orientadas según los ejes de coordenadas. En función de los valores que puede tomar el tercer número cuántico ml (-1, 0 y 1) se obtienen los tres orbitales p simétricos respecto a los ejes X, Z e y. Análogamente al caso anterior, los orbitales p presentan n-2 nodos radiales en la densidad electrónica, de modo que al incrementarse el valor del número cuántico principal la probabilidad de encontrar el electrón se aleja del núcleo atómico. El orbital "p" representa también la energía que posee un electrón y se incrementa a medida que se aleja entre la distancia del núcleo y el orbital.

Los orbitales d tienen orientaciones más diversas. Cuatro de ellos tienen forma de 4 lóbulos de signos alternados (dos planos nodales, en diferentes orientaciones del espacio), y el último es un doble lóbulo rodeado por un anillo (un doble cono nodal). Siguiendo la misma tendencia, presentan n-3 nodos radiales. Este tiene 5 orbitales y corresponde al número cuántico l (azimutal)

La ecuación de Pauli, o ecuación de Schrödinger-Pauli, es una generalización o reformulación de la ecuación de Schrödinger para partículas de espín 1/2 que tiene en cuenta la interacción entre el espín y el campo electromagnético. Esta ecuación es el límite no relativista de la ecuación de Dirac y puede usarse para describir electrones para los cuales los efectos relativistas de la velocidad pueden despreciarse. En general, un efecto de apantallamiento es aquel capaz de atenuar una fuerza o interacción. En física atómica, el efecto pantalla sobre los electrones más externos de un átomo se describe como la atenuación de la fuerza atractiva neta sobre el electrón, debido a la presencia de otros electrones en capas inferiores y del mismo nivel energético. El efecto pantalla es una barrera de electrones de un mismo nivel, los cuales ejercen fuerzas de repulsión sobre electrones de mayor nivel, disminuyendo así la probabilidad de encontrar estos electrones en niveles inferiores. Cada nivel produce efecto de cola pantalla; a mayor número de electrones mayor es el efecto de pantalla.
Dentro de la física cuántica este efecto es la interferencia que existe entre la última orbita de un átomo y su núcleo.
La llamada ecuación de Dirac es la versión relativista de la ecuación de ondas de la mecánica cuántica y fue formulada por Paul Dirac en 1928. Da una descripción de las partículas elementales de espín ½, como el electrón, y es completamente consistente con los principios de la mecánica cuántica y de la teoría de la relatividad especial. Además de dar cuenta del espín, la ecuación predice la existencia de antimateria.
Configuración electrónica
La configuración electrónica indica la manera en la cual los electrones se estructuran, comunican u organizan en un átomo de acuerdo con el modelo de capas electrónicas, en el cual las funciones de ondas del sistema se expresan como un átomo o atómicamente un producto de orbitales antisimetrizadas.[44][45] La configuración electrónica es importante ya que determina las propiedades de combinación química de los átomos y por lo tanto su posición en la tabla periódica de los elementos.
De acuerdo con la mecánica cuántica, los electrones pueden pasar de un orbital atómico a otro ya sea emitiendo o absorbiendo un cuanto de energía, en forma de fotón. Esta transición de un orbital a otro con diferentes energías explican diversos fenómenos de emisión y absorción de radiación electromagnética por parte de los átomos.
Los gases nobles son un grupo de elementos químicos con propiedades muy similares: por ejemplo, bajo condiciones normales, son gases monoatómicos inodoros, incoloros y presentan una reactividad química muy baja. Se sitúan en el grupo 18 (VIIIA)[46] de la tabla periódica (anteriormente llamado grupo 0).
Las propiedades de los gases nobles pueden ser explicadas por las teorías modernas de la estructura atómica: a su capa electrónica de electrones valentes se la considera completa,[47]
La energía de ionización o potencial de ionización (Ei) es la energía necesaria para separar un electrón en su estado fundamental de un átomo de un elemento en estado gaseoso.[48] La reacción puede expresarse de la siguiente forma:
- .
En este caso se forma un ion monoatómico de carga positiva (catión monoatómico)
La afinidad electrónica (Eea) se define como la energía liberada cuando un átomo gaseoso neutro en su estado fundamental (en su menor nivel de energía) captura un electrón y forma un ion mononegativo:
Dado que se trata de energía liberada, pues normalmente al insertar un electrón en un átomo predomina la fuerza atractiva del núcleo, tiene signo negativo. En los casos en los que la energía sea absorbida, cuando ganan las fuerzas de repulsión, tendrán signo positivo.
También podemos recurrir al proceso contrario para determinar la primera afinidad electrónica, ya que sería la energía consumida en arrancar un electrón a la especie aniónica mononegativa en estado gaseoso de un determinado elemento; evidentemente la entalpía correspondiente Eea tiene signo negativo, salvo para los gases nobles y metales alcalinotérreos. Este proceso equivale al de la energía de ionización de un átomo, por lo que la Eea sería por este formalismo la energía de ionización de orden cero.
Esta propiedad nos sirve para prever qué elementos generarán con facilidad especies monoatómicas aniónicas estables.
Enlaces atómicos
Un enlace químico es el proceso químico responsable de las interacciones atractivas entre átomos y moléculas,[49]y que confiere estabilidad a los compuestos químicos diatómicos y poliatómicos. La explicación de tales fuerzas atractivas es un área compleja que está descrita por las leyes de la química cuántica.
Un enlace iónico o electrovalente es el resultado de la presencia de atracción electrostática entre los iones de distinto signo, es decir,un par anión-catión. [50]. La atracción electrostática entre los iones de carga opuesta causa que se enlacen. Para que un enlace iónico se genere es necesario que la diferencia (delta) de electronegatividades sea mayor que 1.7 o igual. (Escala de Pauling; de acuerdo al Triángulo de Van Arkel-Ketelaar).[51]
Cabe resaltar que ningún enlace es totalmente iónico, siempre habrá una contribución en el enlace que se le pueda atribuir a la compartición de los electrones en el mismo enlace (covalencia).[52] El modelo del enlace iónico es una exageración que resulta conveniente ya que muchos datos termodinámicos se pueden obtener con muy buena precisión si se piensa que los átomos son iones y no hay compartición de electrones.
Un enlace covalente está implícito en la estructura de Lewis indicando electrones compartidos entre los átomos. Un enlace covalente entre dos átomos se produce cuando estos átomos se unen, para alcanzar el octeto estable, compartiendo electrones del último nivel[53] (excepto el hidrógeno que alcanza la estabilidad cuando tiene 2 electrones). La diferencia de electronegatividad entre los átomos no es lo suficientemente grande como para que se produzca una unión de tipo iónica. Para que un enlace covalente se genere es necesario que la diferencia de electronegatividad entre átomos sea menor a 1.7.[54]
En química, la teoría del enlace de valencia (TEV) explica la naturaleza de un enlace químico en una molécula, en términos de las valencias atómicas.[55] La teoría del enlace de valencia se resume en la regla de que el átomo central en una molécula tiende a formar pares de electrones, en concordancia con restricciones geométricas, según está definido por la regla del octeto. La teoría del enlace de valencia está cercanamente relacionada con la teoría de los orbitales moleculares.
Un aspecto importante de la teoría del enlace de valencia es la condición de máximo solapamiento que conduce a la formación de los enlaces posibles más fuertes. Esta teoría se usa para explicar la formación de enlaces covalentes en muchas moléculas.
Por ejemplo, en el caso de la molécula F2, el enlace F-F está formado por el solapamiento de orbitales p de dos átomos de flúor diferentes, cada uno conteniendo un electrón desapareado. Dado que la naturaleza de los orbitales es diferente en las moléculas de H2 y F2, la fuerza de enlace y la longitud de enlace diferirán en ambas moléculas.
En una molécula de HF, el enlace covalente está formado por el solapamiento del orbital 1s del H y 2p del F, cada uno conteniendo un electrón desapareado. La compartición mutua de los eletrones entre H y F resulta en la formación de un enlace covalente entre ambos.
En química, se conoce como hibridación a la interacción de orbitales atómicos dentro de un átomo para formar nuevos orbitales híbridos. Los orbitales atómicos híbridos son los que se superponen en la formación de los enlaces, dentro de la teoría del enlace de valencia, y justifican la geometría molecular.

El enlace sigma (enlace σ) es el tipo más fuerte de enlace químico covalente, incluso más fuerte que el enlace pi, el cual forma el doble enlace. El orbital sigma se define de forma más clara para moléculas diatómicas usando el lenguaje y las herramientas de la simetría de grupos.

Los enlaces pi (enlaces π) son enlaces químicos covalentes donde dos lóbulos de un orbital involucrado en el enlace solapan con dos lóbulos del otro orbital involucrado. Estos orbitales comparten un plano nodal que pasa a través de los núcleos involucrados.
El enlace de coordinación o coordinado, igual conocido como enlace covalente dativo o enlace bipolar, es un enlace covalente en el que cada par de electrones compartido por dos átomos es aportado por uno de ellos. El átomo que aporta el par de electrones se denomina dador, y el que lo recibe, receptor.[56]
La teoría de los orbitales moleculares (TOM), es un método para determinar el enlace químico en el que los electrones no están asignados a enlaces individuales entre átomos, sino que se mueven bajo la influencia de los núcleos de toda la molécula.[57]
los orbitales moleculares son regiones del espacio que contienen la densidad electrónica definida por funciones matemáticas que describen el comportamiento ondulatorio que pueden tener los electrones en las moléculas. Estas funciones pueden usarse para calcular propiedades químicas y físicas tales como la probabilidad de encontrar un electrón en una región del espacio. El término orbital fue presentado por primera vez en inglés por Robert S. Mulliken en 1932 como abreviatura de «función de onda orbital de un electrón» (one-electron orbital wave function[58]) a partir de una traducción de la palabra alemana utilizada en 1925 por Erwin Schrödinger, 'Eigenfunktion'. Desde entonces se considera un sinónimo a la región del espacio generada con dicha función. Los orbitales moleculares se construyen habitualmente por combinación lineal de orbitales atómicos centrados en cada átomo de la molécula. Utilizando los métodos de cálculo de la estructura electrónica, como por ejemplo, el método de Hartree-Fock o el de los campos autoconsistente (self-consistent field, SCF), se pueden obtener de forma cuantitativa.
La teoría de campo cristalino (TCC) es un modelo teórico que describe la estructura electrónica de aquellos compuestos de los metales de transición que pueden ser considerados compuestos de coordinación. La teoría de campo cristalino explica exitosamente algunas de las propiedades magnéticas, colores, entalpías de hidratación y estructuras de espinela (octaédrica) de los complejos de los metales de transición, pero no acierta a describir las causas del enlace. La TCC fue desarrollada por los físicos Hans Bethe y John Hasbrouck van Vleck[59] en la década de 1930. La TCC fue posteriormente combinada con la teoría de orbitales moleculares para producir la teoría del campo de ligandos que aunque resulta un poco más compleja también es más ajustada a la realidad, ya que se adentra además en la explicación del proceso de formación del enlace químico en los complejos metálicos.
Un enlace metálico es un enlace químico que mantiene unidos los átomos (unión entre núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos como una nube) de los metales entre sí.[60]
Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. Se trata de líneas tridimensionales que adquieren estructuras tales como: la típica de empaquetamiento compacto de esferas (hexagonal compacta), cúbica centrada en las caras o la cúbica centrada en el cuerpo.
Teoría molecular
Generalidades de las moléculas
Una molécula es un grupo eléctricamente neutro y suficientemente estable de al menos dos átomos en una configuración definida, unidos por enlaces químicos fuertes (covalentes o enlace iónico).[61][62][63][64][65][66]
En este estricto sentido, las moléculas se diferencian de los iones poliatómicos. La geometría molecular se refiere a la disposición tridimensional de los átomos que constituyen una molécula. Determina muchas de las propiedades de las moléculas, reactividad, polaridad, fase, color, magnetismo, actividad biológica, etc. Actualmente, el principal modelo es la teoría de repulsión de pares de electrones de valencia (TRPEV), empleada internacionalmente por su gran predictibilidad.
La simetría molecular describe la simetría de las moléculas y utiliza este criterio para su clasificación. La simetría molecular es un concepto fundamental en química, pues muchas de las propiedades químicas de una molécula, como su momento dipolar y las transiciones espectroscópicas permitidas (basadas en reglas de selección como la regla de Laporte) pueden predecirse o ser explicadas a partir de la simetría de la molécula. Aunque existen varios marcos teóricos en los que la simetría molecular puede estudiarse, la teoría de grupos es el principal. Existen muchas técnicas para establecer empíricamente la simetría molecular, incluyendo la cristalografía de rayos X y varias formas de espectroscopia.
La topología molecular es una parte de la química matemática y trata de la descripción algebraica de los compuestos químicos, permitiendo una caracterización única y fácil de los mismos. La topología no es sensible a los detalles de un campo escalar, y con frecuencia se puede determinar mediante cálculos simplificados. Los campos escalares como la densidad de electrones, el campo de Madelung, el campo covalente y el potencial electrostático se pueden utilizar para establecer el modelo de topología.[67]
Una macromolécula es una molécula de gran tamaño creada comúnmente a través de la polimerización de subunidades más pequeñas (monómeros). Por lo general, se componen de miles, o más, de átomos. Pueden ser tanto orgánicas como inorgánicas y las más comunes en bioquímica son biopolímeros (ácidos nucleicos, proteínas, carbohidratos y polifenoles) y grandes moléculas no poliméricas (como lípidos y macrociclos).[68] Son macromoléculas sintéticas los plásticos comunes y las fibras sintéticas, así como algunos materiales experimentales, como los nanotubos de carbono.[69][70]
Interacciones intermoleculares
En mecánica cuántica, bajo la interpretación probabilística, las partículas no pueden ser consideradas puntuales, sino que se encuentran deslocalizadas espacialmente antes de realizar una medida sobre su posición. La densidad electrónica es una distribución que determina la probabilidad espacial de una o más partículas idénticas.
La polarizabilidad es la tendencia relativa de una distribución de cargas, tal como la nube electrónica de un átomo o molécula, a ser distorsionada de su forma normal por un campo eléctrico externo, que puede ser causado por la presencia de un ion cercano o un dipolo. La polarización electrónica es un desplazamiento de las cargas en presencia de un campo eléctrico externo, es decir en un átomo neutro la nube electrónica se reorienta de tal manera que el átomo se distorsiona ligeramente y pierde su simetría. La dificultad al analizar estos fenómenos varia en el tratamiento de la interacción de muchos cuerpos.
La polarizabilidad electrónica está definida como la razón del momento dipolar inducido de un átomo al campo eléctrico que produce dicho momento dipolar. Una Fuerza intermolecular se refiere a las interacciones que existen entre las moléculas conforme a su naturaleza. Generalmente, la clasificación es hecha de acuerdo a la polaridad de las moléculas que están interaccionando, o sobre la base de la naturaleza de las moléculas, de los elementos que la conforman.[71]
La electronegatividad es la capacidad de un átomo para atraer a densidad electrónica, cuando forma un enlace químico en una molécula.[72] También debemos considerar la distribución de densidad electrónica alrededor de un átomo determinado frente a otros distintos, tanto en una especie molecular como en sistemas o especies no moleculares.
Al formarse una molécula de modo enlace covalente el par de electrones tiende a desplazarse hacia el átomo que tiene mayor electronegatividad. Esto origina una densidad electrónica asimétricas entre los núcleos que forman el enlace, al cual se le denomina como enlace covalente polar. (se forma un dipolo eléctrico). El enlace es más polar cuanto mayor sea la diferencia entre las electronegatividades de los átomos que se enlazan. La polaridad química es una propiedad de las moléculas derivada de la suma vectorial de los momentos dipolos de los enlaces covalentes polares de una molécula. Esta propiedad está íntimamente relacionada con otras propiedades como la solubilidad, el punto de fusión, el punto de ebullición, las fuerzas intermoleculares, etc.
Las interacciones débiles no covalentes se les llama "débiles" porque representan la energía que mantienen unidas a las especies moleculares y que son considerablemente más débiles que los enlaces covalentes. Las interacciones no covalentes fundamentales son:
- La fuerza por puente de hidrógeno
- Las fuerzas de Van der Waals, que podemos clasificar a su vez en:
- ion-dipolo.
- dipolo - dipolo.
- dipolo - dipolo inducido.
- Fuerzas de dispersión de London conocidas como dipolo instantáneo-dipolo instantáneo, provocadas por la .
Teoría cinética molecular
La teoría cinética de los gases es una teoría física y química que explica el comportamiento y propiedades macroscópicas de los gases (ley de los gases ideales), a partir de una descripción estadística de los procesos moleculares microscópicos.

Esta rama de la física describe las propiedades térmicas de los gases. Estos sistemas contienen números enormes de átomos o moléculas, y la única forma razonable de comprender sus propiedades térmicas con base en la mecánica molecular, es encontrar determinadas cantidades dinámicas de tipo promedio y relacionar las propiedades físicas observadas del sistema con estas propiedades dinámicas moleculares en promedio. Las técnicas para relacionar el comportamiento macroscópico global de los sistemas materiales con el comportamiento promedio de sus componentes moleculares constituyen la mecánica estadística.
- El número de moléculas es grande y la separación media entre ellas es grande comparada con sus dimensiones. Por lo tanto, ocupan un volumen despreciable en comparación con el volumen del envase y se consideran masas puntuales.
- Las moléculas obedecen las leyes de Newton, pero individualmente se mueven en forma aleatoria, con diferentes velocidades cada una, pero con una velocidad promedio que no cambia con el tiempo.
- Las moléculas realizan choques elásticos entre sí, por lo tanto se conserva tanto el momento lineal como la energía cinética de las moléculas.
- Las fuerzas entre moléculas son despreciables, excepto durante el choque. Se considera que las fuerzas eléctricas o nucleares entre las moléculas son de corto alcance, por lo tanto solo se consideran las fuerzas impulsivas que surgen durante el choque.
- El gas es considerado puro, es decir todas las moléculas son idénticas.
- El gas se encuentra en equilibrio térmico con las paredes del envase.
- La ley de Graham establece que las velocidades de difusión y efusión de los gases son inversamente proporcionales a las raíces cuadradas de sus respectivas masas molares:
Siendo las velocidades y las masas molares.
La efusión es el flujo de partículas de gas a través de orificios estrechos o poros. Se hace uso de este principio en el método de efusión de separación de isótopos. El fenómeno de efusión está relacionado con la energía cinética de las moléculas. Gracias a su movimiento constante, las partículas de una sustancia se distribuyen uniformemente en el espacio libre. Si hay una aglomeración mayor de partículas en un punto habrá más choques entre sí, por lo que hará que se muevan hacia las regiones de menor número: las sustancias se efunden de una región de mayor aglomeración a una región de menor aglomeración.
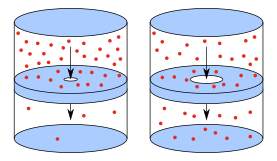
Un gas real, en oposición a un gas ideal o perfecto, es un gas que exhibe propiedades que no pueden ser explicadas enteramente utilizando la ley de los gases ideales. Para entender el comportamiento de los gases reales, lo siguiente debe ser tomado en cuenta:
- - efectos de compresibilidad
- - capacidad calorífica específica variable
- - fuerzas de Van der Waals
- - efectos termodinámicos del no-equilibrio
- - cuestiones con disociación molecular y reacciones elementales con composición variable.
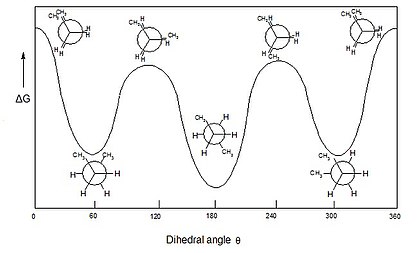
El análisis conformacional es la exploración de todos los confórmeros que se pueden obtener de una molécula dada al realizar torsiones alrededor de enlaces sencillos (grados de libertad conformacionales), observando los cambios en la energía molecular asociados a esas torsiones.
El término macromolécula se refería originalmente a las moléculas que pesaban más de 10.000 dalton de masa atómica,[73] aunque pueden alcanzar millones de UMAs.


La espectroscopia infrarroja explota el hecho de que las moléculas absorben las frecuencias que son características de su estructura. Estas absorciones ocurren en frecuencias de resonancia , es decir, la frecuencia de la radiación absorbida coincide con la frecuencia de vibración. Las energías se ven afectadas por la forma de las superficies de energía potencial molecular, las masas de los átomos y el acoplamiento vibrónico asociado. En particular, en las aproximaciones de Born-Oppenheimer y las armónicas, es decir, cuando el hamiltoniano molecular correspondiente al estado fundamental electrónico se puede aproximar mediante un oscilador armónico en la vecindad de la geometría molecular de equilibrio, las frecuencias resonantes se asocian con los modos normales correspondientes a La superficie de energía potencial del estado fundamental de la electrónica molecular. Las frecuencias de resonancia también están relacionadas con la fuerza del enlace y la masa de los átomos en cada extremo del mismo. Por lo tanto, la frecuencia de las vibraciones está asociada con un modo de movimiento normal particular y un tipo de enlace particular.
Física de la materia condensada
La física de la materia condensada es el campo de la física que se ocupa de las características físicas macroscópicas de la materia. En particular, se refiere a las fases “condensadas” que aparecen siempre en que el número de constituyentes en un sistema sea extremadamente grande y que las interacciones entre los componentes sean fuertes. Los ejemplos más familiares de fases condensadas son los sólidos y los líquidos, que surgen a partir de los enlaces y uniones causados por interacciones electromagnéticas entre los átomos.
Los cuerpos sólidos están formados por átomos densamente empaquetados con intensas fuerzas de interacción entre ellos. Los efectos de interacción son responsables de las propiedades mecánicas, térmicas, eléctricas,magnéticas y ópticas de los sólidos.
Excepto el vidrio y las sustancias amorfas, cuya estructura no aparece ordenada sino desorganizada, toda la materia sólida se encuentra en estado cristalino. En general, se presenta en forma de agregado de pequeños cristales (o policristalinos) como en el hielo, las rocas muy duras, los ladrillos, el hormigón, los plásticos, los metales muy proporcionales, los huesos, etc.
También pueden constituir cristales únicos de dimensiones minúsculas como el azúcar o la sal, las piedras preciosas y la mayoría de los minerales, de los cuales algunos se utilizan en la tecnología moderna por sus sofisticadas aplicaciones, como el cuarzo de los osciladores o los semiconductores de los dispositivos electrónicos.
Los sólidos pueden ser clasificados de acuerdo a la naturaleza del enlace entre sus componentes atómicos o moleculares. La clasificación tradicional distingue cuatro tipos de enlace:[74]
- Enlace covalente, que forma sólidos de red covalente (algunas veces simplemente denominados "sólidos covalentes").
- Enlace iónico, que forma sólidos iónicos.
- Enlace metálico, que forma sólidos metálicos.
- Enlace intermolecular débil, que forma sólidos moleculares.
Sistemas supramoleculares
La química supramolecular es la rama de la química que estudia las interacciones supramoleculares, esto quiere decir entre moléculas. Su estudio está inspirado por la biología y está basada en los mecanismos de la química orgánica e inorgánica sintética.
La química supramolecular estudia el reconocimiento molecular y la formación de agregados supramoleculares lo que nos da paso para comprender e interfasear el mundo biológico, los sistemas complejos y la nanotecnología.La química Supramolecular se define como:
"La química supramolecular es la química de los enlaces intermoleculares, cubriendo las estructuras y funciones de las entidades formadas por asociación de dos o más especies químicas" J-M- Lehn[75]
"La química supramolecular se define como la química más allá de la molecular, una química de interacciones intermoleculares diseñadas" F. Vögtle[76]
Los agregados supramoleculares que son objeto de estudio por la química supramolecular son muy diversos, pudiendo abarcar desde sistemas biológicos donde intervienen un número elevado de moléculas que se organizan espontáneamente formando estructuras más grandes,[77] como monocapas, bicapas, micelas,[78] complejos enzimáticos y lipoproteínas, hasta conjuntos de pocas moléculas que sufren un fenómeno de autoensamblaje molecular,[79] como los catenanos, rotaxanos, poliedros moleculares y otras arquitecturas afines.
Propiedades de la materia ordinaria
Propiedades generales
Las propiedades generales presentan los sistemas materiales básicos sin distinción y por tal motivo no permiten diferenciar una sustancia de otra. Algunas de las propiedades generales se les da el nombre de extensivas, pues su valor depende de la cantidad de materia, tal es el caso de la masa, el peso, volumen. Otras, las que no dependen de la cantidad de materia sino de la sustancia de que se trate, se llaman intensivas. El ejemplo paradigmático de magnitud intensiva de la materia másica es la densidad.
Propiedades extrínsecas o generales
Son las cualidades que nos permiten reconocer a la materia, como la extensión, o la inercia. Son aditivas debido a que dependen de la cantidad de la muestra tomada. Para medirlas definimos magnitudes, como la masa, para medir la inercia, y el volumen, para medir la extensión (no es realmente una propiedad aditiva exacta de la materia en general, sino para cada sustancia en particular, porque si mezclamos por ejemplo 50 ml de agua con 50 ml de etanol obtenemos un volumen de disolución de 96 ml). Hay otras propiedades generales como la interacción, que se mide mediante la fuerza. Todo sistema material interacciona con otros en forma gravitatoria, electromagnética o nuclear. También es una propiedad general de la materia su estructura corpuscular, lo que justifica que la cantidad se mida para ciertos usos en moles.
Propiedades intrínsecas o específicas
Son las cualidades de la materia independientes de la cantidad que se trate, es decir no dependen de la masa. No son aditivas y, por lo general, resultan de la composición de dos propiedades extensivas. El ejemplo perfecto lo proporciona la densidad, que relaciona la masa con el volumen. Es el caso también del punto de fusión, del punto de ebullición, el coeficiente de solubilidad, el índice de refracción, el módulo de Young, etc.
Propiedades químicas de la materia
Son aquellas propiedades distintivas de las sustancias que se observan cuando reaccionan, es decir, cuando se rompen o se forman enlaces químicos entre los átomos, formándose con la misma materia sustancias nuevas distintas de las originales. Las propiedades químicas se manifiestan en los procesos químicos (reacciones químicas), mientras que las propiamente llamadas propiedades físicas, se manifiestan en los procesos físicos, como el cambio de estado, la deformación, el desplazamiento, etc.
Ejemplos de propiedades químicas:
- Cáusticidad de las Base
Definición de materia en otros contextos
Materia y Alma - Cuerpo y Espíritu
Una de las formas de consideración de la materia ha sido en su oposición con el alma. Según esta oposición la materia hace referencia a lo "inerte", lo que no tiene vida.
En esta oposición el alma denota principio de "vida" como capacidad de automovimiento[80] y en el caso de los animales, al menos los animales superiores, capacidad de conciencia; siendo exclusivo del hombre la capacidad de autoconciencia entendida como espíritu y libertad.
El hecho religioso ha concedido históricamente a esta oposición una dimensión cultural importantísima. Pero la ciencia, al prescindir de cualquier dimensión metafísica o religiosa, no puede hacerse eco de esta distinción.
Ciencias materiales y ciencias formales
Las matemáticas y la lógica son ciencias formales porque no tienen ningún objeto material de estudio sino la “formas” válidas de inferencia. Por eso su mejor expresión es simbólica, sin contenido. Las demás ciencias en cuanto que tienen un objeto de estudio concreto son ciencias materiales.
Éticas materiales y éticas formales.
Kant introdujo lo que llamó éticas materiales y éticas formales. Las primeras consisten en establecer los imperativos acerca de lo que hay que hacer, es decir, tienen contenido. Las segundas no dicen lo que se tiene que hacer sino la “forma” en que se debe actuar en cualquier circunstancia.
Materia y forma en las obras artísticas
En las obras de arte, literatura, cine, pintura etc. suele distinguirse entre el contenido de que se trata (tema artístico, tema literario) y la forma en que el tema es tratado. Al primer aspecto se le considera como la materia y al segundo la forma propiamente dicha en la que consiste el arte.[81]
También se denomina "materia" al material del que la obra de arte está hecho y que determina su técnica: materia pictórica (óleo, temple, fresco, etc.), materia escultórica (bronce, mármol, madera, etc.), materia arquitectónica o materiales de construcción (adobe, ladrillo, mampostería, sillares, madera, hierro, cristal, etc.)
Particularmente en pintura, la "materia" se opone al "soporte", en expresiones como "óleo sobre lienzo", "temple sobre tabla", "técnica mixta sobre papel", etc.
Miscelánea
- El kilogramo es una unidad de la cantidad de materia, corresponde a la masa de un dm³ (1 litro) de agua pura a 4 °C de temperatura. A partir de esta medida, se creó un bloque de platino e iridio de la misma masa que se denominó kilogramo patrón. Este se conserva en la Oficina Internacional de Pesos y Medidas de Sèvres (Francia).
- La cantidad de materia también puede ser estimada por la energía contenida en una cierta región del espacio, tal como sugiere la fórmula E = m. c² que da la equivalencia entre masa y energía establecida por la teoría de la relatividad de Albert Einstein.
- "Tabla de densidades" en [kg/m3]: Osmio 22300, Oro 19300 - Hierro 7960 - Cemento 3000 - Agua 1000 - Hielo 920 - Madera 600 a 900 - Aire 1, 29.
- La temperatura es una magnitud que indica el grado de agitación térmica de una sustancia. Asimismo, cuando dos sustancias que están en contacto tienen distintas temperaturas se produce una transferencia de energía térmica (en forma de calor) hasta igualar ambas temperaturas. En el momento en que se igualan las temperaturas se dice que estas dos sustancias están en equilibrio térmico.
- Los tres elementos químicos más abundantes en el universo son H, He y C; algunas de sus propiedades más importantes son:
Véase también
Referencias
- ↑ Corominas, J.; Pascual, J.A. (1980). Diccionario crítico etimológico castellano e hispánico, t. III. (4.ª reimp.). Madrid: Gredos. p. 753. ISBN 84-249-1365-5.
- ↑ «Matter». Online Etymology Dictionary (en inglés). Consultado el 29 de mayo de 2016.
- ↑ «Materia - Glosario de filosofía». Webdianoia. 2015.
- ↑ «Hylo-». Online Etymology Dictionary (en inglés). Consultado el 15 de noviembre de 2016.
- ↑ Ernout, A.; Meillet, A. (1951). Dictionnaire étymologique de la langue latine (3.ª edición). París: Libr. C. Klincksieck. p. 694.
- ↑ «La teoría hilemórfica». Cibernous. Consultado el 29 de mayo de 2016.
- ↑ S.M. Walker, A. King (2005). What is Matter?. Lerner Publications. p. 7. ISBN 0822551314.
- ↑ J.Kenkel, P.B. Kelter, D.S. Hage (2000). Chemistry: An Industry-based Introduction with CD-ROM. CRC Press. p. 2. ISBN 1566703034. «All basic science textbooks define matter as simply the collective aggregate of all material substances that occupy space and have mass or weight.»
- ↑ K.A. Peacock (2008). The Quantum Revolution: A Historical Perspective. Greenwood Publishing Group. p. 47. ISBN 031333448X.
- ↑ M.H. Krieger (1998). Constitutions of Matter: Mathematically Modeling the Most Everyday of Physical Phenomena. University of Chicago Press. p. 22. ISBN 0226453057.
- ↑ ESA (ed.). «El XMM descubre parte de la materia perdida del universo».
- ↑ Real Academia Española. «masa». Diccionario de la lengua española (23.ª edición).
- ↑ SALAS, CRISTINA ESCUDERO; IGLESIAS, PABLO FERNÁNDEZ. Máquinas y equipos térmicos. Ediciones Paraninfo, S.A. ISBN 9788497322614. Consultado el 5 de febrero de 2018.
- ↑ Eric W. Weisstein (2007). «Charge» (en inglés). Consultado el 12 de febrero de 2008.
- ↑ «The NIST Reference on Constants, Units, and Uncertainty: elementary charge». NIST. 2006. Consultado el 28 de febrero de 2008.
- ↑ «Electromagnetismo y Óptica». Archivado desde el original el 3 de junio de 2007. Consultado el 27 de febrero de 2008.
- ↑ Obaidur Rahman (15 de noviembre de 2011). «Story of antimatter». The Daily Star (en inglés). Consultado el 10 de agosto de 2013.
- ↑ Nahuel. «¿Qué es la antimateria?». Espacio Profundo. Consultado el 10 de agosto de 2013. (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- ↑ «Antimateria». Ciencia Popular. Archivado desde el original el 30 de julio de 2013. Consultado el 10 de agosto de 2013.
- ↑ B. Friedrich, D. Herschbach (2003). «Stern and Gerlach: How a Bad Cigar Helped Reorient Atomic Physics». Physics Today 56 (12): 53. Bibcode:2003PhT....56l..53F. doi:10.1063/1.1650229.
- ↑ Gribbin, John (2000). Q is for Quantum - An Encyclopedia of Particle Physics. Simon & Schuster. ISBN 0-684-85578-X.
- ↑ The history of the concept of matter is a history of the fundamental length scales used to define matter. Different building blocks apply depending upon whether one defines matter on an atomic or elementary particle level. One may use a definition that matter is atoms, or that matter is hadrons, or that matter is leptons and quarks depending upon the scale at which one wishes to define matter. B. Povh, K. Rith, C. Scholz, F. Zetsche, M. Lavelle (2004). «Fundamental constituents of matter». Particles and Nuclei: An Introduction to the Physical Concepts (4th edición). Springer. ISBN 3540201688.
- ↑ J. Allday (2001). Quarks, Leptons and the Big Bang. CRC Press. p. 12. ISBN 0750308060.
- ↑ B.A. Schumm (2004). Deep Down Things: The Breathtaking Beauty of Particle Physics. Johns Hopkins University Press. p. 57. ISBN 080187971X.
- ↑ M. Jibu, K. Yasue (1995). Quantum Brain Dynamics and Consciousness. John Benjamins Publishing Company. p. 62. ISBN 1556191839., B. Martin (2009). Nuclear and Particle Physics (2nd edición). Wiley. p. 125. ISBN 0470742755. and K.W. Plaxco, M. Gross (2006). Astrobiology: A Brief Introduction. Johns Hopkins University Press. p. 23. ISBN 0801883679.
- ↑ P.A. Tipler, R.A. Llewellyn (2002). Modern Physics. Macmillan. pp. 89-91, 94-95. ISBN 0716743450.
- ↑ P. Schmüser, H. Spitzer (2002). «Particles». En L. Bergmann et al., ed. Constituents of Matter: Atoms, Molecules, Nuclei. CRC Press. pp. 773 ff. ISBN 0849312027.
- ↑
C. Amsler et al. (Particle Data Group) (2008). Physics Letters. B667: 1 http://pdg.lbl.gov/2008/tables/rpp2008-sum-leptons.pdf
|url=sin título (ayuda). - ↑
C. Amsler et al. (Particle Data Group) (2008). Physics Letters. B667: 1 http://pdg.lbl.gov/2008/listings/s066.pdf
|url=sin título (ayuda). - ↑
C. Amsler et al. (Particle Data Group) (2008). Physics Letters. B667: 1 http://pdg.lbl.gov/2008/tables/rpp2008-sum-quarks.pdf
|url=sin título (ayuda). - ↑ «Five Year Results on the Oldest Light in the Universe». NASA. 2008. Consultado el 2 de mayo de 2008.
- ↑ H.S. Goldberg, M.D. Scadron (1987). Physics of stellar evolution and cosmology. Taylor & Francis. p. 202. ISBN 0677055404.
- ↑ H.S. Goldberg, M.D. Scadron (1987). op. cit... New York: Gordon and Breach. p. 233. ISBN 0677055404.
- ↑ J.-P. Luminet, A. Bullough, A. King (1992). Black Holes. Cambridge University Press. p. 75. ISBN 0521409063.
- ↑ A. Bodmer "Collapsed Nuclei" Phys. Rev. D4, 1601 (1971)
- ↑ E. Witten, "Cosmic Separation Of Phases" Phys. Rev. D30, 272 (1984)
- ↑ «Atom». Compendium of Chemical Terminology (IUPAC Gold Book) (2ª edición). IUPAC. Consultado el 25 de abril de 2015.
- ↑ Real Academia Española. «sustancia». Diccionario de la lengua española (23.ª edición). Consultado el 28 de febrero de 2016.
- ↑ Morris, Hein (2005). Fundamentos de química (11 edición). Thomson. p. 48.
- ↑ Becerra, John W. Moore ... [et al.] ; tr. M. en C. Roberto Luis Escalona García ; rev. técnica María del Consuelo Hidalgo Mondragón ; colaboración especial Armando Martín (2000). El mundo de la química : conceptos y aplicaciones (2a. ed. edición). México: Addison Wesley Logman. ISBN 968-444-365-X.
- ↑ «IUPAC Goldbook: Chemical substance» (en inglés). Consultado el 24 de septiembre de 2015.
- ↑ Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasleigh1990 - ↑ Macy, Rudolph (1 de enero de 1976). Química orgánica simplificada. Reverte. ISBN 9788429173314. Consultado el 15 de diciembre de 2015.
- ↑ Unión Internacional de Química Pura y Aplicada. «configuration (electronic)». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Glosario de términos usados en fotoquímica, Universidad Autònoma de Barcelona, Servei de Publicacions, Bellaterra, 1999. pdf
- ↑ Atkins, Peter; Jones, Loretta (2006). Principios de química: los caminos del descubrimiento. Ed. Médica Panamericana. ISBN 9789500600804. Consultado el 2 de marzo de 2018.
- ↑ Melo, Sergio Hurtado (30 de septiembre de 2014). Operaciones básicas del proceso, mezclas y disoluciones. QUIE0108. IC Editorial. ISBN 9788416207046. Consultado el 2 de marzo de 2018.
- ↑ Unión Internacional de Química Pura y Aplicada. «Ionization energy». Compendium of Chemical Terminology. Versión en línea (en inglés).
- ↑ Gillespie, Ronald J. (agosto de 1988). Química. Reverte. ISBN 9788429171884. Consultado el 11 de febrero de 2018.
- ↑ Quimica. Pearson Educación. 2005. ISBN 9789702606949. Consultado el 2 de febrero de 2018.
- ↑ Fisica Y Quimica. Vol. Iii: Quimica I. Profesores de Educacion Secundaria. Temario Para la Preparacion de Oposiciones. Ebook. MAD-Eduforma. ISBN 9788466505536. Consultado el 2 de febrero de 2018.
- ↑ Química Orgánica, pag 34, en google libros
- ↑ Materia en Google Libros
- ↑ Quimica 2. Ediciones Umbral. ISBN 9789685607209. Consultado el 2 de febrero de 2018.
- ↑ Murrel, JN, Kettle, SF Tedder, JM, The Chemical Bond, John Wiley & Sons (1985), ISBN 0-471-90759-6.
- ↑ Arias, Enrique Battaner (1993). Biomoléculas. Ediciones Universidad de Salamanca. ISBN 9788474817584. Consultado el 6 de febrero de 2018.
- ↑ Daintith, J. (2004). Oxford Dictionary of Chemistry. Nueva York: Oxford University Press. ISBN 0-19-860918-3.
- ↑ Mulliken, Robert S. (julio de 1932). «Electronic Structures of Polyatomic Molecules and Valence. II. General Considerations». Physical Review 41 (1): 49-71. Bibcode:1932PhRv...41...49M. doi:10.1103/PhysRev.41.49.
- ↑ J. H. Van Vleck, "Theory of the Variations in Paramagnetic Anisotropy Among Different Salts of the Iron Group", Phys. Rev. 41, 208 - 215 (1932)[1]
- ↑ PASTOR, ANDREA; ESCOBAR, DIONISIO; MAYORAL, ESTHER; RUIZ, FRANCISCO (2015). Ciencias aplicadas II. Ediciones Paraninfo, S.A. ISBN 9788428337410. Consultado el 2 de febrero de 2018.
- ↑ Unión Internacional de Química Pura y Aplicada: (1994) /M04002.html molecule, Compendium of Chemical Terminology, conocido como Gold Book.
- ↑ Pauling, Linus (1970). General Chemistry. Nueva York: Dover Publications, Inc. ISBN 0-486-65622-5.
- ↑ Ebbin, Darrell, D. (1990). General Chemistry, 3th Ed. Boston: Houghton Mifflin Co. ISBN 0-395-43302-9.
- ↑ Brown, T. L. (2003). Chemistry - the Central Science, 9th Ed. Nueva Jersey: Prentice Hall. ISBN 0-13-066997-0.
- ↑ Chang, Raymond (1998). Chemistry, 6th Ed. Nueva York: McGraw Hill. ISBN 0-07-115221-0.
- ↑ Zumdahl, Steven S. (1997). Chemistry, 4th ed. Boston: Houghton Mifflin. ISBN 0-669-41794-7.
- ↑ Brown, David; Topology and Chemistry; Structural Chemistry Volume 13, Numbers 3–4, 339–355, DOI: 10.1023/A:1015872125545
- ↑ Stryer L, Berg JM, Tymoczko JL (2002). Biochemistry (5th edición). San Francisco: W.H. Freeman. ISBN 0-7167-4955-6.
- ↑ Life cycle of a plastic product Archivado el 17 de marzo de 2010 en Wayback Machine.. Americanchemistry.com. Retrieved on 2011-07-01.
- ↑ Gullapalli, S.; Wong, M.S. (2011). «Nanotechnology: A Guide to Nano-Objects». Chemical Engineering Progress 107 (5): 28-32.
- ↑ Rayner, R. (1995). Pump users handbook (4th ed. edición). Kidlington, Oxford, England: Elsevier Advanced Technology. ISBN 9781856172165.
- ↑ «Electronegativity.» Compendium of Chemical Terminology.
- ↑ Staudinger, H.; Fritschi, J. Über die Hydrierung des Kautschuks und über seine Konstitution. Helv. Chim. Acta 1922, 5, 785–806.
- ↑ Maksic, Zvonimir (1990). «The Concept of the Chemical Bond in Solids». Theoretical Models of Chemical Bonding. New York: Springer-Verlag. pp. 417-452. ISBN 0-387-51553-4.
- ↑ Lehn, J.-M (2002). Toward complex matter: Supramolecular chemistry. PMID 11929970. doi:10.1073/pnas.072065599.
- ↑ Vögtle, Fritz (15 de junio de 2000). Dendrimers II: Architecture, Nanostructure and Supramolecular Chemistry (en inglés). Springer Science & Business Media. ISBN 9783540670971. Consultado el 30 de noviembre de 2015.
- ↑ Arquitecturas supramoleculares generadas por nuevos derivados de ciclodextrinas y ácidos biliares. Antelo Queijo, Álvaro Editor Universidad de Santiago de Compostela. Pág. 7
- ↑ Estudio estructural y dinámico de sistemas organizados mediante sondas fluorescentes. Reija Otero, Belén. Universidad de Santiago de Compostela. Pág. 46
- ↑ Estudios sobre el comportamiento de complejos metálicos con bases de Schiff compartimentales en la obtención de compuestos polinucleares. Ocampo Prado, Noelia. Universidad de Santiago de Compostela. Pág. 4
- ↑ Así concebido el alma como "principio de vida" se considera "inmortal" ligado culturalmente a las creencias religiosas. La ciencia en cambio, hoy define la vida mediante funciones determinadas y no diferenciadas de lo material
- ↑ Véase interpretación
Bibliografía
- Landau & Lifshitz, Teoría clásica de los campos, Ed. Reverté, ISBN 84-291-4082-4.
- Vázquez-Reyna Mario. Reflexiones en torno a la materia, la energía y la masa. Cd. de México (1998). ISBN 970-91797-1-3
- Segura González, Wenceslao, Teoría de campo relativista, eWT Ediciones, 2014, ISBN 978-84-617-1463-6.
Enlaces externos
 Wikcionario tiene definiciones y otra información sobre materia.
Wikcionario tiene definiciones y otra información sobre materia. Wikiquote alberga frases célebres de o sobre Materia.
Wikiquote alberga frases célebres de o sobre Materia.














