Xenón
El xenón es un elemento químico de la tabla periódica cuyo símbolo es Xe y su número atómico el 54. Gas noble inodoro, muy pesado, incoloro, el xenón está presente en la atmósfera terrestre solo en trazas y fue parte del primer compuesto de gas noble sintetizado.
Características principales o particulares[editar]


El xenón es un miembro de los elementos de valencia ocho llamados gases nobles o inertes. La palabra "inerte" ya no se usa para describir esta serie química, dado que algunos elementos de valencia cero forman compuestos. En un tubo lleno de gas xenón, se emite un brillo azul cuando se le excita con una descarga eléctrica. Se ha conseguido xenón metálico aplicándole presiones de varios cientos de kilobares. El xenón también puede formar clatratos con agua cuando sus átomos quedan atrapados en un entramado de moléculas de oxígeno.
El xenón posee el número atómico 54; o sea su núcleo contiene 54 protones. En condiciones estándar de presión y temperatura, el gas puro de xenón posee una densidad de 5.894 kg/m3, unas 4.5 veces más denso que la atmósfera de la Tierra a nivel del mar, 1.217 kg/m3.[1] Como líquido, el xenón posee una densidad de hasta 3.100 g/mL, y la densidad máxima se registra en el punto triple.[2] El xenón líquido tiene una alta polarizabilidad debido a su gran volumen atómico y, por lo tanto, es un excelente disolvente. Puede disolver hidrocarburos, moléculas biológicas e incluso agua.[3] En las mismas condiciones, la densidad del xenón sólido, 3.640 g/cm3, es mayor que la densidad media del granito, 2.75 g/cm3.[2] A presiones elevadas de gigapascales el xenón forma una fase metálica.[4]
El xenón sólido cambia de cúbico centrado en las caras (fcc) a empaquetado compacto hexagonal (hcp) bajo presión y comienza a volverse metálico a aproximadamente 140 GPa, sin que se note cambio de volumen en la fase hcp. Es completamente metálico a 155 GPa. Cuando se metaliza, el xenón aparece de color azul cielo porque absorbe la luz roja y transmite otras frecuencias visibles. Este comportamiento es inusual para un metal y se explica por la anchura relativamente pequeña de las bandas de electrones en ese estado.[5][6]

(animated version)
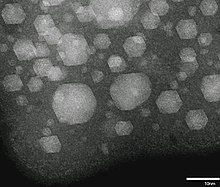
Las nanopartículas de xenón líquidas o sólidas se pueden formar a temperatura ambiente implantando iones Xe+ en una matriz sólida. Muchos sólidos tienen constantes de red más pequeñas que el sólido Xe. Esto da como resultado la compresión del Xe implantado a presiones que pueden ser suficientes para su licuefacción o solidificación.[7]
El xenón es un miembro de los elementos de valencia nula que se llaman noble o gas inerte. Es inerte a las reacciones químicas más comunes (como la combustión, por ejemplo) porque la capa de valencia exterior contiene ocho electrones. Esto produce una configuración de energía mínima estable en la que los electrones externos están estrechamente unidos.[8]
En un tubo lleno de gas, el xenón emite un resplandor azul o lavanda cuando es excitado por una descarga eléctrica. El xenón emite una banda de líneas de emisión que abarcan el espectro visual,[9] pero las líneas más intensas se producen en la región de la luz azul, produciendo la coloración.[10]
Historia[editar]
El xenón (del griego ξενόν xenos que significa "extraño") fue descubierto por William Ramsay y Morris Travers en 1898 en los residuos obtenidos al evaporar los componentes del aire líquido.
Abundancia y obtención[editar]
Se encuentra en trazas en la atmósfera terrestre, apareciendo en una parte por veinte millones. El elemento se obtiene comercialmente por extracción de los residuos del aire licuado. Este gas noble se encuentra naturalmente en los gases emitidos por algunos manantiales naturales. Los isótopos Xe-133 y Xe-135 se sintetizan mediante irradiación de neutrones en reactores nucleares refrigerados por aire.
Compuestos[editar]
Antes de 1962, se consideraba al xenón y los otros gases nobles químicamente inertes e incapaces de formar compuestos. Desde entonces se ha probado que el xenón, junto con otros gases nobles, sí forman compuestos. Algunos de los compuestos del xenón son: diflúor, hexaflúor, perxenato sódico, teraflúor, deuteriuro de xenón, e hidróxido de xenón. También se ha obtenido trióxido de xenón, compuesto altamente explosivo. Se conocen al menos 80 compuestos de xenón en el que este se enlaza con flúor u oxígeno. La mayoría de estos compuestos son incoloros.
Isótopos[editar]
En la naturaleza, el xenón se encuentra en siete isótopos estables y dos ligeramente radioactivos. Además de estas formas estables, se han estudiado 20 isótopos inestables más. El Xe-129 se produce por emisión beta del I-129 (periodo de semidesintegración: 16 millones de años); los isótopos Xe-131, Xe-132, Xe-134 y Xe-136 son productos de fisión tanto del U-238 como del Pu-244.
Al ser el xenón un trazador con dos isótopos padres, la medición de los isótopos de xenón en los meteoritos resulta ser una poderosa herramienta para el estudio de la formación del Sistema Solar. El método I-Xe de datación radiométrica permite calcular el tiempo transcurrido entre la nucleosíntesis y la condensación de un objeto sólido a partir de la nebulosa solar. Los isótopos de xenón también son útiles para entender la diferenciación terrestre. Se cree que el exceso de Xe-129 encontrado en emanaciones gaseosas de dióxido de carbono en Nuevo México se debe al decaimiento de gases derivados del manto poco después de la formación de la Tierra.
Aplicaciones[editar]
El uso principal y más famoso de este gas es en la fabricación de dispositivos emisores de luz tales como lámparas bactericidas, tubos electrónicos, lámparas estroboscópicas y flashes fotográficos, así como en lámparas usadas para excitar láseres de rubí, que generan de esta forma luz coherente. Otros usos son:
- Como anestésico en anestesia general.
- En instalaciones nucleares, se usa en cámaras de burbujas, sondas, y en otras áreas donde el alto peso molecular es una cualidad deseable.
- Los perxenatos se usan como agentes oxidantes en química analítica.
- El isótopo Xe-133 se usa como radioisótopo.
- Se usa en los faros de automóviles.
- Las lámparas de xenón son ampliamente utilizadas en los proyectores de cine.[11]
- Gas de propulsión iónica para satélites.
- En impresoras o fotocopiadoras. para que la tinta selle en la hoja de papel.
Uso en medicina[editar]
El xenón fue identificado por primera vez como anestésico en 1951. Su uso no está aprobado en Estados Unidos, siendo poco probable que llegue a gozar de un uso más extendido debido a que es un gas raro que no puede fabricarse y que debe extraerse del aire, convirtiéndose en un medicamento bastante costoso. A pesar de ello, el xenón presenta características cercanas al de un gas anestésico virtualmente ideal, el cual puede utilizarse en situaciones críticas.
Es muy insoluble en sangre y en tejidos corporales, lo que permite una rápida inducción y posterior recuperación. Es lo suficientemente potente como para generar anestesia quirúrgica cuando se administra con 30 % de oxígeno. Presenta efectos adversos mínimos.
Anestesia[editar]
El xenón ha sido utilizado como un anestésico general, pero es más costoso que otros anestésicos convencionales.[12]
El xenón interactúa con muchos receptores y canales iónicos diferentes y, al igual que muchos anestésicos de inhalación teóricamente multimodales, es probable que estas interacciones sean complementarias. El xenón es un sitio de glicina de alta afinidad antagonista del receptor NMDA.[13] Sin embargo, el xenón se diferencia de otros antagonistas de los receptores NMDA en que no es neurotóxico e inhibe la neurotoxicidad de la ketamina y el óxido nitroso (N2O), mientras que en realidad produce efectos neuroprotectores.[14][15] A diferencia de la ketamina y el óxido nitroso, el xenón no estimula el flujo de dopamina en el núcleo accumbens.[16]
Al igual que el óxido nitroso y el ciclopropano, el xenón activa el canal de potasio de dos poros TREK-1. Un canal relacionado TASK-3 también implicado en las acciones de los anestésicos por inhalación es insensible al xenón.[17] El xenón inhibe los receptores α4β2 acetilcolino nicotínicos que contribuyen a la analgesia gestionada por la espina.[18][19] El xenón es un inhibidor efectivo de la Ca2+ ATPase de la membrana de plasma. El xenón inhibe la Ca2+ ATPase al unirse a un poro hidrofóbico dentro de la enzima y prevenir que la enzima adopte esquemas activos.[20]
El xenón es un inhibidor competitivo del receptor 5-HT3 serotonina.Si bien no es anestésico ni antinociceptivo, reduce las náuseas y los vómitos emergentes de la anestesia.[21]
El xenón posee una concentración alveolar mínima (MAC) de 72% para una edad de 40, lo cual lo hace un 44% más potente que el N2O como anestésico.[22] Por lo tanto se puede utilizar junto con oxígeno en concentraciones que poseen un bajo riesgo de hipoxia. A diferencia del óxido nitroso, el xenón no es un gas de efecto invernadero y se le considera environmentally friendly.[23] Aunque se recicla en los sistemas modernos, el xenón expulsado a la atmósfera solo regresa a su fuente original, sin impacto ambiental.
Neuroprotector[editar]
El xenón induce cardioprotección y neuroprotección robustas a través de una variedad de mecanismos. A través de su influencia sobre el antagonismo de Ca2+, K+, KATP\HIF y NMDA, el xenón es neuroprotector cuando se administra antes, durante y después de episodios isquémicos.[24][25] El xenón es un antagonista de alta afinidad en el sitio de glicina del receptor NMDA.[13] El xenón es cardioprotector en condiciones de isquemia-reperfusión al inducir un farmacológica precondicionamiento no isquémico. El xenón es cardioprotector al activar la PKC-epsilon y la p38-MAPK descendente.[26] El xenón imita el precondicionamiento isquémico neuronal activando los canales de potasio sensibles al ATP.[27] El xenón reduce alostéricamente la inhibición de la activación del canal mediada por el ATP independientemente de la subunidad del receptor 1 de la sulfonilurea, aumentando el tiempo y la frecuencia del canal abierto KATP.[28]
Dopaje deportivo[editar]
La inhalación de una mezcla de xenón y oxígeno activa la producción del factor de transcripción HIF-1-alfa, lo que puede llevar a una mayor producción de eritropoyetina. Se sabe que la última hormona aumenta la producción de glóbulos rojos y el rendimiento deportivo. Según se informa, el dopaje con inhalación de xenón se ha utilizado en Rusia desde 2004 y quizás antes.[29] El 31 de agosto de 2014, la Agencia Mundial Antidopaje (AMA) agregó xenón (y argón) a la lista de sustancias y métodos prohibidos, aunque aún no se han desarrollado pruebas de dopaje confiables para estos gases.[30] Además, hasta el momento no se han demostrado los efectos del xenón sobre la producción de eritropoyetina en humanos.[31]
Imágenes[editar]
La emisión de Gamma del radioisótopo 133Xe de xenón se puede utilizar para obtener imágenes del corazón, los pulmones y el cerebro, por ejemplo, por medio de fotón único en tomografía computarizada por emisión. 133Xe también se ha utilizado para medir el flujo sanguíneo.[32][33][34]
El xenón, en particular el 129Xe hiperpolarizado, es un agente de contraste útil para la resonancia magnética (MRI). En fase gaseosa, puede obtener imágenes de las cavidades de una muestra porosa, de los alvéolos pulmonares o del flujo de gases dentro de los pulmones.[35][36] Como el xenón es soluble tanto en agua como en disolventes hidrofóbicos, puede obtener imágenes de diversos tejidos vivos blandos.[37][38][39]
El xenón-129 se utiliza actualmente como agente de visualización en las resonancias magnéticas. Cuando un paciente inhala xenón-129 hiperpolarizado, la ventilación y el intercambio de gases en los pulmones se pueden visualizar y cuantificar. A diferencia del xenón-133, el xenón-129 no es ionizante y su inhalación es segura, sin efectos adversos.[40]
Cirugía[editar]
El láser excimer de cloruro de xenón tiene ciertos usos dermatológicos.[41]
Precauciones[editar]
El gas puede ser almacenado con seguridad en contenedores convencionales de vidrio sellados a temperatura y presión ambientes. El xenón no es tóxico, pero varios de sus compuestos lo son altamente debido a sus fuertes propiedades de oxidación.
Este gas produce un efecto contrario al helio y al ser inhalado hace su voz más grave.[42]
Véase también[editar]
Referencias[editar]
- ↑ Williams, David R. (19 de abril de 2007). «Earth Fact Sheet». NASA. Consultado el 4 de octubre de 2007.
- ↑ a b Aprile, Elena; Bolotnikov, Aleksey E.; Doke, Tadayoshi (2006). Noble Gas Detectors. Wiley-VCH. pp. 8-9. ISBN 3-527-60963-6.
- ↑ Rentzepis, P. M.; Douglass, D. C. (10 de septiembre de 1981). «Xenon as a solvent». Nature 293 (5828): 165-166. Bibcode:..165R 1981Natur.293 ..165R. S2CID 4237285. doi:10.1038/293165a0.
- ↑ Caldwell, W. A.; Nguyen, J.; Pfrommer, B.; Louie, S.; Jeanloz, R. (1997). «Structure, bonding and geochemistry of xenon at high pressures». Science 277 (5328): 930-933. doi:10.1126/science.277.5328.930.
- ↑ Fontes, E. «Aniversario de oro para el fundador del programa de alta presión en el CHESS». Universidad de Cornell. Consultado el 30 de mayo de 2009.
- ↑ Eremets, Mikhail I.; Gregoryanz, Eugene A.; Struzhkin, Victor V.; Mao, Ho-Kwang; Hemley, Russell J.; Mulders, Norbert; Zimmerman, Neil M. (2000). «Conductividad eléctrica del xenón a presiones megabares». Physical Review Letters 85 (13): 2797-800. Bibcode:2000PhRvL..85.2797E. PMID 10991236. S2CID 19937739. doi:10.1103/PhysRevLett.85.2797.
- ↑ Iakoubovskii, Konstantin; Mitsuishi, Kazutaka; Furuya, Kazuo (2008). «Structure and pressure inside Xe nanoparticles embedded in Al». Physical Review B 78 (6): 064105. Bibcode:2008PhRvB.78f4105I. S2CID 29156048. doi:10.1103/PhysRevB.78.064105.
- ↑ Bader, Richard F. W. «Introducción a la estructura electrónica de átomos y moléculas». McMaster University. Consultado el 27 de septiembre de 2007.
- ↑ Talbot, John. «Espectro de las descargas de gas». Rheinisch-Westfälische Technische Hochschule Aachen. Archivado desde el original el 18 de julio de 2007. Consultado el 10 de agosto de 2006.
- ↑ William Marshall Watts (1904). Una introducción al estudio del análisis del espectro. London: Longmans, Green, and Co.
- ↑ «Xenon - Cinema Technology». Archivado desde el original el 14 de julio de 2014. Consultado el 2009.
- ↑ Neice, A. E.; Zornow, M. H. (2016). «Xenon anaesthesia for all, or only a select few?». Anaesthesia 71 (11): 1259-1272. PMID 27530275. doi:10.1111/anae.13569.
- ↑ a b Banks, P.; Franks, N. P.; Dickinson, R. (2010). «Competitive inhibition at the glycine site of the N-methyl-D-aspartate receptor mediates xenon neuroprotection against hypoxia-ischemia». Anesthesiology 112 (3): 614-22. PMID 20124979. doi:10.1097/ALN.0b013e3181cea398.
- ↑ Ma, D.; Wilhelm, S.; Maze, M.; Franks, N. P. (2002). «Neuroprotective and neurotoxic properties of the 'inert' gas, xenon». British Journal of Anaesthesia 89 (5): 739-46. PMID 12393773. doi:10.1093/bja/89.5.739.
- ↑ Nagata, A.; Nakao Si, S.; Nishizawa, N.; Masuzawa, M.; Inada, T.; Murao, K.; Miyamoto, E.; Shingu, K. (2001). «El xenón inhibe pero el N2O aumenta la expresión de c-Fos inducida por la ketamina en el cíngulo posterior y las cortezas retrospleniales de las ratas». Anesthesia & Analgesia 92 (2): 362-8. PMID 11159233. S2CID 15167421. doi:10.1213/00000539-200102000-00016.
- ↑ Sakamoto, S.; Nakao, S.; Masuzawa, M.; Inada, T.; Maze, M.; Franks, N. P.; Shingu, K. (2006). «Los efectos diferenciales del óxido nitroso y el xenón sobre los niveles de dopamina extracelular en el núcleo accumbens de la rata: un estudio de microdiálisis». Anesthesia & Analgesia 103 (6): 1459-63. PMID 17122223. S2CID 1882085. doi:10.1213/01.ane.0000247792.03959.f1.
- ↑ Gruss, M.; Bushell, T. J.; Bright, D. P.; Lieb, W. R.; Mathie, A.; Franks, N. P. (2004). «Two-pore-domain K+ channels are a novel target for the anesthetic gases xenon, nitrous oxide, and cyclopropane». Molecular Pharmacology 65 (2): 443-52. PMID 14742687. S2CID 7762447. doi:10.1124/mol.65.2.443.
- ↑ Yamakura, T.; Harris, R. A. (2000). «Effects of gaseous anesthetics nitrous oxide and xenon on ligand-gated ion channels. Comparison with isoflurane and ethanol». Anesthesiology 93 (4): 1095-101. PMID 11020766. S2CID 4684919. doi:10.1097/00000542-200010000-00034.
- ↑ Rashid, M. H.; Furue, H.; Yoshimura, M.; Ueda, H. (2006). «Tonic inhibitory role of α4β2 subtype of nicotinic acetylcholine receptors on nociceptive transmission in the spinal cord in mice». Pain 125 (1–2): 125-35. PMID 16781069. S2CID 53151557. doi:10.1016/j.pain.2006.05.011.
- ↑ Lopez, Maria M.; Kosk-Kosicka, Danuta (1995). «How Do Volatile Anesthetics Inhibit Ca2+-ATPases?». The Journal of Biological Chemistry 270 (47): 28239-28245. PMID 7499320. doi:10.1074/jbc.270.47.28239.
- ↑ Suzuki, T.; Koyama, H.; Sugimoto, M.; Uchida, I.; Mashimo, T. (2002). «The diverse actions of volatile and gaseous anesthetics on human-cloned 5-hydroxytryptamine3 receptors expressed in Xenopus oocytes». Anesthesiology 96 (3): 699-704. PMID 11873047. S2CID 6705116. doi:10.1097/00000542-200203000-00028.
- ↑ Nickalls, R.W.D.; Mapleson, W.W. (August 2003). «Age-related iso-MAC charts for isoflurane, sevoflurane and desflurane in man». British Journal of Anaesthesia 91 (2): 170-174. PMID 12878613. doi:10.1093/bja/aeg132.
- ↑ Goto, T.; Nakata Y; Morita S (2003). «Will xenon be a stranger or a friend? : the cost, benefit, and future of xenon anesthesia». Anesthesiology 98 (1): 1-2. PMID 12502969. S2CID 19119058. doi:10.1097/00000542-200301000-00002.
- ↑ Michael Marx, Thomas Glöggl, Egon Reinelt, Helmut Schirmer Uwe (May 2005). «Xenon Attenuates Cerebral Damage after Ischemia in Pigs». Anesthesiology 102 (5): 929-936. PMID 15851879. S2CID 25266308. doi:10.1097/00000542-200505000-00011.
- ↑ Dingley J. Tooley J. Porter H. Thoresen M. (2006). com/rmt/article/view/1340 «Xenon Provides Short- Term Neuroprotection in Neonatal Rats When Administered After Hypoxia-Ischemia». Stroke 37 (2): 501-6. PMID 16373643. doi:10.1161/01.STR.0000198867.31134.ac.
- ↑ Weber, N. C.; Toma, O.; Wolter, J. I.; Obal, D.; Müllenheim, J.; Preckel, B.; Schlack, W. (2005). «El gas noble xenón induce el preacondicionamiento farmacológico en el corazón de la rata in vivo mediante la inducción de la PKC-epsilon y la p38 MAPK». Br J Pharmacol 144 (1): 123-32. PMC 1575984. PMID 15644876. doi:10.1038/sj.bjp.0706063.
- ↑ Bantel, C.; Maze, M.; Trapp, S. (2009). «Precondicionamiento neuronal por anestésicos inhalatorios: evidencia del papel de los canales de potasio sensibles al trifosfato de adenosina plasmalémicos». Anesthesiology 110 (5): 986-95. PMC 2930813. PMID 19352153. doi:10.1097/ALN.0b013e31819dadc7.
- ↑ Bantel, C.; Maze, M.; Trapp, S. (2010). «El gas noble xenón es un nuevo abridor del canal de potasio sensible al trifosfato de adenosina». Anesthesiology 112 (3): 623-30. PMC 2935677. PMID 20179498. doi:10.1097/ALN.0b013e3181cf894a.
- ↑ «Breathe it in». The Economist. 8 de febrero de 2014.
- ↑ «WADA amends Section S.2 .1 of 2014 Prohibited List». 31 de agosto de 2014. Archivado desde el original el 27 de abril de 2021. Consultado el 1 de septiembre de 2014.
- ↑ Jelkmann, W. (2014). «Xenon Misuse in Sports». Deutsche Zeitschrift für Sportmedizin (Deutsche Zeitschrift für Sportmedizin/German Journal of Sports Medicine) 2014 (10): 267-271. S2CID 55832101. doi:10.5960/dzsm.2014.143.
- ↑ Van Der Wall, Ernst (1992). What's New in Cardiac Imaging?: SPECT, PET, and MRI. Springer. ISBN 0-7923-1615-0.
- ↑ Frank, John (1999). «Introduction to imaging: The chest». Student BMJ 12: 1-44. Consultado el 4 de junio de 2008.
- ↑ Chandak, Puneet K. (20 de julio de 1995). «Brain SPECT: Xenon-133». Brigham RAD. Archivado desde el original el 4 de enero de 2012. Consultado el 4 de junio de 2008.
- ↑ Albert M. S. Balamore, D. (1998). «Desarrollo de la resonancia magnética de gases nobles hiperpolarizados». Nuclear Instruments and Methods in Physics Research A 402 (2–3): 441-53. Bibcode:1998NIMPA.402..441A. PMID 11543065. doi:10.1016/S0168-9002(97)00888-7.
- ↑ Irion, Robert (23 de marzo de 1999). «Head Full of Xenon?». Science News. Archivado desde el original el 17 de enero de 2004. Consultado el 8 de octubre de 2007.
- ↑ Wolber, J.; Rowland, I. J.; Leach, M. O.; Bifone, A. (1998). «Entrega intravascular de 129Xenón hiperpolarizado para la RMN in vivo». Resonancia Magnética Aplicada 15 (3-4): 343-352. S2CID 100913538. doi:10.1007/BF03162020.
- ↑ Driehuys, B.; Möller, H.E.; Cleveland, Z.I.; Pollaro, J.; Hedlund, L.W. (2009). «Perfusión pulmonar e intercambio de gases de xenón en ratas: Imágenes de RM con inyección intravenosa de 129Xe hiperpolarizado». Radiology 252 (2): 386-93. PMC 2753782. PMID 19703880. doi:10.1148/radiol.2522081550.
- ↑ Cleveland, Z.I. Möller, H.E. Hedlund, L.W. Driehuys, B. (2009). «Infusión continua de 129Xe hiperpolarizado en soluciones acuosas fluyentes utilizando membranas hidrofóbicas de intercambio de gases». The Journal of Physical Chemistry 113 (37): 12489-99. PMC 2747043. PMID 19702286. doi:10.1021/jp9049582.
- ↑ Marshall, Helen; Stewart, Neil J.; Chan, Ho-Fung; Rao, Madhwesha; Norquay, Graham; Wild, Jim M. (1 de febrero de 2021). «Métodos y aplicaciones in vivo de la resonancia magnética con xenón-129». Progress in Nuclear Magnetic Resonance Spectroscopy (en inglés) 122: 42-62. ISSN 0079-6565. PMC 7933823. PMID 33632417. doi:10.1016/j.pnmrs.2020.11.002.
- ↑ Baltás, E.; Csoma, Z.; Bodai, L.; Ignácz, F.; Dobozy, A.; Kemény, L. (2006). «Tratamiento de la dermatitis atópica con el láser de excímero de cloruro de xenón». Journal of the European Academy of Dermatology and Venereology 20 (6): 657-60. PMID 16836491. S2CID 20156819. doi:10.1111/j.1468-3083.2006.01495.x.
- ↑ http://www.youtube.com/watch?v=X_768xTNT84
Enlaces externos[editar]
- WebElements.com - Xenón
- EnvironmentalChemistry.com - Xenón
- Los Alamos National Laboratory - Xenón
- Instituto Nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del xenón.
 Wikimedia Commons alberga una galería multimedia sobre Xenón.
Wikimedia Commons alberga una galería multimedia sobre Xenón.


