Esclerosis múltiple
| Esclerosis múltiple | ||
|---|---|---|
 Síntomas de la esclerosis múltiple. | ||
| Especialidad | Neurología | |
| Síntomas | Debilidad muscular, trastorno de la sensibilidad, ataxia, visión doble, ceguera unilateral[1] | |
| Inicio habitual | Entre los 20 y los 50 años[2] | |
| Duración | Crónica[3] | |
| Causas | Desconocidas[3] | |
| Diagnóstico | Basado en síntomas y pruebas de evaluación[3] | |
| Tratamiento | Medicación, terapia ocupacional, fisioterapia[3] | |
| Pronóstico | Esperanza de vida de 5 a 10 años más corta respecto a la población[4] | |
| Frecuencia | Prevalencia de 2,5 millones en todo el mundo[3] | |
| Tasa de letalidad | 18 900 (2015)[5] | |



La esclerosis múltiple o esclerosis de placas es una enfermedad neurológica crónica de naturaleza inflamatoria y autoinmunitaria caracterizada por el desarrollo de lesiones desmielinizantes, y de daño axonal en el sistema nervioso central.[6][7] Es una de las principales causas de discapacidad neurológica de origen no traumático en adultos jóvenes, principalmente mujeres, afectando a entre 2,3 y 2,5 millones de personas en el mundo.[8][9][10][11][12][13]
Se desconoce la causa de la enfermedad, aunque se sabe que su desarrollo se asocia a una combinación de factores genéticos, que predisponen a padecer la enfermedad, y factores ambientales e infecciosos (infecciones virales y parasitosis) que favorecen la aparición de la esclerosis múltiple. Entre los factores ambientales se incluyen el déficit de vitamina D, toxinas ambientales, la dieta y hábitos nocivos como el tabaquismo.[9][11][14][13]
Asimismo, en su desarrollo o agravamiento se ha implicado la existencia de una permeabilidad intestinal aumentada o "intestino permeable", que permite el paso incontrolado de sustancias a la sangre (virus, bacterias, toxinas, alimentos no digeridos...), lo que puede provocar la respuesta anormal del sistema inmunitario.[15][16] Los dos factores más potentes que provocan esta excesiva permeabilidad son ciertas bacterias intestinales y el gluten, en cualquier persona que lo come.[16][17]
La inflamación en la esclerosis múltiple se caracteriza por una infiltración linfocítica que produce daño en la mielina y en los axones. Inicialmente la inflamación es transitoria y es seguida de una remielinización variable, de forma tal que el comienzo de la enfermedad suele caracterizarse por períodos de disfunción neurológica seguidos de una recuperación total. Sin embargo, a medida que avanza en el tiempo, los cambios patológicos predominantes consisten en un aumento importante de la actividad de microglias, proliferación de astrocitos y gliosis junto a una neurodegeneración extensa y crónica, correlacionándose con una acumulación progresiva de discapacidad.[18][19]
El cuadro clínico de la esclerosis múltiple es muy hetérogeneo, pues incluye un amplio espectro de síntomas que varían entre pacientes e, incluso, en el mismo individuo. Así, se puede encontrar pacientes con manifestaciones neurológicas leves hasta casos con una enfermedad rápidamente progresiva y discapacitante. Dada la variedad de síntomas que produce, la esclerosis múltiple es conocida como la enfermedad de las mil caras».[20] Se distinguen varios fenotipos de la esclerosis múltiple, principalmente formas recurrentes (con brotes) y poca discapacidad y formas progresivas con discapacidad acumulativa.[9][10][14][21]
La esclerosis múltiple se diagnostica cuando en la evaluación neurológica se encuentran síntomas y signos compatibles, acompañado de la demostración por resonancia magnética (IRM) de lesiones desmielinizantes en el sistema nervioso central. Los criterios de McDonald actualizados en 2017 son los admitidos internacionalmente para el diagnóstico de la esclerosis múltiple. El tratamiento consiste en fármacos que retrasan la acumulación de lesiones (tratamiento modificador de la enfermedad), tratamiento para las recaídas (brotes), tratamiento sintomático y de rehabilitación. Se recomienda un diagnóstico y tratamiento oportunos con el fin de prevenir la progresión de la discapacidad.
Descripción[editar]
La esclerosis múltiple se caracteriza por dos fenómenos:[6]
- Aparición de focos de desmielinización esparcidos en el cerebro y parcialmente también en la médula espinal causados por el ataque del sistema inmunitario contra la vaina de mielina que recubre los nervios.[22]
- Las neuronas, y en especial sus axones se ven dañados por diversos mecanismos.
Como resultado, las neuronas del cerebro pierden parcial o totalmente su capacidad de transmisión, causando los síntomas típicos de adormecimiento, cosquilleo, espasmos, parálisis, fatiga y alteraciones en la vista.
En la variante remitente-recurrente también se ha detectado inflamación en el tejido nervioso y transección axonal, o corte de los axones de las neuronas, lo que hace que las secuelas sean permanentes.
Clasificación[editar]

Se han definido cuatro subtipos de esclerosis múltiple, no obstante, la primera manifestación de la enfermedad suele considerarse como un subtipo aparte denominado síndrome clínico aislado.[9][13][23][24][25][26][27][28]
A menudo, la neuromielitis óptica se diagnostica de forma incorrecta como esclerosis múltiple o se percibe como un tipo de esta, aunque se trata de una enfermedad distinta. De igual forma, la encefalomielitis aguda diseminada también es diagnosticada con frecuencia como un primer ataque grave de esclerosis múltiple, puesto que algunos síntomas pueden ser similares. Sin embargo, la esclerosis múltiple no suele causar síntomas de encefalitis.
- Síndrome clínico aislado es un primer evento con síntomas y signos objetivos que reflejan un trastorno neurológico de tipo inflamatorio desmielinizante, que dura al menos 24 horas y que ocurre en ausencia de fiebre o infección. De demostrarse posteriormente que se trata de una esclerosis múltiple este pasa a ser su «primer ataque». Los síntomas de presentación generalmente son monofocales y evolucionan de forma aguda o subaguda durante días a semanas, con o sin recuperación completa afectando principalmente al nervio óptico, la médula espinal, el tronco encefálico o el cerebelo.[29][30][31]
- Recurrente-remitente (EMRR) es la forma más común de la enfermedad presentándose en el 85 % de los casos, se caracteriza por exacerbaciones periódicas imprevisibles de disfunción neurológica («ataques» o «brotes») que duran semanas o meses, alternados por períodos de resolución completa o parcial de los síntomas («remisiones»).[25][27][32][33][34][35]
- Secundaria progresiva (EMSP) se presenta tras 10 a 20 años de una EMRR. Consiste en un empeoramiento progresivo y gradual de la discapacidad con o sin exacerbaciones agudas. Entre un 30 y un 50 % de los pacientes con la forma recurrente-remitente eventualmente evolucionarán a una forma secundaria progresiva.[25][27][33][34][35][36]
- Primaria progresiva (EMPP) alrededor del 10 % al 15 % de los pacientes lo presenta. En este subtipo no se presentan los ataques o brotes, comienza de manera insidiosa y empeora gradualmente desde el inicio de la enfermedad progresando más rápido en su incapacidad respecto de los otros subtipos.[25][28][34][35][37]
- Progresiva-recurrente (EMPR) o también, progresiva-remitente o progresiva-recidivante. Esta clasificación representa el subtipo más agresivo de la enfermedad que afecta entre un 3 % a un 5 % de los casos. Progresa en forma continua desde el inicio de la enfermedad, presentando exacerbaciones severas periódicas. Este subtipo se considera una forma más severa de la EMPP.[25][27][28][34][35]
La actividad de la enfermedad se establece considerando:
- Cantidad de brotes en un tiempo determinado.
- Grado de discapacidad.
- Lesiones cerebrales visibles en la resonancia magnética.
La enfermedad se considera «no activa», cuando los tres parámetros mencionados no han avanzado.[8]
Historia[editar]
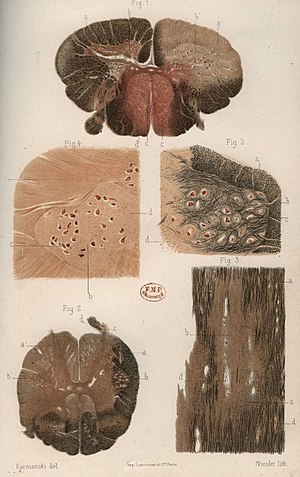
La descripción más antigua de una probable esclerosis múltiple se encuentra en la Saga de Thorlak, de Torlak de Islandia (1133-1193) donde se menciona la ceguera, sordera y los disturbios del lenguaje de Halla, una mujer vikinga, que se habría recuperado milagrosamente. Asimismo, en un texto relacionado se describe el caso de otra mujer llamada Halldora que padecía de parálisis entre 1193 y 1198 cuyo cuadro clínico se corresponde con una esclerosis múltiple remitente-recurrente.[38][39]
Robert Hooper (1773-1835), un patólogo británico y médico en ejercicio, Robert Carswell (1793-1857), profesor británico de patología, y Jean Cruveilhier (1791-1873), un profesor de anatomía patológica francés, fueron los primeros en describir la enfermedad con ilustraciones médicas y detalles clínicos, pero no lo identificaron como una enfermedad distinta. Para ser más exactos, Carswell describió lesiones que eran "remarcables lesiones de la médula espinal acompañadas de atrofia".[40][41]
También usando el microscopio, el patólogo sueco Georg Eduard von Rindfleisch (1836–1908) anotó en 1863 que las lesiones asociadas estaban distribuidas alrededor de los vasos sanguíneos.
Basándose en esto, Jean-Martin Charcot (1825-1893), un neurólogo francés, resumió los datos anteriores y realizó importantes contribuciones con las observaciones clínicas y patológicas propias. Reconoció la esclerosis múltiple (a la que denominó sclérose en plaques disséminées como una enfermedad distinta y separada).
Tras los trabajos de Charcot, varios investigadores como Eugène Devic (1858-1930), Jozsef Balo (1895-1979), Paul Ferdinand Schilder (1886-1940) y Otto Marburg (1874-1948) encontraron casos especiales de la enfermedad que ahora se conocen como formas limítrofes de la esclerosis múltiple, ya que algunos autores los clasifican como esclerosis múltiple y otros no. Estos casos son un caso clínico especial, la enfermedad de Devic, también conocida como esclerosis múltiple óptico-espinal o neuromielitis óptica, NMO), tres formas patológicas (esclerosis concéntrica de Balo, esclerosis de Schilder (o esclerosis difusa) y esclerosis de Marburg, también llamada esclerosis aguda o esclerosis maligna), una forma asociada (neuropatía periférica autoinmune) y una enfermedad asociada (encefalomielitis diseminada aguda o ADEM).
Epidemiología[editar]

Desde la casi completa erradicación de la poliomielitis, la esclerosis múltiple es ―tras la epilepsia― la enfermedad neurológica más frecuente entre los adultos jóvenes y la causa más frecuente de parálisis en los países occidentales. Afecta aproximadamente a 1 de cada 1000 personas, en particular a las mujeres.
Los primeros síntomas suelen aparecer en personas entre los 20 y los 40 años, pero también se puede presentar en niños o sobre los 50 años. En niños y personas jóvenes la incidencia en mujeres es el doble que la de los hombres; por otro lado, en paciente sobre 50 años, la incidencia es igual en ambos sexos.[9] Otra excepción a la mayor incidencia en el sexo femenino es la forma primaria progresiva de la enfermedad (EMPP), ya que se desarrolla por igual en hombres y mujeres.
La esclerosis múltiple es casi inexistente en los africanos negros y en las poblaciones indígenas de América y Oceanía,[18] mientras que es muy prevalente en zonas alejadas del Ecuador, como Canadá y Nueva Zelanda.
En general, uno de cada 25 hermanos de un individuo con la enfermedad también se verá afectado. Si un gemelo univitelino se ve afectado, existe hasta un 50 % de probabilidad que el otro gemelo también enferme. Pero solo uno de cada 20 gemelos bivitelinos se verá afectado si su hermano ha enfermado. Si uno de los padres está afectado por la enfermedad, cada uno de los hijos tendrá una probabilidad de 1 entre 40 de desarrollarla de adulto.
Dos estudios realizados en Canadá y Gran Bretaña muestran la siguiente tabla de probabilidades de enfermar según el grado de parentesco:
| Grado de parentesco | Probabilidad de enfermar |
| En la población | ~ 0,2 % |
| Familia en 1.er grado | ~ 3 % |
| Familia en 2.º grado | ~ 1 % |
| Familia en 3.er grado | ~ 0,9 % |
| Gemelos univitelinos | ~ 35 % |
| Hermanos | ~ 4 % |
Distribución geográfica[editar]

La esclerosis múltiple está ampliamente extendida en Europa septentrional donde su mayor prevalencia (200 por cada 100 000 habitantes) se ha relacionado con la falta de vitamina D. En Europa Central su prevalencia es de 80 por cada 100 000 habitantes; en Estados Unidos 8,3 por cada 100 000; en el Sudeste asiático 2,8 por cada 100 000; en África es de menos de 0,5 por cada 100 000.[9]
En los migrantes, si la migración ocurre antes de los 15 años, el inmigrante adquiere la susceptibilidad a la esclerosis de la región a la que se ha desplazado. Si el desplazamiento ocurre después de los 15 años, la persona mantiene la susceptibilidad de su país de origen.[9]
En cambio, en la península arábiga, Asia, América Central y América del Sur continental la frecuencia es mucho menor. En el África Subsahariana es extremadamente rara. Con excepciones importantes, hay un gradiente norte-sur en el hemisferio norte y sur-norte en el hemisferio sur, con las menores frecuencias en las zonas ecuatoriales. En España este gradiente norte-sur se mantiene, la prevalencia media de la península ibérica se puede cifrar en 45 casos por cada 100 000 habitantes.
La esclerosis múltiple, salvo notables excepciones, es más frecuente en latitudes externas, incluyendo América del Norte, Europa, Australia y Argentina. Sin embargo, la frecuencia de la esclerosis múltiple está aumentando en otras regiones y grupos que antes se consideraban de bajo riesgo, tales como hispanos, asiáticos, afroamericanos, y en otros países de América Latina. En México, la prevalencia se incrementó de 1,6 a 12 pacientes por cada 100 000 habitantes los últimos años.[42][18]
La probabilidad de enfermar es tanto menor cuanto más tiempo se haya convivido con los hermanos. Más de cinco años de contacto reduce el riesgo. La explicación sería que la exposición a temprana edad a infecciones regula hacia abajo la respuesta inmune.[43]
Países asiáticos[editar]
Asia del Este[editar]
- Japón: la prevalencia era de 16.2 cada 100 000 habitantes en 2011. La relación mujer:hombre es de 3,38:1 en 2011. La edad de comienzo promedio es 28.3 años en 2011.[44]
- China: la prevalencia era de 1,39 cada 100 000 habitantes. La relación mujer:hombre es de 3,38:1. La edad de comienzo promedio es 32.6 años en 2006.[44]
- Corea: la prevalencia era de 2,4 a 3,6 cada 100 000 habitantes en 2005. La relación mujer:hombre es de 2:1. La edad de comienzo promedio es 30.4 años.[44]
- Hong Kong: la prevalencia era de 0,77 a 4,8 cada 100 000 habitantes. La relación mujer:hombre es de 3:1 en 2001. La edad de comienzo promedio es 25.9 años.[44]
- Taiwán: la prevalencia era de 2,96 cada 100 000 habitantes el 2005. La relación mujer:hombre es de 2.5:1. La edad de comienzo promedio es entre 30 y 41.88 años.[44]
Sudeste asiático[editar]
- Malasia: la prevalencia era de 2 cada 100 000 habitantes el 2005. Afecta más a mujeres que hombres. La edad de comienzo promedio es entre 28.6 años.[44]
- Tailandia: la prevalencia era de 2 cada 100 000 habitantes el 1993. La relación mujer:hombre es de 6.2:1. La edad de comienzo promedio es entre 33 años.[44]
Asia del Sur[editar]
- India: la prevalencia es de 8,35 cada 100 000 habitantes. La relación mujer:hombre es de 1.6:1. La edad de comienzo promedio es entre 38.3 años.[44]
- Pakistán: La relación mujer:hombre es de 1,45:1. La edad de comienzo promedio es entre 27 años.[44]
- Irán: la prevalencia era de 54.5 cada 100 000 habitantes el 2013. La relación mujer:hombre es de 1.6:1. La edad de comienzo promedio es entre 38.3 años.[44]
Etiología[editar]
La causa de la esclerosis múltiple es desconocida. Se cree que se produce por una combinación de factores predisponentes genéticos e influencias medioambientales. Estas últimas incluyen los niveles de vitamina D, la exposición solar, el tabaquismo y algunas infecciones virales.[42][45][46]
La epigenética de la esclerosis múltiple relaciona ciertas infecciones virales, como la del virus Epstein-Barr, la deficiencia de vitamina D, factores dietéticos (catequinas, isoflavonas o arctigenina), microbiota y exposición a elementos ambientales (tabaco, metales, solventes) con modificaciones en la incidencia de la enfermedad.[10][42] El aumento de la permeabilidad intestinal puede provocar o empeorar la enfermedad, por su relación con el paso incontrolado de sustancias a la sangre, lo que puede desencadenar una respuesta anormal del sistema inmunitario.[15][47]
Factores genéticos[editar]
La prevalencia de la esclerosis múltiple presenta una agregación familiar; comparado con el 0,1 % a 0,3 % de la prevalencia en la población general, los hermanos de individuos afectados por la enfermedad presentan un riesgo de presentarla entre 10 a 20 veces mayor (2 % a 4 %); padres e hijos de afectados por la enfermedad tienen riesgo de un 2 %, y parientes de segundo y tercer grado un 1 %. Los gemelos monocigóticos presentan un riesgo aun mayor (25 % a 30 %).[10][48]
Otro factor que apoya la heredabilidad de la esclerosis múltiple es la distribución mundial de su prevalencia. Las personas que viven en Europa del Norte y Norteamérica presentan una mayor incidencia al compararlos con los europeos del sur. Además, la esclerosis múltiple es rara en ciertos grupos étnicos tales como uzbecos, saamis, turcos, kirguís, kazajos, nativos de Siberia, indígenas de América, japoneses, chinos, negros africanos, y maoríes de Nueva Zelanda. Aunque parte de esta situación puede ser explicada por factores ambientales, la existencia de grupos raciales ancestrales resistentes a la esclerosis múltiple sugiere que la arquitectura del ADN influye en el riesgo de padecer la enfermedad.[10]
La esclerosis múltiple aparece principalmente en caucásicos. Es 20 veces menos frecuente entre los inuit de Canadá que entre los demás canadienses que viven en la misma región. Estos ejemplos señalan que la genética tiene un papel importante en el desarrollo de la enfermedad.
Las observaciones epidemiológicas, especialmente la relación no linear entre la distancia genética de un probando y el riesgo de por vida de desarrollar la esclerosis múltiple, sugieren una herencia poligénica de la enfermedad, siguiendo el paradigma «enfermedad común-variante común» de la genética y la herencia. De acuerdo con este modelo, el riesgo total de padecer la esclerosis múltiple es el resultado de la contribución de múltiples genes polimórficos con alelos de riesgo comunes, cada uno determinando una porción del riesgo total. Este patrón de transmisión no medeliano no es exclusivo de la esclerosis múltiple sino que se puede observar en otras enfermedades autoimunes y crónicas tales como la diabetes tipo II y la obesidad, denominadas en conjunto «enfermedades genéticas complejas» que se caracterizan por el riesgo poligénico y la interacción gen-ambiente multifacético.[10]
Se han encontrado nuevos factores genéticos que causan la esclerosis, como son la mutación R92Q en el gen TNFRSF1A y el síndrome auto inflamatorio TRAPS. También se ha demostrado que el gen IL7RA que codifica a la proteína IL7RA-alfa puede ser un factor que esté relacionado con la esclerosis múltiple. El factor HLA-DRB1 que se encuentra en la región del cromosoma 6, contiene muchos genes que están relacionados con el reconocimiento de los antígenos del sistema inmune, siendo un factor posible relacionado con la esclerosis múltiple.
Complejo mayor de histocompatibilidad y esclerosis múltiple[editar]
La asociación entre el complejo mayor de histocompatibilidad y los antígenos leucocitarios humanos con la esclerosis múltiple se ha observado desde hace décadas. La asociación más fuerte se da en el locus HLA-DRB1.[49]
Genes específicos que se han relacionado con esclerosis múltiple incluyen diferencias en el sistema HLA (human leukocyte antigen), un grupo de genes del cromosoma 6 equivalentes al sistema mayor de histocompatibilidad (MHC). El descubrimiento más importante en la asociación entre la esclerosis múltiple y los alelos del sistema MHC fueron DR15 y DQ6; existen otros loci a los que se les ha asociado un efecto protector, tales como HLA-C554 y HLA-DRB1* 11. Nuevos métodos genéticos han demostrado que al menos existen doce genes fuera del sistema HLA capaces de aumentar la probabilidad de padecer esclerosis múltiple.
Factores ambientales[editar]
Se considera que la esclerosis múltiple aparece cuando se da una combinación de factores ambientales en personas genéticamente predispuestas a adquirirla. El clima, la dieta, toxinas, la luz solar y/o enfermedades infecciosas son algunos de los factores planteados como desencadenantes de la enfermedad.
Diversos virus han sido propuestos como agentes generadores de la esclerosis múltiple, como el virus de Epstein-Barr (EBV), de la varicela o del herpes zóster.[9][13] Un estudio longitudinal publicado en 2022 en el que se realizó un seguimiento de militares estadounidenses activos entre 1993 y 2013 revela que el riesgo de desarrollar esclerosis múltiple aumenta 32 veces después de una infección por el virus de Epstein-Barr.[50]
La presencia de rasgos de autoinmunidad y defectos en la producción de enzimas antioxidantes son factores de riesgo para padecer la enfermedad.[51]

Entre los factores ambientales, diversos componentes dietéticos parecen desempeñar un papel en el desarrollo y progreso de la esclerosis múltiple y otras enfermedades autoinmunes, tales como la carencia de vitamina D, la presencia del gluten y las proteínas de la leche, entre otros.[53]
La esclerosis múltiple es una de las diversas enfermedades que pueden desarrollarse o agravarse como consecuencia de una permeabilidad intestinal aumentada o "intestino permeable". Cuando hay un aumento excesivo de la permeabilidad intestinal, se produce un paso incontrolado de todo tipo de sustancias a la sangre (virus, bacterias, toxinas, alimentos no digeridos...), lo que puede provocar respuestas inmunitarias locales y sistémicas (en cualquier parte del organismo).[15][47] Los dos factores más potentes que causan el aumento de la permeabilidad intestinal son ciertas bacterias intestinales y la gliadina, que es la principal fracción tóxica del gluten,[16] en cualquier persona que lo come e independientemente de la predisposición genética, es decir, tanto en celíacos como en no celíacos.[17][52][47] El descubrimiento del papel de la permeabilidad intestinal en el desarrollo de estas enfermedades desbarata las teorías tradicionales y sugiere que estos procesos pueden ser detenidos si se impide la interacción entre los genes y los factores ambientales desencadenantes, a través del restablecimiento de la función de la barrera intestinal.[16]
Radiación Ultravioleta (UV) y vitamina D[editar]
Los individuos que migran a regiones de alta prevalencia antes de los 15 años tiene mayor riesgo de desarrollar la enfermedad; este fenómeno ha sido atribuido al grado de exposición a los rayos UV, ya que en latitudes de 40° al norte o sur, donde es más frecuente la enfermedad, la exposición a los rayos solares y el índice de radiación UV es menor.[54] Por otro lado, la forma activa de la vitamina D o 1,25-hydroxyvitamin D3, se sintetiza en la piel gracias a la exposición de luz solar. Los niveles bajos en sangre de esta hormona esteroidea ha sido asociada al incremento en el riesgo de padecer esclerosis múltiple atribuido por un efecto en la inmunidad.[55]
Otros factores ambientales[editar]
El tabaquismo, la exposición a metales (mercurio, plata, oro, solventes orgánicos, pegamento), están estrechamente asociados a la aparición o empeoramiento de las lesiones desmielinizantes.[56][57][58] Además de todo esto también se han propuesto otras causas como el estrés, aunque hay pruebas que sustentan que es débilmente relacionado. La vacunación fue estudiada también como un factor causal, sin embargo, no se encontró ninguna relación.
También se ha determinado la hipótesis de la higiene que propone que la exposición a ciertos agentes infecciosos en las primeras etapas de la vida es protectora para esclerosis múltiple, y si existen condiciones higiénicas en extremo, como los países desarrollados, donde se evita este contacto, entonces no se cuenta con esta profilaxis y se desarrolla la enfermedad. Este supuesto no se ha demostrado, por lo que no existe una recomendación para someterse a una exposición innecesaria a agentes infecciosos.
En pacientes con esclerosis múltiple la gota aparece con menos frecuencia y los niveles de ácido úrico son inferiores de lo que cabría esperar. Esto ha llevado a la teoría de que el ácido úrico es protector, aunque su importancia exacta sigue siendo desconocida.[cita requerida]
En 2009 se propuso la relación con una enfermedad vascular conocida como insuficiencia venosa cerebroespinal crónica. No obstante, actualmente las evidencias demuestran que se trata de una hipótesis equivocada.[59]
Fisiopatología[editar]
Las principales características de la esclerosis múltiple son la formación de lesiones en el sistema nervioso central (también denominadas placas), en las cuales hay inflamación y la destrucción de las vainas de mielina (formadas por los oligodendrocitos) que recubren los axones (prolongaciones neuronales). Las lesiones interactúan de una manera compleja dañando el tejido nervioso, lo cual provoca los signos y síntomas de la enfermedad. El daño está causado al menos en parte, por el ataque del sistema nervioso de una persona mediado por su propio sistema inmune.[60][61]
Los tejidos del sistema nervioso y de la médula espinal están protegidos por un sistema de vasos capilares, llamado barrera hematoencefálica, que en los pacientes de esclerosis múltiple disfunciona. Por causas desconocidas, macrófagos y linfocitos pueden cruzar la BHE y comenzar un ataque autoinmune.
Se ha conseguido reconstruir el proceso del ataque del sistema inmunitario a la mielina a partir de observaciones en los tejidos dañados y el estudio de la encefalomielitis experimental autoinmune (o EAE, de sus siglas en inglés), que es una enfermedad similar a la esclerosis múltiple que puede ser inducida en los roedores para fines de investigación.
En la esclerosis múltiple hay inflamación, desmielinización, gliosis reactiva (generación de cicatrices) y daño axonal. El daño al tejido en la esclerosis múltiple es el resultado de una interacción compleja y dinámica entre el sistema inmune, la glía (oligodendrocitos que producen mielina y sus precursores, la microglía y los astrocitos) y las neuronas.
La barrera hematoencefálica (BHE) normalmente protege al sistema nervioso central. En la esclerosis múltiple hay disfunción de la BHE, lo cual permite la infiltración de células del sistema inmune hacia el tejido del sistema nervioso central. Cuando se realizan estudios de resonancia magnética (IRM) se puede detectar el daño en la BHE al observar lesiones que captan el medio de contraste (gadolinio). La permeabilidad vascular anormal precede a la desmielinización inflamatoria, en la cual hay daño a los oligodendrocitos que recubren los axones.
Desmielinización e inflamación en esclerosis múltiple[editar]
Los linfocitos T, llamados células CD4-Th1-T, tienen una función clave en el desarrollo de la enfermedad. Bajo circunstancias normales, estos linfocitos pueden distinguir entre células propias y ajenas. En una persona con esclerosis múltiple, sin embargo, las células reconocen partes sanas del sistema central como ajenas y las atacan como lo harían con un virus. En la esclerosis múltiple, la parte atacada es la mielina, una sustancia grasa que cubre los axones de las células nerviosas y que es importante para una transmisión nerviosa adecuada.
En estado normal, existe una barrera entre el sistema nervioso central y la sangre llamada barrera hematoencefálica, que está formada por células endoteliales tapizando las paredes de los vasos sanguíneos. Por causas desconocidas, en los pacientes de esclerosis múltiple esta barrera no funciona bien, y las células T autorreactivas la cruzan. A partir de este momento, estas células T van a atacar la mielina del sistema nervioso, produciendo desmielinización. La inflamación es facilitada por otras células inmunitarias y elementos solubles, como la citocinas y los anticuerpos. A causa de este comportamiento anormal del sistema inmunitario, la esclerosis múltiple es considerada una enfermedad autoinmunitaria.
La inflamación finalmente lleva al daño de la barrera hematoencefálica, lo que puede acarrear problemas como inflamación (edema). También causa la activación de macrófagos, de metaloproteinasas y otras proteasas y citocinas. Finalmente llevará a la destrucción de la mielina, proceso llamado desmielinización.
Las células involucradas en el daño inflamatorio de origen autoinmune en esclerosis múltiple son principalmente linfocitos (linfocitos T y linfocitos B), macrófagos y microglia. Se han descrito linfocitos T auxiliares (CD4 +) y citotóxicos (CD8 +) en lesiones de esclerosis múltiple: las células T CD4 + están más concentradas en el manguito perivascular, mientras que las células T CD8 + están ampliamente distribuidas dentro del parénquima. A medida que avanza la enfermedad, aumenta la proporción relativa de linfocitos B y las células plasmáticas. El papel de las linfocitos B en esclerosis múltiple también se demuestra al detectar anticuerpos de producción intratecal (bandas oligoclonales). Otras funciones de los linfocitos B son: la presentación de antígenos a los linfocitos T y la producción de citocinas.
La microglia y los macrófagos mantienen un estado crónico de activación en el transcurso de la enfermedad, formando placas que lesionan la mielina y los oligodendrocitos. También los oligodendrocitos pueden volverse disfuncionales y morir, causando daño tisular por pérdida del soporte metabólico a los axones. Entonces, de manera secundaria, hay muerte neuronal y pérdida de tejido (atrofia cerebral). Dicho proceso se autoperpetúa llevando a discapacidad irreversible (Jarius 2017). En las lesiones crónicamente desmielinizadas, los axones desnudos permanecen vulnerables y pueden degenerarse lentamente; posibles mecanismos incluyen el transporte axonal alterado, la disfunción mitocondrial y el aumento de la demanda de energía relacionada con los canales iónicos.
La esclerosis múltiple en su evolución conduce a la pérdida gradual neuroaxonal que se correlaciona con la discapacidad del paciente, atrofia cerebral y múltiples cicatrices gliales escleróticas en la sustancia blanca. La desmielinización también afecta sustancia gris de la corteza, los núcleos de la base y la médula espinal. La neuroplasticidad se encarga de remielinización aunque generalmente de manera incompleta.
La inflamación está presente en todas las etapas de la esclerosis múltiple, pero es más pronunciada en las fases agudas que en las crónicas. A medida que la enfermedad progresa, la inflamación se focaliza dentro del SNC. Se pueden formar estructuras linfáticas terciarias en las meninges,[62] y hay evidencia creciente de que la inflamación meníngea desempeña un papel importante en la patología de la corteza en etapas progresivas.[63]
Tipos de lesiones[editar]
La National Multiple Sclerosis Society (de Estados Unidos) ha lanzado un proyecto llamado The Lesion Project[64] para catalogar todos los tipos de lesiones posibles y desarrollar un modelo más preciso de cómo ocurren las cosas. Se han encontrado cuatro familias de lesiones diferentes pero no hay un consenso en cuanto al significado de este hecho. Unos piensan que esto significa que la esclerosis múltiple es realmente una familia de enfermedades. Otros piensan que las lesiones pueden cambiar de un tipo a otro con el tiempo o según el individuo. Las cuatro familias o "patrones" son los siguientes:
- Patrón I: La lesión presenta células T y macrófagos alrededor de vasos capilares. Los oligodendrocitos están más o menos intactos y no hay signos de activación del sistema inmune complementario (anticuerpos).
- Patrón II: La lesión también presenta células T y macrófagos alrededor de los capilares. Los oligodendrocitos también se preservan, pero aparecen signos de activación del complemento.
- Patrón III: Las lesiones son difusas y presentan inflamación. Los oligodendrocitos presentes están dañados (oligodendrogliopatía distal). Hay también signos de activación de la microglia y pérdida de MAG (proteína constituyente de la mielina, del inglés myelin associated glycoprotein). Las lesiones no rodean los vasos capilares y hay un anillo de mielina intacta alrededor de ellos. También aparece una remielinización parcial y apóptosis de oligodendrocitos.
- Patrón IV: La lesión presenta bordes abruptos y oligodendrocitos degenerados, con un anillo de mielina. Ausencia de oligodendrocitos en el centro de la lesión. No está activado el complemento ni hay perdida de MAG.
Los dos primeros patrones se consideran ataques autoinmunes contra la mielina y los dos últimos contra los oligodendrocitos.[65] Los dos primeros patrones son además similares a los producidos en EAE (encefalomielitis alérgica experimental).
Las formas limítrofes de la esclerosis múltiple también presentan lesiones incluidas en estos patrones. Así la neuromielitis óptica tendría lesiones mediadas por activación de complemento (patrón II). La esclerosis concéntrica de Baló mostraría pérdida de MAG según el patrón III y la esclerosis múltiple progresiva primaria se correlacionaría con el patrón IV.[65]
Tipos de placas en la esclerosis múltiple[editar]
Las lesiones de esclerosis múltiple pueden ser clasificadas en cuatro inmunopatrones sobre la base de la pérdida específica de proteína de la mielina, la extensión de la placa y la topografía, la destrucción de oligodendrocitos, la deposición de inmunoglobulinas y la activación del complemento.[66]
Patrón I: se encuentran en el 15 % de los pacientes con esclerosis múltiple, se asocian principalmente con inflamación de células T, desmielinización activa, con muchos macrófagos activados, ausencia de inmunoglobulina y deposición del complemento. Estas características sugieren que la desmielinización y la lesión tisular pueden estar mediadas por productos tóxicos producidos por macrófagos activados. Estas lesiones tienen bordes claramente demarcados y la típica distribución perivenosa que, por confluencia, da como resultado grandes placas desmielinizadas.
Patrón II: encontradas en el 58 % de pacientes con esclerosis múltiple, muestran no solo infiltración densa con linfocitos T y macrófagos cargados de mielina, sino también deposición de inmunoglobulina y activación del complemento sobre mielina y dentro de macrófagos en sitios desmielinizantes activos sitios, con axones conservados. Este hallazgo sugiere que los mecanismos mediados por anticuerpos y el complemento pueden inducir la desmielinización y la lesión tisular. Estas lesiones también tienen bordes demarcados, típica distribución perivenosa que por confluencia dan grandes placas desmielinizadas, y exhiben pérdida variable de oligodendrocitos en el borde lesional activo, con la reaparición de numerosos oligodendrocitos en el centro de la placa inactiva.
Patrón III: encontradas en el 26 % de pacientes con esclerosis múltiple se definen por apoptosis de oligodendrocitos, inflamación de linfocitos T, activación de macrófagos y microglías y pérdida preferencial temprana de glicoproteína asociada a la mielina. Hay una pérdida pronunciada de oligodendrocitos en el borde de la placa activa. El centro inactivo está desprovisto de oligodendrocitos. La deposición de inmunoglobulina y complemento está ausente. Las lesiones tienen bordes mal definidos y no están centradas en venas o vénulas.
Daño axonal en la esclerosis múltiple[editar]
La neurodegeneración es una parte temprana de esclerosis múltiple que se autoperpetúa y debe considerarse una segunda fase de la esclerosis múltiple, sino un proceso concomitante que ya está en marcha en el momento del diagnóstico clínico.[67] El daño axonal puede detectarse incluso en lesiones de la esclerosis múltiple donde los axones aún están mielinizados y la pérdida de la reserva funcional se correlaciona con la discapacidad.
La esclerosis múltiple es también una enfermedad de la sustancia gris, la desmielinización cortical es más extensa de lo que se creía previamente. La corteza se afecta con placas clásicas desmielinizadas o como pérdida neuronal y atrofia después de la degeneración retrógrada de las lesiones de la sustancia blanca.[68]
Debido a su ubicación, se han descrito tres tipos de lesiones corticales.[69]
Las lesiones subpiales se extienden desde la superficie pial hacia las capas corticales más profundas, alcanzando generalmente la capa cortical tres o cuatro, y son más comunes en la esclerosis múltiple crónica. También pueden extenderse a todo el ancho de la corteza, con o sin afección de la sustancia blanca subcortical, y pueden afectar varias circunvoluciones.
Las lesiones intracorticales son pequeñas perivasculares confinadas a la corteza y que evitan tanto la corteza superficial como la sustancia blanca.
Las lesiones leucocorticales afectan tanto a la sustancia gris como a la blanca en su unión y evitan las capas corticales superficiales.
La desmielinización cortical más extensa se ha detectado en la circunvolución cingulada y las cortezas temporales, frontales, insulares y cerebelosas. También se ha detectado una desmielinización extensa en el hipocampo de pacientes con esclerosis múltiple progresiva. La desmielinización cortical es más prominente en la esclerosis múltiple progresivas, y puede tener un importante correlato patológico de discapacidad irreversible y deterioro cognitivo.[70]
Desmielinización[editar]
En estado normal, existe una barrera entre el sistema nervioso central y la sangre llamada barrera hematoencefálica, que está formada por células endoteliales tapizando las paredes de los vasos sanguíneos. Por causas desconocidas, en los pacientes de esclerosis esta barrera no funciona bien, y las células T autorreactivas la cruzan. A partir de este momento, estas células T van a atacar la mielina del sistema nervioso, produciendo una desmielinización.
A la vez aparece un proceso inflamatorio. La inflamación es facilitada por otras células inmunitarias y elementos solubles, como la citocina y los anticuerpos. A causa de este comportamiento anormal del sistema inmunitario, la esclerosis múltiple es considerada una enfermedad autoinmunitaria.
Ampliamente aceptado es que un subtipo especial de linfocitos, llamados células CD4-Th1-T, tienen una función clave en el desarrollo de la enfermedad. Bajo circunstancias normales, estos linfocitos pueden distinguir entre células propias y ajenas. En una persona con esclerosis múltiple, sin embargo, las células reconocen partes sanas del sistema central como ajenas y las atacan como lo harían con un virus. En la esclerosis, la parte atacada es la mielina, una sustancia grasa que cubre los axones de las células nerviosas y que es importante para una transmisión nerviosa adecuada.
La inflamación finalmente lleva a la apertura de la barrera hematoencefálica, lo que puede acarrear problemas como edemas. También causa la activación de macrófagos, de metaloproteinasas y otras proteasas y citocinas. Finalmente llevará a la destrucción de la mielina, proceso llamado desmielinización.
Remielinización[editar]
Los pacientes con esclerosis múltiple con una mayor capacidad de remielinización tienen menor discapacidad.[71] Más del 40 % de las lesiones crónicas de esclerosis múltiple muestran evidencia de remielinización y en aproximadamente el 20 % de los pacientes con esclerosis múltiple, la remielinización es extensa.[72]
La sustancia gris remieliniza más rápidamente que la sustancia blanca en las lesiones leucocorticales, y puede estar relacionada con niveles más bajos de inhibidores de la remielinización dentro de las lesiones corticales o diferencias en la actividad de las células inmunes innatas.[73]
La remielinización es una de las razones por las que, especialmente en las primeras fases de la enfermedad, los síntomas tienden a disminuir o desaparecer después de días a meses. La remielinización en la esclerosis múltiple también debe considerarse en el contexto del envejecimiento, ya que, independientemente del curso de la enfermedad, los pacientes más jóvenes tienen una mayor probabilidad de recuperación. Aún se desconoce por qué la remielinización es extensa en algunos pacientes cuando falla en otros y por qué las áreas remielinizadas son más vulnerables que la sustancia blanca normal a la desmielinización secundaria.[74] Una hipótesis sería que una lesión inmunomediada inicial también afectaría a las células precursoras de oligodendrocitos y a las nuevas vainas de mielina.[75] Los insultos desmielinizantes repetidos podrían agotar la fuente de las células precursoras de oligodendrocitos,[76] que sumado a la lesión axonal alteran las interacciones apropiadas para la remielinización, ya que los axones proporcionan señales críticas a los oligodendrocitos en el proceso de mielinización.[77] La cicatriz glia densa que se forma dentro de las placas y en sus bordes funciona como una barrera entre el tejido dañado inflamado y el cerebro normal, lo que impide que las células precursoras de oligodendrocitos migren hacia las lesiones.
Daño axonal en esclerosis múltiple[editar]
A través de la resonancia magnética y otros sistemas, se ha demostrado que el daño a los axones es una de los principales causas del desarrollo de discapacidad y pérdida del volumen cerebral (atrofia). Se ha demostrado que esta lesión interviene no solo en formas crónicas o en estadios tardíos de la enfermedad, sino que está presente formas tempranas de la enfermedad.
Los síntomas de la esclerosis múltiple son causados por lesiones múltiples en el sistema nervioso central y pueden variar mucho entre individuos, dependiendo de dónde ocurran las lesiones. La plasticidad del cerebro a menudo puede compensar una parte del daño, sobre todo en las primeras etapas de la enfermedad.
Factores que provocan una recaída[editar]
Un brote o una recaída de la esclerosis múltiple consiste en la aparición de nuevos síntomas o un empeoramiento de los existentes. La frecuencia de los brotes en etapas tempranas de la esclerosis múltiple está relacionada con el grado de discapacidad en el futuro, por lo que evitarlos es clave para mejorar el pronóstico del paciente. Al igual que los síntomas son muy variados, sus desencadenantes también lo son, por lo que los pacientes evitan aquellas circunstancias que consideran que empeoran su estado.
¿Qué factores evitables pueden desencadenar un brote de la esclerosis múltiple?[78]
- El calor y, en particular, los baños de agua caliente: La mayoría de las personas con esclerosis múltiple considera que los ambientes calurosos empeoran de forma transitoria los síntomas de la enfermedad. Se recomienda, por tanto, no exponerse a las altas temperaturas, bañarse con agua templada en invierno y hacerlo frío en verano, y protegerse del calor excesivo en los meses cálidos. Las recaídas tienden a ocurrir con más frecuencia durante la primavera y el verano, y se reducen en las estaciones de más frío, lo que demuestra la gran asociación de la temperatura con el agravamiento de la enfermedad.
- El denominado fenómeno de Uhthoff consiste en el empeoramiento clínico debido al aumento de la temperatura corporal. Por ende, cualquier factor tanto externo como interno que contribuya a incrementar la temperatura podrá ser causante de la aparición de un nuevo brote de esclerosis múltiple. Así, el deporte aumenta la gravedad clínica y por ello se desaconsejan ejercicios extenuantes y la fatiga.
- Infecciones: un catarro, un resfriado o una diarrea aumentan el riesgo de recaída. Además, por lo general, las vacunas con virus vivos atenuados también aumentan la aparición de brotes. La vacuna contra la gripe es inocua y no provoca recaídas como se ha demostrado en diversos estudios recientes. La vacuna del tétanos también se considera inocua, aunque no ha sido estudiada con detalle.
- El embarazo: Los últimos tres meses de embarazo ofrecen una protección natural contra la recaída, mientras que los primeros meses, y especialmente las primeras seis semanas, el riesgo aumenta entre un 20 y un 40 %. La esclerosis múltiple no es una enfermedad genética en sí, por lo que la transmisión de la enfermedad no va a suceder (Ver sección «Genética»).
- El estrés emocional. Varios estudios han concluido que el estrés contribuye en gran parte a la aparición de la enfermedad, si bien los resultados no son del todo concluyentes.
- La contaminación ambiental. Niveles de contaminación elevados se asocian a un mayor riesgo de sufrir brotes, especialmente en los 3 días anteriores al brote. El tabaquismo también es un posible inductor de recaída.
Cuadro clínico[editar]
Los síntomas de la esclerosis múltiple se desarrollan a lo largo de varios días, expresándose de acuerdo a la zona afectada y en un tiempo variable de forma máxima tras transcurrir una a dos semanas de enfermedad, para luego en la mayoría de los casos ir disminuyendo y eventualmente resolverse en semanas o meses. Los síntomas usualmente son múltiples. Pueden quedar síntomas remanentes crónicos, especialmente los sensitivos. Las manifestaciones dependen de la localización del foco de desmielinización, pero típicamente se presenta como un trastorno sensitivo y/o motor en una o más extremidades (50 % de los pacientes), neuritis óptica (síntoma inicial en el 25 % de los pacientes), diplopía, ataxia, vejiga neurogénica, fatiga, disartria, neuralgia del trigémino (en menos del 10 %), nistagmo, vértigo. En forma más rara puede presentarse afasia, apraxia, convulsiones, demencia, corea y rigidez.[13]
El signo de Lhermitte es un rasgo clínico frecuente de la esclerosis múltiple; se trata de una sensación de tipo eléctrico que recorre la espalda en sentido caudal hasta las piernas, cuando se flexiona el cuello. Dicha sensación se da en el 30 % o más de los pacientes.
La fatiga es otro de los síntomas comunes de la esclerosis múltiple, que suele en muchas ocasiones interferir su vida diaria imposibilitando o entorpeciendo su desempeño académico, laboral e incluso sus relaciones interpersonales.
Las lesiones del sistema nervioso central que causan la esclerosis múltiple no siempre se manifiestan directamente como síntomas clínicos detectables y claramente atribuibles a la enfermedad, por lo que en ocasiones se tiende a restar importancia a los primeros signos.
Aunque en algunas ocasiones al principio de la esclerosis múltiple se acumula poca discapacidad y la calidad de vida no se ve demasiado afectada, la realidad es que el sustrato de la enfermedad ya se está desarrollando. De lo que ocurra en las fases iniciales de la esclerosis múltiple, depende en gran medida su evolución posterior. En otras palabras, las lesiones de hoy en el sistema nervioso central, son la causa de la discapacidad de mañana.
Síntomas motores[editar]
Las alteraciones motoras suelen presentarse como diversos grados de debilidad, rara vez presentando pérdida total de la fuerza de algún lado del cuerpo (hemiplejía). Los reflejos tendinosos profundos (p. ej., el rotuliano y el aquileano) suelen estar aumentados y a menudo se presenta una respuesta plantar extensora (signo de Babinski) y clonus. Los diversos grados de debilidad, pueden ir desde una leve paresia hasta grados de debilidad avanzada que puede dejar al paciente confinado a una silla de ruedas y/o cama. Más tarde pueden aparecer espasmos flexores dolorosos en respuesta a los estímulos sensitivos. Las lesiones cerebrales o de la médula espinal con más frecuencia cervical pueden producir una hemiparesia, que a veces es el síntoma de presentación.
Neuritis óptica[editar]
Se manifiesta típicamente con las siguientes características;
- Dolor. La mayoría de las personas que padecen neuritis óptica sienten dolor ocular que empeora con el movimiento del ojo[79].
- Pérdida de visión de un ojo. Se sufre por lo menos alguna reducción temporal de la visión, pero el grado de pérdida varía. La pérdida notoria de visión generalmente se produce con el paso de las horas o después de unos días y mejora en el transcurso de varias semanas o meses.
- Pérdida del campo visual. La pérdida de visión periférica se puede producir en cualquier patrón.
- Pérdida de visión cromática. A menudo afecta la percepción de la intensidad de los colores.
Vértigo[editar]
El vértigo es una sensación en las que las personas tienen la percepción de que el entorno o ellas mismas se mueven. Se calcula que alrededor del 20 % de los afectados de esclerosis múltiple pueden sufrirlo en alguna ocasión, cuando la enfermedad provoca algún problema en la zona del cerebro que controla el equilibrio o como cualquier otra persona, cuando se afecta alguno de los sistemas que regulan la sensación del equilibrio. Las caídas en personas con esclerosis múltiple son un problema común.[7][80]
Sintomatología cognitiva[editar]
Si bien antiguamente se consideraba que no existían déficits cognitivos en la esclerosis múltiple, sino que era una enfermedad fundamentalmente física; actualmente se sabe que es común un patrón de déficit cognitivo específico.
El patrón que siguen los déficits cognitivos es un patrón fronto-subcortical; afectando por tanto a las funciones localizadas en el lóbulo frontal y en las zonas subcorticales.
El déficit cognitivo más acentuado y observado en la esclerosis múltiple es la disminución de la velocidad de procesamiento. Esto es explicado por la desmielinización de los axones de las neuronas, que aparte de proteger el axón de las neuronas, hacen que el impulso nervioso se desplace más rápido. Seguidamente se observan otros déficits cognitivos, pero que pueden deberse al déficit de base anteriormente mencionado. Entre estas otras alteraciones estaría la atención, principalmente atención sostenida, selectiva y alternante. La atención sostenida puede ser difícilmente disociable de la fatiga que estos pacientes muestran. Las alteraciones en la atención conllevan a déficits en la memoria, especialmente en la memoria de trabajo (funciones ejecutivas), y déficits en la codificación y recuperación.
Respecto a los déficits frontales puede haber cambios conductuales (apatía, falta de motivación, pseudodepresión; o por el contrario desinhibición, impulsividad, agresividad e irascibilidad, infantilismo...) y en las funciones ejecutivas (capacidad para planificar, flexibilidad mental, razonamiento...) además de las anteriormente mencionadas.
Los déficits cognitivos que muestran los pacientes son evaluados neuropsicológicamente, y la terapia de rehabilitación suele ayudar a ralentizar el curso de la enfermedad.
Aspectos emocionales[editar]
Dado que la esclerosis múltiple afecta el cerebro y la espina dorsal, es de naturaleza degenerativa y a menudo lleva a una discapacidad progresiva, no es extraño que las personas afectadas sufran dificultades emocionales. Depresión, ansiedad, ira, miedo, junto con otras emociones evidentes se diagnostican a menudo entre las personas que sufren esclerosis múltiple o los allegados.
A pesar de que estos sentimientos son comprensibles, tienen implicaciones sociales, especialmente cuando interfieren con el trabajo, la escuela y la vida familiar. En particular, la depresión lleva asociada el peligro de suicidio.
Todos estos problemas pueden ser solucionados con tratamientos psicológicos y medicación adecuada.
- Depresión
La depresión en estos casos puede originarse tanto en las implicaciones del diagnóstico como en los efectos que produce la enfermedad en el cerebro. El cerebro es un órgano altamente especializado y es el origen de todas las emociones. Cuando un brote afecta la parte del cerebro en que se procesan las emociones, el resultado puede incluir depresiones.
También se ha informado de casos de depresión en algunos pacientes que toman interferón beta (Avonex® o Rebif®) para tratar la enfermedad.
- Ansiedad
La ansiedad también es un problema frecuentemente asociado con la esclerosis múltiple. Al igual que la depresión, puede estar originada por la enfermedad o por las implicaciones del diagnóstico. Las consecuencias cognitivas de la esclerosis múltiple también suelen estar asociadas a ella. No es raro que personas que sufren la enfermedad desarrollen falta de memoria, dificultades en explicar conceptos abstractos, organizar, planificar u olviden determinadas palabras. Estos síntomas pueden generar ansiedad y resultar en una retirada de la vida social.
- Otras alteraciones
La ira es otro sentimiento que puede ir asociado a la esclerosis múltiple y, de hecho, con todas las enfermedades crónicas graves. También se ha informado de la aparición de "risa patológica" y "llanto patológico". Esencialmente se refiere a una reacción inapropiada a la situación, tal como risas en un funeral o llanto al oír buenas noticias. A menudo es consecuencia de la desmielinización de las áreas del cerebro encargadas del juicio.
Diagnóstico de esclerosis múltiple[editar]
El diagnóstico de la esclerosis múltiple depende de la documentación de múltiples episodios neurológicos de exacerbación y remisión de la enfermedad a través del tiempo y en diversos sitios del sistema nervioso central. No existe ninguna prueba o marcador biológico que permita en forma aislada establecer el diagnóstico definitivo de esclerosis múltiple, se requiere en su conjunto de una evaluación clínica que se apoye con estudios paraclínicos como la Resonancia Magnética (IRM), Bandas Oligoclonales en líquido cefalorraquídeo y potenciales evocados.[81][82]
Criterios de diagnóstico[editar]
El Panel Internacional para el Diagnóstico de la Esclerosis Múltiple, estableció las últimas revisiones a los criterios diagnósticos de McDonald en 2017, estos criterios se basan en el número de brotes y la evidencia objetiva de daño neurológico mediante signos clínicos así como en dos pilares fundamentales que son la demostración de la diseminación de las lesiones desmielinizantes en espacio y en el tiempo.[83]
| Número de brotes | Signos clínicos | Requisitos para complementar diagnóstico |
|---|---|---|
| 2 | 2 | Ninguno |
| 2 | 1 | Diseminación en espacio |
| 1 | 2 | Diseminación en tiempo |
| 1 | 1 | Diseminación en tiempo y en espacio |
Brote, recaída o exacerbación-Síntomas de instauración aguda con signos típicos de una afección inflamatoria desmielinizante en SNC, con una duración al menos de 24 horas en ausencia de fiebre o infección.
Signos clínicos-Evidencia Clínica de una lesión desmielinizante que se documenta de forma objetiva mediante la exploración neurológica.
Criterios de Diseminación en espacio de Swanton[editar]
Lesiones desmielinizantes en diferentes regiones del sistema nervioso central. Se requiere al menos una lesión en Resonancia Magnética en secuencia T2 en por lo menos dos de las siguientes 4 áreas:
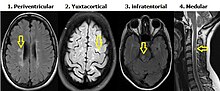
Criterios de Diseminación en tiempo de Montalban[editar]
Afectación en diferentes momentos de la evolución de la enfermedad. La demostración de los cambios temporales de las lesiones desmielinizantes (progresión en número y tamaño de las lesiones), se realiza mediante estudios de seguimiento en IRM cerebral que deben encontrar:
1.-Una nueva lesión en IRM en la secuencia T2
2.-Una lesión que capta gadolinio en el seguimiento por IRM, con referencia a una IRM basal
3.-Presencia de lesiones asintomáticas gadolinio positivas y no gadolinio positivas en cualquier momento.
4.-Nuevo brote.
5.-Bandas Oligoclonales positivas en LCR[84]
Resonancia Magnética
La IRM es la técnica más sensible en la identificación de las placas desmielinizantes, detecta en más del 97 % pacientes con esclerosis múltiple clínicamente definida. Como consecuencia de esta alta sensibilidad, la RM se ha convertido en una técnica esencial, no solo en el diagnóstico de la esclerosis múltiple sino también como marcador pronóstico.
Las lesiones desmielinizantes son múltiples y de pequeño tamaño (menores de 25 mm) de morfología ovoidea o nodular.
Detección de Bandas Oligoclonales (BOC) de IgG
El análisis del LCR sirve para obtener evidencia de la naturaleza inmunitaria e inflamatoria de la enfermedad, en el 50 % de los pacientes hay un incremento discreto de linfocitos en LCR (pleocitosis linfocítica).
El 87-95 % de los pacientes con esclerosis múltiple tiene BOC positivas. Se considera que hay síntesis intratecal de inmunoglobulinas si hay más de dos bandas oligoclonales en el LCR que no se encuentren en suero.
El isoelectroenfoque(IEF) y una tinción inmuno específica para las moléculas de IgG, se ha propuesto como el método más adecuado para la detección de las BOC.[85][86]
Detección de bandas Oligoclonales de IgM
La presencia de BOC de IgM principalmente, las BOC de IgM se han asociado a un pronóstico más agresivo de la enfermedad.
Diagnóstico Diferencial
Dentro de los diagnósticos diferenciales de la esclerosis múltiple hay que descartar principalmente neuromielitis óptica que es más prevalente en la población latinoamericana, EMDA (encefalomielitis diseminada aguda) principalmente en la población pediátrica, manifestaciones neurológicas del VIH, enfermedad de Behcet, sarcoidosis, síndrome de Sjögren, lupus eritematoso sistémico, neuropatía aguda óptica isquémica, síndrome de Susac, síndrome antifosfolípidos, neurosífilis, neurocisticercosis, enfermedad de Lyme, deficiencia de cobre o zinc, enfermedad celíaca, deficiencia de vitamina E, enfermedad de Wilson, porfiria, arteriopatía cerebral autosómica dominante con infartos subcorticales y leucoencefalopatia, linfoma de sistema nervioso central, síndrome paraneoplásico, malformación vascular medular, lesiones desmielinizantes por tóxicos, entre otros.[87]
Criterios de diagnóstico en esclerosis múltiple primaria progresiva
Al menos un año de progresión continua de la enfermedad y al menos 2 de los 3 siguientes hallazgos: IRM de Cráneo con 9 lesiones en T2, IRM medular con 2 lesiones desmielinizantes y un LCR positivo (que demuestre BOC o elevación del índice de IgG).[88]
Tratamiento[editar]
Hasta ahora, no existe un tratamiento curativo disponible para la esclerosis múltiple, de manera que la estrategia se enfoca a reducir la actividad tanto clínica como radiológica y la progresión de discapacidad.[89]
El objetivo primario en el tratamiento de la esclerosis múltiple, especialmente en la variante recurrente, es la reducción de la actividad de la enfermedad para optimizar la reserva neurológica, la cognición y la función física. Esto se consigue mediante el uso de «fármacos modificadores de la enfermedad» tales como interferón, acetato de glatiramer, anticuerpos monoclonales y moduladores del receptor esfingosina-1-fosfato.[21][90]
Los fármacos modificadores de la enfermedad aprobados para el tratamiento de la esclerosis múltiple son:[90]
- IFN 1a
- Cladribina
- Interferón β-1b
- Interferón β-1a
- Peginterferón β-1a
- Acetato de glatiramer
- Dimetilfumarato
- Teriflunomida
- Fingolimod
- Daclizumab beta
- Alemtuzumab
- Natalizumab
- Ocrelizumab
- Mitoxantrona
En general, podemos dividir el tratamiento para esclerosis múltiple en tres apartados:
- terapia modificadora de la enfermedad (TME)
- tratamiento durante las recaídas (tratamiento agudo)
- tratamiento sintomático
TME (terapia modificadora de la enfermedad)[editar]
Las metas de las terapias TME son:
- modificar la historia natural de la enfermedad;
- reducir la actividad inflamatoria en el sistema nervioso central (SNC); y
- prevenir o enlentecer la progresión de la discapacidad.
Según lo anterior, la recomendación actual es «la optimización» del tratamiento, lo cual significa hacer una selección de un fármaco que tenga un perfil de riesgo/beneficio favorable para el paciente de acuerdo a múltiples factores pronósticos que pueden considerarse al iniciar el tratamiento y en el monitoreo subsecuente para lograr definir si la respuesta es adecuada o se requiere un cambio oportuno de fármaco
En 1993, la FDA (Food and Drug Administration: Administración de Alimentos y Medicamentos) autorizó el primer interferón beta para el tratamiento de la esclerosis múltiple; a partir de entonces, múltiples tratamientos se han introducido para su manejo.
Para finales de 2017 se contaban con 11 fármacos aprobados por FDA para el tratamiento de la esclerosis múltiple en su forma recurrente-remitente, lo cual permite una mejor oportunidad de individualizar el manejo según factores pronósticos de cada paciente considerando eficacia, efectos adversos, mecanismos de acción y aspectos de conveniencia[91]
Podemos dividirlos como:
1. Terapias inyectables
Interferones[92]
El Interferón B1b estuvo disponible por primera vez en Australia en 1995. Su mecanismo de acción no es del todo claro, pero se sabe que regula las células y sustancias proinflamatorias, así como su paso al SNC. Se han generado nuevas formulaciones a fin de disminuir la frecuencia de su aplicación y con ello mejorar el apego terapéutico.
Acetato de Glatiramer[93][94]
Su primer estudio pivotal se publicó en 1995; su mecanismo de acción no es completamente claro pero se sabe que genera u cambio en la diferenciación de células pro-inflamatorias a antiinflamatorias y recientemente ha cambiado su presentación de 20mg a 40mg con lo cual su forma de aplicación cambió de ser diaria a ser en días alternos.
2. Terapias orales
La cladribina tabletas fue aprobada por parte de la Agencia Europea de Medicamentos fue agosto de 2017 y a partir de ahí se ha registrado en más de 38 países en todo el mundo.[95] Las tabletas de cladribina son una terapia oral de cursos cortos que se cree que actúa selectivamente sobre los linfocitos. Las tabletas de cladribina se encuentran actualmente bajo investigación clínica y no están aprobadas para el tratamiento de ningún uso en los Estados Unidos. Actualmente ha recibido aprobaciones para pacientes con EMR de alta actividad según lo definido por las características clínicas o de imagen en Argentina, Chile, Emiratos Árabes Unidos, Israel, Líbano y la Unión Europea.
En diciembre de 2017, Canadá y Australia aprobaron tabletas de cladribina para el tratamiento de esclerosis múltiple recurrente-remitente (RRMS).[cita requerida]
El fingolimod, aprobado en más de 60 países, es el primer tratamiento oral modificador de la enfermedad aprobado en primera línea en EE. UU. para la esclerosis múltiple recidivante, la forma más frecuente. En la Unión Europea se aprobó en marzo de 2011 para los pacientes con esclerosis múltiple recidivante-remitente grave de evolución rápida o muy activa.
La esclerosis múltiple progresiva primaria es muy difícil de tratar. Los corticoesteroides a altas dosis cada tres meses pueden tener algún efecto. En principio no existe un tratamiento preventivo efectivo para la esclerosis múltiple progresiva primaria. El tratamiento de los síntomas, y la rehabilitación llevada a cabo principalmente desde terapia ocupacional, fisioterapia y logopedia, tienen un papel importante. Es muy importante, igualmente, la evaluación por parte de un neuropsicólogo para poder abordar cualquier déficit cognitivo que pudiera instaurarse.
Entre las intervenciones dietéticas, en ocasiones se ha empleado la dieta sin gluten, debido a la existencia de casos documentados que confirman la remisión de la esclerosis múltiple simplemente tras la retirada estricta y mantenida de los alimentos que contienen gluten en la dieta.[96][97] Otras intervenciones dietéticas en estudio incluyen la suplementación con vitamina D, ácidos grasos poliinsaturados, antioxidantes (vitaminas A, C y E) y probióticos.[53]
Medicamentos experimentales y terapias alternativas se describen en el artículo Tratamiento de la esclerosis múltiple. El estado de las terapias experimentales, llamadas "pipeline", pueden ser consultadas en sitios especializados.
Es el segundo fármaco oral aprobado (2012) para las formas recurrentes de esclerosis múltiple. Funciona disminuyendo la capacidad de replicación de los linfocitos responsables de la inflamación en el SNC con lo cual se busca una reducción de actividad clínica y radiológica de la enfermedad según los estudios clínicos. Es el único fármaco oral que ha mostrado eficacia en fases tempranas de la enfermedad (Síndrome Clínico Aislado).
Está disponible en nuestro país para formas recurrentes de esclerosis múltiple. La dosis es una toma cada 12h. Su mecanismo de acción no está bien entendido pero sus efectos son antiinflamatorios e inmunomoduladores a través de la regulación de la función del sistema inmunológico al estrés oxidativo, lo cual ha demostrado reducir la cantidad de recaídas y las lesiones vistas en la resonancia magnética.
3. Anticuerpos monoclonales
Primer anticuerpo monoclonal aprobado en 2004 en Estados Unidos y en 2006 por la Unión Europea para el tratamiento de la esclerosis múltiple. Su indicación es como monoterapia en pacientes con formas recurrentes que han presentado respuesta inadecuada a otros fármacos o como primera opción en casos de enfermedad agresiva.
Su mecanismo de acción es evitar el paso de las células del sistema inmunológico (linfocitos) al Sistema Nervioso Central (SNC), limitando así el proceso inflamatorio con lo que disminuye el número de recaídas clínicas, la progresión de discapacidad y el número de lesiones por Resonancia Magnética, siendo considerado uno de los medicamentos con mayor eficacia. Se aplica de manera mensual con pocas reacciones asociadas a la infusión.
Es un anticuerpo monoclonal aprobado para pacientes con esclerosis múltiple recurrente-remitente en la Unión Europea desde 2013 y más recientemente en Estados Unidos. Su indicación es como monoterapia en pacientes con formas recurrentes y activas de esclerosis múltiple.
Su mecanismo de acción consiste en reducir el número de linfocitos en la sangre de manera significativa y después de algunas semanas generar una repoblación de estas células generando un nuevo balance del sistema inmunológico, con lo cual que ha demostrado una reducción significativa en el número de recaídas, la progresión de discapacidad, las lesiones vistas en resonancia magnética incluyendo el nivel de atrofia cerebral, etc. Su forma de administración es a través de una infusión que dura alrededor de 4 horas en dos ciclos de tratamiento, el primero de ellos administrando una dosis diaria por cinco días y el segundo doce meses después aplicando una dosis diaria por tres días.
El efecto clínico de estas aplicaciones se mantiene a largo plazo en los estudios clínicos, aunque de ser necesario, los pacientes pueden recibir más ciclos de tratamiento de acuerdo a su evolución.
4. Trasplante autólogo de células madre[92]
Con la finalidad de reconstituir el sistema inmunológico de los pacientes. Sin embargo, no se cuenta con un protocolo definido y tiene muchas limitantes, por lo que se considera aún como un tratamiento experimental en desarrollo.
Tratamiento agudo[editar]
Es importante que los paciente que cursan con la enfermedad reconozcan cuales son los signos y síntomas de un brote, que traduce actividad clínica de la enfermedad, y así puedan acudir a la brevedad posible a su neurólogo, quien deberá identificar el brote o bien descartar procesos infecciosos o condiciones que simulan un brote "pseudobrotes", instaurando el tratamiento médico en agudo.
En pacientes con esclerosis múltiple tipo RR en brote, con síntomas neurológicos que condicionan discapacidad o involucro en la visión, la fuerza o la función cerebelosa, se recomienda el tratamiento con glucocorticoides. La metilprednisolona vía intravenosa es de elección, sin embargo estudios también sugieren que el régimen oral es igual de efectivo. Los brotes que condicionen síntomas sensitivos moderados no deben ser tratados.[109]
La inyección con corticotropina en gel es una alternativa para pacientes en brote, los cuales no pueden tolerar altas dosis de glucocorticoides vía intravenosa. Se deben descartar procesos infecciosos.[110]
En pacientes que cursan con déficit neurológico agudo, severo, con poca respuesta al tratamiento con altas dosis de glucocorticoides, se sugiere el tratamiento con plasmaferesis.[111]
En los pacientes con esclerosis múltiple tipo remitente recurrente con actividad manifestada por síntomas clínicos o por lesiones que realzan al contraste, se debe ofrecer terapia modificadora de la enfermedad.
Tratamiento sintomático[editar]
Entre los problemas sintomáticos que padecen los pacientes con esclerosis múltiple se encuentran la disfunción cognitiva, la depresión, la fatiga y las alteraciones en la marcha, las cuales se presentan con mayor frecuencia con la progresión de la enfermedad. La espasticidad, el temblor, las crisis epilépticas, la disfunción esfintérica y vesical pueden también complicar la progresión de la enfermedad.[112]
Trastornos urológicos[editar]
Es importante categorizar al paciente en el tipo de disfunción: falla del detrusor por hiperactividad, falla en el vaciamiento por hipoactividad de la vejiga, o una combinación de ambas fallas.
Las metas para el tratamiento del paciente con disfunción vesical neurogenica incluyen: preservar la función renal, minimizar las complicaciones del tracto urinario y lograr continencia.
El tratamiento de la disfunción vesical en pacientes con esclerosis múltiple involucra suprimir la urgencia y asegurar un adecuado drenaje urinario.
La terapia inicial para el ajuste de la disfunción esfintérica incluye restricción de líquidos ≤2 L al día y coordinar los tiempos para realizar la micción.[113]
En pacientes con hiperctivdad del detrusor, los medicamentos anticolinérgicos y antimuscarinicos representan la primera opción. La Oxibutinina es el medicamento de primera elección. Otros medicamentos anticolinérgicos incluyen tolterodina, propantelina, propiverina, fesoterodina y solifenacina.
Una terapia adjunta con cateterización intermitente puede ser de ayuda en el vaciado eficaz vesical y la continencia.
La terapia dual es efectiva y bien tolerada en algunos pacientes, se pueden incluir medicamentos con diferentes mecanismos de acción como anticolinérgicos, agonistas colinérgicos, bloqueadores alfa adrenérgicos, antidepresivos tricíclicos y agentes simpaticomiméticos.
Se debe tener cuidado con los efectos adversos de los anticolinergicos que incluyen confusión, sobre todo en pacientes mayores.
La inyección con toxina botulínica es una opción en pacientes con disfunción vesical debido a hiperactividad del detrusor que son resistentes a tratamiento o intolerantes a terapia con anticolinérgicos/ antimuscarínicos.[114]
La hiperactividad del detrusor que no responde al tratamiento con toxina botulínica puede beneficiarse con la neuromodulación sacra y estimulación eléctrica a nivel de raíces S3, así como de la estimulación nerviosa del nervio periférico del nervio dorsal del pene, clítoris o nervio tibial posterior.[115] Dicho tratamiento inhibe el reflejo de micción.
En pacientes con disinergia del esfínter del detrusor, los alfa antagonistas como prazocina, terazocina, doxacocina y tamosulocina pueden ser beneficiosos.
La desmopresina es una buena opción para tratar la nicturia.[116]
Los pacientes con infecciones recurrentes del tracto urinario deben ser investigados con ultrasonido y cistoscopia para descartar anormalidades que puedan estar subyacentes, de ser así el caso, se recomienda iniciar con dosis bajas de antibióticos de forma preventiva.[117]
Trastornos intestinales[editar]
Los problemas comunes incluyen constipación, falta de evacuación, e incontinencia.
Otras causas de disfunción intestinal son consecuencia de la disminución en la actividad física y motilidad, lo cual puede impactar en la frecuencia del movimiento intestinal, de manera secundaria otras condiciones médicas relacionadas con la esclerosis múltiple y los efectos adversos de los medicamentos relacionados con el tratamiento de la espasticidad, dolor y disfunción vesical.
El estreñimiento se trata mediante una dieta rica en fibra y una ingesta hídrica adecuada. Si esto no es suficiente, se pueden asociar laxantes.[118]
Las terapias de biofeedback han demostrado también su utilidad.[119]
El tratamiento de la incontinencia es sintomático, se basa en asegurar una dieta rica en fibra para producir heces blandas pero formadas que resultan más fáciles de controlar que las heces líquidas, en terapias de biofeedback y, en casos extremos, en el uso de obturadores anales.
Deterioro cognitivo[editar]
Las alteraciones más comunes son la falta de atención, en la función ejecutiva, conceptualización abstracta, memoria a corto plazo, recordar palabras, lenguaje y procesamiento de la información. Es importante evaluar la depresión, las alteraciones en la higiene del sueño, síndromes dolorosos y la fatiga en todos los pacientes con déficit cognitivo, ya que dichos problemas pueden tener impacto en las experiencias de los pacientes. El régimen de medicación deberá ser analizado para medicamentos asociados con efectos sedantes, hipnóticos y efectos psicomotores.
Tratamiento farmacológico[editar]
No hay terapias que prueben eficacia para el tratamiento del déficit cognitivo relacionado con esclerosis múltiple, sin embargo los efectos de algunos agentes modificadores de la enfermedad en esclerosis múltiple e inhibidores de la colinestersada se encuentran en estudio en relación de su beneficio e impacto en la función cognitiva.[120]
Los inhibidores de la colinesterasa fueron investigados inicialmente para el tratamiento de la enfermedad de Alzheimer, donde existe un déficit colinérgico en la corteza.[121] Se sabe también que existe un déficit colinerico asociado con esclerosis múltiple, sin embargo ensayos pequeños sugieren que el donepezilo puede tener un beneficio modesto en el tratamiento.[122]
Tratamiento y estrategias no farmacológicas[editar]
Organizadores de uso personal, como alarmas, pueden ser de utilidad en pacientes con dificultad en la áreas de la memoria y la organización. Recordatorios por escrito, directorios, logos telefónicos son otros instrumentos que cumplen con el mismo propósito.
La neurorrehabilitacion se plantea como un apoyo importante para estos pacientes. Tiene como objetivo intentar mejorar el déficit de atención y memoria, recuperar habilidades deterioradas, así como potenciar el desarrollo de mecanismos de adaptación y habilidades compensadoras. No obstante, la evidencia de su utilidad es escasa.[123]
Depresión[editar]
Entre el 15 y el 50 % de los pacientes con esclerosis múltiple presentan síntomas de depresión mayor. El tratamiento con interferón no parece aumentar las tasas de depresión como inicialmente se sugirió.[124] Se recomienda un abordaje integral, psicoterapéutico y farmacológico en estos pacientes. Los antidepresivos tricíclicos y los inhibidores de la recaptura de la serotonina pueden ser útiles en el tratamiento; la elección debe individualizarse en función de la situación basal de cada paciente y el perfil de efectos secundarios.[125]
Fatiga[editar]
Es un síntoma frecuente en los pacientes con esclerosis múltiple. Se debe intentar identificar y tratar los posibles factores concomitantes que puedan generar o empeorar la fatiga, como los trastornos del sueño, la depresión o el dolor.
Algunos fármacos como el interferón o los empleados en el tratamiento sintomático de la espasticidad pueden ser causa de fatiga.
Ciertas medidas no farmacológicas como planificar la mayor parte de la actividad a primera hora de la mañana, realizar descansos regulares, ejercicio físico o estructurar los horarios pueden resultar útiles. Si la fatiga persiste, se puede valorar el tratamiento farmacológico.
El único tratamiento que ha demostrado tener cierta base para su uso es la amantadina.[126]
Alteraciones en la marcha[editar]
Las alteraciones en la marcha en pacientes con esclerosis múltiple pueden ser el resultado de diversas complicaciones como la espasticidad, debilidad, fatiga, alteraciones sensoriales, pérdida visual y disfunción vestibular. La fampridina, un bloqueador de los canales de potasio, es el primer tratamiento aprobado con la indicación de mejorar la capacidad de la marcha de los pacientes con esclerosis múltiple.[127] Esta contraindicada en pacientes con historia de crisis epilépticas y en pacientes que reciben fármacos inhibidores del transportador de cationes orgánicos 2 (OCT2) renal.
Dolor[editar]
Existen síndromes dolorosos paroxísticos asociados a la esclerosis múltiple como la neuralgia del trigémino y el fenómeno de Lhermitte. Episodios recurrentes del signo de Lhermitte, incluyendo aquellos sin lesión medular, pueden responder a terapia con gabapentina, pregabalina y cabamazepina. La terapia farmacológica utilizada de primera línea incluye carbamazepina, oxcarbazepina y como segunda línea baclofeno, lamotrigina y misoprostol Síntomas paroxísticos. Los ataques paroxísticos pueden responder con dosis bajas de antiepilépticos como carbamazepina, ácido valproico después de varias semanas a meses, usualmente sin recurrencia.[128]
Espasticidad[editar]
Es uno de los factores que más contribuye a la discapacidad en la esclerosis múltiple, limitando la movilidad, generando dolor, condicionando posiciones articulares erróneas y, en fases más avanzadas, dificultando la higiene. En pacientes con debilidad en las extremidades, el desarrollo de espasticidad puede conllevar una mejoría funcional, por lo que su desaparición implicaría un empeoramiento de la discapacidad. En otras ocasiones la espasticidad, o su empeoramiento se debe a la existencia de otros factores (por ejemplo, infecciones), por lo que es importante identificar la causa y tratarla.[129]
La decisión de tratar la espasticidad requiere una evaluación cuidadosa e individualizada. En los casos leves la espasticidad puede aliviarse con fisioterapia y ejercicio.Hay que considerar el tratamiento con fármacos orales cuando el tratamiento rehabilitador fracase o la espasticidad sea moderada. Si la monoterapia no es efectiva, se pueden combinar fármacos con distintos mecanismos de acción. Dentro de las terapias farmacológicas para el tratamiento de la espasticidad se encuentran el baclofeno, el dantroleno, la tizanidina, diazepam, gabapentina y toxina botulínica tipo A.[130] El baclofeno, la gabapentina y la tizanidina orales se utilizan a menudo para el tratamiento de primera línea. Se considera el diazepam o el dantroleno para los pacientes que no responden o no toleran los fármacos previos.[131]
Todos los tratamientos mencionados anteriormente son ineficaces en aproximadamente el 40 % de los casos. En estos casos se pueden utilizar otras intervenciones como el baclofeno intratecal que es eficaz y bien tolerado, no obstante su administración requiere de unidades especializadas, bombas e higiene, y es una opción costosa. Del mismo modo, la quimioinervación y la implantación de neuromoduladores exige una alta experiencia.[131]
Ataxia y temblor[editar]
Hasta un 80 % de los pacientes con esclerosis múltiple referirían temblor o ataxia a lo largo de la evolución de la enfermedad. Las terapias rehabilitadoras pueden resultar útiles en el tratamiento de la ataxia.[132] Dentro de los medicamentos utilizados para el temblor se encuentran la isoniacida. El propranolol no ha demostrado utilidad en pacientes con esclerosis múltiple. Entre los fármacos antiepilépticos, la carbamazepina puede ser útil en el tratamiento del temblor de origen cerebeloso.[133]
Disfunción sexual[editar]
Requiere un manejo multidisciplinario, pues puede existir un componente psicogeno asociado. La disfunción eréctil en varones con esclerosis múltiple es frecuente. La utilidad de los inhibidores de la fosfodiesterasa-5, como el sildenafilo, vardenafilo o tadalafilo, se ha estudiado en pacientes con esclerosis múltiple. Los dispositivos de vacío y las prótesis peneanas constituyen el último escalón del tratamiento.[134]
Entre las mujeres, los principales problemas son: anorgasmia, falta de lubricación vaginal y disminución de la libido. La falta de lubricación vaginal se resuelve con lubricantes. La anorgasmia en ocasiones puede mejorar con dosis bajas de estrógenos en crema de aplicación vaginal. El sildenafilo se ha probado en mujeres con esclerosis múltiple y disfunción sexual sin éxito.[135]
Terapias alternativas y complementarias[editar]
En esclerosis múltiple entre 30 y 80 % de los pacientes utilizan terapias alternativas y complementarias,[136][137] que son terapias no convencionales pueden utilizarse como ayuda o en lugar de tratamientos establecidos de la enfermedad, principalmente como parte del manejo de síntomas específicos relacionados con la enfermedad.[138][139] Es importante reiterar que ninguna de estas terapias ha demostrado tener un efecto en modificar la actividad y progresión de la enfermedad, aunque algunas de ellas han demostrado tener un impacto positivo en la calidad de vida de los pacientes, siendo algunas de ellas relacionadas con rehabilitación física y ejercicio, alimentación, técnicas de meditación-relajación o psicoterapia.[140]
Terapia física[editar]
Las terapias de rehabilitación física tienen un impacto positivo en la recuperación de secuelas y en mejorar la movilidad, disminuir el grado de espasticidad e incrementar la fuerza de extremidades. Específicamente se ha descrito mejoría en velocidad de marcha y estabilidad.[141][142]
Otras terapias alternativas como yoga, pilates o taichí han mostrado en algunos estudios de calidad de vida mejoría similar o mejor a actividad física regular en fuerza muscular, estabilidad postural, disminuyendo niveles de estrés, específicamente en yoga, que es practicado en aproximadamente 30 % de los pacientes con esclerosis múltiple.[143][144] Resultados similares se han visto en quienes realizan pilates y taichí[145][146] al ser ejercicios que involucran estiramiento muscular y ejercitan músculos que mejoran la estabilidad postural, incluso en ciertos estudios comentando mejoría en fatiga.[147][148]
Psicoterapia / Meditación / Reflexología / Biofeedback / Mindfulness[editar]
Así como la discapacidad física está presente en pacientes con esclerosis múltiple, la presencia de síntomas neuropsiquiátricos como trastornos depresivos, alteraciones cognoscitivas y de la conducta son síntomas bastante frecuentes en la enfermedad.[136][137] Si bien la terapia psicológica no interfiere con la actividad inflamatoria o la progresión de la discapacidad, si impacta positivamente en la calidad de vida de los pacientes con esclerosis múltiple.[149][150]
Terapias alternativas como biofeedback, mindfulness o meditación disminuyen niveles de estrés y mejora la capacidad de respuesta al mismo, encontrando en algunos estudios mejoría principalmente en la autopercepción de la discapacidad y calidad de vida.[136][137]
Algunos estudios relacionan terapia con masajes y reflexología con disminución de niveles de estrés y reducción de secuelas sensitivas, como parestesias, en pacientes con esclerosis múltiple.[136][138]
Terapias herbales[editar]
Cannabis[editar]
Tanto la marihuana como sus derivados canabinoides han probado tener una efectividad como relajante muscular y como terapia para la espasticidad, ya sea por eventos traumáticos, vasculares, congénitos o como en este caso, en pacientes con esclerosis múltiple, así como el manejo de ciertos tipos de dolor neuropático crónico.[151] Sin embargo, no hay ningún ensayo clínico que apoye que fumar marihuana sea beneficioso para los pacientes con esclerosis múltiple. En algunos países donde el uso de cannabis ha sido legalizado para su uso médico se puede utilizar un fármaco derivado del cannabis llamado nabiximols, que ha demostrado tener efectos modestos sobre el dolor y la espasticidad en la esclerosis múltiple.[131]
Sin embargo, no ha logrado relacionarse con modificación en la tasa de recaídas o la aparición de lesiones nuevas en T2 en resonancia magnética o lesiones captantes de gadolinio.[137] También es bien conocido el efecto negativo en la cognición a largo plazo, por lo que no puede ser recomendado como terapia complementaria en esclerosis múltiple, salvo que sea para tratar específicamente espasticidad o manejo de dolor crónico, solo si no hay respuesta a tratamientos alternativos.[152]
Ginkgo biloba[editar]
No se ha demostrado su eficacia en mejorar la cognición, concentración o atención en pacientes con esclerosis múltiple, sin embargo hay reportes que afirman su efectividad en el manejo de la fatiga, otro síntoma muy importante y discapacitante en estos pacientes.[136]
Ozonoterapia y oxígeno hiperbárico[editar]
Se ha utilizado la ozonoterapia para en múltiples enfermedades con el objetivo de mejorar la oxigenación tisular y disminuir el efecto nocivo de especies reactivas de oxígeno[153] siendo este último punto uno de los target terapéutico de la esclerosis múltiple, incluso con una TME que actúa a este nivel.[154] Desgraciadamente no hay artículos confiables en los que se haya demostrado eficacia en reducir número de reacaídas, progresión discapacidad o presencia de lesiones nuevas en resonancia magnética (signos que indican actividad de la enfermedad) con este tipo de terapias en pacientes con esclerosis múltiple[136]
Intervenciones en estilos de vida[editar]
Tabaco[editar]
Es ampliamente conocida la relación negativa del consumo de tabaco con la actividad de la enfermedad. Múltiples estudios demuestran la asociación de mayor número de recaídas, aparición de nuevas lesiones y progresión de la discapacidad en pacientes fumadores versus su contraparte no fumadora,[155] asociado principalmente al incremento de radicales libres generados.[156]
Alcohol[editar]
Al momento no hay una relación directa entre el consumo de alcohol y la progresión de la enfermedad, incluso un artículo sugiere disminución de riesgo.[157] Sin embargo esto no es suficiente para poder recomendar su uso. Por otra parte, al haber en el paciente con esclerosis múltiple síntomas y secuelas que alteran la función de equilibrio y cognitiva.
Sobrepeso y obesidad[editar]
Múltiples estudios han demostrado la incidencia que tiene el sobrepeso/obesidad en estados inflamatorios, dado principalmente por el incremento de estados proinflamatorios y reducción de estados antiinflamatorios[158][159] demostrado a nivel celular y por la expresión de citosinas correspondientes. Específicamente en esclerosis múltiple, el sobrepeso/obesidad se ha relacionado con incremento de la actividad inflamatoria de la enfermedad, tanto en población mundial, como específicamente en población mexicana.[160] Si bien como medida aislada, no puede considerarse el control de peso como tratamiento de la enfermedad, si se ha demostrado que estilos de vida saludables, que lleven a mantener un peso adecuado, puede estar relacionado con disminución de la actividad inflamatoria, con mejoría en el estado funcional de pacientes con esclerosis múltiple.
Alimentación[editar]
La única intervención nutricional que ha demostrado resultados en algunos estudios, que ha mostrado cambios en el estado inflamatorio de los pacientes con esclerosis múltiple, así como la cantidad de recaídas es la complementación con ácidos grasos omega 3 derivados de pescado.[137] Otros ácidos grasos, así como suplementación con vitaminas B, C, E, limitación calórica o dietas específicas no han mostrado diferencias significativas con respecto a placebo en enfermedad remitente-recurrente o en modalidades progresivas.[139]
Si bien es conocida la relación de la deficiencia de vitamina D como probable factor ambiental para el desarrollo de esclerosis múltiple, la suplementación con esta vitamina no ha mostrado resultados significativos en la disminución de la actividad de la enfermedad per se.[136] Sin embargo, la disminución de niveles de vitamina D se relaciona con osteopenia y aumento de fracturas en pacientes con y sin esclerosis múltiple,[161][162] lo que empeora la funcionalidad, por lo que es recomendable complementación con vitamina D en todos los pacientes en los que se diagnostique esclerosis múltiple.[136][137] Por otro lado, en el 2021 se realizó un trabajo cuyos resultados se encuentran en línea con estudios previos vinculados al Glutamato con la patogénesis de la esclerosis múltiple.[163]
Estrés[editar]
Hay un número considerable de estudios que sugieren una relación directa entre el nivel de estrés emocional con el incremento de recaídas clínicas y presencia de lesiones captantes de gadolinio por resonancia magnética.[164][165] Al ser este el sustrato principal en la fisiopatogenia de la esclerosis múltiple, es esperada esta respuesta en pacientes sometidos a estrés crónico o aumento transitorio de situaciones de estrés laboral, personal o social.
Calidad de sueño[editar]
Se ha propuesto en varios estudios la disminución en la función cognitiva y calidad de vida en pacentes con esclerosis múltiple.[166][167] Si bien es ampliamente conocido que una buena calidad de sueño mejora la calidad de vida percibida en la población general y disminuye riesgo de enfermedades cardiovasculares y estado anímico, no se han realizado estudios que relacionen este rubro con la actividad inflamatoria o estado de discapacidad en esclerosis múltiple.
Actividad física[editar]
Los pacientes con esclerosis múltiple no están exentos de desarrollar otro tipo de patologías relacionadas con estilos de vida. Mantener una vida sedentaria, tanto en personas con esclerosis múltiple como en población sana, es un importante factor de riesgo para el desarrollo de enfermedades cardiovasculares y sus complicaciones,[142] por lo que debe fomentarse la importancia de mantener estilos de vida saludables que incluyan actividad física regular. Cuando además hay secuelas motoras o de coordinación, realizar ejercicio de manera habitual, así como la terapia específica de rehabilitación física, puede ayudar a mantener un adecuado tono muscular, peso saludable y articulaciones suficientemente laxas para mejorar la movilidad de los pacientes, así como disminuir globalmente niveles de estrés.[144]
Pronóstico[editar]
Actualmente no hay pruebas clínicas establecidas que permitan un pronóstico o decidir una respuesta terapéutica, aunque existen investigaciones prometedoras que necesitan ser confirmadas, como la detección de los anticuerpos anti-MOG (anticuerpo sérico contra la MOG [myelin oligodendrocyte glycoprotein: ‘glicoproteína de la mielina de los oligodendrocitos’]) y anti-MBP (anticuerpo contra la MBP [myelin basic protein: ‘proteína básica de la mielina’]), como factores predictores de evolución a la enfermedad instaurada. La incertidumbre es uno de los aspectos psicológicos que resulta más difíciles de llevar en la esclerosis múltiple.
Debido a la mejora en el tratamiento de complicaciones como infecciones pulmonares o en la vejiga urinaria, la esperanza de vida de las personas diagnosticadas con esclerosis múltiple solo se ve ligeramente reducida.
Cuanto más joven se es cuando aparece la enfermedad, más lentamente avanza la discapacidad. Esto se debe a que en personas mayores es más frecuente la forma crónica progresiva, con una acumulación mayor de discapacidad.
La discapacidad tras cinco años se corresponde con la discapacidad a los 15 años: 2/3 de los pacientes con esclerosis múltiple que tengan poca discapacidad a los 5 años, no se deteriorarán mucho en los 10 años siguientes. Otros casos de esclerosis múltiple en la familia no influyen en la progresión de la enfermedad. Uno de cada tres pacientes seguirá siendo capaz de trabajar después de 15 a 20 años.
Pérdida de visión o síntomas sensoriales (entumecimiento u hormigueo) como síntomas iniciales son signos de un pronóstico benigno. Perturbaciones en el andar y cansancio son signos de un pronóstico negativo.
Una rápida regresión de los síntomas iniciales, edad a la que aparece la enfermedad por debajo de los 35, solo un síntoma inicialmente, desarrollo rápido de los síntomas iniciales y corta duración de la última recaída indican un buen pronóstico.
Si la forma es con recaídas y remisiones, estadísticamente serán necesarios 20 años hasta que la silla de ruedas sea necesaria. Esto quiere decir que muchos pacientes nunca la necesitarán. Si la forma es progresiva primaria, como media, se necesitará una silla de ruedas tras 6 o 7 años. Hay que tener en cuenta que estos datos a largo plazo fueron tomados antes de la llegada de los medicamentos inmunomoduladores modernos, a principios de los años 2000. Estos medicamentos consiguen retrasar el progreso de la enfermedad varios años.
Información general[editar]
Necesidades no cubiertas[editar]
Las personas que padecen esclerosis múltiple enfrentan diversas situaciones que afectan su calidad de vida. El vivir con esclerosis múltiple puede causar deterioro en diversos ámbitos de la vida que pueden influir en la vida familiar, laboral y actividades de la vida diaria. La forma en que evoluciona la enfermedad puede causar incertidumbre y limitar el desarrollo de planes a futuro lo cual genera importante estrés psicológico. Las necesidades de los pacientes son muy variadas y dependerá de entre otros factores de la edad, sexo, gravedad de la enfermedad, tipo de empleo, redes de apoyo con los que cuenten los pacientes.
Algunas de las principales necesidades identificadas tanto en pacientes como en familiares y cuidadores son: mayor conocimiento y entendimiento de la enfermedad, apoyo psicológico a pacientes, familiares y cuidadores sobre todo en pacientes cuya enfermedad ha causado algún grado de discapacidad, acceso a tratamientos multidisciplinarios, un diagnóstico y tratamientos oportunos que modifiquen el curso de la enfermedad y eviten discapacidad. Otros puntos que se han identificado son la necesidad de una mejor comunicación con todos los involucrados en el cuidado de los pacientes con esclerosis múltiple (médicos, enfermeras, rehabilitadores, psicólogos, cuidadores). Acceso a grupos de apoyo a nivel local.[168] Es muy importante para los pacientes el poder sentir que tienen control de su vida, sentirse productivos y tener soporte emocional.[169]
Día Mundial de la Esclerosis Múltiple[editar]
Desde 2009 la MSIF (Multiple Sclerosis International Federation: Federación Internacional de Esclerosis Múltiple), inició con la campaña de celebrar cada año el Día Mundial de la Esclerosis Múltiple. Con esta campaña se ha llegado a miles de personas y cada año se centra en un tema diferente.[170] Se considera que es un día para celebrar la solidaridad mundial y la esperanza para el futuro. El Día Mundial de la Esclerosis Múltiple está establecido el último miércoles del mes de mayo pero los eventos y campañas se celebran durante todo el mes de mayo. Reúne a la comunidad global de esclerosis múltiple para compartir historias, sensibilizar y hacer campaña con y para todos los afectados por la esclerosis múltiple.[171]
Comités para el tratamiento e investigación en esclerosis múltiple[editar]
Los comités para el tratamiento e investigación en esclerosis múltiple a nivel mundial son asociaciones sin fines de lucro las cuales tienen como principal objetivo entender y tratar a la esclerosis múltiple. Estos comités contribuyen a nivel global trabajando con investigadores y clínicos en el desarrollo de investigación tanto básica como clínica, apoyan educación y enseñanza en la materia, estimulan a investigadores jóvenes a involucrarse en la esclerosis múltiple, organizan congresos anuales, crean alianzas y colaboraciones a nivel internacional todo con el fin de tener un mejor entendimiento de la enfermedad.
Existen diversos comités a nivel mundial divididos por continentes y dentro de estos hay países que han formado sus propios comités. Uno de los más grandes y que fue creado hace más de 30 años es ECTRIMS (European Committe for treatment and research in Multiple Sclerosis) organiza anualmente el congreso anual que convoca al mayor número de personas interesadas en una sola enfermedad.[172] Otros comités a nivel continental son ACTRIMS (American Committe for treatment and research in Multiple Sclerosis),[173] LACTRIMS (Latin American Committe for treatment and research in Multiple Sclerosis)[174] PACTRIMS (Pan Asian Committe for treatment and research in Multiple Sclerosis)[175] MENACTRIMS (Middle East North Africa Committe for treatment and research in multiple sclerosis),[176] los cuales tiene como objeto el desarrollo de investigación y conocimiento de la enfermedad en las diferentes regiones. Existen también algunos países que han creado sus propios comités como MEXCTRIMS (Mexican Committe for treatment and research in Multiple Sclerosis),[177] BCTRIMS (Brazilian Committe for Treatment and research in Multiple Sclerosis).[178] Estas asociaciones también se encargan de difundir y concientizar acerca del conocimiento de la enfermedad.
Existen también otras iniciativas a nivel global como MS Brain Health las cuales buscan alertar de la importancia de un diagnóstico y tratamiento oportunos, generando información para población general y para todas las personas involucradas en el cuidado de los pacientes con esclerosis múltiple.[179]
En modelos murinos se ha logrado reducir la infiltración por linfocitos T CD4 de la vaina de mielina y las lesiones desmielinizantes características de la esclerosis múltiple utilizando naltrexona en dosis bajas (LDN).[180] Dicho tratamiento restablece los niveles circulantes de 5-metaencefalina que se encontraban reducidos en sujetos con esclerosis múltiple[181] y tras 8 semanas de uso, se reducen citocinas proinflamatorias fuertemente implicadas en su fisiopatología.[182] Tres ensayos clínicos han encontrado que este tratamiento es seguro, no causa eventos adversos serios y su uso es bien tolerado[183] además de mejorar la calidad de vida[184] y reducir la espasticidad en sujetos con esclerosis múltiple.[185] Todo ello ha justificado la realización de ensayos clínicos en diferentes patologías tales como: CHRON, fibromialgia, cáncer, etc.[186]
Véase también[editar]
- Epidemiología de la esclerosis múltiple en España
- Habla escandida
- Trastornos neurológicos relacionados con el gluten
- Ataxia
- Carles Vilariño-Güell
- Fumarato de diroximel
Referencias[editar]
- ↑ «Multiple Sclerosis Information Page: National Institute of Neurological Disorders and Stroke (NINDS)». web.archive.org. 13 de febrero de 2016. Archivado desde el original el 13 de febrero de 2016. Consultado el 25 de abril de 2021.
- ↑ Milo, Ron; Kahana, Esther (2010-03-XX). «Multiple sclerosis: Geoepidemiology, genetics and the environment». Autoimmunity Reviews (en inglés) 9 (5): A387-A394. doi:10.1016/j.autrev.2009.11.010. Consultado el 25 de abril de 2021.
- ↑ a b c d e Tafti, Dawood; Ehsan, Moavia; Xixis, Kathryn L. (2021). Multiple Sclerosis. StatPearls Publishing. PMID 29763024. Consultado el 25 de abril de 2021.
- ↑ Compston, Alastair; Coles, Alasdair (2008-10-XX). «Multiple sclerosis». The Lancet (en inglés) 372 (9648): 1502-1517. doi:10.1016/S0140-6736(08)61620-7. Consultado el 25 de abril de 2021.
- ↑ Wang, Haidong; Naghavi, Mohsen; Allen, Christine; Barber, Ryan M; Bhutta, Zulfiqar A; Carter, Austin; Casey, Daniel C; Charlson, Fiona J et al. (2016-10-XX). «Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015». The Lancet (en inglés) 388 (10053): 1459-1544. PMC 5388903. PMID 27733281. doi:10.1016/S0140-6736(16)31012-1. Consultado el 25 de abril de 2021.
- ↑ a b Compston, Alastair. (2005). McAlpine's multiple sclerosis (4th ed edición). Churchill Livingstone Elsevier. ISBN 978-0-443-07271-0. OCLC 460934298. Consultado el 28 de enero de 2021.
- ↑ a b Piryonesi, S. Madeh; Rostampour, Sorour; Piryonesi, S. Abdurrahman (2021-04). «Predicting falls and injuries in people with multiple sclerosis using machine learning algorithms». Multiple Sclerosis and Related Disorders (en inglés) 49: 102740. doi:10.1016/j.msard.2021.102740. Consultado el 28 de enero de 2021.
- ↑ a b Hegen, H.; Bsteh, G.; Berger, T. (septiembre de 2018). «‘No evidence of disease activity’ – is it an appropriate surrogate in multiple sclerosis?» ['No hay evidencia de enfermedad activa' - ¿es un sucedáneo apropiado en la esclerosis múltiple?]. Eur J Neurol (en inglés) 25 (9): 1107-e101. PMID 29687559. doi:10.1111/ene.13669. Consultado el 4 de octubre de 2018.
- ↑ a b c d e f g h Koriem, Khaled Mohamed Mohamed (mayo de 2017). «Corrigendum to ‘Multiple sclerosis: New insights and trends’» [Corrección de «Esclerosis múltiple: consideraciones y tendencias nuevas»]. En Hainan Medical University, ed. Asian Pacific Journal of Tropical Biomedicine (en inglés) (El Cairo, Egipto: Elsevier B.V.) 7 (5): 493-504. doi:10.1016/j.apjtb.2017.02.001. Consultado el 13 de enero de 2018.
- ↑ a b c d e f Didonna, Alessandro; Oksenberg, Jorge R. (noviembre de 2017). «Chapter 1. The Genetics of Multiple Sclerosis» [Capítulo 1. La genética de la esclerosis múltiple]. En Zagon, I. S.; McLaughlin, P. J., eds. Multiple Sclerosis: Perspectives in Treatment and Pathogenesis [Internet] [Esclerosis múltiple: perspectivas en el tratamiento y la patogenia [Internet]] (en inglés). Brisbane, Australia: Codon Publications. PMID 29261259. doi:10.15586/codon.multiplesclerosis.2017.ch1. Consultado el 13 de enero de 2018.
- ↑ a b Zahoor, Insha; Haq, Ehtishamul (noviembre de 2017). «Chapter 5. Vitamin D and Multiple Sclerosis: An Update» [Capítulo 5. Vitamina D y esclerosis múltiple: una actualización]. En Zagon, I. S.; McLaughlin, P. J., eds. Multiple Sclerosis: Perspectives in Treatment and Pathogenesis [Internet] [Esclerosis múltiple: perspectivas en el tratamiento y la patogenia [Internet]] (en inglés). Brisbane, Australia: Codon Publications. PMID 29261266. doi:10.15586/codon.multiplesclerosis.2017.ch5. Consultado el 13 de enero de 2018.
- ↑ García Merino, A.; Ara Callizo, J.R.; Fernández Fernández, O.; Landete Pascual, L.; Moral Torres, E.; Rodríguez-Antigüedad Zarrantz, A. (marzo de 2017). «Consenso para el tratamiento de la esclerosis múltiple 2016». En Sociedad Española de Neurología, ed. Neurología (English Edition) (Elsevier España, S.L.U.) 32 (2): 113-119. doi:10.1016/j.nrl.2016.02.026. Consultado el 13 de enero de 2018.
- ↑ a b c d e Domínguez Morenoa, Rogelio; Morales Esponda, Mario; Rossiere Echazarreta, Natalia Lorena; Olan Triano, Román; Gutiérrez Morales, José Luis (septiembre a octubre de 2012). «Esclerosis múltiple: revisión de la literatura médica». Rev. Fac. Med. (Méx.) vol.55 no.5 Ciudad de México sep./oct. 2012 (Ciudad de México: Scielo) 55 (5): 26-35. ISSN 2448-4865. Consultado el 13 de enero de 2018.
- ↑ a b Choi, Bo Young; Jung, Jong Won; Suh, Sang Won (octubre de 2017). «The Emerging Role of Zinc in the Pathogenesis of Multiple Sclerosis» [El rol emergente del zinc en la patogenia de la esclerosis múltiple]. Int J Mol Sci (en inglés) (Multidisciplinary Digital Publishing Institute (MDPI)) 18 (10): 2070. PMID 28956834. doi:10.3390/ijms18102070. Consultado el 13 de enero de 2018.
- ↑ a b c d Mu Q, Kirby J, Reilly CM, Luo XM (23 de mayo de 2017). «Leaky Gut As a Danger Signal for Autoimmune Diseases». Front Immunol (Revisión) 8: 598. PMC 5440529. PMID 28588585. doi:10.3389/fimmu.2017.00598.
- ↑ a b c d e f Fasano, A (2011 Jan). «Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer». Physiol Rev 91 (1): 151-75. PMID 21248165. doi:10.1152/physrev.00003.2008. Archivado desde el original el 26 de agosto de 2015.
- ↑ a b c Leonard MM, Sapone A, Catassi C, Fasano A (2017). «Celiac Disease and Nonceliac Gluten Sensitivity: A Review». JAMA (Revisión) 318 (7): 647-656. PMID 28810029. doi:10.1001/jama.2017.9730. «Previous studies have shown that gliadin can cause an immediate and transient increase in gut permeability. This permeating effect is secondary to the binding of specific undigestible gliadin fragments to the CXCR3 chemokine receptor with subsequent release of zonulin, a modulator of intercellular tight junctions. This process takes place in all individuals who ingest gluten. For the majority, these events do not lead to abnormal consequences. However, these same events can lead to an inflammatory process in genetically predisposed individuals when the immunologic surveillance system mistakenly recognizes gluten as a pathogen.»
- ↑ a b c Hollenbach, Jill A.; Oksenberg, Jorge R. (noviembre de 2015). «The Immunogenetics of Multiple Sclerosis: A Comprehensive Review» [La inmunogenética de la esclerosis múltiple: una revisión comprehensiva]. J Autoimmun (en inglés) 64: 13-25. PMID 26142251. doi:10.1016/j.jaut.2015.06.010. Consultado el 10 de octubre de 2018.
- ↑ Compston, Alastair; Coles, Alasdair (25 de octubre de 2008). «Multiple sclerosis» [Esclerosis múltiple]. The Lancet (en inglés) 372 (9648). ISSN 0140-6736. doi:10.1016/S0140-6736(08)61620-7. Consultado el 3 de octubre de 2018.
- ↑ «esclerosis múltiple: la enfermedad de las mil caras.».
- ↑ a b Dargahi, Narges; Katsara, Maria; Tselios, Theodore; Androutsou, Maria-Eleni; de Courten, Maximilian; Matsoukas, John; Apostolopoulos, Vasso (julio de 2017). «Multiple Sclerosis: Immunopathology and Treatment Update» [Esclerosis múltiple: Actualización de la inmunopatología y el tratamiento]. Brain Sci (en inglés) (Multidisciplinary Digital Publishing Institute (MDPI)) 7 (7): 78. PMID 28686222. doi:10.3390/brainsci7070078. Consultado el 13 de enero de 2018.
- ↑ «Multiple Sclerosis». Brooks Rehabilitation (en inglés estadounidense). Consultado el 20 de septiembre de 2022.
- ↑ Goldenberg, Marvin M. (marzo de 2012). «Multiple Sclerosis Review» [Revisión de esclerosis múltiple]. P T. 2012 (en inglés) (Estados Unidos: MediMedia, USA) 37 (3): 175-184. PMID 22605909. Consultado el 14 de enero de 2018.
- ↑ National Multiple Sclerosis Society (ed.). «Types of MS» [Tipos de esclerosis múltiple] (en inglés). Consultado el 7 de octubre de 2018.
- ↑ a b c d e Martínez Sánchez, Adriana; Medina Rodríguez, María de las Mercedes (2018). «Biomarcadores en esclerosis múltiple». Trabajo de fin de grado (Vallalodid (España): Universidad de Vallalodid). Consultado el 7 de octubre de 2018.
- ↑ Cuevas-García, Carlos (enero a marzo de 2017). «Esclerosis múltiple: aspectos inmunológicos actuales». Rev. alerg. Méx (en inglés) (Ciudad de México) 64 (1): 76-86. ISSN 2448-9190. doi:10.29262/ram.v64i1.253. Consultado el 7 de octubre de 2018.
- ↑ a b c d Rebollo Quintero, Juan José (2017). «Esclerosis múltiple, una enfermedad desmielinizante». Trabajo de fin de grado (Sevilla (España): Universidad de Sevilla). Facultad de Farmacia. Consultado el 7 de octubre de 2018.
- ↑ a b c «Guía clínica 2010 esclerosis múltiple». Guía clínica (Santiago de Chile: Ministerio de Salud). 2010. Consultado el 7 de octubre de 2018.
- ↑ National Multiple Sclerosis Society (ed.). «Clinically Isolated Syndrome (CIS)» [Síndrome clínico aislado] (en inglés). Consultado el 7 de octubre de 2018.
- ↑ Mantero, Vittorio; Abate, Lucia; Balgera, Roberto; La Mantia, Loredana; Salmaggi, Andrea (julio de 2018). «Clinical Application of 2017 McDonald Diagnostic Criteria for Multiple Sclerosis» [Aplicación clínica de los criterios diagnósticos de McDonald 2017 para la esclerosis múltiple]. J Clin Neurol (en inglés) 14 (3): 387-392. PMID 29971979. doi:10.3988/jcn.2018.14.3.387. Consultado el 7 de octubre de 2018.
- ↑ Thompson, Alan J.; Banwell, Brenda L.; Barkhof, Frederik; Carroll, William M.; Coetzee, Timothy; Comi, Giancarlo; et al (febrero de 2018). «Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria» [Diagnóstico de esclerosis múltiple: revisiones de 2017 de los criterios de McDonald]. Lancet (en inglés) (Elsevier Limited) (2): 162-173. doi:10.1016/S1474-4422(17)30470-2. Consultado el 7 de octubre de 2018. (requiere suscripción).
- ↑ National Multiple Sclerosis Society (ed.). «Relapsing-remitting MS (RRMS)» [Esclerosis múltiple recurrente-remitente (EMRR)] (en inglés). Consultado el 7 de octubre de 2018.
- ↑ a b Gómez González, Carolina (junio de 2018). «Terapia con alemtuzumab en la esclerosis múltiple». Trabajo de fin de grado (Cantabria: Universidad de Cantabria). Consultado el 7 de octubre de 2018.
- ↑ a b c d Spain, Rebecca (2018). U.S. Department of Veterans Affairs, ed. «Multiple Sclerosis Centers of Excellence» (en inglés). Consultado el 7 de octubre de 2018.
- ↑ a b c d Tanasescu, Radu; Ionete, Carolina; Chou, I-Jun; Constantinescu, Cris S. (marzo a abril de 2014). «Advances in the Treatment of Relapsing – Remitting Multiple Sclerosis» [Avances en el tratamiento de la esclerosis múltiple remitente-recurrente]. Biomed J (en inglés) 37 (2): 41-49. doi:10.4103/2319-4170.130440. Consultado el 7 de octubre de 2018.
- ↑ National Multiple Sclerosis Society (ed.). «Secondary progressive MS (SPMS)» [esclerosis múltiple secundaria progresiva (EMSP)] (en inglés). Consultado el 7 de octubre de 2018.
- ↑ National Multiple Sclerosis Society (ed.). «Primary progressive MS (PPMS)» [esclerosis múltiple primaria progresiva (EMPP)] (en inglés). Consultado el 7 de octubre de 2018.
- ↑ Covo Torres, Pedro (enero a marzo de 2015). «Introducción a la historia de la esclerosis múltiple». Acta Neurol Colomb. vol.31 no.1 Bogotá Jan./Mar. 2015 (Colombia) 31 (1): 119-124. doi:10.22379/2422402217. Consultado el 5 de octubre de 2018.
- ↑ Holmøy, Trygve (febrero de 2006). «A Norse Contribution to the History of Neurological Diseases» [Una contribución nórdica a la historia de las enfermedades neurológicas]. Eur Neurol (en inglés) (Basilea (Suiza): S. Karger) 55: 57-58. doi:10.1159/000091431. Consultado el 5 de octubre de 2018.
- ↑ Lassmann, H (octubre de 1999). «The pathology of multiple sclerosis and its evolution» [La patología de la esclerosis multiple y su evolución]. Phil. Trans. R. Soc. Lond (en inglés) 354 (1390): 1635-1640. ISSN 0962-8436. PMID 10603616. doi:10.1098/rstb.1999.0508. Consultado el 5 de octubre de 2018.
- ↑ Compston, Alastair (octubre de 1988). «The 150th anniversary of the first depiction of the lesions of multiple sclerosis» [Aniversario 150º de la primera descripción de las lesiones de la esclerosis múltiple]. Journal of Neurology, Neurosurgery, and Psychiatry (en inglés) 51 (10): 1249-1252. ISSN 0022-3050. PMID 3066846. doi:10.1136/jnnp.51.10.1249. Consultado el 5 de octubre de 2018.
- ↑ a b c Rito, Yamel; Torre-Villalvazo, Ivan; Flores, José; Rivas, Verónica; Corona, Teresa (febrero de 2016). «Epigenetics in Multiple Sclerosis: Molecular Mechanisms and Dietary Intervention» [Epigenética en la esclerosis mñultiple: mecanismos moleculares e intervención dietaria]. Central Nervous System Agents in Medicinal Chemistry (en inglés) (Bentham Science Publishers) 18 (1): 8-15. PMID 26915659. doi:10.2174/1871524916666160226131842. Consultado el 7 de octubre de 2018.
- ↑ Ponsonby, Anne-Louise; van der Mei, Ingrid; Dwyer, Terence; Blizzard, Leigh; Taylor, Bruce; Kemp, Andrew; et al (enero de 2005). «Exposure to Infant Siblings During Early Life and Risk of Multiple Sclerosis» [Exposición a hermanos pequeños durante la vida temprana y riesgo de esclerosis múltiple]. JAMA (en inglés) (American Medical Association) 293 (4): 463-469. doi:10.1001/jama.293.4.463. Consultado el 7 de octubre de 2018.
- ↑ a b c d e f g h i j Eskandarieh, S.; Heydarpour, P.; Minagar, A.; Pourmand, S.; Sahraian, M.A. (abril de 2016). «Multiple Sclerosis Epidemiology in East Asia, South East Asia and South Asia: A Systematic Review» [Epidemiología de la esclerosis múltiple en Asia del Este, el Sudeste asiático y Asia del Sur: una revisión sistemática]. Neuroepidemiology (en inglés) (Basilea: S. Karger AG) 46 (3): 209-221. doi:10.1159/000444019. Consultado el 7 de octubre de 2018.
- ↑ Katz Sand, Ilana (agosto de 2018). «The Role of Diet in Multiple Sclerosis: Mechanistic Connections and Current Evidence» [El rol de la dieta en la esclerosis múltiple: conexiones mecanísticas y evidencia actual]. Curr Nutr Rep (en inglés) (Springer) 7 (3): 150-160. PMID 30117071. doi:10.1007/s13668-018-0236-z. Consultado el 7 de octubre de 2018.
- ↑ Flores-Alvarado, Luis Javier; Gabriel-Ortiz, Genaro; Pacheco-Moisés, Fermín P.; Bitzer-Quintero, Oscar K. (junio de 2015). «Mecanismos patogénicos en el desarrollo de la esclerosis múltiple: ambiente, genes, sistema inmune y estrés oxidativo.». Invest Clin 56 (2): 1-14. Consultado el 7 de octubre de 2018.
- ↑ a b c d Fasano, A (2012 Oct). «Intestinal permeability and its regulation by zonulin: diagnostic and therapeutic implications». Clin Gastroenterol Hepatol 10 (10): 1096-100. PMC 3458511. PMID 22902773. doi:10.1016/j.cgh.2012.08.012.
- ↑ Patsopoulos, Nikolaos A. (julio de 2018). «Genetics of Multiple Sclerosis: An Overview and New Directions» [Genética de la esclerosis múltiple: una perspectiva general y nuevos lineamientos]. Cold Spring Harb Perspect Med (en inglés) (Cold Spring Harbor Laboratory Press) 8 (7): a028951. ISSN 2157-1422. PMID 29440325. doi:10.1101/cshperspect.a028951. Consultado el 9 de octubre de 2018.
- ↑ Baranzini, Sergio E. (enero de 2011). «Revealing the genetic basis of multiple sclerosis: Are we there yet?» [Revelando las bases genéticas de la esclerosis múltiple: ¿Ya llegamos?]. Curr Opin Genet Dev (en inglés) 21 (3): 317-324. ISSN 0959-437X. PMID 21247752. doi:10.1016/j.gde.2010.12.006. Consultado el 10 de octubre de 2018.
- ↑ Bjornevik, K..; Cortese, M.; Healy, B. C.; Kuhle, J.; Mina, M. J.; Leng, Y.; Elledge, S. J.; Niebuhr, D. W.; Scher, A. I.; Munger, K. L.; Ascherio, A. (21 de enero de 2022). «Longitudinal analysis reveals high prevalence of Epstein-Barr virus associated with multiple sclerosis.». Science (en inglés). PMID 35025605. doi:10.1126/science.abj8222.
- ↑ Flores-Alvarado LJ, Gabriel-Ortiz G, Pacheco-Mois FP, Bitzer-Quintero K (2015 Jun). «[Pathogenic mechanisms of neuronal damage in multiple sclerosis]». Invest Clin 56 (6): 201-14. PMID 26299060.
- ↑ a b Hollon, J; Puppa, EL; Greenwald, B; Goldberg, E; Guerrerio, A; Fasano, A (2015 Feb 27). «Effect of gliadin on permeability of intestinal biopsy explants from celiac disease patients and patients with non-celiac gluten sensitivity». Nutrients 7 (3): 1565-76. PMID 25734566. doi:10.3390/nu7031565.
- ↑ a b Von Geldern, G.; y Mowry, E. M. (2012 Dec). «The influence of nutritional factors on the prognosis of multiple sclerosis». Nat Rev Neurol 8 (12): 678-89. PMID 23026980. doi:10.1038/nrneurol.2012.194.
- ↑ Taylor, B.V.; Lucas, R.M.; Dear, K.; Kilpatrick, T.J.; Pender, M.P.; van der Mei, I.A.; Chapman, C.; Coulthard, A.; Dwyer, T.; McMichael, A.J.; Valery, P.C.; Williams, D.; Ponsonby, A.L., Latitudinal variation in incidence and type of first central nervous system demyelinating events. Multiple sclerosis (Houndmills, Basingstoke, England), 2010, 16, (4), 398-405
- ↑ Munger, K.L.; Levin, L.I.; Hollis, B.W.; Howard, N.S.; Ascherio, A., Serum 25-hydroxyvitamin D levels and risk of multiple sclerosis. Jama, 2006, 296, (23), 2832-2838.
- ↑ Healy, B.C.; Ali, E.N.; Guttmann, C.R.; Chitnis, T.; Glanz, B.I.; Buckle, G.; Houtchens, M.; Stazzone, L.; Moodie, J.; Berger, A.M.; Duan, Y.; Bakshi, R.; Khoury, S.; Weiner, H.; Ascherio, A., Smoking and disease progression in multiple sclerosis. Archives of neurology, 2009, 66, (7), 858-864.
- ↑ Martinez-Zamudio, R.; Ha, H.C., Environmental epigenetics in metal exposure. Epigenetics: official journal of the DNA Methylation Society, 2011, 6, (7), 820-827.
- ↑ Barragan-Martinez, C.; Speck-Hernandez, C.A.; Montoya-Ortiz, G.; Mantilla, R.D.; Anaya, J.M.; Rojas-Villarraga, A., Organic solvents as risk factor for autoimmune diseases: a systematic review and meta-analysis. PloS one, 2012, 7, (12), e51506.
- ↑ Kugler N, Patel PJ, Lee CJ (2015 Mar). «Chronic Cerebrospinal Venous Insufficiency in Multiple Sclerosis: A Failed Concept». Vasc Specialist Int 31 (1): 11-4. PMC 4480289. PMID 26217638. doi:10.5758/vsi.2015.31.1.11.
- ↑ Reich, Daniel S.; Lucchinetti, Claudia F.; Calabresi, Peter A. (11 de enero de 2018). «Multiple Sclerosis». New England Journal of Medicine (en inglés) 378 (2): 169-180. ISSN 0028-4793. doi:10.1056/nejmra1401483. Consultado el 4 de agosto de 2018.
- ↑ «MEXCTRIMS: ¿Qué es el sistema inmune y por qué es importante en esclerosis múltiple?».
- ↑ «Microglia: scapegoat, saboteur, or something else?». Microglia: scapegoat, saboteur, or something else?. doi:10.1126/science.1227901.
- ↑ «Glia Disease and Repair-Remyelination.». Glia Disease and Repair-Remyelination. doi:10.1101/cshperspect.a020594.
- ↑ The Lesion Project Archivado el 12 de octubre de 2007 en Wayback Machine., artículo en el sitio web de la National Multiple Sclerosis Society.
- ↑ a b Miguel Guerrero Fernández. «Revista nº 12 - Actualidad». Archivado desde el original el 2 de octubre de 2007. Consultado el 31 de mayo de 2017.
- ↑ «Heterogeneity of multiple sclerosis lesions: implications for the pathogenesis of demyelination.». Heterogeneity of multiple sclerosis lesions: implications for the pathogenesis of demyelination. Consultado el 4 de agosto de 2018.
- ↑ «Direct MRI detection of impending plaque development in multiple sclerosis.». Direct MRI detection of impending plaque development in multiple sclerosis. doi:10.1212/NXI.0000000000000145.
- ↑ «Neocortical neuronal, synaptic, and glial loss in multiple sclerosis.». Neocortical neuronal, synaptic, and glial loss in multiple sclerosis. doi:10.1212/01.wnl.0000237551.26858.39.
- ↑ «Transected neurites, apoptotic neurons, and reduced inflammation in cortical multiple sclerosis lesions.».
- ↑ «Widespread demyelination in the cerebellar cortex in multiple sclerosis.». Widespread demyelination in the cerebellar cortex in multiple sclerosis. doi:10.1111/j.1750-3639.2006.00041.x.
- ↑ «A reversible form of axon damage in experimental autoimmune encephalomyelitis and multiple sclerosis.». A reversible form of axon damage in experimental autoimmune encephalomyelitis and multiple sclerosis. doi:10.1038/nm.2324.
- ↑ «Remyelination is extensive in a subset of multiple sclerosis patients.». Remyelination is extensive in a subset of multiple sclerosis patients. doi:10.1093/brain/awl217.
- ↑ «Pathological mechanisms in progressive multiple sclerosis.». Pathological mechanisms in progressive multiple sclerosis. doi:10.1016/S1474-4422(14)70256-X.
- ↑ «Demyelination versus remyelination in progressive multiple sclerosis.». Demyelination versus remyelination in progressive multiple sclerosis. doi:10.1093/brain/awq250.
- ↑ «Modelling large areas of demyelination in the rat reveals the potential and possible limitations of transplanted glial cells for remyelination in the CNS.». Modelling large areas of demyelination in the rat reveals the potential and possible limitations of transplanted glial cells for remyelination in the CNS.
- ↑ «Differentiation block of oligodendroglial progenitor cells as a cause for remyelination failure in chronic multiple sclerosis.». Differentiation block of oligodendroglial progenitor cells as a cause for remyelination failure in chronic multiple sclerosis. doi:10.1093/brain/awn096.
- ↑ «Axonal signals in central nervous system myelination, demyelination and remyelination.». Axonal signals in central nervous system myelination, demyelination and remyelination. doi:10.1016/j.jns.2005.03.029.
- ↑ «Sufro esclerosis múltiple, ¿qué puedo hacer para evitar los brotes?». www.emyaccion.com. Consultado el 15 de mayo de 2020.
- ↑ Petzold, A; Fraser CL; Abegg, M et al. «Diagnosis and classification of optic neuritis» (en inglés). Consultado el 27 de septiembre de 2022.
- ↑ Mazumder, Rajarshi; Murchison, Charles; Bourdette, Dennis; Cameron, Michelle (25 de septiembre de 2014). «Falls in People with Multiple Sclerosis Compared with Falls in Healthy Controls». En Ramagopalan, Sreeram V., ed. PLoS ONE (en inglés) 9 (9): e107620. ISSN 1932-6203. PMC 4177842. PMID 25254633. doi:10.1371/journal.pone.0107620. Consultado el 28 de enero de 2021.
- ↑ Thompson, A. J. et al. Diagnosis of multiple sclerosis: 2017 revisions of the McDonald criteria. Lancet Neurol. 2017; 17:162–173.
- ↑ WI McDonald. (2001). Recommended diagnostic criteria for multiple sclerosis: guidelines from the International Panel on the diagnosis of multiple sclerosis. In: Annals of neurology. Band 50, Nummer 1, Juli 2001, S. 121–127, PMID 11456302.
- ↑ Polman CH, Reingold SC, Banwell B, et al. Diagnostic criteria for multiple sclerosis: 2010 revisions to the McDonald Criteria. Ann Neurol 2011; 69: 292–302.
- ↑ Filippi M, Rocca MA, Ciccarelli O, et al. MRI criteria for the diagnosis of multiple sclerosis: MAGNIMS consensus guidelines. Lancet Neurol 2016; 15: 292–303.
- ↑ R Dobson, S Ramagopalan, A Davis, G Giovannoni (2013).Cerebrospinal fluid oligoclonal bands in multiple sclerosis and clinically isolated syndromes: a meta-analysis of prevalence, prognosis and effect of latitude. J Neurol Neurosurg Psychiatry. 2013 Aug;84(8):909-14. doi: 10.1136/jnnp-2012-304695.
- ↑ E Thouvenot.(2018).Multiple sclerosis biomarkers: Helping the diagnosis?. Rev Neurol (Paris). 2018 Jun;174(6):364-371.doi: 10.1016/j.neurol.2018.04.002.
- ↑ YD Fragoso, FG Elso and A Carra. (2017). Differential diagnosis of multiple sclerosis in Latin America. Multiple Sclerosis Journal Experimental, Translationaland Clinical. July-September 2017: 17. DOI: 10.1177/2055217317714279.
- ↑ Montalban X, Sastre-Garriga J, Filippi M, et al. Primary progressive multiple sclerosis diagnostic criteria: a reappraisal. Mult Scler2009;15:1459–1465.
- ↑ ECTRIMS/EAN Guideline on the pharmacological treatment of people with multiple sclerosis (6). pp. 449-457. ISSN 0035-3787. doi:10.1177/1352458517751049. Consultado el 4 de agosto de 2018.
- ↑ a b Pardo, Gabriel; Jones, David E. (septiembre de 2017). «The sequence of disease-modifying therapies in relapsing multiple sclerosis: safety and immunologic considerations» [La secuencia de terapias modificadores de la enfermedad en la esclerosis múltiple recidivante: seguridad y consideraciones inmunológicas]. J Neurol (en inglés) 264 (12): 2351-2374. PMID 28879412. doi:10.1007/s00415-017-8594-9. Consultado el 14 de enero de 2018.
- ↑ Le Page, E.; Edan, G. (2018-06). «Induction or escalation therapy for patients with multiple sclerosis?». Revue Neurologique 174 (6): 449-457. ISSN 0035-3787. doi:10.1016/j.neurol.2018.04.004. Consultado el 4 de agosto de 2018.
- ↑ a b Sedal, Leslie; Winkel, Antony; Laing, Joshua; Law, Lai Yin; McDonald, Elizabeth (septiembre de 2017). «Current concepts in multiple sclerosis therapy» [Conceptos actuales en la terapia de la esclerosis múltiple]. Degenerative neurological and neuromuscular disease (en inglés) (Dovepress) 2017 (7). doi:10.2147/DNND.S109251. Consultado el 4 de octubre de 2018.
- ↑ McKeage, Kate (24 de abril de 2015). «Glatiramer Acetate 40 mg/mL in Relapsing–Remitting Multiple Sclerosis: A Review». CNS Drugs (en inglés) 29 (5): 425-432. ISSN 1172-7047. doi:10.1007/s40263-015-0245-z. Consultado el 4 de agosto de 2018.
- ↑ Cohen, Jeffrey; Belova, Anna; Selmaj, Krzysztof; Wolf, Christian; Sormani, Maria Pia; Oberyé, Janine; Tweel, Evelyn van den; Mulder, Roel et al. (1 de diciembre de 2015). «Equivalence of Generic Glatiramer Acetate in Multiple Sclerosis: A Randomized Clinical Trial». JAMA Neurology (en inglés) 72 (12): 1433-1441. ISSN 2168-6149. doi:10.1001/jamaneurol.2015.2154. Consultado el 4 de agosto de 2018.
- ↑ [https://www.prnewswire.com/news-releases/fda-accepts-file-for-cladribine-tablets-as-potential-treatment-for-relapsing-forms-of-multiple-sclerosis-829471781.html
- ↑ El-Chammas K, Danner E (Jun 2011). «Gluten-free diet in nonceliac disease». Nutr Clin Pract (Revisión) 26 (3): 294-9. PMID 21586414. doi:10.1177/0884533611405538. «Historically, a GFD was occasionally used in the management of multiple sclerosis (MS), because anecdotal reports indicated a positive effect (reversal of symptoms) of a GFD in MS patients. (GFD=gluten-free diet) TRADUCCIÓN: Históricamente, la DSG se ha utilizado ocasionalmente en el tratamiento de la esclerosis múltiple, porque casos documentados indican un efecto positivo (reversión de los síntomas) de una DSG en pacientes con esclerosis múltiple. DSG=dieta sin gluten».
- ↑ Hernández-Lahoz C, Rodrigo L (2013 Apr 15). «Gluten-related disorders and demyelinating diseases». Med Clin (Barc) (Revisión) 140 (7): 314-9. PMID 22998972. doi:10.1016/j.medcli.2012.07.009.
- ↑ O'Connor, Paul; Comi, Giancarlo; Freedman, Mark S.; Miller, Aaron E.; Kappos, Ludwig; Bouchard, Jean-Pierre; Lebrun-Frenay, Christine; Mares, Jan et al. (8 de marzo de 2016). «Long-term safety and efficacy of teriflunomide: Nine-year follow-up of the randomized TEMSO study». Neurology (en inglés) 86 (10): 920-930. ISSN 0028-3878. PMC 4782117. PMID 26865517. doi:10.1212/WNL.0000000000002441. Consultado el 4 de agosto de 2018.
- ↑ Miller, Aaron E. (2017-12). «Oral teriflunomide in the treatment of relapsing forms of multiple sclerosis: clinical evidence and long-term experience». Therapeutic Advances in Neurological Disorders 10 (12): 381-396. ISSN 1756-2856. PMC 5703103. PMID 29204190. doi:10.1177/1756285617722500. Consultado el 4 de agosto de 2018.
- ↑ Miller, Aaron E; Wolinsky, Jerry S; Kappos, Ludwig; Comi, Giancarlo; Freedman, Mark S; Olsson, Tomas P; Bauer, Deborah; Benamor, Myriam et al. (2014-10). «Oral teriflunomide for patients with a first clinical episode suggestive of multiple sclerosis (TOPIC): a randomised, double-blind, placebo-controlled, phase 3 trial». The Lancet Neurology 13 (10): 977-986. ISSN 1474-4422. doi:10.1016/s1474-4422(14)70191-7. Consultado el 4 de agosto de 2018.
- ↑ Xu, Zhu; Zhang, Feng; Sun, FangLi; Gu, KeFeng; Dong, Shuai; He, Dian (22 de abril de 2015). The Cochrane Library (en inglés). John Wiley & Sons, Ltd. doi:10.1002/14651858.cd011076.pub2. Consultado el 4 de agosto de 2018.
- ↑ Burness, Celeste B.; Deeks, Emma D. (13 de marzo de 2014). «Dimethyl Fumarate: A Review of Its Use in Patients with Relapsing-Remitting Multiple Sclerosis». CNS Drugs (en inglés) 28 (4): 373-387. ISSN 1172-7047. doi:10.1007/s40263-014-0155-5. Consultado el 4 de agosto de 2018.
- ↑ Cree, Bruce A. C.; Stuart, William H.; Tornatore, Carlo S.; Jeffery, Douglas R.; Pace, Amy L.; Cha, Choon H. (2011-4). «Efficacy of natalizumab therapy in patients of African descent with relapsing multiple sclerosis: analysis of AFFIRM and SENTINEL data». Archives of Neurology 68 (4): 464-468. ISSN 1538-3687. PMID 21482925. doi:10.1001/archneurol.2011.45. Consultado el 4 de agosto de 2018.
- ↑ Radue, Ernst-Wilhelm; Stuart, William H.; Calabresi, Peter A.; Confavreux, Christian; Galetta, Steven L.; Rudick, Richard A.; Lublin, Fred D.; Weinstock-Guttman, Bianca et al. (15 de mayo de 2010). «Natalizumab plus interferon beta-1a reduces lesion formation in relapsing multiple sclerosis». Journal of the Neurological Sciences 292 (1-2): 28-35. ISSN 1878-5883. PMID 20236661. doi:10.1016/j.jns.2010.02.012. Consultado el 4 de agosto de 2018.
- ↑ Horga, A.; Horga de la Parte, J. F. (2007 Sep 1-15). «[Natalizumab in the treatment of multiple sclerosis]». Revista De Neurologia 45 (5): 293-303. ISSN 0210-0010. PMID 17876741. Consultado el 4 de agosto de 2018.
- ↑ «Alemtuzumab CARE-MS I 5-year follow-up: Durable efficacy in the absence of continuous MS therapy». Neurology 90 (16): 755. 17 de abril de 2018. ISSN 1526-632X. PMID 29661899. doi:10.1212/WNL.0000000000004908. Consultado el 4 de agosto de 2018.
- ↑ Caon, Christina; Namey, Marie; Meyer, Cathy; Mayer, Lori; Oyuela, Pedro; Margolin, David H.; Rizzo, Marco (2015-07). «Prevention and Management of Infusion-Associated Reactions in the Comparison of Alemtuzumab and Rebif®Efficacy in Multiple Sclerosis (CARE-MS) Program». International Journal of MS Care (en inglés estadounidense) 17 (4): 191-198. ISSN 1537-2073. PMC 4542714. PMID 26300705. doi:10.7224/1537-2073.2014-030. Consultado el 4 de agosto de 2018.
- ↑ Coles, Alasdair J.; Cohen, Jeffrey A.; Fox, Edward J.; Giovannoni, Gavin; Hartung, Hans-Peter; Havrdova, Eva; Schippling, Sven; Selmaj, Krzysztof W. et al. (12 de septiembre de 2017). «Alemtuzumab CARE-MS II 5-year follow-up: Efficacy and safety findings». Neurology 89 (11): 1117-1126. ISSN 1526-632X. PMC 5595276. PMID 28835403. doi:10.1212/WNL.0000000000004354. Consultado el 4 de agosto de 2018.
- ↑ Brusaferri, Fabio; Candelise, Livia (21 de junio de 2000). «Steriods for multiple sclerosis and optic neuritis: a meta-analysis of randomized controlled clinical trials». Journal of Neurology 247 (6): 435-442. ISSN 0340-5354. doi:10.1007/s004150070172. Consultado el 5 de agosto de 2018.
- ↑ Thompson, A. J.; Kennard, C.; Swash, M.; Summers, B.; Yuill, G. M.; Shepherd, D. I.; Roche, S.; Perkin, G. D. et al. (1 de julio de 1989). «Relative efficacy of intravenous methylprednisolone and ACTH in the treatment of acute relapse in MS». Neurology 39 (7): 969-969. ISSN 0028-3878. doi:10.1212/wnl.39.7.969. Consultado el 5 de agosto de 2018.
- ↑ Bashir, Khurram. Demyelinating Disorders of the Central Nervous System in Childhood. Cambridge University Press. pp. 87-91. ISBN 9780511974373. Consultado el 5 de agosto de 2018.
- ↑ Chow, Y. W.; Pietranico, R.; Mukerji, A. (27 de octubre de 1975). «Relation between objective and subjective measures of bladder dysfunction in multiple sclerosis.». Biochemical and Biophysical Research Communications 66 (4): 1424-1431. ISSN 0006-291X. PMID 6.
- ↑ 3. Fowler CJ, Panicker JN, Drake M, et al. A UK consensus on the management of the bladder in multiple sclerosis. J Neurol Neurosurg Psychiatry 2009; 80:470.
- ↑ Chow, Y. W.; Pietranico, R.; Mukerji, A. (27 de octubre de 1975). [3. Fowler CJ, Panicker JN, Drake M, et al. A UK consensus on the management of the bladder in multiple sclerosis. J Neurol Neurosurg Psychiatry 2009; 80:470. «Studies of oxygen binding energy to hemoglobin molecule»]. Biochemical and Biophysical Research Communications 66 (4): 1424-1431. ISSN 0006-291X. PMID 6. Consultado el 4 de agosto de 2018.
- ↑ Marniemi, J.; Parkki, M. G. (1 de septiembre de 1975). «Radiochemical assay of glutathione S-epoxide transferase and its enhancement by phenobarbital in rat liver in vivo». Biochemical Pharmacology 24 (17): 1569-1572. ISSN 0006-2952. PMID 9. Consultado el 4 de agosto de 2018.
- ↑ Fowler, C. J.; Panicker, J. N.; Drake, M.; Harris, C.; Harrison, S. C. W.; Kirby, M.; Lucas, M.; Macleod, N. et al. (1 de octubre de 2009). «A UK consensus on the management of the bladder in multiple sclerosis». Postgraduate Medical Journal (en inglés) 85 (1008): 552-559. ISSN 0032-5473. PMID 19789195. doi:10.1136/jnnp.2008.159178. Consultado el 4 de agosto de 2018.
- ↑ Phé, Véronique; Pakzad, Mahreen; Curtis, Carmel; Porter, Bernadette; Haslam, Collette; Chataway, Jeremy; Panicker, Jalesh N (18 de febrero de 2016). «Urinary tract infections in multiple sclerosis». Multiple Sclerosis Journal (en inglés) 22 (7): 855-861. ISSN 1352-4585. doi:10.1177/1352458516633903. Consultado el 4 de agosto de 2018.
- ↑ Wiesel, P. H (1 de agosto de 2000). «Gut focused behavioural treatment (biofeedback) for constipation and faecal incontinence in multiple sclerosis». Journal of Neurology, Neurosurgery & Psychiatry 69 (2): 240-243. ISSN 0022-3050. doi:10.1136/jnnp.69.2.240. Consultado el 4 de agosto de 2018.
- ↑ Wiesel, P. H (1 de agosto de 2000). «Gut focused behavioural treatment (biofeedback) for constipation and faecal incontinence in multiple sclerosis». Journal of Neurology, Neurosurgery & Psychiatry 69 (2): 240-243. ISSN 0022-3050. doi:10.1136/jnnp.69.2.240. Consultado el 4 de agosto de 2018.
- ↑ Bellman, Susan (2017-09). «Pharmacological treatment for memory disorder in multiple sclerosis». International Journal of Evidence-Based Healthcare: 1. ISSN 1744-1595. doi:10.1097/xeb.0000000000000123. Consultado el 4 de agosto de 2018.
- ↑ Patti, Francesco (9 de agosto de 2012). «Treatment of cognitive impairment in patients with multiple sclerosis». Expert Opinion on Investigational Drugs 21 (11): 1679-1699. ISSN 1354-3784. doi:10.1517/13543784.2012.716036. Consultado el 4 de agosto de 2018.
- ↑ Krupp, L. B.; Christodoulou, C.; Melville, P.; Scherl, W. F.; MacAllister, W. S.; Elkins, L. E. (8 de noviembre de 2004). «Donepezil improved memory in multiple sclerosis in a randomized clinical trial». Neurology 63 (9): 1579-1585. ISSN 0028-3878. doi:10.1212/01.wnl.0000142989.09633.5a. Consultado el 4 de agosto de 2018.
- ↑ Rosti-Otajärvi, Eija M; Hämäläinen, Päivi I (11 de febrero de 2014). «Neuropsychological rehabilitation for multiple sclerosis». Cochrane Database of Systematic Reviews. ISSN 1465-1858. doi:10.1002/14651858.cd009131.pub3. Consultado el 4 de agosto de 2018.
- ↑ Patten, S B; Metz, L M (2001-08). «Interferon β-1a and depression in relapsing - remitting multiple sclerosis: an analysis of depression data from the PRISMS clinical trial». Multiple Sclerosis Journal 7 (4): 243-248. ISSN 1352-4585. doi:10.1177/135245850100700406. Consultado el 4 de agosto de 2018.
- ↑ Cooper, Cindy (6 de diciembre de 2012). «Cognitive behavioural therapy software for the treatment of depression in people with multiple sclerosis». http://isrctn.org/>. Consultado el 4 de agosto de 2018.
- ↑ Murray, T.J. (1985-08). «Amantadine Therapy for Fatigue in Multiple Sclerosis». Canadian Journal of Neurological Sciences / Journal Canadien des Sciences Neurologiques 12 (03): 251-254. ISSN 0317-1671. doi:10.1017/s0317167100047107. Consultado el 4 de agosto de 2018.
- ↑ Minagar, A. (2011-01). «A Phase 3 Trial of Extended Release Oral Dalfampridine in Multiple Sclerosis». Yearbook of Neurology and Neurosurgery 2011: 106-107. ISSN 0513-5117. doi:10.1016/j.yneu.2011.03.003. Consultado el 4 de agosto de 2018.
- ↑ Sakurai, Masaki; Kanazawa, Ichiro (1999-01). «Positive symptoms in multiple sclerosis: their treatment with sodium channel blockers, lidocaine and mexiletine». Journal of the Neurological Sciences 162 (2): 162-168. ISSN 0022-510X. doi:10.1016/s0022-510x(98)00322-0. Consultado el 4 de agosto de 2018.
- ↑ Chou, Roger; Peterson, Kim; Helfand, Mark (2004-08). «Comparative efficacy and safety of skeletal muscle relaxants for spasticity and musculoskeletal conditions: a systematic review». Journal of Pain and Symptom Management 28 (2): 140-175. ISSN 0885-3924. doi:10.1016/j.jpainsymman.2004.05.002. Consultado el 4 de agosto de 2018.
- ↑ Feldman, R. G.; Kelly-Hayes, M.; Conomy, J. P.; Foley, J. M. (1 de noviembre de 1978). «Baclofen for spasticity in multiple sclerosis Double-blind crossover and three-year study». Neurology 28 (11): 1094-1094. ISSN 0028-3878. doi:10.1212/wnl.28.11.1094. Consultado el 4 de agosto de 2018.
- ↑ a b c Fragoso, Yara Dadalti; Carra, Adriana; Macias, Miguel Angel (2 de agosto de 2020). «Cannabis and multiple sclerosis». Expert Review of Neurotherapeutics 20 (8): 849-854. ISSN 1473-7175. PMID 32515670. doi:10.1080/14737175.2020.1776610. Consultado el 4 de enero de 2023.
- ↑ Armutlu, Kadriye; Karabudak, Rana; Nurlu, Gülay (2001-09). «Physiotherapy Approaches in the Treatment of Ataxic Multiple Sclerosis: A Pilot Study». Neurorehabilitation and Neural Repair 15 (3): 203-211. ISSN 1545-9683. doi:10.1177/154596830101500308. Consultado el 4 de agosto de 2018.
- ↑ Sechi, G. P.; Zuddas, M.; Piredda, M.; Agnetti, V.; Sau, G.; Piras, M. L.; Tanca, S.; Rosati, G. (1 de agosto de 1989). «Treatment of cerebellar tremors with carbamazepine: A controlled trial with long-term follow-up». Neurology 39 (8): 1113-1113. ISSN 0028-3878. doi:10.1212/wnl.39.8.1113. Consultado el 4 de agosto de 2018.
- ↑ Zorzon, M.; Zivadinov, R.; Bosco, A.; Monti Bragadin, L.; Moretti, R.; Bonfigli, L.; Morassi, P.; Iona, L.G. et al. (1 de junio de 1999). «Sexual dysfunction in multiple sclerosis: a case-control study. I. Frequency and comparison of groups». Multiple Sclerosis 5 (6): 418-427. ISSN 1477-0970. doi:10.1191/135245899678846456. Consultado el 4 de agosto de 2018.
- ↑ DasGUPTA, RANAN; WISEMAN, OLIVER J.; KANABAR, GORANDE; FOWLER, CLARE J. (2004-03). «Efficacy of Sildenafil in the Treatment of Female Sexual Dysfunction Due to Multiple Sclerosis». The Journal of Urology 171 (3): 1189-1193. ISSN 0022-5347. doi:10.1097/01.ju.0000113145.43174.24. Consultado el 4 de agosto de 2018.
- ↑ a b c d e f g h Yadav, V.; Bever, C.; Bowen, J.; Bowling, A.; Weinstock-Guttman, B.; Cameron, M.; Bourdette, D.; Gronseth, G. S. et al. (24 de marzo de 2014). «Summary of evidence-based guideline: Complementary and alternative medicine in multiple sclerosis: Report of the Guideline Development Subcommittee of the American Academy of Neurology». Neurology 82 (12): 1083-1092. doi:10.1212/WNL.0000000000000250.
- ↑ a b c d e f Yadav, Vijayshree; Shinto, Lynne; Bourdette, Dennis (10 de enero de 2014). «Complementary and alternative medicine for the treatment of multiple sclerosis». Expert Review of Clinical Immunology 6 (3): 381-395. doi:10.1586/eci.10.12.
- ↑ a b Moawad, Heidi; Shepard, Katie M.; Satya-Murti, Saty (de febrero de 2015). «Complementary and alternative medicine in multiple sclerosis». Neurology: Clinical Practice 5 (1): 74-79. doi:10.1212/CPJ.0000000000000020.
- ↑ a b Fox, R. J. (24 de marzo de 2014). «Complementary and alternative medicine in multiple sclerosis». Neurology 82 (12): e103-e107. doi:10.1212/WNL.0000000000000307.
- ↑ Claflin, Suzi B; van der Mei, Ingrid A F; Taylor, Bruce V (de enero de 2018). «Complementary and alternative treatments of multiple sclerosis: a review of the evidence from 2001 to 2016». Journal of Neurology, Neurosurgery & Psychiatry 89 (1): 34-41. doi:10.1136/jnnp-2016-314490.
- ↑ Motl, Robert W; Sandroff, Brian M; Kwakkel, Gert; Dalgas, Ulrik; Feinstein, Anthony; Heesen, Christoph; Feys, Peter; Thompson, Alan J (2017-10). «Exercise in patients with multiple sclerosis». The Lancet Neurology 16 (10): 848-856. ISSN 1474-4422. doi:10.1016/s1474-4422(17)30281-8. Consultado el 11 de septiembre de 2018.
- ↑ a b Sá, Maria José (22 de noviembre de 2013). «Exercise therapy and multiple sclerosis: a systematic review». Journal of Neurology (en inglés) 261 (9): 1651-1661. ISSN 0340-5354. doi:10.1007/s00415-013-7183-9. Consultado el 19 de septiembre de 2018.
- ↑ Claflin, Suzi B.; Mei, Ingrid A. F. van der; Taylor, Bruce V. (1 de enero de 2018). «Complementary and alternative treatments of multiple sclerosis: a review of the evidence from 2001 to 2016». J Neurol Neurosurg Psychiatry (en inglés) 89 (1): 34-41. ISSN 0022-3050. PMID 28768821. doi:10.1136/jnnp-2016-314490. Consultado el 19 de septiembre de 2018.
- ↑ a b Yadav, V.; Bever, C.; Bowen, J.; Bowling, A.; Weinstock-Guttman, B.; Cameron, M.; Bourdette, D.; Gronseth, G. S. et al. (24 de marzo de 2014). «Summary of evidence-based guideline: Complementary and alternative medicine in multiple sclerosis: Report of the Guideline Development Subcommittee of the American Academy of Neurology». Neurology (en inglés) 82 (12): 1083-1092. ISSN 0028-3878. PMC 3962995. PMID 24663230. doi:10.1212/wnl.0000000000000250. Consultado el 19 de septiembre de 2018.
- ↑ Zou, Liye; Wang, Huiru; Xiao, ZhongJun; Fang, Qun; Zhang, Mark; Li, Ting; Du, Geng; Liu, Yang (9 de febrero de 2017). «Tai chi for health benefits in patients with multiple sclerosis: A systematic review». PLOS ONE (en inglés) 12 (2): e0170212. ISSN 1932-6203. PMC 5300172. PMID 28182629. doi:10.1371/journal.pone.0170212. Consultado el 19 de septiembre de 2018.
- ↑ Duff, Whitney R.D.; Andrushko, Justin W.; Renshaw, Doug W.; Chilibeck, Philip D.; Farthing, Jonathan P.; Danielson, Jana; Evans, Charity D. (2018-03). «Impact of Pilates Exercise in Multiple Sclerosis». International Journal of MS Care (en inglés estadounidense) 20 (2): 92-100. ISSN 1537-2073. PMC 5898921. PMID 29670495. doi:10.7224/1537-2073.2017-066. Archivado desde el original el 20 de septiembre de 2018. Consultado el 19 de septiembre de 2018.
- ↑ Soysal Tomruk, Melda; Uz, Muhammed Zahid; Kara, Bilge; İdiman, Egemen (2016-05). «Effects of Pilates exercises on sensory interaction, postural control and fatigue in patients with multiple sclerosis». Multiple Sclerosis and Related Disorders 7: 70-73. ISSN 2211-0348. doi:10.1016/j.msard.2016.03.008. Consultado el 19 de septiembre de 2018.
- ↑ Bulguroglu, I.; Guclu-Gunduz, A.; Yazici, G.; Ozkul, C.; Irkec, C.; Nazliel, B.; Batur-Caglayan, H.Z. (14 de octubre de 2017). «The effects of Mat Pilates and Reformer Pilates in patients with Multiple Sclerosis: A randomized controlled study». NeuroRehabilitation (en inglés) 41 (2): 413-422. ISSN 1053-8135. doi:10.3233/nre-162121. Consultado el 19 de septiembre de 2018.
- ↑ Alghwiri, Alia A.; Khalil, Hanan; Al-Sharman, Alham; El-Salem, Khalid (2018-08). «Depression is a predictor for balance in people with multiple sclerosis». Multiple Sclerosis and Related Disorders 24: 28-31. ISSN 2211-0348. doi:10.1016/j.msard.2018.05.013. Consultado el 19 de septiembre de 2018.
- ↑ Pagnini, Francesco; Bosma, Colin M; Phillips, Deborah; Langer, Ellen (30 de noviembre de 2014). «Symptom changes in multiple sclerosis following psychological interventions: a systematic review». BMC Neurology (en inglés) 14 (1). ISSN 1471-2377. PMC 4253984. PMID 25433519. doi:10.1186/s12883-014-0222-z. Consultado el 19 de septiembre de 2018.
- ↑ Rudroff, Thorsten; Sosnoff, Jacob (2018). «Cannabidiol to Improve Mobility in People with Multiple Sclerosis». Frontiers in Neurology (en inglés) 9. ISSN 1664-2295. PMC 5874292. PMID 29623067. doi:10.3389/fneur.2018.00183. Consultado el 19 de septiembre de 2018.
- ↑ Nielsen, Suzanne; Germanos, Rada; Weier, Megan; Pollard, John; Degenhardt, Louisa; Hall, Wayne; Buckley, Nicholas; Farrell, Michael (2018-02). «The Use of Cannabis and Cannabinoids in Treating Symptoms of Multiple Sclerosis: a Systematic Review of Reviews». Current Neurology and Neuroscience Reports (en inglés) 18 (2). ISSN 1528-4042. doi:10.1007/s11910-018-0814-x. Consultado el 19 de septiembre de 2018.
- ↑ Gabriel, Ortiz, Genaro; Ángel, Macías-Islas, Miguel; P., Pacheco-Moisés, Fermín; A., Cruz-Ramos, José; Silvia, Sustersik,; Alejandro, Barba, Elías; Adriana, Aguayo,. «Oxidative Stress is Increased in Serum from Mexican Patients with Relapsing-Remitting Multiple Sclerosis». Disease Markers (en inglés) 26 (1). ISSN 0278-0240. PMC 3833233. PMID 19242067. doi:10.3233/dma-2009-0602. Consultado el 19 de septiembre de 2018.
- ↑ Gold, Ralf; Giovannoni, Gavin; Phillips, J Theodore; Fox, Robert J; Zhang, Annie; Meltzer, Leslie; Kurukulasuriya, Nuwan C (2 de julio de 2014). «Efficacy and safety of delayed-release dimethyl fumarate in patients newly diagnosed with relapsing–remitting multiple sclerosis (RRMS)». Multiple Sclerosis Journal (en inglés) 21 (1): 57-66. ISSN 1352-4585. PMC 4361464. PMID 24990854. doi:10.1177/1352458514537013. Consultado el 19 de septiembre de 2018.
- ↑ Manouchehrinia, Ali; Tench, Christopher R.; Maxted, Jonathan; Bibani, Rashid H.; Britton, John; Constantinescu, Cris S. (11 de junio de 2013). «Tobacco smoking and disability progression in multiple sclerosis: United Kingdom cohort study». Brain (en inglés) 136 (7): 2298-2304. ISSN 1460-2156. PMC 3692034. PMID 23757766. doi:10.1093/brain/awt139. Consultado el 19 de septiembre de 2018.
- ↑ Hedström, Anna Karin; Katsoulis, Michail; Hössjer, Ola; Bomfim, Izaura L.; Oturai, Annette; Sondergaard, Helle Bach; Sellebjerg, Finn; Ullum, Henrik et al. (8 de junio de 2017). «The interaction between smoking and HLA genes in multiple sclerosis: replication and refinement». European Journal of Epidemiology (en inglés) 32 (10): 909-919. ISSN 0393-2990. PMC 5680370. PMID 28597127. doi:10.1007/s10654-017-0250-2. Consultado el 19 de septiembre de 2018.
- ↑ Andersen, Christina; Søndergaard, Helle Bach; Bang Oturai, Ditte; Laursen, Julie Hejgaard; Gustavsen, Stefan; Larsen, Nanna Katrine; Magyari, Melinda; Just-Østergaard, Emilie et al. (20 de agosto de 2018). «Alcohol consumption in adolescence is associated with a lower risk of multiple sclerosis in a Danish cohort». Multiple Sclerosis Journal (en inglés): 135245851879541. ISSN 1352-4585. doi:10.1177/1352458518795418. Consultado el 19 de septiembre de 2018.
- ↑ Guerrero-García, José de Jesús; Carrera-Quintanar, Lucrecia; López-Roa, Rocío Ivette; Márquez-Aguirre, Ana Laura; Rojas-Mayorquín, Argelia Esperanza; Ortuño-Sahagún, Daniel (2016). «Multiple Sclerosis and Obesity: Possible Roles of Adipokines». Mediators of Inflammation (en inglés) 2016: 1-24. ISSN 0962-9351. PMC 5046034. PMID 27721574. doi:10.1155/2016/4036232. Consultado el 19 de septiembre de 2018.
- ↑ Munger, Kassandra L; Bentzen, Joan; Laursen, Bjarne; Stenager, Egon; Koch-Henriksen, Nils; Sørensen, Thorkild IA; Baker, Jennifer L (2 de abril de 2013). «Childhood body mass index and multiple sclerosis risk: a long-term cohort study». Multiple Sclerosis Journal (en inglés) 19 (10): 1323-1329. ISSN 1352-4585. PMC 4418015. PMID 23549432. doi:10.1177/1352458513483889. Consultado el 19 de septiembre de 2018.
- ↑ Correale, Jorge; Farez, Mauricio F; Gaitán, María Inés (2017-06). «Environmental factors influencing multiple sclerosis in Latin America». Multiple Sclerosis Journal – Experimental, Translational and Clinical (en inglés) 3 (2): 205521731771504. ISSN 2055-2173. PMC 5472234. PMID 28638627. doi:10.1177/2055217317715049. Consultado el 19 de septiembre de 2018.
- ↑ Pierrot-Deseilligny, Charles (28 de abril de 2009). «Clinical implications of a possible role of vitamin D in multiple sclerosis». Journal of Neurology (en inglés) 256 (9): 1468-1479. ISSN 0340-5354. PMC 2733195. PMID 19399382. doi:10.1007/s00415-009-5139-x. Consultado el 19 de septiembre de 2018.
- ↑ Hossein-nezhad, Arash; Holick, Michael F. (2013-07). «Vitamin D for Health: A Global Perspective». Mayo Clinic Proceedings 88 (7): 720-755. ISSN 0025-6196. PMC 3761874. PMID 23790560. doi:10.1016/j.mayocp.2013.05.011. Consultado el 19 de septiembre de 2018.
- ↑ Pappolla, Agustín; Sánchez, Francisco; Patrucco, Liliana; Varela, Lucia; Castañares, Clara; Lopez, Pablo H.; Cristiano, Edgardo; Rojas, Juan I. (2021). «Valor pronóstico del glutamato en el líquido cefalorraquídeo en esclerosis múltiple». Fundación Revista Medicina 81 (5).
- ↑ Weygandt, Martin; Meyer-Arndt, Lil; Behrens, Janina Ruth; Wakonig, Katharina; Bellmann-Strobl, Judith; Ritter, Kerstin; Scheel, Michael; Brandt, Alexander U. et al. (22 de noviembre de 2016). «Stress-induced brain activity, brain atrophy, and clinical disability in multiple sclerosis». Proceedings of the National Academy of Sciences (en inglés) 113 (47): 13444-13449. ISSN 0027-8424. PMC 5127380. PMID 27821732. doi:10.1073/pnas.1605829113. Consultado el 19 de septiembre de 2018.
- ↑ Marrie, Ruth Ann; Reingold, Stephen; Cohen, Jeffrey; Stuve, Olaf; Trojano, Maria; Sorensen, Per Soelberg; Cutter, Gary; Reider, Nadia (12 de enero de 2015). «The incidence and prevalence of psychiatric disorders in multiple sclerosis: A systematic review». Multiple Sclerosis Journal (en inglés) 21 (3): 305-317. ISSN 1352-4585. PMC 4429164. PMID 25583845. doi:10.1177/1352458514564487. Consultado el 19 de septiembre de 2018.
- ↑ Braley, Tiffany J.; Kratz, Anna L.; Kaplish, Neeraj; Chervin, Ronald D. (2016-08). «Sleep and Cognitive Function in Multiple Sclerosis». Sleep (en inglés) 39 (8): 1525-1533. ISSN 0161-8105. PMC 4945311. PMID 27166237. doi:10.5665/sleep.6012. Consultado el 19 de septiembre de 2018.
- ↑ Veauthier, Christian; Gaede, Gunnar; Radbruch, Helena; Wernecke, Klaus-Dieter; Paul, Friedemann; Veauthier, Christian; Gaede, Gunnar; Radbruch, Helena et al. (21 de julio de 2015). «Sleep Disorders Reduce Health-Related Quality of Life in Multiple Sclerosis (Nottingham Health Profile Data in Patients with Multiple Sclerosis)». International Journal of Molecular Sciences (en inglés) 16 (7): 16514-16528. PMC 4519963. PMID 26197315. doi:10.3390/ijms160716514. Consultado el 19 de septiembre de 2018.
- ↑ Lorefice, Lorena; Mura, Gioia; Coni, Giulia; Fenu, Giuseppe; Sardu, Claudia; Frau, Jessica; Coghe, Giancarlo; Melis, Marta et al. (15 de noviembre de 2013). «What do multiple sclerosis patients and their caregivers perceive as unmet needs?». BMC Neurology (en inglés) 13 (1). ISSN 1471-2377. PMC 3840560. PMID 24237586. doi:10.1186/1471-2377-13-177. Consultado el 4 de agosto de 2018.
- ↑ «Unmet Needs of Patients Feeling Severely Affected by Multiple Sclerosis in Germany: A Qualitative Study» (en inglés). doi:10.1089/jpm.2013.0497.
- ↑ «Home | MS International Federation». MS International Federation (en inglés estadounidense). Consultado el 4 de agosto de 2018.
- ↑ «Sobre el Día Mundial de la Esclerosis Múltiple». World MS Day 2018. Consultado el 4 de agosto de 2018.
- ↑ «Home - ECTRIMS | European Committee for Treatment and Research in Multiple Sclerosis». ECTRIMS | European Committee for Treatment and Research in Multiple Sclerosis (en inglés estadounidense). Consultado el 4 de agosto de 2018.
- ↑ «Welcome». ACTRIMS (en inglés estadounidense). Consultado el 4 de agosto de 2018.
- ↑ «LACTRIMS ORG – Otro sitio realizado con WordPress». www.lactrimsweb.org. Consultado el 4 de agosto de 2018.
- ↑ «PACTRIMS – Pan-Asian Committee for Treatment and Research in Multiple Sclerosis». www.pactrims.org (en inglés estadounidense). Consultado el 4 de agosto de 2018.
- ↑ «MENA Committee for Research and Treatment in Multiple Sclerosis». www.menactrims.com (en inglés). Consultado el 4 de agosto de 2018.
- ↑ «Mexctrims». mexctrims.com (en inglés). Consultado el 4 de agosto de 2018.
- ↑ «BCTRIMS». www.bctrims.com.br. Consultado el 4 de agosto de 2018.
- ↑ «Multiple Sclerosis Brain Health initiative». MS Brain Health (en inglés). Consultado el 4 de agosto de 2018.
- ↑ Hammer LA, Waldner H, Zagon IS, McLaughlin PJ. (2016 Jan). Opioid growth factor and low-dose naltrexone impair central nervous system infiltration by CD4 + T lymphocytes in established experimental autoimmune encephalomyelitis, a model of multiple sclerosis. 1. pp. 71-8. doi:10.1177/1535370215596384. Consultado el 12 de agosto de 2018.
- ↑ Ludwig, M. D., Zagon, I. S., & McLaughlin, P. J. (2017). Serum [Met 5 ]-enkephalin levels are reduced in multiple sclerosis and restored by low-dose naltrexone. Experimental Biology and Medicine 15 (24). pp. 1524-1533. Consultado el 12 de agosto de 2018.
- ↑ Parkitny L, Younger J. (abr 2017). Reduced Pro-Inflammatory Cytokines after Eight Weeks of Low-Dose Naltrexone for Fibromyalgia. 5 (18). p. 2. doi:10.3390/biomedicines5020016.
- ↑ Sharafaddinzadeh N, Moghtaderi A, Kashipazha D, Majdinasab N, Shalbafan B. (2010 Aug). The effect of low-dose naltrexone on quality of life of patients with multiple sclerosis: a randomized placebo-controlled trial.. doi:10.1177/1352458510366857.
- ↑ Cree BA, Kornyeyeva E, Goodin DS. (2010 Aug). Pilot trial of low-dose naltrexone and quality of life in multiple sclerosis. (68). doi:10.1002/ana.22006.
- ↑ Gironi M, Martinelli-Boneschi F, Sacerdote P, Solaro C, Zaffaroni M, Cavarretta R, Moiola L, Bucello S, Radaelli M, Pilato V, Rodegher M, Cursi M, Franchi S, Martinelli V, Nemni R, Comi G, Martino G. (2008). A pilot trial of low-dose naltrexone in primary progressive multiple sclerosis.. doi:10.1177/1352458508095828.
- ↑ «LDN SCIENCE».
Bibliografía[editar]
- «MS (multiple sclerosis: esclerosis múltiple): esperanza en la investigación», extenso artículo en el sitio web del National Institute of Neurological Disorders and Stroke; publicado bajo dominio público.
- OMIM 126200
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Esclerosis múltiple.
Wikimedia Commons alberga una categoría multimedia sobre Esclerosis múltiple.
