Cloruro de sodio
| Cloruro de sodio | ||
|---|---|---|
 Cristal de cloruro de sodio. | ||
 | ||
| Nombre IUPAC | ||
| Cloruro de sodio. | ||
| General | ||
| Otros nombres |
Cloruro sódico Sal común Sal de cocina Sodio cloruro Nombre mineral: Halita | |
| Fórmula molecular | NaCl | |
| Identificadores | ||
| Número CAS | 7647-14-5[1] | |
| Número RTECS | VZ4725000 | |
| ChEBI | 26710 | |
| ChEMBL | CHEMBL1200574 | |
| ChemSpider | 5044 | |
| DrugBank | 09153 | |
| PubChem | 5234 | |
| UNII | 451W47IQ8X | |
| KEGG | D02056 C13563, D02056 | |
| Propiedades físicas | ||
| Apariencia | Incoloro; aunque parece blanco si son cristales finos o pulverizados. | |
| Densidad | 2160 kg/m³; 2,16 g/cm³ | |
| Masa molar | 58,443 g/mol | |
| Punto de fusión | 1074 K (801 °C) | |
| Punto de ebullición | 1738 K (1465 °C) | |
| Estructura cristalina | f.c.c. | |
| Índice de refracción (nD) | 1,544202 | |
| Propiedades químicas | ||
| Solubilidad en agua | 359 g/L en agua | |
| Producto de solubilidad | 37,79 mol² | |
| Termoquímica | ||
| ΔfH0gas | -181,42 kJ/mol | |
| ΔfH0líquido | -385,92 kJ/mol | |
| ΔfH0sólido | -411,12 kJ/mol | |
| S0gas, 1 bar | 229,79 J·mol–1·K | |
| S0líquido, 1 bar | 95,06 J·mol–1·K–1 | |
| S0sólido | 72,11 J·mol–1·K–1 | |
| Peligrosidad | ||
| NFPA 704 |
0
0
0
| |
| Riesgos | ||
| Ingestión | Peligroso en grandes cantidades; su uso a largo plazo en cantidades normales puede traer problemas en los riñones; Su consumo excesivo también está relacionado con la hipertensión arterial. | |
| Inhalación | Puede producir irritación en altas cantidades. | |
| Piel | Puede producir resequedad. | |
| Ojos | Puede producir irritación y molestia. | |
| Compuestos relacionados | ||
| Cloruros alcalinos | Cloruro de potasio, cloruro de litio, cloruro de cesio | |
| Haluros de sodio | Bromuro sódico, fluoruro sódico, ioduro sódico | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El cloruro de sodio, sal común o sal de mesa, denominada en su forma mineral como halita, es un compuesto químico con la fórmula NaCl. El cloruro de sodio es una de las sales responsables de la salinidad del océano y del fluido extracelular de muchos organismos. Es también el componente de la sal común, usada como condimento y conservante de alimentos.
Con masas molareses de 22,99 y 35,45 g/mol respectivamente, 100 g de NaCl contienen 39,34 g de Na y 60,66 g de Cl. En su forma comestible, la sal (también conocida como sal de mesa) se utiliza habitualmente como condimento y curado y conservante de alimentos Se utilizan grandes cantidades de cloruro sódico en muchos procesos industriales, y es una fuente importante de compuestos de sodio y cloro utilizados como materias primas para posteriores síntesis químicas. Otra aplicación importante del cloruro sódico es la descongelación de carreteras cuando el clima es bajo cero.
En la antigüedad, el cloruro de sodio era muy apetecido como un bien transable y como condimento, y se remuneraba en la época preclásica romana a los soldados que construían la Vía Salaria, que empezaba en las canteras de Ostia hasta Roma, con un generoso salarium argentum.
Propiedades químicas[editar]
Es un compuesto iónico formado por un catión sodio (Na+) y un anión cloruro (Cl-), y puede sufrir las reacciones características de cualquiera de estos dos iones. Como cualquier otro cloruro iónico soluble, precipita cloruros insolubles cuando es agregado a una disolución de una sal metálica apropiada, como nitrato de plata:
Otro método para separar ambos componentes es mediante la electrólisis.
Si se aplica una corriente eléctrica continua con un elevado potencial a una salmuera alcalina, el producto anódico es gas dicloro (Cl2) y los catódicos son hidróxido de sodio (NaOH) y dihidrógeno (H2).
- electrólisis: 2 NaCl(aq) → 2 NaOH(aq) + Cl2(gas) + H2(gas)
Como la mayoría de las sales iónicas confiere propiedades coligativas a sus disoluciones, es decir, es capaz de variar la presión de vapor de la disolución, elevar el punto de ebullición y descender el punto de congelación según su concentración molal.
Estructura cristalina[editar]
Cuando el cloruro de sodio está en estado sólido, sus átomos se acomodan en una estructura cristalina cúbica, como es de esperarse en una unión iónica ocasionada por los campos electrostáticos de sus átomos. Cada ion se acomoda en el centro de un octaedro regular quedando rodeado por 6 iones de cargas opuestas distribuidos en los vértices del octaedro.
Esta misma estructura básica se encuentra en muchos otros compuestos y es comúnmente conocida como la estructura cristalina de halita o sal de roca. Se puede representar como una red cúbica centrada en la cara (fcc) con una base de dos átomos o como dos redes cúbicas centradas en la cara interpenetrantes. El primer átomo se encuentra en cada punto de celosía.
Producción[editar]
El cloruro de sodio es producido en masa por la evaporación de agua de mar o salmuera de otros recursos, como lagos salados, y minando la roca de sal, llamada halita.
En 2002, la producción mundial de sal se estimó en 210 millones de toneladas métricas, y los principales países productores fueron Estados Unidos (40.3 millones de toneladas), China (32.9), Alemania (17.7), India (14.5) y Canadá (12.3).[2] A
Regulación fisiológica[editar]
El ion Na+ es causante de la regulación osmótica celular regulando el potencial de membrana expulsando el ion K +, facilita en gran manera el impulso nervioso y es aportado al organismo en gran medida como sal de mesa.
Aplicaciones[editar]
El cloruro de sodio es usado universalmente como aditivo alimentario. También se usa en la producción de papel y celulosa, en los productos de baño y en detergentes. Además de los usos domésticos familiares de la sal, las aplicaciones más dominantes de la producción de aproximadamente 250 millones de toneladas por año (datos de 2008) incluyen productos químicos y descongelación.[3]
Antiséptico local y preservante de alimentos[editar]
La sal, gracias a su elevado poder osmótico, es capaz de deshidratar un amplio espectro de virus y bacterias en estado no esporulado, por lo que se usa como un doloroso antiséptico para desinfectar heridas.
Muy pocos microorganismos, como los halófilos y organismos superiores como los crustáceo braquiópodos conocidos como las Artemias, pueden resistirse al poder osmótico de la sal. Entre los microorganismos resistentes a la salinidad está el caso de la bacteria B. marismortui, encontrada en el mar Muerto.
La salazón de la carne es una forma de preservar ésta de la acción bacteriana, ya que la sal retrasa la descomposición proteínica. Para preservar alimentos, el cloruro de sodio extrae el agua de estos, impidiendo el crecimiento de las bacterias.[4][5]
Usos industriales diversos[editar]
El cloruro sódico es muy utilizado, por lo que incluso aplicaciones relativamente menores pueden consumir cantidades masivas. En la exploración de petróleo y gas, la sal es un componente importante de los fluidos de perforación en la perforación de pozos. Se utiliza para flocularizar y aumentar la densidad del fluido de perforación para superar las altas presiones de gas de fondo de pozo. Cada vez que un taladro golpea una formación salina, se añade sal al fluido de perforación para saturar la solución con el fin de minimizar la disolución dentro del estrato salino.[3] La sal también se utiliza para aumentar el curado del hormigón en las carcasas cementadas.[6]>.
En textiles y tintorería, la sal se utiliza como enjuague de salmuera para separar contaminantes orgánicos, para promover el "salado" de precipitados de colorantes y para mezclar con colorantes concentrados para estandarizarlos[aclaración requerida]. Una de sus principales funciones es proporcionar la carga iónica positiva para promover la absorción de los iones de carga negativa de los colorantes.[6]
También se utiliza en el procesamiento de aluminio, berilio, cobre, acero y vanadio. En la industria del papel y la pasta de papel, la sal se utiliza para blanquear la pasta de madera. También se utiliza para fabricar clorato sódico, que se añade junto con ácido sulfúrico y agua para fabricar dióxido de cloro, un excelente producto químico blanqueador a base de oxígeno. El proceso del dióxido de cloro, que se originó en Alemania después de la Primera Guerra Mundial, es cada vez más popular debido a las presiones medioambientales para reducir o eliminar los compuestos blanqueadores clorados. En el curtido y el tratamiento del cuero, la sal se añade a las pieles de los animales para inhibir la actividad microbiana en la parte inferior de las pieles y para atraer la humedad de vuelta a las pieles.[6]
En la fabricación de caucho, la sal se utiliza para fabricar buna, neopreno y caucho blanco. La salmuera y el ácido sulfúrico se utilizan para coagular un látex emulsionado hecho de butadieno clorado.[6][3]
También se añade sal para asegurar el suelo y dar firmeza a los cimientos sobre los que se construyen las autopistas. La sal actúa para minimizar los efectos del desplazamiento causado en el subsuelo por los cambios de humedad y la carga de tráfico.[6]
El cloruro sódico se utiliza a veces como desecante barato y seguro debido a sus propiedades higroscópicas, lo que hace de la salazón un método eficaz de conservación de alimentos históricamente; la sal extrae el agua de las bacterias mediante presión osmótica, impidiendo que se reproduzcan, una de las principales fuentes de deterioro de los alimentos. Aunque existen desecantes más eficaces, pocos son seguros para la ingestión humana.
Fundente del hielo[editar]
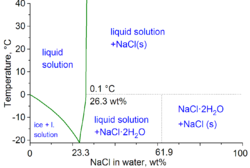
El cloruro de sodio en salmuera (la mezcla comercial para una solución saturada alcanza los 270 g por litro) es el fundente del hielo y de la nieve más usado en vialidad. Al disolverse la sal en el agua, baja el punto de congelación de ésta. En contacto con el agua provoca una reacción endotérmica que precisa de aporte de calor, que toma del ambiente o de la superficie de contacto, entalpía, (ΔH= -385.820 KJ/mol).
La segunda aplicación más importante de la sal es el deshielo y el antihielo de las carreteras, tanto en depósitos de arena como esparcida por vehículos de servicio invernal. En previsión de las nevadas, las carreteras se "antihielan" de forma óptima con salmuera (solución concentrada de sal en agua), que impide la adherencia entre la nieve y la superficie de la carretera. Este procedimiento evita el uso intensivo de sal tras la nevada. Para el deshielo, se utilizan mezclas de salmuera y sal, a veces con agentes adicionales como cloruro de calcio y/o cloruro de magnesio. El uso de sal o salmuera se vuelve ineficaz por debajo de −10 grados Celsius (14 °F).

La sal para deshielo en el Reino Unido procede predominantemente de una única mina de Winsford en Cheshire. Antes de su distribución, se mezcla con <100 ppm de ferrocianuro de sodio como agente antiaglomerante, lo que permite que la sal gema fluya libremente fuera de los vehículos de arenado a pesar de haber sido almacenada antes de su uso. En los últimos años, este aditivo también se ha utilizado en la sal de mesa. Se han utilizado otros aditivos en la sal de carretera para reducir los costes totales. En EE. UU., por ejemplo, se mezcló con sal gema una solución de carbohidratos subproducto del procesado de la remolacha azucarera que se adhirió a la superficie de las carreteras un 40% mejor que la sal gema suelta. Al permanecer más tiempo en la carretera, el tratamiento no tenía que repetirse varias veces, lo que ahorraba tiempo y dinero.[6]
En términos técnicos de fisicoquímica, el punto de congelación mínimo de una mezcla de agua y sal es de −21,12 grados Celsius (−6,0 °F) para un 23,31% en peso de sal. Sin embargo, la congelación cerca de esta concentración es tan lenta que el punto eutéctico de −22,4 grados Celsius (−8,3 °F) puede alcanzarse con un 25 % en peso de sal.[7]
Efectos medioambientales[editar]
La sal de carretera acaba en masas de agua dulce y podría perjudicar a las plantas y animales acuáticos al alterar su capacidad de osmorregulación.[8] La omnipresencia de la sal plantea un problema en cualquier aplicación de revestimientos costeros, ya que las sales atrapadas causan grandes problemas de adherencia. Las autoridades navales y los constructores de barcos controlan las concentraciones de sal en las superficies durante la construcción. Las concentraciones máximas de sal en las superficies dependen de la autoridad y de la aplicación. La normativa de la IMO es la más utilizada y fija los niveles de sal en un máximo de 50 mg/m2 de sales solubles medidas como cloruro sódico. Estas mediciones se realizan mediante un test de Bresle. La salinización (aumento de la salinidad, también conocido como síndrome de salinización del agua dulce) y el consiguiente aumento de la lixiviación de metales es un problema constante en toda América del Norte y en las vías fluviales dulces europeas.[9].
En el deshielo de carreteras, la sal se ha asociado a la corrosión de los tableros de los puentes, los vehículos de motor, las barras y alambres de refuerzo y las estructuras de acero sin protección utilizadas en la construcción de carreteras. La escorrentía superficial, la pulverización de vehículos y las acciones del viento también afectan al suelo, a la vegetación de los bordes de las carreteras y a los suministros locales de aguas superficiales y subterráneas. Aunque se han encontrado pruebas de carga ambiental de sal durante los picos de uso, las lluvias y deshielos primaverales suelen diluir las concentraciones de sodio en la zona donde se aplicó la sal.[6] Un estudio de 2009 descubrió que aproximadamente el 70% de la sal de carretera que se aplica en el área metropolitana de Minneapolis-Saint Paul se retiene en la cuenca local.[10]
Plantas[editar]
El sodio es un nutriente no esencial para las plantas, que lo necesitan en dosis muy bajas. Excepcionalmente, ciertos grupos de plantas, como las plantas C4, o la CAM, necesitan dosis mayores de este elemento.
Por otra parte, el exceso de sal en el medio resulta perjudicial para la mayor parte de las plantas (salinidad del suelo o sustrato), ya que provoca su desecación por ósmosis (el agua se desplaza hacia el ámbito más salino). Un síntoma característico son las quemaduras de los bordes de las hojas. Solamente las plantas llamadas halofitas han desarrollado un proceso que evita esa pérdida de agua.
Industria alimentaria y agricultura[editar]
Muchos microorganismoss no pueden vivir en un medio salado: el agua sale de sus células por ósmosis. Por esta razón, la sal se utiliza para conservar algunos alimentos, como el tocino, el pescado o la col.
La sal se añade a los alimentos, ya sea por el productor o por el consumidor, como potenciador del sabor, conservante, aglutinante, aditivo de control de la fermentación, agente de control de la textura y revelador del color. El consumo de sal en la industria alimentaria se subdivide, en orden descendente de consumo, en otros productos de elaboración de alimentos, envasadores de carne, enlatado, panadería, productos lácteos y molinería de cereales. La sal se añade para favorecer el desarrollo del color en el tocino, el jamón y otros productos cárnicos procesados. Como conservante, la sal inhibe el crecimiento de bacterias. La sal actúa como aglutinante en los embutidos para formar un gel aglutinante compuesto de carne, grasa y humedad. La sal también actúa como potenciador del sabor y como ablandador.[6]
En muchas industrias lácteas, la sal se añade al queso como agente de control del color, la fermentación y la textura. El subsector lácteo incluye empresas que fabrican mantequilla de nata, leche condensada y evaporada, postres congelados, helados, queso natural y procesado, y productos lácteos especiales. En el enlatado, la sal se añade principalmente como potenciador del sabor y conservante. También se utiliza como portador de otros ingredientes, agente deshidratante, inhibidor de enzimas y ablandador. En panadería, la sal se añade para controlar la velocidad de fermentación de la masa de pan. También se utiliza para fortalecer el gluten (el complejo elástico proteína-agua de ciertas masas) y como potenciador del sabor, por ejemplo como cobertura de productos horneados. La categoría de procesado de alimentos también incluye productos de molinería. Estos productos consisten en moler harina y arroz y fabricar cereales para el desayuno y harina mezclada o preparada. La sal también se utiliza como condimento, por ejemplo, en patatas fritas, pretzels y comida para perros y gatos.[6]
El cloruro sódico se utiliza en medicina veterinaria como agente emesis-causante. Se administra como solución saturada caliente. La emesis también puede ser causada por la faringe colocación de pequeñas cantidades de sal común o cristales de sal.
Medicina[editar]
Es el antídoto natural del nitrato de plata, metabolizándolo en cloruro de plata, sustancia prácticamente atóxica que el cuerpo puede excretar con seguridad.[11]
Referencias[editar]
- ↑ Número CAS
- ↑ Susan R. Feldman. Sodium chloride. Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. Published online 2005. doi 10.1002/0471238961.1915040902051820.a01.pub2
- ↑ a b c Westphal, Gisbert et al. (2002) "Sodium Chloride" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim .
- ↑ Parra, Sergio (6 de agosto de 2015). «El secreto para conservar alimentos durante la historia: sal, acidez y bacterias del propio alimento». Consultado el 13 de agosto de 2017.
- ↑ Andresrguez (18 de febrero de 2010). «¿Por qué se emplean las salazones para conservar alimentos?». Ciencias y cosas. Consultado el 13 de agosto de 2017.
- ↑ a b c d e f g h i Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasusgs - ↑ Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasu1 - ↑ Rastogi, Nina (16 de febrero de 2010) ¿La sal de carretera perjudica al medio ambiente? slate.com.
- ↑ «Las vías fluviales salinas están creando peligrosos 'cócteles químicos'». phys.org.
- ↑ «La mayor parte de la sal de carretera llega a lagos y ríos». www.sciencedaily.com. Universidad de Minnesota. 20 de febrero de 2009. Consultado el 27 de septiembre de 2015.
- ↑ Calabrese, Alberto I.; Astolfi, Emilio A. (enero de 1969). Toxicología. Buenos Aires, Argentina: Kapelusz. p. 190. OCLC 14501248.

