Diferencia entre revisiones de «Metabolismo»
+catabolismo |
+digestión |
||
| Línea 91: | Línea 91: | ||
El conjunto de reacciones catabólicas más común en eanimales puede ser separado en tres etapas distintas. En la primera, moléculas orgánicas grandes como las protínas, polisacáridos o lípidos son digeridos en componentes más pequeño fuera de las células. Luego, estas moléculas pequeñas son llevadas a las células y convertidas en moléculas aún más pequeñas, generalmente [[acetil CoA]], que libera energía. Finlamente, el grupo acetil en la molécula de acteil CoA es oxidada en agua y dióxido de carbono, liberan energía que se retiene al reducir la coenzima [[nicotinamida adenina dinucleótido]] (NAD<sup>+</sup>) en NADH. |
El conjunto de reacciones catabólicas más común en eanimales puede ser separado en tres etapas distintas. En la primera, moléculas orgánicas grandes como las protínas, polisacáridos o lípidos son digeridos en componentes más pequeño fuera de las células. Luego, estas moléculas pequeñas son llevadas a las células y convertidas en moléculas aún más pequeñas, generalmente [[acetil CoA]], que libera energía. Finlamente, el grupo acetil en la molécula de acteil CoA es oxidada en agua y dióxido de carbono, liberan energía que se retiene al reducir la coenzima [[nicotinamida adenina dinucleótido]] (NAD<sup>+</sup>) en NADH. |
||
=== Digestión === |
|||
{{AP|Digestión|Aparato digestivo}} |
|||
Macromoléculas como el almidón, celulosa o proteínas no pueden ser tomadas por las células rápidamente, por lo que necesitan que se degraden en unidades más simples antes de usarlas en el metabolismo celular. Muchas enzimas digieren estos polímeros. Estas enzimas incluyen [[peptidasa]] que digiere proteínas en aminoácidos; también incluyen [[glicósido|glicosida hidrolasada]] que digieren polisacáridos en monosacáridos. |
|||
[[Microbios]] simplemente segregan enzimas degestivas en sus alrededores<ref>{{cite journal |author=Häse C, Finkelstein R |title=Bacterial extracellular zinc-containing metalloproteases |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=8302217 |journal=Microbiol Rev |volume=57 |issue=4 |pages=823-37 |year=1993 |pmid=8302217}}</ref><ref>{{cite journal |author=Gupta R, Gupta N, Rathi P |title=Bacterial lipases: an overview of production, purification and biochemical properties |journal=Appl Microbiol Biotechnol |volume=64 |issue=6 |pages=763-81 |year=2004 |pmid=14966663}}</ref> mientras que los [[animal]]es solo segregan estas enzimas de células especializadas en sus [[aparato digestivo|aparatos digestivos]].<ref>{{cite journal |author=Hoyle T |title=The digestive system: linking theory and practice |journal=Br J Nurs |volume=6 |issue=22 |pages=1285-91 |year=1997 |pmid=9470654}}</ref> Los aminoácidos liberados por estas enzimas extracelulares son absorbidas por las células por proteínas específicas de transporte.<ref>{{cite journal |author=Souba W, Pacitti A |title=How amino acids get into cells: mechanisms, models, menus, and mediators |journal=JPEN J Parenter Enteral Nutr |volume=16 |issue=6 |pages=569-78 |year=1992 |pmid=1494216}}</ref><ref>{{cite journal |author=Barrett M, Walmsley A, Gould G |title=Structure and function of facilitative sugar transporters |journal=Curr Opin Cell Biol |volume=11 |issue=4 |pages=496-502 |year=1999 |pmid=10449337}}</ref> |
|||
<!-- [[Image:Catabolism schematic.svg|thumb|left|300px|Un diagrama simplificado del catabolismo de [[proteína]]s, [[carbohidratos]] y [[lípido]]s (en inglés)]] --> |
|||
== Referencias == |
== Referencias == |
||
Revisión del 13:28 21 abr 2007
El metabolismo es el conjunto de reacciones químicas que ocurren en una célula. Estos procesos son la base de la vida, y permiten a las célula crecer, reproducirse, mantener sus estructuras, y responder a su ambiente. El metabolismo se divide en dos categorías. Reacciones catabólicas liberan y acarrean energía; un ejemplo es la degradación de comida en la respiración celular. Las reacciones anabólicas, en cambio, usan esta energía liberada para construir componentes de las célula como lo son las proteínas y los ácidos nucleicos.
Las reacciones químicas del metabolismo son organizadas en rutas metabólicas, donde un químico es transformado en otro por una secuencia de enzimas. Las enzimas son cruciales en el metabolismo porque permiten a las células transformar reacciones termodinámicas deseadas pero deseadas en favorables. Las enzimas también permiten la regulización de rutas metabólicas en respuesta al ambiente de la célula, o señales a otras células.
El metabolismo de un organismo determina que sustancias encontrará nutritivas y cuales encontrará venenosas. Por ejemplo, algunas procariotas usan sulfuro de hidrógeno como nutriente, pero este gas es venenoso para animales.[1]. La velocidad del metabolismo, el rango metabólico, también influye en cuánto alimento el organismo va a requerir.
Una característica del metabolismo es la similitud de las rutas metabólicas básicas entre varias especies diferentes. Por ejemplo, los pasos químicos como el ciclo de Krebs es universal en todas las células vivas y diverso como la bacteria unicelular Escherichia coli y muchos organismos pluricelulares como el elefante.[2]. Esta estructura metabólica compartida es el resultado de estas rutas altamente efectivas, y su aparición temprana en la historia evolutiva.[3][4]
Bioquímicos principales
La mayor parte de las estructuras que componen a los animales, plantas y microbios son compuestos por tres moléculas básicsa: aminoácidos, hidratos de carbono y lípidos (también denominados grasas). Como estas moléculas son vitales para la vida, el metabolismo se centra en sintetizar estas moléculas, en la contrucción de células y tejidos, o en degradarlas y usarlas como recurso de energía, en la digestión y el uso del alimento. Muchos bioquímicos importantes pueden ser juntados para crear polímeros como el ADN (ácido desoxirribonucleico) y proteínas. Estas macromoléculas son esenciales en los organismos vivos. Polímeros conocidos se listan en la siguiente tabla:
| Tipo de molécula | Nombre de forma de monómero | Nombre de formas de polímero |
|---|---|---|
| Aminoácidos | Aminoácidos | Proteínas |
| Carbohidratos | Monosacáridos | Polisacáridos |
| Ácidos nucleicos | Nucleótidos | Polinucleótidos |
Aminoácidos y proteínas
Las proteínas están compuestas por los aminoácidos, arreglados en una cadena lineal y unidos por enlaces peptídicos. Muchas proteínas son las enzimas que catabolizan las reacciones químicas en el metabolismo. Otras proteínas tienen funciones estructurales o mecánicas, como las proteínas del citoesqueleto que forman un sistema de andamio para mantener la forma de la célula.[5][6]. Las proteínas también son partícipes en la comunicación celular, respuesta inmune, adhesión celular y el ciclo celular.[7]
Lípidos
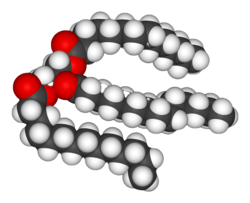
Los lípidos son los bioquímicos más diversos. Sus usos estructurales básicos son ser parte de la membrana biológica como una membrana celular, o como recurso de energía.[7] Los lípidos son denominados hidrófobos, como moléculas biológicas que se disuelven en un solvente orgánico como la bencina o cloroformo.[8]. Las grasas son un grupo de compuestos que incluyen ácidos grasos y glicerol; una molécula de glicerol junto a a tres ácidos grasos éster es un triglicérido.[9] Hay variaciones en esta estrucutra básica, e incluyen columnas como grupos hidrófilos, que incluyen grupos fosfato en fosfolípidos. Esteroides como el colesterol son otra clase mayor de lípidos sintetizados en las células.[10]
Carbohidratos

Los carbohidratos son aldehídos o cetonas con grupos hidroxilo que pueden existir como cadenas o anillos. Los carbohidratos son las moléculas biológicas más abundantes, y tienen varios roles; algunos son el almacenamiento de energía (almidón y glucógeno) y componentes estructurales (celulosa en las plantas, quitina en los animales). [7] Los carbohidratos básicos son llamados monosacáridos e incluyen galactosa, fructosa, y más importante glucosa. Los monosacáridos se pueden sintetizar y formar polisacáridos.[11]
Nucleótidos
Los polímeros ADN y ARN son cadenas de los nucleótidos. Estas moléculas son críticas para el almacenamiento y uso de información genética por el proceso de transcripción y biosíntesis de proteínas[7]. Esta información es protegida por mecanismo de reparación del ADN y propagada por replicación del ADN. Algunos virus tienen un genoma de ARN, por ejemplo el HIV, y utilizan retrotranscripción para crear ADN a partir de su genoma viral de ARN.[12]; estos virus son llamados retrovirus. El ARN en ribozimas como los ribosomas es similar a las enzimas y puede catabolizar reacciones químicas. Nucleósidos individuales son hechos al unir bases nitrogenadas con ribosa. Estas bases son anillos que contienen nitrógeno, clasificado como purina y pirimidinas. Los nucleótidos también actúan como coenzimas en reacciones metabólicas de transferencia en grupo.[13]
Coenzimas
El metabolismo conlleva un gran arraigo de reacciones químicas, pero muchas por mayoría caen en algunos tipos básicos de reacción de transferencia en grupo.[14] Esta química común permite a células utilizar los intermedios metabólicos para logra grupos químicos entre diferentes reacciones.[13] Este grupo de transferencia intermediaria son las coenzimas. Cada clase de reacción de grupo es llevada a cabo por una coenzima particular, que es un sustrato para un grupo de enzimas que lo producen, y un grupo de enzimas que lo consumen. Estas coenzimas son, por ende, continuamente hechas, consumidas y luego recicladas.[15]
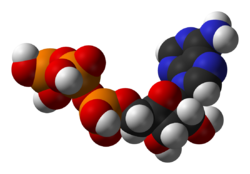
La coenzima más central es adenosín trifosfato (ATP). Este nucleótido es usado para transferir energía química entre distintas reacciones químicas. Sólo hay una pequeña parte de ATP en las células, pero como es continuamente regenerado, el cuerpo humano usa su propia altura de ATP por día.[15] El ATP actúa como un puente entre el catabolismo y el anabolismo, con reacciones catabólicas que generan ATP y las anabólicas las consumen. También sisrve para trasnportar de grupos fosgato en reacciones de fosforilación.
Una vitamina es un compuesto orgánico necesitado en pequeñas cantidas que no puede ser sintetizado en células. En la nutrición humana, las mayoría de las vitaminas trabajan como coenzimas modificadas; por ejemplo, todas las vitaminas que se disuelven en agua son fosforilatadas o juntadas con nucleótidos cuando son usadas en células.[16]
La nicotinamida adenina dinucleótido (NAD), una derivante de la vitamina B, es una importante coenzima que actúa como aceptador del hidrógeno. Cientos de dehidrogenados remueven electrones de sus sustancias y reducen NAD+ en NADH. Esta forma reducida de coenzima es luego un sustrato para cualquier reductase en la célula que necesite reducir su sus sustancias.[17] El NAD existe en dos formas relacionadas en la célula, NADH y NADPH. El NAD+/NADH es más importante en reacciones catabólicas, mientras que el NADP+/NADPH es usado en razones anabólicas.
Minerales y cofactores
Elementos inorgánicos juegan un rol crítico en el metabolismo; algunos son abundantes (sodio y potasio, por ejemplo), mientras que otros funcionan en concentraciones momentáneas. Alrededor del 99% de la masa de un mamífero es de los elementos carbono, nitrógeno, calcio, sodio, cloro, potasio, hidrógeno, oxígeno y azufre.[18]. Los compuestos orgánicos (proteínas, lípidos y carbohidratos) contienen, en su mayoría, carbono y nitorógeno, mientras que la mayoría del oxígeno y el hidrógeno está presente en el agua.[18]
Los elementos inorgánicos actúan como electrolitos iónicos. Lo más importantes iones son sodio, potasio, calcio, magnesio, cloruro y fosfato, y el ion orgánico bicarbonato. La gradiente iónica a lo largo de las membranas de la célula mantienen la presión osmótica y el PH.[19] Los iones son también críticos para nervios y músculos, como el potencial de acción en el tejido son producidos por el intercambio de electrolitos entre el fluido extracelular y el citosol.[20] Los electrolitos entran y salen de la célula a través de proteínas en la membrana plasmática, llamados canales iónicos. Por ejemplo, la contracción muscular depende del movimiento del calcio, sodio y potasio a través de los canales iónicos en la membrana y los túbulos T.[21]
Los metales de transición están presentes en el organismo, con zinc y hierro, que son más abundantes.[22][23] Estos metales son usados en algunas proteínas como cofactores y son esenciales para la actividad de enzimas como catalasa y proteínas transportadoras de oxígeno como la hemoglobina.[24] Estos cofactores están estrechamente ligados a una proteína; aunque los cofacores de enzimas pueden ser modificados durante catálisis, los cofactores siempre vuelven a su estado original antes de que la catálisis tuviera lugar. Los micronutrientes son alcanzados a los organismos por trasportadores ligados a las proteínas como la ferritina cuando no se están usando.[25][26]
Catabolismo
El catabolismo es el conjunto de procesos metabólicos que liberan energía. Estos incluyen [degradación y oxidación de moléculas de alimento, así como reacciones que retienen la energía del Sol. El propósito de estás reacciones catabólicas es proveer energía y componenentes necesitados por reacciones anabólicas. La naturaleza de estas reacciones catabólicas difiere de organismo en organimo. Sin embargo, estas diferentes formas de catabolismo dependen en reacciones de reducción-oxidación que involucran transferencia de electrones de moléculas orgánicas reducidas donantes como las moléculas orgánicas, agua, amoníaco, sulfuro de hidrógeno y iones ferrosos a aceptadores de moléculas como el oxígeno, nitrato o sulfato.[27]
En los animales, estas reacciones conllevan moléculas orgánicas complejas que son degradadas en unas más simples, como el dióxido de carbono y H2O. En organismos fotosintéticos como plantas y cianobacteria, estas transferencias de electrones no liberan energía, pero son usadas como un medio para almacenar energía solar.[28]
El conjunto de reacciones catabólicas más común en eanimales puede ser separado en tres etapas distintas. En la primera, moléculas orgánicas grandes como las protínas, polisacáridos o lípidos son digeridos en componentes más pequeño fuera de las células. Luego, estas moléculas pequeñas son llevadas a las células y convertidas en moléculas aún más pequeñas, generalmente acetil CoA, que libera energía. Finlamente, el grupo acetil en la molécula de acteil CoA es oxidada en agua y dióxido de carbono, liberan energía que se retiene al reducir la coenzima nicotinamida adenina dinucleótido (NAD+) en NADH.
Digestión
Macromoléculas como el almidón, celulosa o proteínas no pueden ser tomadas por las células rápidamente, por lo que necesitan que se degraden en unidades más simples antes de usarlas en el metabolismo celular. Muchas enzimas digieren estos polímeros. Estas enzimas incluyen peptidasa que digiere proteínas en aminoácidos; también incluyen glicosida hidrolasada que digieren polisacáridos en monosacáridos.
Microbios simplemente segregan enzimas degestivas en sus alrededores[29][30] mientras que los animales solo segregan estas enzimas de células especializadas en sus aparatos digestivos.[31] Los aminoácidos liberados por estas enzimas extracelulares son absorbidas por las células por proteínas específicas de transporte.[32][33]
Referencias
- ↑ Friedrich C (1998). «Physiology and genetics of sulfur-oxidizing bacteria». Adv Microb Physiol 39: 235-89. PMID 9328649.
- ↑ Smith E, Morowitz H (2004). «Universality in intermediary metabolism». Proc Natl Acad Sci U S A 101 (36): 13168-73. PMID 15340153.
- ↑ Ebenhöh O, Heinrich R (2001). «Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems». Bull Math Biol 63 (1): 21-55. PMID 11146883.
- ↑ Meléndez-Hevia E, Waddell T, Cascante M (1996). «The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution». J Mol Evol 43 (3): 293-303. PMID 8703096.
- ↑ Michie K, Löwe J (2006). «Dynamic filaments of the bacterial cytoskeleton». Annu Rev Biochem 75: 467-92. PMID 16756499.
- ↑ Educa.rcanaria.es
- ↑ a b c d Nelson, David L.; Michael M. Cox (2005). Lehninger Principles of Biochemistry. New York: W. H. Freeman and company. p. 841. ISBN 0-7167-4339-6.
- ↑ Fahy E, Subramaniam S, Brown H, Glass C, Merrill A, Murphy R, Raetz C, Russell D, Seyama Y, Shaw W, Shimizu T, Spener F, van Meer G, VanNieuwenhze M, White S, Witztum J, Dennis E (2005). «A comprehensive classification system for lipids». J Lipid Res 46 (5): 839-61. PMID 15722563.
- ↑ «Nomenclature of Lipids». IUPAC-IUB Commission on Biochemical Nomenclature (CBN). Consultado el 8 de marzo de 2007.
- ↑ Hegardt F (1999). «Mitochondrial 3-hydroxy-3-methylglutaryl-CoA synthase: a control enzyme in ketogenesis». Biochem J. 338 (Pt 3): 569-82. PMID 10051425.
- ↑ Raman R, Raguram S, Venkataraman G, Paulson J, Sasisekharan R (2005). «Glycomics: an integrated systems approach to structure-function relationships of glycans». Nat Methods 2 (11): 817-24. PMID 16278650.
- ↑ Sierra S, Kupfer B, Kaiser R (2005). «Basics of the virology of HIV-1 and its replication». J Clin Virol 34 (4): 233-44. PMID 16198625.
- ↑ a b Wimmer M, Rose I (1978). «Mechanisms of enzyme-catalyzed group transfer reactions». Annu Rev Biochem 47: 1031-78. PMID 354490.
- ↑ Mitchell P (1979). «The Ninth Sir Hans Krebs Lecture. Compartmentation and communication in living systems. Ligand conduction: a general catalytic principle in chemical, osmotic and chemiosmotic reaction systems». Eur J Biochem 95 (1): 1-20. PMID 378655.
- ↑ a b Dimroth P, von Ballmoos C, Meier T (2006). «Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series». EMBO Rep 7 (3): 276-82. PMID 16607397.
- ↑ Plantilla:Ref-artículo
- ↑ Pollak N, Dölle C, Ziegler M (2007). «The power to reduce: pyridine nucleotides--small molecules with a multitude of functions». Biochem J 402 (2): 205-18. PMID 17295611.
- ↑ a b Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R (1991). «Chemical and elemental analysis of humans in vivo using improved body composition models». Am J Physiol 261 (2 Pt 1): E190-8. PMID 1872381.
- ↑ Sychrová H (2004). «Yeast as a model organism to study transport and homeostasis of alkali metal cations». Physiol Res. 53 Suppl 1: S91-8. PMID 15119939.
- ↑ Levitan I (1988). «Modulation of ion channels in neurons and other cells». Annu Rev Neurosci 11: 119-36. PMID 2452594.
- ↑ Dulhunty A (2006). «Excitation-contraction coupling from the 1950s into the new millennium». Clin Exp Pharmacol Physiol 33 (9): 763-72. PMID 16922804.
- ↑ Mahan D, Shields R (1998). «Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight». J Anim Sci 76 (2): 506-12. PMID 9498359.
- ↑ Husted S, Mikkelsen B, Jensen J, Nielsen N (2004). «Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics». Anal Bioanal Chem 378 (1): 171-82. PMID 14551660.
- ↑ Finney L, O'Halloran T (2003). «Transition metal speciation in the cell: insights from the chemistry of metal ion receptors». Science 300 (5621): 931-6. PMID 12738850.
- ↑ Cousins R, Liuzzi J, Lichten L (2006). «Mammalian zinc transport, trafficking, and signals». J Biol Chem 281 (34): 24085-9. PMID 16793761.
- ↑ Dunn L, Rahmanto Y, Richardson D (2007). «Iron uptake and metabolism in the new millennium». Trends Cell Biol 17 (2): 93-100. PMID 17194590.
- ↑ Nealson K, Conrad P (1999). «Life: past, present and future». Philos Trans R Soc Lond B Biol Sci 354 (1392): 1923-39. PMID 10670014.
- ↑ Nelson N, Ben-Shem A (2004). «The complex architecture of oxygenic photosynthesis». Nat Rev Mol Cell Biol 5 (12): 971-82. PMID 15573135.
- ↑ Häse C, Finkelstein R (1993). «Bacterial extracellular zinc-containing metalloproteases». Microbiol Rev 57 (4): 823-37. PMID 8302217.
- ↑ Gupta R, Gupta N, Rathi P (2004). «Bacterial lipases: an overview of production, purification and biochemical properties». Appl Microbiol Biotechnol 64 (6): 763-81. PMID 14966663.
- ↑ Hoyle T (1997). «The digestive system: linking theory and practice». Br J Nurs 6 (22): 1285-91. PMID 9470654.
- ↑ Souba W, Pacitti A (1992). «How amino acids get into cells: mechanisms, models, menus, and mediators». JPEN J Parenter Enteral Nutr 16 (6): 569-78. PMID 1494216.
- ↑ Barrett M, Walmsley A, Gould G (1999). «Structure and function of facilitative sugar transporters». Curr Opin Cell Biol 11 (4): 496-502. PMID 10449337.
