Ácido sulfhídrico
| Ácido sulfhídrico | ||
|---|---|---|
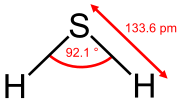 Geometría del sulfuro de hidrógeno. | ||
 | ||
| Nombre IUPAC | ||
| Sulfuro de hidrógeno | ||
| General | ||
| Otros nombres | Ácido sulfhídrico (aq) | |
| Fórmula semidesarrollada | HSH | |
| Fórmula estructural |
 | |
| Fórmula molecular | H2S | |
| Identificadores | ||
| Número CAS | [7783-06-4][1] | |
| Número RTECS | MX1225000 | |
| ChEBI | 16136 | |
| ChEMBL | CHEMBL1200739 | |
| ChemSpider | 391 | |
| PubChem | 18779926 402, 18779926 | |
| UNII | YY9FVM7NSN | |
| KEGG | C00283 | |
| Propiedades físicas | ||
| Apariencia | gas incoloro | |
| Masa molar | 341 g/mol | |
| Punto de fusión | 187 K (−86 °C) | |
| Punto de ebullición | 213 K (−60 °C) | |
| Propiedades químicas | ||
| Acidez | 6,89 pKa | |
| Solubilidad en agua | 0,33 | |
| Momento dipolar | 0,97 D | |
| Termoquímica | ||
| ΔfH0gas | -20,5 kJ/mol | |
| S0gas, 1 bar | 205,77 J·mol–1·K | |
| Peligrosidad | ||
| Punto de inflamabilidad | 190,6 K (−83 °C) | |
| NFPA 704 |
4
4
0
| |
| Frases R | R12, R26, R50 | |
| Frases S | (S1/2), S9, S16, S36, S38, S45, S61 | |
| Riesgos | ||
| Ingestión | puede causar náuseas y vómitos. | |
| Inhalación | peligroso; puede ser fatal. | |
| Piel | puede causar picazón y dolor. | |
| Ojos | puede causar quemaduras. | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido sulfhídrico en disolución acuosa (H2S (aq)), es un hidrácido de fórmula H2S. Este gas, más pesado que el aire, es inflamable, incoloro, tóxico, odorífero: su olor es el de materia orgánica en descomposición, similar al olor de los huevos podridos. A pesar de ello, en el organismo humano desempeña funciones esenciales.
En la nomenclatura química la desinencia -uro corresponde a los haluros, es decir, a las sales que no contienen oxígeno. Puesto que sal "es un compuesto iónico formado por un catión distinto de H+ y un anión distinto de OH- u O2-: ácido + base --> sal + agua",[2] la expresión «sulfuro de hidrógeno» resulta extraña, pues implica que el hidrógeno se sustituye a sí mismo.
Para evitar esta incongruencia en su denominación, al H2S se le podría considerar como disolución acuosa (aq en la fórmula), es decir ácido sulfhídrico.
Con bases fuertes genera sales: los sulfuros. Su punto de ebullición es de 212,86 K.
Generalidades
[editar]El ácido sulfhídrico se encuentra de forma natural en petróleo, gas natural, gases emitidos en procesos asociados a fenómenos volcánicos y manantiales de aguas termales.
Se puede generar por descomposición de la materia orgánica existente en condiciones anaerobias (el ácido sulfhídrico proviene de proteínas que contienen aminoácidos que disponen de azufre, tales como metionina, cistina y cisteína, que son más abundantes en cuernos, uñas y pelo), por la acción de bacterias también en condiciones anaerobias que reducen los sulfatos presentes en el agua, por contacto de un sulfuro o un sulfhídrato con un ácido, con agua ácida o incluso neutra, o por combustión de un hidrocarburo o hidrógeno en contacto con azufre.
Puede existir en aguas pantanosas, lagunas o aguas estancadas, desagües, estanques de harina o de aceite de pescado, fosas de purines, tolvas para despojo de desechos orgánicos (carne, etc.), decantadores, depósitos y balsas de estaciones depuradoras de aguas residuales (tanto biológicas como físico-químicas), lugares donde se trabaja con sulfuros o sulfhidratos, refinerías de petróleo, sótanos con aguas encharcadas o restos de materiales biológicos, instalaciones de industrias donde se trabaja con compuestos azufrados, bodegas de los barcos pesqueros y redes de alcantarillado.
El ácido sulfhídrico (H2S) es un gas inflamable, incoloro, de olor característico a huevos podridos, perceptible en contenidos muy bajos. Este olor proviene de H2S generado por descomposición bacteriana de proteínas que contienen azufre.[2] Se lo conoce comúnmente como ácido hidrosulfúrico o gas de alcantarilla. Es uno de los compuestos destacados como causantes de molestias por malos olores.
La presencia de ácido sulfhídrico da lugar a efectos perjudiciales como olores molestos y riesgos para la salud debido a la alta toxicidad del ácido sulfhídrico. Es habitual que obreros del sector portuario se vean afectados, con resultados fatales, cuando entran en bodegas que han transportado productos derivados de la pesca.
Se han llegado a producir muertes en lagos o lagunas estancadas cuando el ácido sulfhídrico borbota desde las profundidades, en que se origina (por cualquiera de los fenómenos mencionados anteriormente, de origen natural, por descomposición de materia orgánica o por cualquier otra causa), y alcanza a personas en la superficie. Como este ácido es más denso que el aire se generan fraccionamientos por diferencias de densidad, quedando el ácido sulfhídrico sobre la superficie del agua, que desplaza el aire hacia capas más altas.
Por esto se han desarrollado diversos procesos de desodorización que lo eliminan de corrientes contaminadas. Ejemplos: los tratamiento de gas con aminas en la industria y la utilización de nitrato de calcio en aguas residuales.
El ácido sulfhídrico es extremadamente nocivo para la salud. Bastan 20-50 partes por millón (ppm) en el aire para causar un malestar agudo que conlleva a la asfixia y a la muerte por sobreexposición. Por alto grado de toxicidad se le compara con el ácido cianhídrico (HCN), que ha sido el gas usado habitualmente en la pena capital mediante cámara de gas.
Síntesis
[editar]En el laboratorio, el sulfhídrico se puede generar convenientemente por reacción de ácido clorhídrico (HCl) con sulfuro ferroso (FeS). Otro método consiste en calentamiento de una mezcla de parafina con azufre (S) elemental.
En la industria, el sulfhídrico es un subproducto de la limpieza del gas natural o de biogás, en los cuales suele existir con contenidos de hasta 10 %.
Aplicaciones
[editar]Tradicionalmente el ácido sulfhídrico se ha empleado en analítica cualitativa, en la marcha catiónica para precipitar los cationes de metales pesados del grupo II de la marcha analítica, que luego se separan por otros métodos. Los precipitados amorfos pueden ser negros (en su mayoría) o blancos.
Una sal conjugada, el sulfuro de sodio (Na2S), se usa como envejecedor (simulación de antigüedad) de bronces (candados, orfebrerías). También el Na2S se utiliza por ejemplo en preparación de cuero (curtiduría).
En estudios recientes se ha conseguido inducir la hibernación en ratones aplicando sulfhídrico.
El ácido sulfhídrico es responsable del ennegrecimiento de algunas pinturas basadas en carbonato de plomo, por formación de sulfuro plumboso (sulfuro de plomo II), (PbS), de color negro. En algunos casos esto se puede remediar mediante aplicación de peróxido de hidrógeno (agua oxigenada): (H2O2), que oxida el PbS a sulfato de plomo (II) (PbSO4), de color blanco. Es compuesto de partida en algunas síntesis orgánicas.
Recientes estudios parecen demostrar que si bien en determinadas dosis, disuelto en agua, el ácido sulfhídrico es venenoso para animales y plantas, en pequeñas dosis (1 parte por 1000 millones) puede incrementar la velocidad de crecimiento de las mismas. Así lo afirma un estudio de los profesores Fredeirck D. Dooley, Suven p. Nair y Peter D. Ward de la Universidad de Washington.[cita requerida]
Analítica
[editar]El ácido sulfhídrico se detecta comúnmente por su mal olor, a huevos podridos. Químicamente se manifiesta por surgimiento de una mancha negra de PbS en un papel húmedo impregnado con acetato de plomo: Pb(CH3COO)2. Ocurre la reacción siguiente:
Fuentes
[editar]Este ácido es común encontrarlo en:
- Cámaras confinadas de aguas servidas.
- Estanques de almacenamiento de aceite de pescado.
- Sentinas de buques pesqueros.
- Cueros tratados y degradados en curtiduría.
- Plantas de galvanotecnia.
- Degradación de reactivos de flotación a base de sulfuros usados en minería.
- Cámaras de aguas de lavadero de pesquerías.
- Aguas estancadas o con flujo laminar de marismas, cenotes y lagunas de pantano con procesos de putrefacción en el fondo.
- Ciertas regiones de las profundidades marinas donde existen fuentes volcánicas subacuáticas, en las cuales hay géiseres que emanan materias sulfuradas que se combinan con el ácido carbónico (por densidad, la parte sulfurada se va al fondo).
- Estaciones depuradoras de aguas residuales.
Toxicidad
[editar]La toxicidad del ácido sulfhídrico es elevada, pudiendo llegar a provocar la muerte en el humano a concentraciones en el ambiente muy reducidas, del mismo orden de las del ácido cianhídrico (usado en las ejecuciones con cámara de gas en Estados Unidos), o mucho más bajas que las del monóxido de carbono para provocar la muerte (que es origen de numerosas intoxicaciones mortales con calefactores por combustión en lugares mal ventilados). Tan solo teniendo en cuenta que existe una mucho mayor probabilidad de exposición al ácido sulfhídrico que al ácido cianhídrico, el índice de mortalidad por ácido sulfhídrico es inferior al del ácido cianhídrico, probablemente porque está provisto de una "propiedad de aviso", que es su fuerte olor.
No obstante, el conocimiento de que presenta un olor maloliente incluso a una concentración muy por debajo de la que provoca la muerte, puede dar lugar a situaciones de falsa seguridad, ya que cuando se incrementa la concentración del gas, el sentido del olfato rápidamente se satura o se narcotiza, desapareciendo el olor, por lo que a las víctimas potenciales de la exposición les puede pasar desapercibida su presencia en el aire hasta que se manifiestan sus efectos, posiblemente mortales.
Así, basta con 2 ppm en el aire para percibirlo olfatívamente, cuando se considera que es mortal a partir de las 20 o 25 ppm en aire. Pero a partir de 5 ppm, provoca un efecto narcotizante en las células receptoras del olfato, por lo que las personas afectadas ya no perciben su hedor.
Como la densidad del sulfhídrico es mayor que la del aire, suele acumularse en lugares bajos y mal ventilados, tales como pozos, redes de alcantarillado, etcétera, que por otra parte son lugares también proclives a acumular materia orgánica que por descomposición generan habitualmente este gas, por lo que son lugares donde habitualmente se producen víctimas. En estos lugares, denominados técnicamente "espacios confinados", cuando se produce un accidente por intoxicación suele acabar afectando sucesivamente a varias personas (una primera persona es afectada, cayendo inconsciente, y después resultan afectados también todos los demás que, sin el equipo de protección respiratoria adecuado, acuden a su rescate) con resultados habitualmente fatales para todos ellos.
No existe filtro adecuado para este gas, por lo que la protección respiratoria debe hacerse con un equipo provisto de suministro de aire independiente del ambiente contaminado con este gas (equipo de respiración autónoma, semiautónoma o asistido).
Igual que sucede con las sales del ácido cianhídrico, los cianuros, las sales del ácido sulfhídrico, los sulfuros, han de manejarse con sumo cuidado, evitando que puedan entrar en contacto con ácidos o disoluciones ácidas (incluso ligeramente ácidas o neutras), que darían lugar a la emanación del tóxico ácido sulfhídrico. El volcado manual de un saco de sulfuro de sodio sobre una disolución ligeramente ácida provoca la generación súbita de una nube de ácido sulfhídrico que rápidamente cubre la zona de respiración de la persona que realiza la operación, provocándole la muerte.
El sulfhídrico parece actuar sobre todo en los centros metálicos de las enzimas, bloqueándolas, de forma que se impide su funcionamiento. Para tratamiento se recomienda llevar al afectado lo más rápidamente posible al aire fresco y aplicar oxígeno puro.
Además, el ion sulfuro S2- se combina con la hemoglobina del mismo modo que el oxígeno, y acelera la asfixia del organismo.
La exposición a niveles bajos de ácido sulfhídrico puede producir irritación de ojos, nariz o garganta. También es factible que provoque dificultades respiratorias a personas asmáticas. Exposiciones breves a contenidos altos (mayores de 500 ppm) de ácido sulfhídrico pueden causar pérdida del conocimiento y hasta la muerte.
En la mayoría de los casos, quienes pierden el conocimiento parecen recuperarse sin padecer otros efectos. Sin embargo, algunas personas parecen sufrir efectos permanentes o a largo plazo, tales como dolor de cabeza, escasa capacidad de concentración, mala memoria y mala función motora.
No se han detectado efectos en la salud en personas expuestas al ácido sulfhídrico en los contenidos comúnmente existentes en el ambiente (0,00011-0,00033 ppm). Los científicos no tienen información por la cual se demuestre fallecimientos de personas intoxicadas por ingerir ácido sulfhídrico.
Los científicos poseen poca información acerca de qué sucede cuando la piel de una persona se expone al ácido sulfhídrico. Sin embargo, se sabe que es necesario ser precavidos con el ácido sulfhídrico líquido comprimido, ya que puede causar quemaduras de la piel por congelación.
A pesar de la alta toxicidad del gas sulfhídrico en los mamíferos, hay microorganismos que tienen una capacidad de adaptación evolutiva que toleran elevados contenidos de este gas, o incluso se alimentan de él. Hay teorías en las que se relaciona la metabolización del gas sulfhídrico —como existe por ejemplo cerca de fuentes volcánicas subacuáticas— con el desarrollo inicial de la vida en la Tierra con unas condiciones ambientales muy afectadas por las numerosas erupciones volcánicas que cabría esperar en un planeta en proceso de formación.
En el año 2012 se supo de al menos dos casos en los que varias personas parecen haberse intoxicado con ácido sulfhídrico. En uno de ambos casos los resultados fueron fatales.[3][4][5]
Fuente
[editar]- Rui Wang, «La función dual del sulfuro de hidrógeno», Investigación y Ciencia, 404, mayo de 2010, págs. 56-61.
Referencias
[editar]- ↑ [7783-06-4 Número CAS]
- ↑ a b Química. Raymond Chang. McGraw-Hill, 2003.
- ↑ Fallecen seis obreros en Ixtaczoquitlán, Veracruz, envenenadas con ácido sulfhídrico Nota en la sección Estados, p. 38 de La Jornada, viernes 13 de julio de 2012 (consultado el 14 de julio de 2012)
- ↑ Intoxicación con ácido sulfhídrico de empleados del Instituto de la Propiedad en Honduras (periódico La Tribuna (consultado 14 de julio de 2012
- ↑ Intoxicación de al menos 21 empleados con gas metano y/o ácido sulfhídrico (sulfuro de hidrógeno) (consultado el sábado 14 de julio de 2012
Enlaces externos
[editar]- ATSDR en español - Resumen de Salud Pública: Ácido sulfhídrico.
- - Sensores H2S.
- ATSDR en español - ToxFAQs™: Ácido sulfhídrico.
- ATSDR en español - Resumen de Salud Pública: Ácido sulfhídrico.
- Instituto Nacional de Seguridad e Higiene en el Trabajo de España - Ficha internacional de seguridad química del sulfuro de hidrógeno
- http://radio.uchile.cl/2015/03/04/dos-fallecidos-en-clinica-de-vitacura-por-explosion-de-gas

