Furano
| Furano | |
|---|---|

| |
| Nombre IUPAC | Furano (u oxol) |
| Otros nombres | Furfurano, óxido de divinileno |
| Fórmula empírica | C4H4O |
| Masa molecular | 68,08 g/mol |
| Estado físico/Color | Líquido/Incoloro a marranoso |
| Número CAS | 110-00-9 |
| Propiedades | |
| Densidad | 0,94 g/cm³ a 20 °C |
| Punto de fusión | –85,6 °C (187,6 K) |
| Punto de ebullición | 31,3 °C (304,4 K) |
| Solubilidad en agua | 10 g/l a 25 °C |
| Información de Seguridad | |
 
| |
| Frases R: R45, R12, R20/22, R38, R48/22, R52/53, R68
Frases S: S53,S45,S61 | |
| Exenciones y Referencias[1][2][3] | |
El furano es un compuesto orgánico heterocíclico aromático de cinco miembros, que incluye un átomo de oxígeno. Es un líquido claro, incoloro, altamente inflamable y muy volátil, con un punto de ebullición cercano al de la temperatura ambiente. Es tóxico y puede ser carcinógeno.
Historia[editar]
El nombre furano viene del latín furfur que significa salvado.[4] El primer derivado del furano fue descrito como ácido 2-furoico, por Carl Wilhelm Scheele en 1780. Otro derivado importante, el furfural fue descrito por Johann Wolfgang Döbereiner en 1831 y caracterizado nueve años después por John Stenhouse. El furano como tal fue preparado por vez primera por Heinrich Limpricht en 1870, aunque en esa ocasión fue denominado tetrafenol.[5][6]
Síntesis[editar]
- Síntesis de Paal-Knorr: Consiste en la deshidratación mediante P2O5 (o P4010) de un compuesto 1,4-dicarbonílico dando lugar al heterociclo furano.

La síntesis de Paal-Knorr se emplea para formar furanos por cierre de un sistema con grupos funcionales 1,4 con oxígeno. Los carbonilos de aldehído o cetona son requeridos para que el sistema sea aromático.
Otros sistemas relacionados se pueden obtener por el mismo principio para obtenerse sistemas furanoides parcial o totalmente insaturados:
- En el caso del tetrahidrofurano, el cierre se lleva a cabo a partir de un 1,4-diol
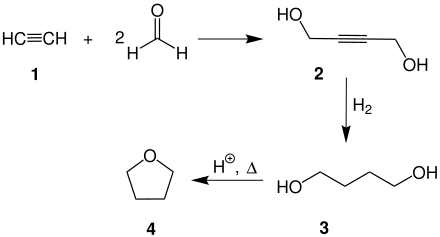
- Cuando los extremos son un alcohol y un carbonilo de cetona o aldehído, se cierra por formación de un lactol. Este es el mecanismo por el cual se forman las furanosas:

Se puede lograr la aromatización del anillo furanoide de una pentofuranosa para formar furfural. Este aldehído puede ser obtenido por la destilación destructiva de la mazorca del maíz en presencia de ácido sulfúrico, en la que se hidrolizan y deshidratan las pentosanas.[7]

El anillo simple de furano puede ser obtenido del furfural por oxidación y descarboxilación del ácido furano-2-carboxílico resultante. Éste es el principal método de preparación industrial del furano.
Las hexosas, sin importar si son furanosas o piranosas, forman el hidroximetilfurfural (HMF) por un procedimeinto análogo:

Estas reacciones son fundamento de la prueba de Seliwanoff, una prueba química que se usa para distinguir aldosas y cetosas.
Este compuesto es precursor del ácido 2,5-furanodicarboxílico (FDCA):

Este compuesto es precursor de diversas materias primas con anillo de furano
![Figure 2: Derivatives of FDCA[8][9]](http://upload.wikimedia.org/wikipedia/commons/thumb/8/80/Conversions_of_FDCA.tif/lossy-page1-450px-Conversions_of_FDCA.tif.jpg)
En una síntesis relacionada, se parte del alcohol maleico con un oxidante, el cual convierte uno de los alcoholes al aldehído correspondiente:

- Si los extremos son un alcohol y un ácido carboxílico, se forma la oxolan-2-ona, conocida también como butanólido o γ-butirolactona:

Algunos butenólidos pueden prepararse por oxidación parcial de un monosacárido adecuado. Por ejemplo, en el caso del ácido ascórbico, el anillo de butenólido se puede obtener de forma sintética por medio del proceso Reichstein, modificado posteriormente por Kurt Heyns.[10]

- Si los extremos son dos ácidos carboxílicos, se forma el anhídrido succínico, el cual es el tautómero ceto más estable del 2,5-dihidroxifurano:

- Otro método de síntesis orgánica es la Síntesis de furanos de Feist–Benary:

- Se pueden obtener furanos a partir de alenilcetonas:

- Otro método para preparar furanos es a partir de aciloínas:

- También se pueden obtener furanos a partir de alquiniloxiranos:

- Para los casos de furanos fusionados con anillos de benceno, consúltese isobenzofurano, benzofurano y dibenzofurano.
Aromaticidad[editar]


El furano es un compuesto aromático que respeta la regla de Hückel. El furano posee seis electrones deslocalizados: cuatro pertenecientes a los dobles enlaces y dos del átomo de oxígeno (uno de los dos pares no enlazados solamente, que se encuentra en un orbital perpendicular al plano del anillo). Cada carbono aporta un electrón, mientras que el oxígeno aporta dos a la nube deslocalizada. Los carbonos son híbridos sp2. El furano resulta entonces con una energía de resonancia de entre 62,3-96,2 kJ/mol. Esta energía es inferior a aquella del benceno, del tiofeno y del pirrol por lo que el furano es menos aromático que éstos. Esta débil aromaticidad explica por qué él mismo actúa como un dieno cíclico en ciertas reacciones de Diels-Alder
El átomo de oxígeno posee un efecto mesómero como donante y un efecto inductivo electroatrayente. La deslocalización del par libre de electrones contribuye al efecto mesómero del oxígeno mientras que la atracción de los electrones de los enlaces C-O hacia el átomo de oxígeno corresponden al efecto inductivo. La naturaleza electroatrayente del oxígeno tiene efectos sobre la distribución electrónica en el ciclo pero este hecho no alcanza para que se contrarreste el efecto mesómero. Por consiguiente, entonces, el oxígeno aporta globalmente una densidad electrónica suplementaria al ciclo. Esta contribución electrónica del oxígeno se traduce por los valores de densidad electrónica superiores a 1 para los carbonos del ciclo. El efecto mesómero donante del oxígeno da origen a una carga positiva sobre el mismo y una carga negativa sobre los carbonos en cuatro de las cinco estructuras resonantes del ciclo.
El oxígeno posee además otro par de electrones que no está deslocalizado. El furano es un compuesto plano e igualmente a sus homólogos (tiofeno y pirrol), es un sistema π excedente debido a la distribución de 6 electrones π deslocalizados en cinco átomos; la densidad electrónica es por lo tanto claramente más importante que en sus análogos del benceno. Por otra parte, contrariamente a los ciclos aromáticos simples de 6 elementos, solo una de sus estructuras de resonancia es neutra; mientras que las otras formas existen en forma de zwitterión. Estas formas cargadas contribuyen minoritariamente al híbrido de resonancia, pero por esto también, la química del furano será en parte aquella la de los compuestos aromáticos y en parte a aquella de los dienos.

Reactividad[editar]
Protonación[editar]
Los anillos de furano funcionan como bases de Brønsted-Lowry.

El furano y sus derivados alquilados son relativamente estables a los ácidos minerales acuosos, aunque el furano se descompone instantáneamente con el ácido sulfúrico concentrado o por ácidos de Lewis tales como el cloruro de aluminio. El furano reacciona lentamente con cloruro de hidrógeno ya sea como ácido acuoso concentrado o en un disolvente orgánico no hidroxílico. Los ácidos minerales acuosos calientes diluidos causan apertura hidrolítica del anillo. En condiciones suaves, en medio acuoso acidificado, el furano hidroliza dando lugar al correspondiente compuesto 1,4-dicarbonílico. Sería la reacción inversa a la de Paal-Knorr.[11][12]

Sustituciones electrofílicas aromáticas[editar]
Debido a la deslocalización del par de electrones del átomo de oxígeno por el anillo, π-excedente, el furano es más reactivo frente a la sustitución electrófila aromática que el benceno. Su reactividad recuerda considerablemente a la de los derivados bencénicos más reactivos, el fenol y la anilina. Puede reaccionar tanto en la posición 2 como en la 3.[13]
Nitración[editar]
La sensibilidad del furano a los ácidos impide el uso de ácido concentrado en mezclas de nitración. La reacción del furano con nitrato de acetilo (producido con anhídrido acético y ácido nítrico) produce aductos no aromáticos, los cuales aromatizan por eliminación del acetato al adicionar una base débil, como piridina.[14][15][16][17][18]

Halogenación[editar]
El furano reacciona vigorosamente con el cloro y el bromo a temperatura ambiente para dar productos polihalogenados, pero no reacciona en absoluto con el yodo. La monocloración se lleva a cabo a –40 °C con cloro. Condiciones más controladas pueden dar 2-bromofurano en un proceso que probablemente procede a través de un 1,4-dibromo-l,4-dihidro-aducto; de hecho, dichas especies se han observado a baja temperatura usando espectroscopía 1H-RMN. La reacción con bromo en dimetilformamida o en dioxano a temperatura ambiente sin problemas produce 2-bromo y 2,5-dibromofuranos.[19][20][21][22][23][24][25][26][27][28][29]

Se ha reportado la monoyodación de furanos con yodo en zeolita.[30]

Sulfonación[editar]
El furano y sus derivados alquilados simples se descomponen con los reactivos ácidos fuertes utilizados para la sulfonación de benceno, pero puede utilizarse un complejo formado con piridina y trióxido de azufre. La disustitución de furano se observa incluso en a temperatura ambiente.[31]

Se pueden formar furilbencensulfonas con ácidos arilsulfónicos:

Alquilación de Friedel-Crafts[editar]
La alquilación de Friedel-Crafts tradicional no es generalmente factible en la serie del furano debido en parte a que el catalizador produce polimerización y en parte porque se producen productos polialquilados. Las alquilaciones se llevan a cabo por otros métodos.
Formilación y acilación[editar]
Los furanos se pueden formilar por las técnicas utilizadas para fenoles, tales como la reacción de Vilsmeier-Haack y la reacción de Reimer–Tiemann.[32]

Los anhídridos y halogenuros de ácidos carboxílicos normalmente requieren la presencia de un ácido de Lewis para acilar un anillo aromático. El más utilizado para anillos de furano es el trifluoruro de boro. El anhídrido trifluoroacético reacciona sin requerir el ácido de Lewis.[33][34]

Aminometilación[editar]
Los furanos proceden con la reacción de Mannich:[35]

Metalaciones[editar]
Las metalaciones (Reacciones donde el furano forma un anión y se une con un metal) proceden mediante distintos mecanismos. A continuación se enunciarán los más comunes:
Litiación[editar]
La litiación con alquilitios procede selectivamente en una posición. La preferencia por una desprotonación está bien establecida por la demostración de que el 3-litiofurano es producido a partir del 3-bromofurano por intercambio metal/halógeno a –78 °C, se equilibra a la especie más estable, 2-litiofurano, si la temperatura aumenta a > –40 °C. Condiciones más vigorosas llevan al derivado 1,2 dilitiado:[36] [37]

Reactivo de Grignard[editar]
Los furanos forman el reactivo de Grignard bajo el mismo mecanismo de los halogenuros de alquilo y arilo:[38]

Compuestos con zinc[editar]
Los furanos forman organozincs con zinc metálico y un bromofurano:[39]

Mercuriación[editar]
Se pueden obtener 2-mercurofuranos por reacciones con furanos o sales carboxílicas en presencia de cloruro mercúrico:[40]

Sililación[editar]
Se obtienen furanos sililados a partir de los organolitios correspondientes y halogenuros de alquilsilicio:[41]

Estannación[editar]
Los furilestaños se pueden preparar con un furilitio y una sal de estaño:[42]

Reacciones nucleofílicas con metalofuranos[editar]
Muchos metalofuranos funcionan como nucleófilos para llevar a cabo condensaciones y alquilaciones alternativas a la reacción de Friedel-Crafts:[43][44]

Acoplamientos con metales[editar]
El furano puede alquilarse por acoplamientos de Heck, Suzuki y Stille.[45][46][47][48]

Oxidaciones y reducciones[editar]
La hidrogenación con níquel Raney produce el tetrahidrofurano correspondiente. La reducción con el método de Birch produce 2,5-dihidrofuranos:[49]

La reacción de furano con carboxilatos de plomo (IV) producen 2,5-diaciloxi-2,5-dihidrofuranos. Muchos oxidantes destruyen el anillo formando 1,4-dionas Δ2-insaturadas en los isómeros E o Z. Para este propósito se utilizan reactivos tales como bromo en acetona acuosa, ácido metacloroperbenzoico, o hipoclorito de sodio.[50][51]

Los furanos pueden presentar reacciones de cicloadición de oxígeno singulete.[52]

La ozonólisis puede producir aldehídos o cetales de acuerdo al patrón de oxidación.[53]

Reacción de Achmatowicz[editar]
- Reacción de Achmatowicz donde el furano se convierte en un dihidropirano.[54]
Reacciones pericíclicas[editar]
- El furano tiene carácter de dieno en la reacción de Diels-Alder, reaccionando con dienófilos pobres en electrones.[55]

- El furano en presencia de luz puede producir fotociclodímeros en cicloadiciones [2+2]. Un ejemplo es la Reacción de Paterno-Büchi:[56]

Reacciones de derivados[editar]
- Los carbonos saturados de grupos alquilo conectados directamente al anillo de furano lo activan por hiperconjugación.
- Los grupos carbonílicos y grupos nitro desactivan el anillo de furano.
- Los carbonos conectados con halógenos pueden dar reacciones SNA.
- Los alquil litios reemplazan el halógeno por un carbanión con el catión litio como contraión.
- Para la reactividad de los anillos de furano fusionados, consúltese isobenzofurano y benzofurano.
Aplicaciones[editar]
Se usa principalmente como intermedio en la producción industrial de tetrahidrofurano.
Se utiliza en la producción de lacas, como disolvente para resinas y en la síntesis de productos químicos para la agricultura (insecticidas), estabilizantes y productos farmacéuticos (química fina).
Es útil también para sintetizar nitrofuranos, un grupo de fármacos con actividad antibacteriana, antituberculosa e incluso antitumoral.
Presencia en la naturaleza[editar]
El anillo de furano se forma en diversos compuestos de diferente naturaleza biosintética.
- Furanos que provienen de monosacáridos:
Estos furanos se producen biosintéticamente por deshidratación natural de pentosas y hexosas. El furfural se encuentra presente naturalmente en los volátiles de frutas y verduras. El ácido osbéckico es un componente de la zanahoria (Daucus carota).[57] Phallus indusiatus, un hongo de Australia, contiene hidroximetilfurfural en su cuerpo fructífero:

|
 |
 |
| Ácido osbéckico | Furfural | Hidroximetilfurfural |
- Furanos que provienen de ácidos grasos
La wierona y el óxido de carlina son fitoalexinas de la haba y el cardo dorado[58][59]

|
 |
| Wierona | Óxido carlina |
Los ácidos (5-alquil-2-furil)alcanoicos (F-ácidos grasos) son derivados tri-o tetrasustituidos del furano que provienen de una oxidación por acción de las lipooxigenasas (LOX o LO) en ácidos grasos insaturados.

Los F-ácidos son generados en grandes cantidades en las algas, pero son también producidos por las plantas y microorganismos. Los peces y los mamíferos marinos consumen F-ácidos en su alimentación y los incorporan en fosfolípidos y ésteres de colesterol.

Los F-ácidos se catabolizan a ácidos dibásicos (ácidos urofuránicos), que se excretan en la orina. El precursor biogenético del F-ácido más abundante,el F6, es el ácido linoleico. La capacidad de captación de radicales de F-ácidos pueden contribuir a las propiedades protectoras de las dietas de pescado o sus aceites frente a la mortalidad por enfermedades del corazón.[60]

Furanos que provienen de terpenos
Muchos mono- y sesquiterpenos lineales forman anillos de furano por oxidación.
| Nombre | Estructura | Fuentes naturales y actividad biológica |
| Rosefurano |  |
Constituyente menor del aroma de la rosa (Rosa damascena).[61] Es una feromona sexual de los ácaros del género Caloglyphus.[62] |
| α-Clausenano |  |
Presente en los aceites esenciales de Clausena.[63] |
| Elsholtzidiol |  |
Presente en el aceite esencial de Elsholtzia densa.[64] |
| Lepalona |  |
|
| Egomacetona |  |
Constituyente de Perilla frutescens ( albahaca japonesa).[65] |
| Perilleno |  |
Encontrado en los volátiles de Pleurotus ostreatus.[66] |
| Merrekentrona D |  |
Aislada de las raíces y los injertos de Merremia kentrokaulus.[67] |
| Miomontanona |  |
Aislado de Myoporum montanum.[68] |
| Dendrolasina | 
|
Feromona sexual de varios insectos. Aislada de la hormiga Lasius fuliginosus.[69] |
| Ácido cristático |  |
Aislado del hongo Albatrellus cristatus. Tiene actividad antibiótica sobre bacterias Gram-negativas.[70] |
| Furodendina |  |
Reportada en la esponja Phyllospongia dendyi.[71] |
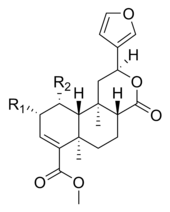
Muchos clerodanos presentan un anillo de furano en sus cadenas laterales, como las salvinorinas:
Otro ejemplo son los limonoides, los cuales presentan en su mayoría un anillo lateral de furano:

El anillo de tetrahidrofurano y el de 2,5-dihidrofurano se encuentran ampliamente distribuidos en la naturaleza en forma de β-lactonas (como en el caso de los ácidos tetrónicos) anhídridos maleicos (como en el caso de los nonádridos) y furanosas.[72]
 |
 |
 |
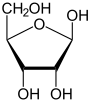 |
| Pulvinona, un ácido tetrónico | Ácido bisoclámico, un nonádrido | Ácido ascórbico, una lactona. | Ribofuranosa, una furanosa |
Véase también[editar]
Referencias[editar]
- ↑ «Fichas internacionales de seguridad química (FISQ)». Archivado desde el original el 18 de diciembre de 2008. Consultado el 31 de enero de 2009.
- ↑ Fichas de datos de seguridad (FDS)
- ↑ Hazardous Substances Data Bank (HSDB)
- ↑ Alexander Senning. Elsevier's Dictionary of Chemoetymology. Elsevier, 2006. ISBN 0-444-52239-5.
- ↑ Limpricht, H. (1870). «Ueber das Tetraphenol C4H4O». Berichte der deutschen chemischen Gesellschaft 3 (1): pp. 90-91. doi:10.1002/cber.18700030129.
- ↑ Rodd, Ernest Harry (1971). Chemistry of Carbon Compounds: A Modern Comprehensive Treatise. Elsevier.
- ↑ "Furan". Org. Synth.; Coll. Vol. 1: 274.
- ↑ Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasLewkowski - ↑ Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasWerpy - ↑ Brönnimann, C. et al. (1994): Direct oxidation of L-sorbose to 2-Keto-L-gulonic acid with molecular oxygen on Platinum- and Palladium-based catalysts. In: J. Catal. 150(1), S. 199–211; doi:10.1006/jcat.1994.1336
- ↑ Carmody, M. P., Cook, M. J., Dassanayake, N. L., Katritzky, A. R., Linda, P. Tack, R. D., Tetrahedron (1976) v. 32 p. 1767
- ↑ Wiersum, U. E. y Wynberg, H., Tetrahedron Lett. (1967) p. 2951.
- ↑ Paquette, L. A. Fundamentos de química heterocíclica 1.ª Ed. Limusa (1990).
- ↑ Michels, J. G. y Hayes, K. J. Am. Chem. Soc. (1958) v. 80 p. 1114.
- ↑ Darling, V. M., S. D., Koster, D. F. y Meyers, C. Y., J. Org.Chem. (1984) v. 49 p. 1636.
- ↑ Clauson-Kaas, N. and Faklstorp, J., Ada Chem. Scand., Ser. B (1947) p. 210
- ↑ Rinkes, I. J., Reel. Tray. Chim. Pays-Bas (1930) v.49 p. 1169.
- ↑ Doddi, G., Stegel, F. y Tanasi, M. T. J. Org. Chem. (1978) v.43 p.4303.
- ↑ Terent'ev, A. P., Belen'kii, L. L. y Yanovskaya, L. A., Zhur. Obschei Khim., 1954, 24,1265 {Chem. Abs., 1955, 49, 12327).
- ↑ Baciocchi, E., Clementi, S. y Sebastiani, G. V., J. Chem. Soc, Chem. Commun. (1975) p. 875.
- ↑ Keegstra, M. A., Klomp, A. J. A. y Brandsma, L., Synth. Commun. (1990) v.20 p.3371.
- ↑ Ross, S. D., Finkelstein, M., and Uebel, J., J. Org. Chem. (1969) v.34 p.1018.
- ↑ Burness, D. M., Org. Synth., Coll. Vol. V, 1973, p. 403.
- ↑ Malanga, C, Mannucci, S. y Lardicci, L., Tetrahedron Lett. (1998) v.39 p.5615
- ↑ Weinberg, N. L. y Weinberg, H. R., Electrochemical oxidation of organic compounds, Chem. Rev. (1968) v.68 p. 449.
- ↑ D'Annibale, A. y Scettri, A., Tetrahedron Lett. (1995) v.36 p.4659.
- ↑ Kress, T. J. y Szymanski, E., J. Heterocycl. Chem. (1983) v.20 p. 1721.
- ↑ Chadwick, D. J., Chambers, J., Meakins, G. D. y Snowden, R. L., J. Chem. Soc,Perkin Trans. 1 (1973) p. 1766.
- ↑ Wang, E. S., Choy, Y. M. y Wong, H. N. C, Tetrahedron (1996) v.52 p.12137.
- ↑ W. Holderich, M. Hesse and F. Naumann Angew. Chem., Int. Ed. Engl.(1988) v.27 p.226.
- ↑ 11. Scully, J. F. y Brown, E. V., J. Org. Chem., 1954, 79, 894.
- ↑ Traynelis, V. J., Miskel, J. J. y Sowa, J. R., J. Org. Chem. (1957) v.22 p. 1269.
- ↑ Ciranni, G. y Clementi, S., Tetrahedron Lett. (1971) p. 3833.
- ↑ Finan, P. A. y Fothergill, G. A., J. Chem. Soc. (1963) p. 2723.
- ↑ Gill, E. W. y Ing, H. R., J. Chem. Soc (1958) p. 4728.
- ↑ Bock, L, Bornowski, H., Ranft, A. y Theis, H., Tetrahedron (1990) v.46 p. 1199.
- ↑ Chadwick, D. J. y Willbe, C, J. Chem. Soc, Perkin Trans. 1 (1977) p. 887.
- ↑ S M. Piller, Knochel P. Synthesis (2011) v.11 p.1751
- ↑ Knochel, Paul; Matthias A. Schade, Sebastian Bernhardt, Georg Manolikakes, Albrecht Metzger, Fabian M. Piller, Christoph J. Rohbogner y Marc Mosrin Beilstein J. Org. Chem. (2011) v.7 p. 1261.
- ↑ Kutney, J. P., Hanssen, H. W. y Nair, G. V., Tetrahedron (1971) v.27 p. 3323.
- ↑ Carpenter, A. J. y Chadwick, D. J. Tetrahedron Lett. (1985) v.26 p. 1111.
- ↑ Bailey, T. R. Synthesis (1991) p. 242.
- ↑ Sotoyama, T., Hara, S., y Suzuki, A., Bull. Chem. Soc Jpn. (1979)
- ↑ Chadwick, D. J., McKnight, M. V. y Ngochindo, R. J. Chem. Soc, Perkin Trans. 1, (1982) p. 1343.
- ↑ Ohta, A., Akita, Y., Ohkuwa, T., Chiba, M., Fukunaga, R., Miyafuji, A., Nakata, T.,Tani, N. y Aoyagi, Y. Heterocycles (1990) v.31 p. 1951.
- ↑ Yang, Y., Synth. Commun. (1989) v.19 p. 1001
- ↑ Fujiwara, Y., Maruyama, O., Yoshidomi, M. y Taniguchi, H., J. Org. Chem. v.46 p. 851.
- ↑ 66. Bach, T. y Kriiger, L., Synlett (1998) p. 1185.
- ↑ Birch, A. J. y Slobbe, J. Tetrahedron Lett. (1975) p. 627.
- ↑ Trost, B. M. y Shi, Z., J. Am. Chem. Soc. (1996) v.118 p. 3037.
- ↑ Adger, B. M., Barrett, C, Brennan, J., McKervey, M. A. y Murray, R. W., J. Chem.Soc. Chem. Commun. (1991) p. 1553.
- ↑ Fering, B. C. «Photo-oxidation of furans.» Reel. Trav. Chim. Pays Bas (1987) v.106 p. 469.
- ↑ Pearlman, Bruce A., Amphlett G. Padilla, John T. Hach, Jeffrey L. Havens, Muniraj D. Pillai. Org. Lett. (2006) V.8(10) p. 2111.
- ↑ Achmatowicz, O.; P. Bukowski, B. Szechner, Z. Zwierzchowska y A. Zamojsk. Tetrahedron (1971) V.27(10) p. 1973.
- ↑ Stockmann, H. J. Org. Chem. (1961) v.26 p. 2025.
- ↑ Nakano, T., Rivas, C, Perez, C, y Tori, K., J. Chem. Soc, Perkin Trans. 1 (1973) p. 2322.
- ↑ Lichtenthaler, Frieder W.; Jürgen Klotz, Katsumi Nakamura. «Daucic acid: Proof of d-lyxo configuration, synthesis of its d-ribo, d-xylo, l-arabino and l-lyxo analogs, and biosynthetic implications.» Tetrahedron: Asymmetry (2003) V. 14(24: pp. 3973–3986.
- ↑ Herrmann, F., Hamoud, R., Sporer, F., Tahrani, A., Wink, M. «Carlina oxide--a natural polyacetylene from Carlina acaulis (Asteraceae) with potent antitrypanosomal and antimicrobial properties.» Planta Med. (2011) v.77(17): pp. 1905-11.
- ↑ Hargreavesa, John A.; John W. Mansfield, David T. Coxonb, Keith R. Priceb. «Wyerone epoxide as a phytoalexin in Vicia faba and its metabolism by Botrytis cinerea and B. fabae in vitro.» Phytochemistry (1976) V.15(7): pp. 1119–1121.
- ↑ Spiteller G. Lipids (2005) v.40 pp. 755–771
- ↑ Gunther Ohloff (1978). «Importance of minor components in flavors and fragrances». Perfumer & Flavorist 3 (1): 11-22.
- ↑ Naoki Mori; Kuwahara, Yasumasa; Kurosa, Kazuyoshi (1998). «Rosefuran: the sex pheromone of an acarid mite, Caloglyphus sp.». Journal of Chemical Ecology 24 (11): 1771-1779.
- ↑ The occurrence of furan derivatives in volatile oils–II α-clausenan and di-α-clausenan B. Sanjiva Rao and K. S. subramaniam. Proceeding mathematical Sciences. (1935) v.2(6):pp. 574-579
- ↑ Structure of elsholtzidiol, a new bisubstituted furan of Elsholtzia densa Benth.V. N. Vashist, C. K. AtalCellular and molecular Life Sciences (1970) V.26(8):pp.817-818
- ↑ Hoppmann, A. et al. Tetrahedron (1978) v.34:p.1723
- ↑ Bioconversion of β-myrcene to perillene by Pleurotus ostreatus.Krings, Ulrich; Hapetta, Darius; Berger, Ralf G. Biocatalysis and Biotransformation (2008) V.26(4):pp. 288-295
- ↑ K. Jenett-Siems, K. Siems, L. Witte and E. Eich, J. Nat. Prod. (2001) v.64:p.1471
- ↑ P. L. Metra and M. D. Sutherland. Tetrahedron Lett. (1983) v.24:p.1749
- ↑ On the biosynthesis of dendrolasin, a body constituent of the ant Lasius fuliginosus Latr. Waldner EE, Schlatter C, Schmid H. Helv Chim Acta. (1969) v.52(1):pp. 15-24.
- ↑ Fürstner A., Gastner T. Org. Lett. (2000) v.2(16): pp 2467–2470
- ↑ R. Kazlauskas, P. T. Murphy, R. J. Wells. Experientia (1980) V.36: pp.814
- ↑ Paul M. Dewick (2009). Medicinal natural products: a biosynthetic approach. John Wiley and Sons. ISBN 9780470741689.
Bibliografía[editar]
- K. Peter C. Vollhardt (1994). Química Orgánica. Barcelona: Ediciones Omega S.A. ISBN 84-282-0882-4.
- W.R. Peterson (1996). Formulación y nomenclatura química orgánica. Barcelona: EDUNSA - Ediciones y distribuciones universitarias S.A. ISBN 84-85257-03-0.
- J. A. Joule, K. Mills y G. F. Smith (1995). «15». Heterocyclic Chemistry (en inglés) (Third edición). Chapman & Hall. pp. 280. ISBN 0 412 41340 X.