Síndrome de Stevens-Johnson
| Síndrome de Stevens-Johnson | ||
|---|---|---|
 El rostro de un hombre afectado por el síndrome de Stevens-Johnson. | ||
| Especialidad | dermatología | |
El síndrome de Stevens-Johnson (SJS) y la necrólisis epidérmica tóxica (NET)[1] son dos formas de una enfermedad de la piel que amenaza a la vida, en la que la muerte celular hace que la epidermis se separe de la dermis. El síndrome se cree que es un complejo de hipersensibilidad que afecta a la piel y a las mucosas. Aunque la mayoría de casos sea idiopática (causa desconocida), la principal de las causas confirmadas es la medicación, seguida por las infecciones y, rara vez, cáncer.
Historia[editar]
El síndrome recibe su nombre por Albert Mason Stevens y Frank Chambliss Johnson, pediatras estadounidenses que en 1922 publicaron conjuntamente una descripción del desorden en el American Journal of Diseases.[2][3][4]
Genética[editar]
Algunas poblaciones estudiadas del oriente asiático (los Han y los tailandeses), el SJS inducido por carbamazepina y fenitoína está muy relacionado con HLA-B*1502 (HLA-B75), un serotipo HLA-B del serotipo más amplio HLA-B15.[5][6][7] Un estudio en Europa sugirió que el marcador génico solo era relevante para los asiáticos orientales.[8][9]
Basándose en las conclusiones de Asia, estudios similares en Europa mostraron que un 61 % de los pacientes con un SJS/TEN inducido por alopurinol presentaban el HLA-B58 (la frecuencia del fenotipo del alelo B*5801 en los europeos es normalmente del 3 %). Un estudio concluyó: “... incluso cuando los alelos HLA-B actúan como fuertes factores de riesgo, en el caso del alopurinol, no son ni suficientes ni necesarios para explicar la enfermedad”.[10]
Causas[editar]
Se cree que el síndrome de Stevens-Johnson proviene de un desorden del sistema inmunológico.[11] La reacción inmune puede ser provocada por infecciones, drogas o medicaciones. En algunos grupos, la reacción a las drogas puede ser agravada por factores genéticos. El síndrome de Stevens-Johnson es idiopático en el 50 %. En el resto de los casos puede ser una reacción alérgica a uno de los siguientes factores:
- Virus (en particular herpes simple, virus de Epstein-Barr, virus de la varicela, Coxsackie, ecovirus, y virus de la poliomielitis)[12]
- Infecciones bacterianas (especialmente por micoplasmas o por Yersinia, brucelosis, difteria, tularemia, tuberculosis e infecciones por protozoos)[12]
- Medicamentos (sobre todo sulfonamidas, oxicames, penicilinas, cefalosporinas, macrolidos, triazoles, anticonvulsivantes y salicilatos)[12]
- Vacunas (difteria, tifus, BCG, vacuna oral de la polio)[12]
- Cambios hormonales de la menstruación y embarazo maligno[12]
- Artritis reactiva[12]
- Sarcoidosis.[12]
Infecciones[editar]
El síndrome de Stevens-Johnson puede ser causado por infecciones. Esto por lo general incluye infecciones comunes como el herpes simple, la gripe, las paperas, la enfermedad por arañazo de gato, la histoplasmosis, el virus de Epstein-Barr, mycoplasma pneumoniae o similares.
Medicamentos/drogas[editar]
Aunque el síndrome de Stevens-Johnson pueda ser causado por infecciones virales, malignidades o reacciones severas alérgicas a la medicación, la causa principal parece ser el empleo de medicinas de sulfas y antibióticos.
El SJS puede ser causado por la reacción adversa a medicamentos como alopurinol, fenitoína, ácido valproico, levofloxacino, diclofenaco, etravirina, isotretinoína, fluconazol,[13] valdecoxib, sitagliptina, oseltamivir, penicilinas, barbitúricos, sulfamida, azitromicina, oxcarbazepina, zonisamida, modafinilo,[14] lamotrigina, nevirapina, pirimetamina, ibuprofeno,[15] etosuximida, carbamazepina, nistatina y medicamentos contra la gota.[16][17]
Entre los medicamentos que tradicionalmente se conocía que inducían al síndrome de Stevens-Johnson, eritema multiforme y la necrólisis epidérmica tóxica, se incluyen los sulfamidas, penicilinas, barbitúricos, lamotriginas y fenitoína. La combinación de lamotrigina con valproato de sodio aumenta el riesgo de padecer el síndrome. Los antiinflamatorios no esteroideos son una causa rara del SJS en adultos; el riesgo es más alto para pacientes de mayor edad, mujeres y aquellos que están iniciando el tratamiento.[18] Típicamente, los síntomas del SJS inducidos por el consumo de drogas surgen una semana después de comenzar la medicación. Las personas con lupus o con infecciones de VIH son más susceptibles al SJS inducido por drogas.[11]
El SJS también puede producirse por el consumo de cocaína.[19]
Epidemiología[editar]
El síndrome de Stevens-Johnson es de condición rara, con una incidencia relatada de alrededor de 2,6[11] a 6,1[18] casos por millón de personas por año. En los Estados Unidos, hay aproximadamente 300 nuevos diagnósticos por año. La condición es más común en niños y adultos jóvenes. Los varones se ven más afectados que las mujeres, con casos que ocurren en una proporción de dos a uno (2:1).[18]
Clínica[editar]
Factores de riesgo[editar]
Los factores de riesgo son historia previa de eritema multiforme o de Stevens-Johnson.[12]
Sintomatología[editar]

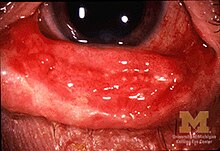
El síndrome se caracteriza por un desarrollo súbito y progresivo de un rash pleomórfico con vesículas y ampollas en piel y membranas mucosas.[12] Por lo general comienza con fiebre de 39 a 40 °C, cefalea severa, dolor de garganta y fatiga, que es mal diagnosticado y, por lo tanto, mal tratado con antibióticos. El signo de Nikolsky es negativo en la mayoría de casos. Las úlceras y otras lesiones empiezan a aparecer en las mucosas, casi siempre en la boca y labios, pero también en las regiones genitales y anales. Las que aparecen en la boca son por lo general sumamente dolorosas y reducen la capacidad del paciente de comer o beber. La conjuntivitis ocurre en aproximadamente el 30 % de los niños que desarrollan el SJS. Un brote de heridas redondas de aproximadamente una pulgada surge sobre la cara, el tronco, brazos y piernas, y las plantas de los pies, pero por lo general no en el cuero cabelludo.[11]
En los casos más graves, pueden aparecer alteraciones del balance electrolítico, taquipnea y disnea, hematuria, albuminuria, arritmias cardíacas, pericarditis, fallo cardíaco congestivo, estupor y coma.[12]
Patología[editar]
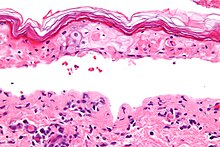
El síndrome, al igual que la necrólisis epidérmica tóxica y el eritema multiforme, está caracterizado por la confluente necrosis epidérmica con la inflamación mínima asociada. La agudeza es evidente observando el patrón de la capa córnea.
Diagnóstico diferencial[editar]
Hay que diferenciarlo de: impétigo ampolloso, pénfigo vulgar, septicemia, penfigoide, enfermedad vascular del colágeno, meningococemia, síndrome de Behçet. Se deben hacer cultivos bacteriológicos de las fuentes sospechosas de infección.
Desde el punto de vista patológico, el hallazgo más característico es la necrólisis epidérmica, espongiosis, edema intracelular, cambios vacuolares en la unión dermoepidérmica, edema y extravasación de eritrocitos. La biopsia de piel puede confirmar el diagnóstico.
Clasificación[editar]
Existe un consenso en la literatura médica especializada que considera al síndrome de Stevens-Johnson como una forma más suave de necrólisis epidérmica tóxica (NET). Estas condiciones se reconocieron por primera vez en 1922.[18] Ambas enfermedades pueden confundirse con el eritema multiforme. El eritema multiforme a veces es causado por una reacción a una medicación, pero es más a menudo una reacción de hipersensibilidad tipo III a una infección (causado con frecuencia por el herpes simple) y es relativamente benigno. Aunque tanto SJS como NET también pueden ser causados por infecciones, son más a menudo los efectos adversos de medicaciones. Sus consecuencias son potencialmente más peligrosas que las de eritema multiforme.
Tratamiento[editar]
El SJS constituye una emergencia dermatológica.
Debe ser hospitalizado para su vigilancia continua y manejo de las complicaciones que van surgiendo.
Todas las medicaciones deberían ser interrumpidas, en particular aquellas que se sabe que causan reacciones del SJS. Los pacientes con infecciones documentadas del mycoplasma pueden ser tratados con macrólidos orales o doxiciclina oral.[11]
Al principio, el tratamiento es similar a esto para pacientes con quemaduras y el cuidado continuado solo puede ser de apoyo (por ejemplo terapia intravenosa y sonda nasogástrica o nutrición parenteral) y sintomático (por ejemplo el aclarado analgésico de boca para la úlcera bucal). Algunas veces las lesiones de la piel requieren de analgesia con opiáceos. Para aliviar los ardores de la cavidad oral, usar enjuagues con suero salino templado o una solución de difenhidramina. La conjuntivitis se puede tratar con lidocaína. En las mucosas puede usarse una crema anestésica como la EMLA.
Debería consultarse a un oftalmólogo inmediatamente, debido a que el SJS con frecuencia causa la formación de tejido cicatrizado dentro de los párpados, llevando a una vascularización de la córnea, visión comprometida y una multitud de otros problemas oculares.
Los dermatólogos y cirujanos tienden a discrepar sobre si la piel debería ser desbridada.[11]
Más allá de esta clase de cuidado de apoyo, no hay ningún tratamiento aceptado para el SJS. El tratamiento con corticosteroides es polémico. Recientes estudios retrospectivos sugirieron que los corticosteroides aumentan las permanencias en el hospital y los niveles de complicaciones. No hay ninguna prueba de corticosteroides para el SJS y puede ser manejado satisfactoriamente sin ellos.[11]
Se han utilizado otros agentes, incluyendo la ciclofosfamida y la ciclosporina, pero ninguno ha demostrado demasiado éxito terapéutico. El tratamiento con inmunoglobulina intravenosa (IVIG) ha mostrado algún avance a la hora de reducir la longitud de la reacción y mejorar los síntomas.[20] Otras medidas comunes de apoyo incluyen el empleo de anestésicos y antisépticos para el tratamiento del dolor, manteniendo un entorno caliente, y analgésicos intravenosos.
Pronóstico[editar]
El SJS propiamente dicho (con menos del 10 % de la superficie de cuerpo implicada) tiene un índice de mortalidad de alrededor del 5 %. El riesgo de muerte se estima usando la escala de SCORTEN, que toma un número de indicadores de pronóstico a tener en consideración.[19] Otras consecuencias pueden ser el fallo o daño de órganos, el rasgado de córnea y la ceguera.
Complicaciones más comunes[editar]
- Síndrome de ojo seco
- Fotofobia
- Ceguera
- Sepsis (síndrome de respuesta inflamatoria sistemática)
- Síndrome de Estrés Postraumático
Las más frecuentes son las infecciones secundarias y las complicaciones pulmonares.[12] También se han descrito deshidrataciones y alteraciones de los electrolitos, necrosis tubular aguda, complicaciones oftálmicas y arritmias.[12] La muerte sobreviene en el 5 al 15 % de los casos sin tratar. El riesgo de recurrencia es del 37 % o más.[12]
Casos notables[editar]
- Padma Lakshmi, actriz, modelo, celebridad y escritora de libros de cocina.[21]
- Manute Bol, jugador profesional de baloncesto y miembro de los equipos de la NBA Washington Bullets, Golden State Warriors, Philadelphia 76ers y Miami Heat, quien murió por las complicaciones del síndrome.[22]
Referencias[editar]
- ↑ Merck Manual: Stevens-Johnson syndrome
- ↑ Stevens AM, Johnson FC (1922). «A new eruptive fever associated with stomatitis and ophthalmia; report of two cases in children». Am J Dis Child 24: 526-533.
- ↑ Stevens–Johnson syndrome - Definitions from Dictionary.com
- ↑ American Medical Association (1922). American journal of diseases of children. American Medical Association. pp. 526-. Consultado el 5 de junio de 2010.
- ↑ Chung WH, Hung SI, Hong HS, et al. (abril de 2004). «Medical genetics: a marker for Stevens–Johnson syndrome». Nature 428 (6982): 486. PMID 15057820. doi:10.1038/428486a.
- ↑ Locharernkul C, Loplumlert J, Limotai C, et al. (julio de 2008). «Carbamazepine and phenytoin induced Stevens–Johnson syndrome is associated with HLA-B*1502 allele in Thai population». Epilepsia 49 (12): 2087. PMID 18637831. doi:10.1111/j.1528-1167.2008.01719.x.
- ↑ Man CB, Kwan P, Baum L, et al. (mayo de 2007). «Association between HLA-B*1502 allele and antiepileptic drug-induced cutaneous reactions in Han Chinese». Epilepsia 48 (5): 1015-8. PMID 17509004. doi:10.1111/j.1528-1167.2007.01022.x.
- ↑ Alfirevic A, Jorgensen AL, Williamson PR, Chadwick DW, Park BK, Pirmohamed M (septiembre de 2006). «HLA-B locus in Caucasian patients with carbamazepine hypersensitivity». Pharmacogenomics 7 (6): 813-8. PMID 16981842. doi:10.2217/14622416.7.6.813.
- ↑ Lonjou C, Thomas L, Borot N, et al. (2006). «A marker for Stevens–Johnson syndrome ...: ethnicity matters». Pharmacogenomics J. 6 (4): 265-8. PMID 16415921. doi:10.1038/sj.tpj.6500356.
- ↑ Lonjou C, Borot N, Sekula P, et al. (febrero de 2008). «A European study of HLA-B in Stevens–Johnson syndrome and toxic epidermal necrolysis related to five high-risk drugs». Pharmacogenet. Genomics 18 (2): 99-107. PMID 18192896. doi:10.1097/FPC.0b013e3282f3ef9c.
- ↑ a b c d e f g Tigchelaar H, Kannikeswaran N and Kamat D (1 de diciembre de 2008). «Stevens-Johnson Syndrome: An Intriguing Diagnosis». Consultant for Pediatricians.
- ↑ a b c d e f g h i j k l m Sindrome de Stevens Johnson
- ↑ Medsafe Data Sheet March 8, 2005. Accessed April 26, 2007.
- ↑ US FDA 2007 Safety Alerts for Drugs, Biologics, Medical Devices, and Dietary Supplements
- ↑ Raksha MP, Marfatia YS (2008). «Clinical study of cutaneous drug eruptions in 200 patients». Indian J Dermatol Venereol Leprol 74 (1): 80. PMID 18193504. doi:10.4103/0378-6323.38431.
- ↑ Fagot J, Mockenhaupt M, Bouwes-Bavinck J, Naldi L, Viboud C, Roujeau J (2001). «Nevirapine and the risk of Stevens–Johnson syndrome or toxic epidermal necrolysis». AIDS 15 (14): 1843-8. PMID 11579247. doi:10.1097/00002030-200109280-00014.
- ↑ Devi K, George S, Criton S, Suja V, Sridevi P (1 de septiembre de 2005). «Carbamazepine--the commonest cause of toxic epidermal necrolysis and Stevens–Johnson syndrome: a study of 7 years». Indian J Dermatol Venereol Leprol 71 (5): 325-8. PMID 16394456. doi:10.4103/0378-6323.16782.
- ↑ a b c d Ward, K. E.; Archambault, R.; Mersfelder, T. L. (2010). «Severe adverse skin reactions to nonsteroidal antiinflammatory drugs: A review of the literature». American Journal of Health-System Pharmacy 67 (3): 206-213. PMID 20101062. doi:10.2146/ajhp080603.
- ↑ a b Stevens–Johnson Syndrome - http://emedicine.medscape.com/article/1197450-overview
- ↑ Molgó M, Carreño N, Hoyos-Bachiloglu R, Andresen M, González S. Use of intravenous immunoglobulin for the treatment of toxic epidermal necrolysis and Stevens-Johnson/toxic epidermal necrolysis overlap syndrome. Review of 15 cases. Rev Med Chil. 2009 Mar;137(3):383-9. Epub 2009 Jun 15
- ↑ Jess Cartner-Morley, "Beautiful and Damned", The Guardian, 8 de abril de 2006
- ↑ FanHouse Staff (junio de 2010). «Manute Bol Dies at Age 47». Fanhouse. Archivado desde el original el 21 de junio de 2010. Consultado el 20 de junio de 2010.
- Bibliografía
- Del Pozzo-Magana BR, Lazo-Langner A, Carleton B, Castro-Pastrana LI, Rieder MJ. A systematic review of treatment of drug-induced Stevens-Johnson syndrome and toxic epidermal necrolysis in children. J Popul Ther Clin Pharmacol. 2011;18:e121-33
- French LE. Toxic epidermal necrolysis and Stevens Johnson syndrome: our current understanding. Allergol Int. 2006 Mar;55(1):9-16
- Molgó M, Carreño N, Hoyos-Bachiloglu R, Andresen M, González S. Use of intravenous immunoglobulin for the treatment of toxic epidermal necrolysis and Stevens-Johnson/toxic epidermal necrolysis overlap syndrome. Review of 15 cases. Rev Med Chil. 2009 Mar;137(3):383-9. Epub 2009 Jun 15
- Pasternack MS, Swartz MN. Cellulitis, necrotizing fasciitis, and subcutaneous tissue infections. In: Mandell GL, Bennett JE, Dolin R, eds. Principles and Practice of Infectious Diseases. 7th ed. Philadelphia, Pa: Elsevier Churchill Livingstone; 2009:chap 90.
- Schumann-Gable N. Dermatology. In: Custer JW, Rau RE, eds. The Harriet Lane Handbook. 18th ed. Philadelphia, Pa: Elsevier Mosby; 2009:chap 8.
- Wetter DA, Camilleri MJ.Clinical, etiologic, and histopathologic features of Stevens-Johnson syndrome during an 8-year period at Mayo Clinic. Mayo Clin Proc. 2010 Feb;85(2):131-8.
