Ácido cafeico
| Ácido cafeico | ||
|---|---|---|
 | ||
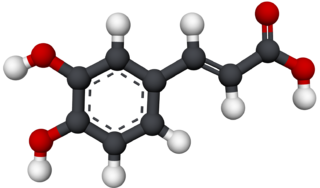 | ||
| Nombre IUPAC | ||
| Ácido (E)-3-(3,4-dihidroxifenil)prop-2-enoico | ||
| General | ||
| Otros nombres |
Ácido 3,4-dihidroxicinámico Ácido 3-(3,4-dihidroxifenil)-2-propenoico trans-cafeato | |
| Fórmula estructural | Estructura en Jmol | |
| Fórmula molecular | C9H8O4 | |
| Identificadores | ||
| Número CAS | 331-39-5[1] | |
| Número RTECS | GD8950000 | |
| ChEBI | 16433 | |
| ChEMBL | CHEMBL145 | |
| ChemSpider | 600426 | |
| DrugBank | DB01880 | |
| PubChem | 689043 | |
| UNII | U2S3A33KVM | |
| KEGG | C01481 | |
| Propiedades físicas | ||
| Apariencia | Cristales amarillos (imagen) | |
| Densidad | 1480 kg/m³; 1,48 g/cm³ | |
| Masa molar | 18 015 742 g/mol | |
| Punto de fusión | 223 °C (496 K) | |
| Punto de ebullición | 416,82 °C (690 K) | |
| Índice de refracción (nD) | 1.71 | |
| Propiedades químicas | ||
| Acidez | 4,62 a 25 °C pKa | |
| Solubilidad en agua | 54,1 g/L a 25 °C | |
| Peligrosidad | ||
| Punto de inflamabilidad | 493,18 K (220 °C) | |
| NFPA 704 |
0
2
0
| |
| Frases R | R36/37/38 R40 | |
| Frases S | S26 S36/37 | |
| Riesgos | ||
| Ingestión | Enjuagar con agua, atención médica. | |
| Inhalación | Irritación. Dar aire fresco, respiración artificial de ser necesario, atención médica. | |
| Piel | Irritación. Lavar con jabón y abundante agua, atención médica. | |
| Ojos | Irritación. Enjuagar con abundante agua por al menos 15 minutos, atención médica. | |
| Más información | Se descompone entre 223-225 °C[2] | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido cafeico es un compuesto orgánico que es clasificado como un ácido hidroxicinámico. Este sólido amarillo contiene grupos funcionales fenólico y acrílico. Se encuentra en todas las plantas debido a que es un intermediario clave en la biosíntesis de la lignina, una de las principales formas de biomasa.[3]
Ocurrencia y función biológica
[editar]El ácido cafeico puede encontrarse en la corteza de Eucalyptus globulus.[4] Puede encontrarse también en el helecho de agua dulce Salvinia molesta[5] o en el hongo Phellinus linteus.[6]
Presencia en alimentos
[editar]El ácido cafeico es uno de los principales fenoles naturales en el aceite de Argán.[7]
Metabolismo
[editar]Biosíntesis
[editar]El ácido cafeico es biosintetizado mediante la hidroxilación del cumaroil éster del éster quínico. Esta hidroxilación produce el ester cafeico del ácido shikímico, el cual se convierte a ácido clorogénico. Es el precursor del ácido ferúlico, alcohol coniferílico, y alcohol sinapílico, todos ellos pilares significativos en la lignina.[3] La transformación a ácido ferúlico es catalizada por la enzima ácido cafeico-O-metiltransferasa.
El ácido cafeico y su derivado fenetil éster del ácido cafeico (CAPE) son producidos en muchos tipos de plantas.[8][9][10]
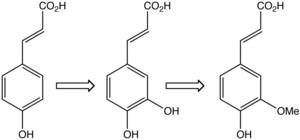
En las plantas, el ácido cafeico (centro) es formado a partir del ácido 4-hidroxicinámico (izquierda) y es transformado a ácido ferúlico.
La dihidroxifenilalanina amoníaco-liasa es una enzima que usa L-3,4 dihidroxifenilalanina (L-dopa) para producir trans-cafeato y NH3.
Biotransformación
[editar]La cafeato O-metiltransferasa es una enzima responsable de la transformación del ácido cafeico en ácido ferúlico.
Biodegradación
[editar]La cafeato 3,4-dioxigenasa es una enzima que utiliza el ácido cafeico y oxígeno para producir 3-(2-carboxietenil)-cis,cis-muconato.
Glucósidos
[editar]El ácido 3-O-cafeoilshikímico (ácido dactilífrico) y sus isómeros, son sustratos de dorado enzimático encontrados en dátiles (frutas Phoenix dactylifera).[11]
Farmacología
[editar]El ácido cafeico tiene una variedad de efectos farmacológicos potenciales en estudios in vitro y en modelos animales, pero no han sido demostrados efectos clínicos en humanos.
Es un antioxidante in vitro y también in vivo.[10] También muestra actividad inmunomodulatoria y antiinflamatoria. El ácido cafeico superó a los otros antioxidantes, reduciendo la producción de aflatoxinas en más del 95 por ciento. Los estudios son los primeros en mostrar que el estrés oxidativo que de otra manera habría provocado o mejorado la producción de aflatoxinas del Aspergillus flavus, puede ser obstaculizado por el ácido cafeico. Esto abre la puerta para utilizar métodos fungicidas naturales mediante el suplemento de árboles con antioxidantes.[12]
Estudios de la carcinogenicidad del ácido cafeico tienes resultados mixtos. Algunos estudios han mostrado que inhibe la carcinogénesis, y otros experimentos muestran efectos carcinogénicos.[13] La administración oral de altas dosis de ácido cafeico en ratas ha causado papilomas estomacales.[13] En el mismo estudio, altas dosis de antioxidantes combinados, incluyendo al ácido cafeico, mostraron una disminución significativa en el crecimiento de tumores del colon en esas mismas ratas. Ningún efecto significativo fue notado aparte de eso. El ácido cafeico está listado en algunas Hojas de Datos de Riesgo como carcinógenos potenciales,[14] tal como ha sido listado por la Agencia Internacional de Investigación del Cáncer (IARC) como carcinógeno del Grupo 2B, "posiblemente carcinógeno para los humanos".[15] Datos más recientes muestran que las bacterias en los intestinos de ratas pueden alterar la formación de metabolitos del ácido cafeico.[16][17] No ha habido efectos nocivos conocidos del ácido cafeico en humanos.
Otros usos
[editar]El ácido cafeico puede ser el ingrediente activo en el cafenol, un revelador fotográfico blanco y negro casero hecho a partir de café instantáneo.[18] La química del revelado es similar a la del catecol o el pirogallol.[19]
Es utilizado también como una matriz en análisis de espectrometría de masas MALDI-TOF.[20]
Referencias
[editar]- ↑ Número CAS
- ↑ Toxicology Data Network
- ↑ a b Boerjan, Wout; Ralph, John; Baucher, Marie (2003). «Ligninbiosynthesis». Annual Review of Plant Biology 54: 519-46. PMID 14503002. doi:10.1146/annurev.arplant.54.031902.134938..
- ↑ Santos, Sónia A. O.; Freire, Carmen S. R.; Domingues, M. Rosário M.; Silvestre, Armando J. D.; Neto, Carlos Pascoal (2011). «Characterization of Phenolic Components in Polar Extracts of Eucalyptus globulus Labill. Bark by High-Performance Liquid Chromatography–Mass Spectrometry». Journal of Agricultural and Food Chemistry 59 (17): 9386-93. PMID 21761864. doi:10.1021/jf201801q.
- ↑ Choudhary, M. Iqbal; Naheed, Nadra; Abbaskhan, Ahmed; Musharraf, Syed Ghulam; Siddiqui, Hina; Atta-Ur-Rahman (2008). «Phenolic and other constituents of fresh water fern Salvinia molesta». Phytochemistry 69 (4): 1018-23. PMID 18177906. doi:10.1016/j.phytochem.2007.10.028.
- ↑ Lee YS, Kang YH, Jung JY et al. (octubre de 2008). «Protein glycation inhibitors from the fruiting body of Phellinus linteus». Biological & Pharmaceutical Bulletin 31 (10): 1968-72. PMID 18827365. doi:10.1248/bpb.31.1968.
- ↑ ., Z. Charrouf; ., D. Guillaume (2007). «Phenols and Polyphenols from Argania spinosa». American Journal of Food Technology 2 (7): 679. doi:10.3923/ajft.2007.679.683.
- ↑ Red Clover Flowers Herbal Information
- ↑ «Dr. Duke's Phytochemical and Ethnobotanical Databases». Archivado desde el original el 5 de diciembre de 2000.
- ↑ a b Olthof MR, Hollman PC, Katan MB (enero de 2001). «Chlorogenic acid and caffeic acid are absorbed in humans». J. Nutr. 131 (1): 66-71. PMID 11208940.
- ↑ 3-O-caffeoylshikimic acid (dactylifric acid) and its isomers, a new class of enzymic browning substrates. V.P. Maier, D.M. Metzler and A. F. Huber, Biochemical and Biophysical Research Communication, 1964, 14(2), pages 124-128, PubMed
- ↑ «Nuts’New Aflatoxin Fighter: Caffeic Acid?».
- ↑ a b M Hirose, Y Takesada, H Tanaka, S Tamano, T Kato and T Shirai (1998). «Carcinogenicity of antioxidants BHA, caffeic acid, sesamol, 4- methoxyphenol and catechol at low doses, either alone or in combination, and modulation of their effects in a rat medium-term multi-organ carcinogenesis model». Carcinogenesis 19 (1): 207-212. PMID 9472713. doi:10.1093/carcin/19.1.207.
- ↑ «Caffeic Acid (IARC Summary & Evaluation, Volume 56, 1993)».
- ↑ Agents Classified by the IARC Monographs Archivado el 25 de octubre de 2011 en Wayback Machine., Agencia Internacional de Investigación del Cáncer
- ↑ MA Peppercorn and P Goldman (1972). «Caffeic acid metabolism by gnotobiotic rats and their intestinal bacteria». Proceedings of the National Academy of Sciences 69 (6): 1413-1415. PMC 426714. PMID 4504351. doi:10.1073/pnas.69.6.1413.
- ↑ M-P Gonthier, M-A Verny, C Besson, C Rémésy and A Scalbert (1 de junio de 2003). «Chlorogenic acid bioavailability largely depends on its metabolism by the gut microflora in rats». Journal of Nutrition 133 (6): 1853-1859. PMID 12771329.
- ↑ Caffenol blog "Caffenol-C-M, recipe"
- ↑ Williams, Scott "A Use for that Last Cup of Coffee: Film and Paper Development", Technical Photographic Chemistry 1995 Class, Imaging and Photographic Technology Department, School of Photographic Arts and Sciences Rochester Institute of Technology
- ↑ Beavis RC, Chait BT (diciembre de 1989). «Cinnamic acid derivatives as matrices for ultraviolet laser desorption mass spectrometry of proteins». Rapid Commun. Mass Spectrom. 3 (12): 432-5. PMID 2520223. doi:10.1002/rcm.1290031207.
Bibliografía adicional
[editar]- Cadenas/Packer. «15: Caffeic Acid and Related Antioxidant Compounds: Biochemical and Cellular Effects (João Laranjinha)». Handbook of Antioxidants, Revised and Expanded (en inglés). Volumen 8 de Oxidative stress and diseases (2a edición). p. 279. ISBN 9780824745103. Consultado el 12 de noviembre de 2012.
Enlaces externos
[editar] Wikimedia Commons alberga una categoría multimedia sobre Ácido cafeico.
Wikimedia Commons alberga una categoría multimedia sobre Ácido cafeico.- (en inglés) Datos de la SRC PhysProp Database (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).
- «Caffeic Acid as Carbocyclic Carboxylic Acid». Chemical Land (en inglés).
- Webbook para el ácido cafeico
- (en inglés) Ficha en Alfa Aesar
- (en inglés) Ficha en Sigma-Aldrich
- (en inglés) Ficha en Santa Cruz Biotechnology
- Esta obra contiene una traducción derivada de «Caffeic acid» de Wikipedia en inglés, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.


