Metaloproteína
Metaloproteína: proteína + metal. Es un término genérico para una proteína que contiene un ion metálico como cofactor.[1] Las funciones de las metaloproteínas son muy variadas en las células, actuando como enzimas, proteínas de transporte y almacenamiento, y en la transducción de señales. De hecho, aproximadamente un cuarto a un tercio de todas las proteínas requieren metales para llevar a cabo sus funciones.[2] El metal suele estar coordinado por átomos de nitrógeno, oxígeno o azufre pertenecientes a los aminoácidos de la cadena polipeptídica y/o un ligando macrocíclico incorporado en la proteína. La presencia de los iones metálicos en las metaloenzimas les permite llevar a cabo funciones tales como reacciones redox que no pueden ser fácilmente realizadas por el conjunto limitado de grupos funcionales que se encuentran en los aminoácidos.[3]
Metaloproteínas de almacenamiento y transporte[editar]
Transportadores de oxígeno[editar]
La hemoglobina es el principal transportador de oxígeno en humanos tiene cuatro subunidades en las que el ion de hierro(II) es coordinado por el ligando plano macrocíclico protoporfirina IX (PIX) y el átomo de nitrógeno del imidazol de un residuo de histidina. El sexto sitio de coordinación contiene una molécula de agua o una molécula de dioxígeno. El sitio activo se encuentra en un bolsillo hidrofóbico; esto es importante, ya que de otro modo el hierro(II) se oxidaría de forma irreversible a hierro(III). La constante de equilibrio para la formación de HbO2 es tal que el oxígeno es tomado o liberado en función de la presión parcial de oxígeno en los pulmones o en los músculos. En la hemoglobina las cuatro subunidades muestran un efecto cooperativo que permite una fácil transferencia de oxígeno de la hemoglobina a la mioglobina.
La hemoritrina es otro transportador de oxígeno que contiene hierro. El oxígeno sitio de unión a oxígeno es un centro de hierro binuclear. Los átomos de hierro están coordinados a la proteína a través de carboxilatos de las cadenas laterales de glutamato, aspartato y cinco residuos de histidina. La incorporación de O2 por la hemoritrina es acompañado por la oxidación de dos electrones del centro reducido binuclear, con la producción de peróxido (OOH-). Los mecanismos de captura y liberación de oxígeno son conocidos en detalle.[4][5]
Las hemocianinas transportan oxígeno en la sangre de la mayoría de los moluscos y algunos artrópodos como el cangrejo herradura. Le sigue a la hemoglobina en cuanto a abundancia como forma de transporte de oxígeno. En la oxigenación los dos átomos de cobre(I) del sitio activo se oxidan a cobre(II) y las moléculas de dioxígeno se reducen a peróxido, O22-.[6][7]
Citocromos[editar]
Los citocromos poseen un átomo de hierro que en la mayoría de los casos se encuentra coordinado a un grupo hemo. Los citocromos funcionan como vectores de transferencia de electrones oxidando hierro(II) a hierro(III). Las diferencias entre los citocromos radica en las distintas cadenas laterales; por ejemplo el citocromo a tiene un grupo prostético hemo a y un citocromo b tiene un grupo prostético hemo b. Estas diferencias se traducen en diferentes potenciales redox Fe2+/Fe3+ de tal manera que son varios los citocromos que participan en la cadena de transporte de electrones mitocondrial.[8]
Las enzimas del citocromo P450 desempeñan la función de la inserción de un átomo de oxígeno en un enlace C-H, una reacción de oxidación.[9][10]
Rubredoxina[editar]
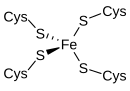
La rubredoxina es un portador de electrones encontrado en bacterias y arqueas que metabolizan azufre. El sitio contiene un ion de hierro que es coordinado por los átomos de azufre de cuatro residuos de cisteína que forman un tetraedro casi regular. Las rubredoxinas realizan procesos de transferencia de un electrón. El estado de oxidación del átomo de hierro cambia entre los estados +2 y +3. En ambos estados de oxidación del metal hay un alto espín lo que ayuda a minimizar los cambios estructurales.
Almacenamiento y transferencia de hierro[editar]
El hierro es almacenado como hierro(III) en la ferritina. La naturaleza exacta del sitio de unión no se ha determinado todavía. El hierro parece estar presente como un producto de hidrólisis, como FeO(OH) y es transportado por la transferrina cuyo sitio de unión consiste en dos tirosinas, un ácido aspártico y una histidina.[11]
El cuerpo humano no tiene ningún mecanismo de excreción de hierro, esto puede conducir a problemas de sobrecarga de hierro en pacientes tratados con transfusiones de sangre, como, por ejemplo, con β-talasemia.
Ceruloplasmina[editar]
La ceruloplasmina es la principal proteína portadora de cobre en la sangre. Exhibe actividad oxidasa, la cual está asociada con la posible oxidación del Fe2+ (ion ferroso) en Fe3+ (ion férrico), por lo tanto, ayuda en su transporte en el plasma, en asociación con la transferrina, que sólo pueden llevar el hierro en estado férrico.
Metaloenzimas[editar]
Las metaloenzimas tienen una característica en común, que el ion metálico se une a la proteína con un sitio coordinación lábil. Como ocurre con todas las enzimas, la forma del sitio activo es crucial; el metal normalmente se encuentra en un bolsillo, cuya forma se adapta el sustrato. Los iones metálicos catalizan reacciones que son difíciles de lograr en la química orgánica.
Anhidrasa carbónica[editar]

- CO2 + H2O <-> H2CO3
Esta reacción es muy lenta en ausencia de un catalizador, pero rápida en presencia del ion hidróxido
- CO2 + OH- <-> HCO3-
Una reacción similar a esta es casi instantánea con la anhidrasa carbónica. La estructura del sitio activo es bien conocida; se compone de un ion de zinc coordinado por tres átomos de nitrógeno del imidazol a partir de tres unidades de histidina. El cuarto sitio de coordinación está ocupado por una molécula de agua. Esta coordinación de iones de zinc es aproximadamente tetraédrica, la carga positiva de iones polariza la molécula de agua coordinada y ocurre un ataque nucleofílico por el hidróxido cargado negativamente del dióxido de carbono. El ciclo catalítico produce iones de bicarbonato y de hidrógeno[1] ya que el equilibrio favorece la disociación del ácido carbónico a valores de pH fisiológico.[12]
- H2CO3 <-> HCO3- + H+
Enzimas dependientes de vitamina B12[editar]
La vitamina B12 cataliza la transferencia de metilo (-CH3) entre dos grupos de moléculas, lo que implica la ruptura de enlaces C-C, un proceso que es energéticamente caro en reacciones orgánicas. Los iones de metal disminuye la energía de activación para el proceso de transición mediante la formación de un enlace transitorio Co-CH3.[13] La estructura de esta coenzima la determinó Dorothy Hodgkin, para lo cual recibió un premio Nobel.[14] Constiste de un ion de cobalto (II) coordinado por cuatro átomos de nitrógeno de un anillo de corrina y un quinto átomo de nitrógeno del grupo imidazol. En el estado de reposo hay un enlace σ Co-C con el carbono 5 ' de la adenosina.[15] Este es un compuesto organometálicos que se encuentra en la naturaleza, lo que explica su función en la transmetilación, como la llevada a cabo por la metionina sintasa.
Nitrogenasa[editar]
La enzima nitrogenasa es uno de las pocos enzimas que pueden catalizar el proceso de fijación de nitrógeno atmosférico. Posee un átomo de molibdeno en el sitio activo y centros de hierro-azufre grupos que participan en el transporte de los electrones necesarios para reducir el nitrógeno. La reacción puede ser escrita como:
La estructura exacta del sitio activo ha sido difícil de determinar. Parece contener un centro de MoFe7S8 que es capaz de unirse a la molécula de dinitrógeno y, probablemente, permitir que comience el proceso de reducción.[16] Los electrones son transportados por el centro asociado "P", que contiene dos centros cúbicos Fe4S4 por unidos por puentes de azufre.[17]
Superóxido dismutasa[editar]

El ion superóxido, O2- se genera en los sistemas biológicos por la reducción de oxígeno molecular. Tiene un electrón desapareado, por lo que se comporta como un radical libre y es un poderoso agente oxidante. Estas propiedades hacen que el ion superóxido sea muy tóxico y lo utilicen los fagocitos para matar a microorganismos invasores. En caso contrario, el superóxido debe ser destruido antes de que haga daño no deseado a las células. La enzima superóxido dismutasa realiza esta función de manera muy eficiente.[18]
El estado de oxidación de los átomos de oxígeno es ½. En soluciones a pH neutro, el ion superóxido dismuta a oxígeno molecular y peróxido de hidrógeno:
- 2 O2− + 2 H+ → O2 + H2O2
La superóxido, abreviada como SOD, aumenta la tasa de reacción hasta casi el límite de difusión.[20] La clave de acción de estas enzimas es el ion metálico con estados de oxidación variable que puede actuar como agente oxidante o como reductor.
- Oxidación: M(n+1)+ + O2− → Mn+ + O2
- Reducción: Mn+ + O2− + 2H+ → M(n+1)+ + H2O2.
En humanos el metal activo es cobre, como Cu2+ o Cu+, coordinado como tetraedro por residuos de histidina. Esa enzima tiene también iones de zinc. Otras isoenzimas pueden contener hierro, manganeso o níquel. Ni-SOD es particularmente interesante ya que involucra al níquel(III), un estado de oxidación inusual para este elemento. La geometría del sitio activo con N cicla de un cuadrado plano Ni(II), con tiolato (Cys2 y Cys6) y nitrógeno (His1 y Cys2), a un cuadrado piramidal con Ni(III) con una His1 axial como ligando.[19]
Clorofila[editar]
La clorofila desempeña un papel crucial en la fotosíntesis. Contiene un ion de magnesio encerrado en un anillo de clorina. Sin embargo, el ion magnesio no está directamente implicado en la función fotosintética y pueden ser sustituido por otro ion divalente con solo un poco de pérdida de actividad. Por el contrario, el fotón es absorbido por el anillo de clorina, cuya estructura electrónica está adaptada para este fin.
Inicialmente, la absorción de un fotón provoca que un electrón sea excitado a un estado singulete de la banda Q. El estado excitado se somete a un cruce intersistema de un estado singulete a un estado triplete en el que hay dos electrones con espín paralelo. Esta especie es un radical libre, por lo cual es muy reactivo y permite a un electrón ser transferidos a aceptores adyacentes a la clorofila en el cloroplasto. En este proceso la clorofila es oxidada. Luego en el ciclo fotosintético es reducida aceptando un electrón y el producto final de la oxidación es oxígeno molecular cuyos átomos provienen de moléculas de agua.
Metaloproteínas de transducción de señal[editar]
Calmodulina[editar]
La calmodulina es un ejemplo de transducción de señal de proteínas. Se trata de una pequeña proteína que contiene cuatro motivos mano EF, cada uno de los cuales puede unirse a un ion de Ca2+.
En un bucle de mano EF los iones de calcio es coordinado en una configuración pentagonal bipiramidal. Seis residuos de ácido glutámico y ácido aspártico participan en la unión en las posiciones 1, 3, 5, 7, 9, de la cadena del polipéptido. En la posición 12 hay un ligando de glutamato o aspartato, que se comporta como un (ligando bidentado), proveyendo de dos átomos de oxígeno. El noveno residuo en el bucle debe ser necesariamente una glicina debido a exigencias conformacionales de la cadena polipeptídica. La esfera de coordinación del calcio contiene sólo átomos de oxígeno del carboxilato y ningún átomo de nitrógeno.
La proteína tiene dos dominios de aproximadamente simétricos, separados por una región "bisagra" flexible. La unión de calcio provoca un cambio conformacional en la proteína. La calmodulina participa en los sistemas de señalización intracelular al actuar como un segundo mensajero ante los primeros estímulos.[20][21]
Factores de transcripción[editar]

Muchos factores de transcripción contienen una estructura conocida como dedo de zinc, se trata de un módulo estructural donde una región de la proteína se pliega en torno a un ion de zinc. El zinc no toma contacto con el ADN al cual se unen estas proteínas, en su lugar el cofactor es esencial para la estabilidad de la cadena de la proteína ajustadamente plegada.[22] En estas proteínas el ion de zinc generalmente se encuentra coordinado por pares de cisteína e histidina de las cadenas laterales.
Otras metaloenzimas[editar]
| Ion | Ejemplos de enzimas conteniendo este ion |
|---|---|
| Magnesio | Glucosa 6-fosfatasa Hexoquinasa ADN polimerasa |
| Vanadio | Vanabina |
| Manganeso | Arginasa |
| Hierro | Catalasa Hidrogenasa IRE-BP Aconitasa |
| Níquel[23] | Ureasa Hidrogenasa |
| Cobre | Citocromo oxidasa Plastocianina Lacasa |
| Zinc | Alcohol deshidrogenasa Carboxipeptidasa Aminopeptidasa |
| Molibdeno | Nitrato reductasa
Sulfito Oxidasa Xantina Oxidasa Nitrogenasa (Mo y Fe) |
| Selenio | Glutatión peroxidasa |
| Varios | Metalotioneina Fosfatasa |
Referencias[editar]
- ↑ Shriver, D.F.; Atkins, P.W. (1999). «Chapter 19, Bioinorganic chemistry». Inorganic chemistry (3rd. edición). Oxford University Press. ISBN 019 850330X.
- ↑ Waldron KJ, Robinson NJ (enero de 2009). «How do bacterial cells ensure that metalloproteins get the correct metal?». Nat. Rev. Microbiol. 7 (1): 25-35. PMID 19079350. doi:10.1038/nrmicro2057.
- ↑ Messerschmidt, A; Huber, R.; Wieghardt,K.; Poulos, T. (2001). Handbook of Metalloproteins. Wiley. ISBN 0-471-62743-7.
- ↑ Stenkamp, R.E. (1994). «Dioxygen and hemerythrin». Chem. Rev. 94: 715-726. doi:10.1021/cr00027a008.
- ↑ Wirstam M., Lippard, S.J., Friesner R.A. (2003). «Reversioble Dioxygen Binding to Hemerythrin». J. Am. Chem. Soc. 125: 3980-3987. doi:10.1021/ja017692r.
- ↑ K. D. Karlin, R. W. Cruse, Y. Gultneh, A. Farooq, J. C. Hayes and J. Zubieta (1987). «Dioxygen-copper reactivity. Reversible binding of O2 and CO to a phenoxo-bridged dicopper(I) complex». J. Am. Chem. Soc. 109 (9): 2668-2679. doi:10.1021/ja00243a019.
- ↑ N. Kitajima, K. Fujisawa, C. Fujimoto, Y. Morooka, S. Hashimoto, T. Kitagawa, K. Toriumi, K. Tatsumi and A. Nakamura (1992). «A new model for dioxygen binding in hemocyanin. Synthesis, characterization, and molecular structure of the μ-η2:η2 peroxo dinuclear copper(II) complexes, [Cu(HB(3,5-R2pz)3)]2(O2) (R = isopropyl and Ph)». J. Am. Chem. Soc. 114 (4): 1277-1291. doi:10.1021/ja00030a025.
- ↑ Moore, G.R.; Pettigrew, G.W. (1990). Cytochrome c:structural and physicochemical aspects. Berlin: Springer.
- ↑ Astrid Sigel, Helmut Sigel and Roland K.O. Sigel, ed. (2007). The Ubiquitous Roles of Cytochrome450 Proteins. Metal Ions in Life Sciences 3. Wiley. ISBN 978-0-470-01672-5.
- ↑ Ortiz de Montellano, P.R. (2005). Cytochrome P450 Structure, Mechanism, and Biochemistry (3rd. edición). Springer. ISBN 978-0-306-48324-0.
- ↑ Anderson BF, Baker HM, Dodson EJ, et al. (abril de 1987). «Structure of human lactoferrin at 3.2-A resolution». Proc. Natl. Acad. Sci. U.S.A. 84 (7): 1769-73. PMC 304522. PMID 3470756.
- ↑ Lindskog S (1997). «Structure and mechanism of carbonic anhydrase». Pharmacol. Ther. 74 (1): 1-20. PMID 9336012. doi:10.1016/S0163-7258(96)00198-2.
- ↑ Astrid Sigel, Helmut Sigel and Roland K.O. Sigel, ed. (2008). Metal Ions in Life Sciences - Metal-carbon bonds in enzymes and cofactors 6. Wiley. ISBN 978-1-84755-915-9.
- ↑ «The Nobel Prize in Chemistry 1964». Nobelprize.org.
- ↑ Hodgkin, D.C. (1965). «The Structure of the Corrin Nucleus from X-ray Analysis». Proc. Roy. Soc. A 288: 294-305. doi:10.1098/rspa.1965.0219.
- ↑ Orme-Johnson, W.H. (1993). Steifel, E.I; Coucouvannis, D.; Newton, D.C., ed. Advances in chemystry, Symposium series no. 535 - Molybdenum enzymes, cofactors and model systems. Washington, DC: American Chemical Society. p. 257.
- ↑ Chan, M.K.; Kim, J.; Rees, D.C. (1993). «The nitrogenase FeMo-cofactor and P-cluster pair: 2.2 A resolution structures». Science 260: 792. PMID 8484118. doi:10.1126/science.8484118.
- ↑ Packer, L. (editor) (2002). Superoxide Dismutase: 349 (Methods in Enzymology). Academic Press. ISBN 0121822524.
- ↑ Barondeau, D.P.; Kassmann C.J.; Bruns C.K.; Tainer J.A.; Getzoff E.D. (2004). «Nickel superoxide dismutase structure and mechanism». Biochemistry 43 (25): 8038-8047. PMID 15209499. doi:10.1021/bi0496081.
- ↑ Stevens FC (1983). «Calmodulin: an introduction». Can. J. Biochem. Cell Biol. 61 (8): 906-10. PMID 6313166.
- ↑ Chin D, Means AR (2000). «Calmodulin: a prototypical calcium sensor». Trends Cell Biol. 10 (8): 322-8. doi:10.1016/S0962-8924(00)01800-6.
- ↑ Berg JM (1990). «Zinc finger domains: hypotheses and current knowledge». Annu Rev Biophys Biophys Chem 19: 405-21. PMID 2114117. doi:10.1146/annurev.bb.19.060190.002201.
- ↑ Astrid Sigel, Helmut Sigel y Roland K.O. Sigel (2008). Metal Ions in Life Sciences - Nickel and Its Surprising Impact in Nature 2. Wiley. ISBN 978-0-470-01671-8.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Metaloproteína.
Wikimedia Commons alberga una categoría multimedia sobre Metaloproteína.- Metaloproteínas en MeSH
