Anhidrasa carbónica
| Anhidrasa carbónica | ||||
|---|---|---|---|---|
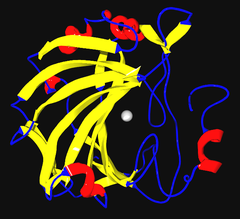 Diagrama de Richardson de la anhhidrasa carbónica humana II, con el ion de zinc visible en el centro | ||||
| Estructuras disponibles | ||||
| PDB | ||||
| Identificadores | ||||
| Identificadores externos |
Bases de datos de enzimas
| |||
| Número EC | 4.2.1.1 | |||
| Número CAS | 9001-03-0 | |||
| Ortólogos | ||||
| Especies |
| |||
| PubMed (Búsqueda) |
| |||
| PMC (Búsqueda) |
| |||
La anhidrasa carbónica (AC, carbonato-deshidratasa: EC 4.2.1.1) es una enzima que pertenece a una familia de metaloenzimas (enzimas que contienen uno o más átomos metálicos como componente funcional de la enzima) y que catalizan la conversión rápida de dióxido de carbono y agua a bicarbonato y protones, una reacción que ocurre más lenta en ausencia del catalizador.[1] La anhidrasa carbónica incrementa significativamente la tasa de reacción, donde las típicas tasas catalíticas de las diferentes formas de esta enzima tienen valores que alternan entre 104 y 106 reacciones por segundo.[2] El centro activo de la mayoría de las anhidrasas carbónicas contiene un ion de Zinc (Zn).
Estructura y función de la anhidrasa carbónica[editar]
En la naturaleza se encuentran varias formas de anhidrasa carbónica. En la más estudiada, anhidrasa carbónica de tipo α, presente en animales, el ion zinc está coordinado con los átomos de nitrógeno de los anillos de imidazol de tres residuos de histidina, His94, His 96 e His119. La función primaria de la enzima en animales es interconvertir el dióxido de carbono y el bicarbonato para mantener el equilibrio ácido-base en la sangre y otros tejidos, y ayudar al transporte de dióxido de carbono fuera de los tejidos.
Las plantas contienen una forma diferente llamada anhidrasa carbónica de tipo β, la cual, desde un punto inicial evolutivo, aun siendo una enzima distinta participa en la misma reacción y también tiene un ion zinc en el sitio activo. En plantas, la anhidrasa carbónica ayuda a elevar la concentración de CO2 dentro del cloroplasto para incrementar la tasa de carboxilación de la enzima Rubisco. Esta es la reacción que integra el CO2 en carbohidratos durante la fotosíntesis, y puede usar únicamente la forma del carbono en el CO2, y no el ácido carbónico o el bicarbonato.
En el 2000 se encontró una anhidrasa carbónica que contiene cadmio, la cual se expresa en diatomeas marinas debido a la limitación de zinc. En el océano abierto, el zinc se encuentra frecuentemente en baja concentración y puede ser un elemento limitante en el crecimiento de fitoplancton tales como diatomeas; así la existencia de una anhidrasa carbónica que usa un ion metálico diferente podría ser beneficiosa en esos ambientes. Antes de este descubrimiento, el cadmio se había considerado como un elemento metálico pesado tóxico sin función biológica. En el 2005, esta particular anhidrasa carbónica constituye la única reacción biológica conocida que depende de cadmio.
Reacción catalizada por la anhidrasa carbónica:
CO
2 + H
2O H
2CO
3 HCO−
3 + (H+
):[3] en tejidos - alta concentración de CO
2
La tasa de acción de la anhidrasa carbónica es una de las más rápidas de todas en las que participan enzimas, y su tasa está limitada típicamente por la tasa de difusión de sus sustratos.
La reacción reversa es relativamente lenta (cinética en el rango de 15 segundos), lo que explica por qué una bebida carbonatada no hace un efecto instantáneo liberador de gas cuando se abre el contenedor, pero rápidamente degasificará en la boca cuando la anhidrasa carbónica se adiciona con la saliva.
(HCO−
3) + (H+
) CO
2 + H
2O H
2CO
3: en los pulmones y las nefronas del riñón - alta concentración de CO
2, en células vegetales.
Mecanismo[editar]
Un grupo prostético de zinc en la enzima está coordinado en tres posiciones por las cadenas laterales de histidina. La cuarta posición de coordinación está ocupada por agua. Esto causa la polarización del enlace hidrógeno-oxígeno, haciendo que el oxígeno sea ligeramente negativo, debilitándolo.
Una cuarta histidina está ubicada cerca al sustrato de agua y acepta un protón, en un ejemplo de catálisis ácido-base. Esto deja un hidróxido unido al ion zinc.
El sitio activo también contiene un bolsillo con especificidad por el dióxido de carbono, llevándolo cerca al grupo hidróxido. Esto permite al hidróxido rico en electrones reaccionar con el dióxido de carbono, formando bicarbonato.
Familias de la anhidrasa carbónica[editar]
Hay al menos cinco familias distintas de anhidrasa carbónica (α, β, γ, δ y ε). Estas familias no tienen una secuencia aminoacídica significativa y, en la mayoría de los casos, se piensa que son un ejemplo de evolución convergente. Las AC-α se encuentran en seres humanos.
AC-α[editar]
Las enzimas AC encontradas en mamíferos se dividen cuatro amplios subgrupos,[4] los cuales, a su vez se dividen en varias isoformas:
- las AC citosólicas (AC-I, AC-II, AC-III, AC-VII y AC-XIII) (AC1, AC2, AC3, AC7, AC13)
- AC mitocondriales (AC-A y AC-B) (AC5A, AC5B)
- AC secretadas (AC-VI) (AC6)
- AC asociadas a membranas (AC-IV, AC-IX, AC-XII, AC-XIV y AC-XV) (AC4, AC9, AC12, AC14)
Hay tres isoformas "acatalíticas" de anhidrasa carbónica (AC-VIII, AC-X, y AC-XI) (AC8, AC10, AC11) cuyas funciones permanecen desconocidas.[5]
| Isoforma | Gen | Masa molecular[6] | Localización (celular) | Localización (tisular)[6] | Actividad relativa[6] | Sensibilidad a sulfonamidas[6] | |
|---|---|---|---|---|---|---|---|
| AC-I | AC1|1368 | 29 kDa | citoplasma | RBCs y tracto GI | 15% | alta | |
| AC-II | AC2|1373 | 29 kDa | citoplasma | ACsi ubicua | 100% | alta | |
| AC-III | AC3|1374 | 29 kDa | citoplasma | 8% de proteína soluble tipo I en músculo | 1% | baja | |
| AC-IV | AC4|1375 | 35 kDa | extracelularmente unida a GPI | Ampliamente distribuida, p.ej. epitelio transportador de ácido | ~100% | moderada | |
| AC-VA | AC5A | mitocondria | |||||
| AC-VB | AC5B | mitocondria | células secretantes | ||||
| AC-VI | AC6|1380 | ||||||
| AC-VII | AC7|1381 | citoplasma | |||||
| AC-IX | AC9|1383 | asociada a membrana celular | |||||
| AC-XII | AC12|1371 | 44 kDa | sitio activo localizado extracelularmente | ciertos cánceres | ~30% | ||
| AC XIII | AC13|14914 | citoplasma | |||||
| AC-XIV | AC14|1372 | 54 kDa | sitio activo localizado extracelularmente | riñón, corazón, músculo estriado, cerebro | |||
| y AC-XV |
AC-β[editar]
La mayoría de los procariotas y los cloroplastos en vegetales pertenecen a la familia beta. Dos modelos de esta familia han sido identificados:
- C-[SA]-D-S-R-[LIVM]-x-[AP]
- [EQ]-[YF]-A-[LIVM]-x(2)-[LIVM]-x(4)-[LIVMF](3)-x-G-H-x(2)-C-Ghola
AC-γ[editar]
La clase gamma de las AC viene de las bacterias productoras de metano que crecen en fuentes termales.
AC-δ[editar]
La clase delta de AC ha sido descrita en diátomos. No obstante, la distinción de esta clase de AC se ha convertido recientemente en un interrogante.[7]
AC-ε[editar]
La clase épsilon de las Ac ocurre exclusivamente en bacterias en unos pocos quimiolitotrofos y cianobacterias marinas que contienen cso-carboxisomas.[8] Análisis recientes tridimensionales[7] sugieren que las AC-ε tienen alguna semejanza estructural con las AC-β cerca del sitio del ion metálico. Así, las dos formas podrían ser distántemente relacionadas, incluso cuando la secuencia aminoacídica subyacente haya divergido desde entonces considerablemente.
Efectos fisiológicos[editar]
La anhidrasa carbónica es diana de fármacos con efecto diurético de baja potencia como la acetazolamida y la dorzolamida, empleados en el tratamiento de la hipertensión intracraneal y el glaucoma. También es usado como beta bloqueador de receptores m 2.
Referencias[editar]
- ↑ Badger MR, Price GD (1994). «The role of carbonic anhydrase in photosynthesis». Annu. Rev. Plant Physiol. Plant Mol. Bio. 45: 369-392. doi:10.1146/annurev.pp.45.060194.002101.
- ↑ Lindskog S (1997). «Structure and mechanism of carbonic anhydrase». Pharmacol. Ther. 74 (1): 1-20. PMID 9336012. doi:10.1016/S0163-7258(96)00198-2.
- ↑ El ácido carbónico tiene un pKa de alrededor de 6.36 (el valor exacto depende de una media), luego, a un pH de 7 un pequeño porcentaje de bicarbonato está protonado. Ver ácido carbónico para obtener detalles concernientes al equilibrio de HCO−
3 + H+
H
2CO
3 y H
2CO
3 CO
2 + H
2O - ↑ Breton S (2001). «The cellular physiology of carbonic anhydrases». JOP 2 (4 Suppl): 159-64. PMID 11875253. Archivado desde el original el 27 de septiembre de 2008. Consultado el 19 de diciembre de 2007.
- ↑ Lovejoy DA, Hewett-Emmett D, Porter CA, Cepoi D, Sheffield A, Vale WW, Tashian RE (1998). «Evolutionarily conserved, "acatalytic" carbonic anhydrase-related protein XI contains a sequence motif present in the neuropeptide sauvagine: the human CA-RP XI gene (CA11) is embedded between the secretor gene cluster and the DBP gene at 19q13.3». Genomics 54 (3): 484-93. PMID 9878252. doi:10.1006/geno.1998.5585.
- ↑ a b c d Unless else specified: Walter F., PhD. Boron (2005). Medical Physiology: A Cellular And Molecular Approaoch. Elsevier/Saunders. ISBN 1-4160-2328-3. Page 638
- ↑ a b Sawaya MR, Cannon GC, Heinhorst S, Tanaka S, Williams EB, Yeates TO, Kerfeld CA (2006). «The structure of beta-carbonic anhydrase from the carboxysomal shell reveals a distinct subclass with one active site for the price of two». J. Biol. Chem. 281 (11): 7546-55. PMID 16407248. doi:10.1074/jbc.M510464200.
- ↑ So AK, Espie GS, Williams EB, Shively JM, Heinhorst S, Cannon GC (2004). «A novel evolutionary lineage of carbonic anhydrase (epsilon class) is a component of the carboxysome shell». J. Bacteriol. 186 (3): 623-30. PMID 14729686. doi:10.1128/JB.186.3.623-630.2004.

