Presión parcial
En una mezcla de gases, cada gas constituyente tiene una presión parcial que es la presión teórica de ese gas constituyente si ocupase por sí solo el volumen completo de la mezcla original, a la misma temperatura.[1] La presión total de una mezcla de gases ideales es la suma de las presiones parciales de los gases en la mezcla (Ley de Dalton).
La presión parcial de un gas es una medida de la actividad termodinámica de las moléculas del gas. Los gases se disuelven, se difunden y reaccionan de acuerdo con sus presiones parciales y no de acuerdo con sus concentraciones en mezclas de gases o líquidos. Esta propiedad general de los gases también es cierta en las reacciones químicas de los gases en biología. Por ejemplo, la cantidad necesaria de oxígeno para la respiración humana, y la cantidad que es tóxica, se establece solo por la presión parcial del oxígeno. Esto es cierto en un amplio rango de diferentes concentraciones de oxígeno presentes en varios gases respiratorios inhalados o disueltos en la sangre.[2] Las presiones parciales de oxígeno y dióxido de carbono son parámetros importantes en las pruebas de gases en sangre arterial, pero también pueden medirse en, por ejemplo, líquido cefalorraquídeo.
Símbolo[editar]
El símbolo de presión es generalmente o , que puede usar un subíndice para identificar la presión, y las especies de gas también se mencionan por subíndice. Cuando se combinan estos subíndices se aplican recursivamente.[3][4]
Ejemplos:
- o = presión en el tiempo 1
- o = presión parcial de hidrógeno
- o = presión parcial venosa de oxígeno
La ley de Dalton de las presiones parciales[editar]

La ley de Dalton expresa el hecho de que la presión total de una mezcla de gases es igual a la suma de las presiones parciales de los gases individuales en la mezcla.[5] Esta igualdad surge del hecho de que en un gas ideal las moléculas están tan separadas que no interactúan entre sí. La mayoría de los gases reales del mundo real se acercan mucho a este ideal. Por ejemplo, dada una mezcla gaseosa ideal de nitrógeno (N2), hidrógeno (H2) y amoníaco (NH3):
| donde: | |
| = presión total de la mezcla de gases | |
| = presión parcial de nitrógeno (N2) | |
| = presión parcial de hidrógeno (H2) | |
| = presión parcial de amoniaco (NH3) |
Mezclas de gases ideales[editar]
Idealmente, la relación de presiones parciales es igual a la relación del número de moléculas. Es decir, la fracción molar de un componente de gas individual en una mezcla de gas ideal puede expresarse en términos de la presión parcial del componente o los moles del componente:
y la presión parcial de un componente de gas individual en un gas ideal puede obtenerse usando esta expresión:
| Símbolo | Nombre |
|---|---|
| Fracción molar de cualquier componente de gas individual en una mezcla de gases | |
| Presión parcial de cualquier componente de gas individual en una mezcla de gases | |
| Moles de cualquier componente de gas individual en una mezcla de gas | |
| Moles totales de la mezcla de gases | |
| Presión total de la mezcla de gases |
La fracción molar de un componente gaseoso en una mezcla gaseosa es igual a la fracción volumétrica de ese componente en una mezcla gaseosa.[6]
La relación de presiones parciales se basa en la siguiente relación isoterma:
| Símbolo | Nombre |
|---|---|
| Volumen parcial de cualquier componente de gas individual () | |
| Volumen total de la mezcla de gases | |
| Presión parcial del gas () | |
| Presión total de la mezcla de gases | |
| Cantidad de sustancia de gas () | |
| Cantidad total de sustancia en la mezcla de gases |
Volumen parcial (ley de Amagat del volumen aditivo)[editar]
El volumen parcial de un gas particular en una mezcla es el volumen de un componente de la mezcla de gas. Es útil en mezclas de gases, por ejemplo, aire, para concentrarse en un componente de gas en particular, por ejemplo, oxígeno.
Puede ser aproximado tanto de la presión parcial como de la fracción molar:[7]
- Vx es el volumen parcial de un componente de gas individual X en la mezcla
- Vtot es el volumen total de la mezcla de gases.
- px es la presión parcial del gas X
- ptot es la presión total de la mezcla de gases
- nx es la cantidad de sustancia del gas X
- ntot es la cantidad total de sustancia en la mezcla de gases
Presión de vapor[editar]
La presión de vapor es la presión de un vapor en equilibrio con sus fases sin vapor (es decir, líquido o sólido). Más a menudo, el término se usa para describir la tendencia de un líquido a evaporarse. Es una medida de la tendencia de las moléculas y los átomos a escapar de un líquido o un sólido. El punto de ebullición de la presión atmosférica de un líquido corresponde a la temperatura a la que su presión de vapor es igual a la presión atmosférica circundante y, a menudo, se denomina punto de ebullición normal.
Cuanto mayor sea la presión de vapor de un líquido a una temperatura dada, menor será el punto de ebullición normal del líquido.
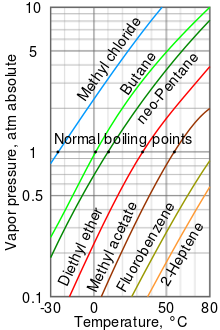
El gráfico de presión de vapor que se muestra tiene gráficos de las presiones de vapor en función de las temperaturas para una variedad de líquidos.[8] Como puede verse en la tabla, los líquidos con las presiones de vapor más altas tienen los puntos de ebullición normales más bajos.
Por ejemplo, a cualquier temperatura dada, el cloruro de metilo tiene la presión de vapor más alta de cualquiera de los líquidos en la tabla. También tiene el punto de ebullición normal más bajo (-24,2 °C), que es donde la curva de presión de vapor del cloruro de metilo (la línea azul) cruza la línea de presión horizontal de una atmósfera (atm) de presión de vapor absoluta. Tenga en cuenta que a mayores altitudes, la presión atmosférica es inferior a la del nivel del mar, por lo que se reducen los puntos de ebullición de los líquidos. En la cima del Monte Everest, la presión atmosférica es de aproximadamente 0,333 atm, por lo que al usar el gráfico, el punto de ebullición del éter dietílico sería de aproximadamente 7,5 °C contra 34,6 °C a nivel del mar (1 atm).
Constantes de equilibrio de reacciones involucrando mezclas de gases[editar]
Es posible calcular la constante de equilibrio para una reacción química que involucra una mezcla de gases dada la presión parcial de cada gas y la fórmula de reacción general. Para una reacción reversible que involucre reactivos de gas y productos de gas, tales como:
La constante de equilibrio de la reacción sería:
| Símbolo | Nombre |
|---|---|
| Constante de equilibrio de la reacción | |
| Coeficiente de reactivo | |
| Coeficiente de reactivo | |
| Coeficiente de producto | |
| Coeficiente de producto | |
| Presión parcial de | |
| Presión parcial de | |
| Presión parcial de | |
| Presión parcial de |
Para reacciones reversibles, los cambios en la presión total, la temperatura o las concentraciones de reactantes cambiarán el equilibrio para favorecer el lado derecho o izquierdo de la reacción de acuerdo con el Principio de Le Chatelier. Sin embargo, la cinética de la reacción puede oponerse o mejorar el cambio de equilibrio. En algunos casos, la cinética de reacción puede ser el factor primordial a considerar.
La ley de Henry y la solubilidad de los gases[editar]
Los gases se disolverán en los líquidos en una medida determinada por el equilibrio entre el gas no disuelto y el gas que se ha disuelto en el líquido (llamado solvente ).[9] La constante de equilibrio para ese equilibrio es:
- (1)
donde: = la constante de equilibrio para el proceso de solvatación. = presión parcial del gas en equilibrio con una solución que contiene algo del gas = la concentración del gas en la solución líquida
La forma de la constante de equilibrio muestra que la concentración de un gas soluto en una solución es directamente proporcional a la presión parcial de ese gas sobre la solución . Esta declaración es conocida como la ley de Henry y la constante de equilibrio. es a menudo referido como la constante de la ley de Henry.[9][10][11]
La ley de Henry se escribe a veces como:[12]
- (2)
dónde también se conoce como la constante de la ley de Henry.[12] Como puede verse comparando las ecuaciones (1) y (2) anteriores, es el recíproco de . Dado que ambos pueden ser denominados como la constante de la ley de Henry, los lectores de la literatura técnica deben tener mucho cuidado de notar qué versión de la ecuación de la ley de Henry se está utilizando. La ley de Henry es una aproximación que solo se aplica para soluciones diluidas, ideales y para soluciones donde el solvente líquido no reacciona químicamente con el gas que se disuelve.
En buceo[editar]
En el buceo, los efectos fisiológicos de los componentes individuales de los gases respiratorios son una función de la presión parcial.
Usando términos de buceo, la presión parcial se calcula como:
Para el gas componente "i":
Por ejemplo, a 50 metros (164 pies) bajo el agua, la presión absoluta total es 6 bares (600 kPa) (es decir, 1 bar de presión atmosférica + 5 bar de presión de agua) y las presiones parciales de los componentes principales del aire, oxígeno 21 % en volumen y nitrógeno aproximadamente 79 % en volumen son:
- ppN2 = 6 bar × 0,79 = 4,7 bar absoluto
- ppO2 = 6 bar × 0,21 = 1,3 bar absoluto
| donde: | |
| ppi | = presión parcial del componente de gas i = |
|---|---|
| PAG | = presión total = |
| Fi | = fracción de volumen del componente de gas i = fracción molar, |
| ppN2 | = presión parcial de nitrógeno = |
| ppO2 | = presión parcial de oxígeno = |
El límite inferior de seguridad mínimo para las presiones parciales de oxígeno en una mezcla de gases es de 0,16 bares (16 kPa) absoluto. La hipoxia y la inconsciencia repentina se convierten en un problema con una presión parcial de oxígeno de menos de 0,16 bar absolutos. La toxicidad por oxígeno, que involucra convulsiones, se convierte en un problema cuando la presión parcial de oxígeno es demasiado alta. El Manual de Buceo de la NOAA recomienda una exposición única máxima de 45 minutos a 1,6 bar absolutos, de 120 minutos a 1,5 bar absolutos, de 150 minutos a 1,4 bar absolutos, de 180 minutos a 1,3 bar absolutos y de 210 minutos a 1,2 bar absolutos. La toxicidad del oxígeno se convierte en un riesgo cuando se superan estas presiones y exposiciones parciales de oxígeno. La presión parcial de oxígeno determina la profundidad máxima de operación de una mezcla de gases.La narcosis es un problema cuando se respiran gases a alta presión. Por lo general, la presión parcial total máxima de los gases narcóticos utilizados al planificar el buceo técnico puede ser de alrededor de 4,5 bar absolutos, basada en una profundidad narcótica equivalente de 35 metros (114,8 pies).El efecto de un contaminante tóxico como el monóxido de carbono en el gas respirable también está relacionado con la presión parcial cuando se respira. Una mezcla que puede ser relativamente segura en la superficie podría ser peligrosamente tóxica en la profundidad máxima de una inmersión, o un nivel tolerable de dióxido de carbono en el circuito de respiración de un rebreather de buceo puede llegar a ser intolerable en segundos durante el descenso cuando la presión parcial aumenta, y podría llevar al pánico o incapacitación del buceador.
En medicina[editar]
Las presiones parciales de oxígeno en particular ( ) y dióxido de carbono ( ) son parámetros importantes en las pruebas de gases en sangre arterial , pero también pueden medirse en, por ejemplo, líquido cefalorraquídeo.
| Unidad | Gasometría arterial | Gas de sangre venosa | Fluido cerebroespinal | Presiones de gases pulmonares alveolares | |
|---|---|---|---|---|---|
| kPa | 11–13[13] | 4,0–5,3[13] | 5,3–5,9[13] | 14,2 | |
| mmHg | 75–100[14] | 30–40[15] | 40–44[16] | 107 | |
| kPa | 4,7–6,0[13] | 5,5–6,8[13] | 5,9–6,7[13] | 4,8 | |
| mmHg | 35–45[14] | 41–51[15] | 44–50[16] | 36 |
Véase también[editar]
| Destilación | |
|---|---|
| |
| Ramas | |
| Ley de Raoult / Ley de Dalton / Reflujo / Ecuación de Fenske / Método de McCabe-Thiele / Plato teórico / Presión parcial / Equilibrio vapor-líquido | |
| Procesos industriales | |
| Métodos de laboratorio | |
| Técnicas | |
Referencias[editar]
- ↑ Charles Henrickson (2005). Chemistry. Cliffs Notes. ISBN 0-7645-7419-1.
- ↑ «Gas Pressure and Respiration». Lumen Learning.
- ↑ Staff. «Symbols and Units». Respiratory Physiology & Neurobiology : Guide for Authors. Elsevier. Consultado el 3 de junio de 2017. «All symbols referring to gas species are in subscript,».
- ↑ IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book"). Compiled by A. D. McNaught and A. Wilkinson. Blackwell Scientific Publications, Oxford (1997). XML on-line corrected version: http://goldbook.iupac.org (2006-) created by M. Nic, J. Jirat, B. Kosata; updates compiled by A. Jenkins. ISBN 0-9678550-9-8. https://doi.org/10.1351/goldbook. Last update: 2014-02-24; version: 2.3.3. DOI of this term: https://doi.org/10.1351/goldbook.P04819.
- ↑
- ↑
- ↑ Página 200 en: Biofísica médica. Flemming Cornelius. 6ª edición, 2008.
- ↑ Perry, R.H. and Green, D.W. (Editors) (1997). Perry's Chemical Engineers' Handbook (7th edición). McGraw-Hill. ISBN 0-07-049841-5.
- ↑ a b
- ↑ Francis L. Smith; Allan H. Harvey (September 2007). «Avoid Common Pitfalls When Using Henry's Law». CEP (Chemical Engineering Progress). ISSN 0360-7275.
- ↑ «Introductory University Chemistry, Henry's Law and the Solubility of Gases». Archivado desde el original el 4 de mayo de 2012. Consultado el 29 de enero de 2019.
- ↑ a b Notas de clase de química de la Universidad de Arizona Archivado el 7 de marzo de 2012 en Wayback Machine.
- ↑ a b c d e f Derivado de los valores de mmHg utilizando 0,133322 kPa / mmHg
- ↑ a b Normal Reference Range Table Archivado el 25 de diciembre de 2011 en Wayback Machine. from The University of Texas Southwestern Medical Center at Dallas. Used in Interactive Case Study Companion to Pathologic basis of disease.
- ↑ a b La División de Educación Médica de Brookside Associates -> ABG (Gasometría Arterial) obtenido el 6 de diciembre de 2009
- ↑ a b [https://web.archive.org/web/20120222145250/http://www.pathology.ubc.ca/path425/SystemicPathology/Neuropathology/CerebrospinalFluidCSFDrGPBondy.rtf Archivado el 22 de febrero de 2012 en Wayback Machine. PATHOLOGY 425 CEREBROSPINAL FLUID [CSF]] (enlace roto disponible en este archivo). at the Department of Pathology and Laboratory Medicine at the University of British Columbia. By Dr. G.P. Bondy. Retrieved November 2011


























































