Hidrocortisona
| Hidrocortisona | ||
|---|---|---|
 | ||
 | ||
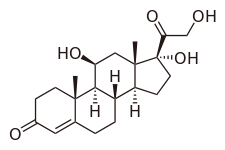
| Nombre (IUPAC) sistemático | ||
| (11β)-11,17,21-trihidroxipregn-4-eno-3,20-diona | ||
| Identificadores | ||
| Número CAS | 50-23-7 | |
| Código ATC | A01AC03 | |
| PubChem | 5754 | |
| DrugBank | DB00741 | |
| ChemSpider | 5551 | |
| UNII | WI4X0X7BPJ | |
| KEGG | D00088 | |
| ChEBI | 17650 | |
| ChEMBL | 389621 | |
| Datos químicos | ||
| Fórmula | C21H30O5 | |
| Peso mol. | 362,460 g/mol | |
|
O=C4\C=C2/[C@]([C@H]1[C@@H](O)C[C@@]3([C@@](O)(C(=O)CO)CC[C@H]3[C@@H]1CC2)C)(C)CC4
| ||
|
InChI=1S/C21H30O5/c1-19-7-5-13(23)9-12(19)3-4-14-15-6-8-21(26,17(25)11-22)20(15,2)10-16(24)18(14)19/h9,14-16,18,22,24,26H,3-8,10-11H2,1-2H3/t14-,15-,16-,18+,19-,20-,21-/m0/s1
Key: JYGXADMDTFJGBT-VWUMJDOOSA-N | ||
| Sinónimos | Cortisol; 11β,17α,21-Trihidroxipregn-4-eno-3,20-diona | |
| Datos clínicos | ||
| Cat. embarazo | A (AU) No hay estudios en humanos. El fármaco solo debe utilizarse cuando los beneficios potenciales justifican los posibles riesgos para el feto. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | S4 (AU) ? (UK) OTC (EUA) | |
| Vías de adm. | Oral (tabletas), intravenosa, tópica, rectal | |
La hidrocortisona, que se vende con varios nombres comerciales, es el nombre de la hormona cortisol cuando se suministra como medicamento.[1] Los usos incluyen afecciones como insuficiencia adrenocortical, síndrome adrenogenital, calcio en sangre elevado, tiroiditis, artritis reumatoide, dermatitis, asma y EPOC.[2] Es el tratamiento de elección para la insuficiencia adrenocortical.[3] Se puede administrar por vía oral, por vía tópica o por inyección.[2] La interrupción del tratamiento después de un uso prolongado debe hacerse lentamente.[2]
Los efectos secundarios pueden incluir cambios en el estado de ánimo, mayor riesgo de infección e hinchazón.[2] Con el uso a largo plazo, los efectos secundarios comunes incluyen osteoporosis, malestar estomacal, debilidad física, moretones con facilidad e infecciones por hongos.[2] Mientras se usa, no está claro si es seguro durante el embarazo.[4] Funciona como un antiinflamatorio y supresor inmunológico.[2]
La hidrocortisona fue descubierta en 1955.[5] Está en la Lista de medicamentos esenciales de la Organización Mundial de la Salud, los medicamentos más efectivos y seguros que se necesitan en un sistema de salud.[6] Está disponible como un medicamento genérico.[2] El costo mayorista en países en vías desarrollo es de aproximadamente US$0,27 por día para el año 2014 para la fórmula oral.[7] En los Estados Unidos cuesta menos de US$25 para un mes típico de tratamiento.[3]
Farmacología[editar]
Hidrocortisona es el término farmacéutico para el cortisol utilizado en la administración oral, la inyección intravenosa o la aplicación tópica. Se usa como un fármaco inmunosupresor, administrado por inyección en el tratamiento de reacciones alérgicas graves como anafilaxis y angioedema, en lugar de prednisolona en pacientes que necesitan tratamiento con esteroides pero no pueden tomar medicamentos orales, y perioperatoriamente en pacientes que reciben tratamiento con esteroides a largo plazo para prevenir la enfermedad de Addison. También se puede inyectar en articulaciones inflamadas como resultado de enfermedades como la gota.
En comparación con la hidrocortisona, la prednisolona es aproximadamente cuatro veces más fuerte y la dexametasona aproximadamente cuarenta veces más fuerte en su efecto antiinflamatorio.[8] La prednisolona también se puede usar como reemplazo del cortisol, y a niveles de dosis de reemplazo (en lugar de niveles antiinflamatorios), la prednisolona es aproximadamente ocho veces más potente que el cortisol.[9] Para efectos secundarios, ver corticosteroides y prednisolona.
Se puede usar tópicamente para erupciones alérgicas, eccema, psoriasis, picazón y otras afecciones inflamatorias de la piel. Las cremas tópicas de hidrocortisona y los ungüentos están disponibles en la mayoría de los países sin receta médica en concentraciones que van del 0,05% al 2,5% (según las regulaciones locales) con formas más potentes disponibles solo con receta. Cubrir la piel después de la aplicación aumenta la absorción y el efecto. Esta mejora a veces se prescribe, pero de lo contrario se debe evitar para no llevar a una sobredosis y un impacto sistémico.
Enlace proteico[editar]
La mayoría del cortisol sérico (todo menos el 4%) está unido a proteínas, incluida la globulina de unión a corticosteroides (CBG) y la albúmina sérica. El cortisol libre pasa fácilmente a través de las membranas celulares, donde se une a los receptores de cortisol intracelular.[10]
Química[editar]
La hidrocortisona, también conocida como 11β, 17α, 21-trihidroxipregn-4-eno-3,20-diona, es un esteroide de pregnano natural .[11]
Efectos adversos[editar]
Se conocen principalmente los siguientes:
- distribución anormal de grasas (obesidad troncal, cara de luna llena, etc.)
- hiperglucemia
- diabetes por esteroides
- hipercolesterolemia
- hipertrigliceridemia
- retraso del crecimiento en niños
Referencias[editar]
- ↑ Becker, Kenneth L. (2001). Principles and Practice of Endocrinology and Metabolism (en inglés). Lippincott Williams & Wilkins. p. 762. ISBN 9780781717502.
- ↑ a b c d e f g «Hydrocortisone». Drugs.com. American Society of Health-System Pharmacists. 9 de febrero de 2015. Archivado desde el original el 20 de septiembre de 2016. Consultado el 30 de agosto de 2016.
- ↑ a b Hamilton, Richart (2015). Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. p. 202. ISBN 9781284057560.
- ↑ «Hydrocortisone Pregnancy and Breastfeeding Warnings». Drugs.com. Archivado desde el original el 20 de septiembre de 2016. Consultado el 1 de septiembre de 2016.
- ↑ Walker, S. R. (2012). Trends and Changes in Drug Research and Development (en inglés). Springer Science & Business Media. p. 109. ISBN 9789400926592.
- ↑ «WHO Model List of Essential Medicines (19th List)». World Health Organization. April 2015. Archivado desde el original el 13 de diciembre de 2016. Consultado el 8 de diciembre de 2016.
- ↑ «Hydrocortisone». International Drug Price Indicator Guide. Consultado el 1 de septiembre de 2016.
- ↑ «Dexamethasone». drugs.com. Archivado desde el original el 21 de junio de 2013. Consultado el 14 de junio de 2013.
- ↑ Caldato, Milena C. F.; Fernandes, Vânia T.; Kater, Claudio E. (1 de octubre de 2004). «One-year clinical evaluation of single morning dose prednisolone therapy for 21-hydroxylase deficiency». Arquivos Brasileiros de Endocrinologia e Metabologia 48 (5): 705-712. ISSN 0004-2730. PMID 15761542. doi:10.1590/S0004-27302004000500017.
- ↑ Medical Physiology (2nd edición). Philadelphia: Saunders. 2011. ISBN 1-4377-1753-5.
- ↑ J. Elks (14 de noviembre de 2014). The Dictionary of Drugs: Chemical Data: Chemical Data, Structures and Bibliographies. Springer. p. 316. ISBN 978-1-4757-2085-3.
