Pila de combustible

Pila de combustible, también llamada célula de combustible o celda de combustible, (comúnmente nombrada fuel cell en inglés) es un dispositivo electroquímico en el cual un flujo continuo de combustible y oxidante sufren una reacción química controlada que da lugar a los productos y suministra directamente corriente eléctrica a un circuito externo.
Se trata de un dispositivo electroquímico de conversión de energía similar a una batería. Se diferencia en que está diseñada para permitir el abastecimiento continuo de los reactivos consumidos. Es decir, produce electricidad de una fuente externa de combustible y de oxígeno[1] u otro agente oxidante, en contraposición a la capacidad limitada de almacenamiento de energía que posee una batería. Además, en una batería los electrodos reaccionan y cambian según cómo esté de cargada o descargada; en cambio, en una celda de combustible los electrodos son catalíticos y relativamente estables.
El proceso electroquímico que tiene lugar es de alta eficiencia y mínimo impacto ambiental. En efecto, dado que la obtención de energía en las pilas de combustible está exenta de cualquier proceso térmico o mecánico intermedio, estos dispositivos alcanzan eficiencias mayores que las máquinas térmicas, que están limitadas por la eficiencia del Ciclo de Carnot. En general, la eficiencia energética de una pila de combustible está entre 40-60 %, y puede llegar hasta un > 85%-90 % en cogeneración, si se captura el calor residual para su uso. Por otra parte, dado que el proceso no implica la combustión de los reactivos, las emisiones contaminantes son mínimas.[2]
Es importante establecer las diferencias fundamentales entre las pilas convencionales y las pilas de combustible. Las baterías convencionales son dispositivos de almacenamiento de energía: en su interior hay unos reactivos que producen energía hasta que se consumen. Sin embargo, en la pila de combustible los reactivos se suministran como un flujo continuo desde el exterior, lo que permite generar energía de forma ininterrumpida.
En principio, las pilas de combustible podrían procesar una amplia variedad de reductores y oxidantes. Puede ser un reductor cualquier sustancia que se pueda oxidar en una reacción química y que se pueda suministrar de forma continua (como un fluido) al ánodo de una pila de combustible. Del mismo modo, el oxidante podría ser cualquier fluido que se pueda reducir (a una velocidad adecuada) en la reacción química que tiene lugar en el cátodo.[3]
Una de las primeras aplicaciones prácticas de las células de combustible fue en vehículos espaciales, basadas en la reacción de hidrógeno y oxígeno, dando como resultado agua, la cual puede usarse por los astronautas para beber, o para refrigerar los sistemas de la nave.[4]
El mercado de las pilas de combustible está creciendo. Pike Research estimaba que en 2020 se comercializarán pilas de combustible estacionarias, alcanzando todas ellas una potencia conjunta de 50 Gw.[5]
El fabricante de automóviles japonés Honda, la única firma que ha obtenido la homologación en Japón y Estados Unidos para comercializar su vehículo impulsado por este sistema, el FCX Clarity, ha desarrollado también la (HES) Home Energy Station (en:), un sistema autónomo y doméstico que permite obtener hidrógeno a partir de gas natural para repostar vehículos de pila de combustible y aprovecha el proceso para generar electricidad y agua caliente para el hogar.
Historia[editar]
Aunque parezca algo muy reciente, la historia de las pilas de combustible comenzó hace casi dos siglos, en 1838,[6] con los primeros estudios del científico Christian Friedrich Schönbein en Suiza y, paralelamente, con los del físico y jurista galés Sir William Robert Grove sobre baterías gaseosas, cuyos resultados publicaría en 1843. Hoy en día, se continúa con el empleo de estas células en diversas aplicaciones, tanto portátiles (ejemplo: teléfonos móviles) como estacionarias (ejemplo: generación de energía para edificios), así como en diversos medios de transporte (desde submarinos hasta vehículos particulares). Sin embargo, su desarrollo ha atravesado periodos de olvido, debido a las numerosas dificultades técnicas que presentan en comparación con otros métodos de obtención de electricidad. El interés por las células de combustible, y por tanto su desarrollo, se ha dado en periodos de escasez de recursos energéticos - por ejemplo, la crisis del petróleo de 1973 que precipita el desarrollo de tecnologías alternativas de energía, incluyendo las células de combustible[7] -. Esto se debe a que estas células, comparadas con otros dispositivos, tienen mayor eficiencia energética y por tanto necesitan menos combustible para producir la misma energía.
1843[editar]
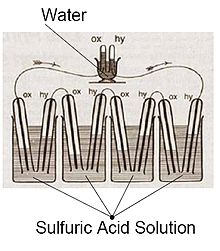
En la figura se muestra el dispositivo presentado a la comunidad científica por William Robert Grove en su publicación "On the Gas Voltaic Battery".[8][9] Para su preparación, utilizó dos electrodos de platino sumergidos en ácido sulfúrico, que alimentaba con oxígeno e hidrógeno, respectivamente. A partir de la disociación del H2SO4, la reducción tenía lugar en el electrodo alimentado con O2 (cátodo), que reaccionaba con los iones H+ formando agua. En esta reacción intervenían los electrones, que se generaban en el ánodo durante la oxidación del H2, que reaccionaba con el ion SO42- para formar ácido sulfúrico[2]. Grove conectó eléctricamente cincuenta de estas celdas, generando el potencial suficiente como para producir la reacción de electrólisis del agua.
1882[editar]
El físico británico Lord Rayleigh mejoró esta configuración original. Rayleigh se interesó por los trabajos de Grove y en 1882 presentó una nueva versión más eficiente, debido al aumento de la superficie de contacto entre el platino, los gases reactivos y el electrolito.[10]
Ludwig Mond y Charles Langer utilizaron por primera vez el término "pila de combustible" para referirse a este tipo de dispositivos. En 1889, estos dos científicos realizaron un gran avance, resolviendo el problema asociado a la inmersión de los electrodos en el electrolito líquido y por tanto, a la dificultad del acceso de los gases reactivos a los puntos activos. Su prototipo permitía retener el electrolito en una matriz sólida no conductora, cuya superficie estaba cubierta por una fina capa de Platino u Oro.[10]
1950 y 1960[editar]
A mediados del siglo XX, el desarrollo tecnológico de estos dispositivos experimentó un gran avance. En 1954, el científico inglés Francis Thomas Bacon construyó una planta energética de 5 kW con una pila de combustible alcalina. La pila consistía en un ánodo de níquel, un cátodo de óxido de níquel y litio, y un electrolito de hidróxido de potasio concentrado al 85 %. Se alimentaba con hidrógeno y oxígeno.[11] Esta pila era capaz de accionar una máquina de soldadura. En los años 60, las patentes de Bacon (licenciadas por Pratt y Whitney en los Estados Unidos-al menos la idea original) se utilizaron en el programa espacial de Estados Unidos para proveer a los astronautas de electricidad y de agua potable, a partir del hidrógeno y oxígeno disponibles en los tanques de la nave espacial.
En 1959, un equipo encabezado por Harry Ihrig construyó un tractor basado en una célula de combustible de 15 kW para Allis-Chalmers. Se expuso en EE. UU. en las ferias del estado. Este sistema utilizó hidróxido de potasio como electrolito e hidrógeno y oxígeno comprimidos como reactivos.[12]
Paralelamente a Pratt & Whitney Aircraft, General Electric desarrolló la primera pila de membrana de intercambio de protones (PEMFCs) para las misiones espaciales Gemini de la NASA. La primera misión que utilizó PEFCs fue la Gemini V. Sin embargo, las misiones del Programa Apolo y las subsecuentes Apolo-Soyuz, del Skylab y del transbordador utilizaban celdas de combustible basadas en el diseño de Bacon, desarrollado por Pratt & Whitney Aircraft.[13]
1970 y 1980[editar]
Entre 1970 y 1980, como consecuencia de la crisis del petróleo y la búsqueda de tecnologías energéticas alternativas, se investiga en el desarrollo de los materiales necesarios, la identificación de las fuentes óptimas de combustible y la reducción drástica en el coste de la tecnología asociada a las pilas de combustible.
Durante la década de 1980, se comenzó a probar el uso de las células de combustible en los servicios públicos y también se intentó en la fabricación de automóviles. En la década de los 1990, se desarrollan grandes células de combustible estacionarias (fijas) para locales comerciales e industriales.
1993 y 2007[editar]
En 1993, la empresa canadiense Ballard desarrolló el primer vehículo comercial con pila de combustible, utilizando la tecnología PEM.[14]
En 2007, las células de combustible se comercializan para aplicaciones estacionarias y auxiliares. En 2008, Honda comienza la venta de un vehículo eléctrico basado en pila de combustible, FCX Clarity. Ese mismo año, se concede el Premio Nobel de Química a Gerhard Ertl, cuyos estudios permitieron conocer cómo funcionan las pilas de combustible.[cita requerida]
Panasonic fue la primera empresa en el mundo en vender la pila de combustible para uso doméstico. Desde su lanzamiento (mayo de 2009) hasta septiembre de 2013, vendió 31 000 unidades en Japón.[15]
2013[editar]
En 2013, se presenta una pila de combustible que podría representar la transición a las pilas asequibles. La empresa británica "ACAL Energy" ha desarrollado una pila de combustible que ha logrado un tiempo de ejecución de 10 000 horas en las pruebas de resistencia de una pila de combustible[16] utilizando su tecnología FlowCath. A diferencia del diseño de una pila de combustible convencional de hidrógeno, la tecnología FlowCath de ACAL no se basa en el platino como catalizador, ofreciendo así una alternativa de coste potencialmente menor. Ha sustituido el platino por un catalizador líquido patentado, que actúa como refrigerante y catalizador para las células y mejora radicalmente la durabilidad de la pila de combustible, al tiempo que reduce el coste del sistema.[17]
Tecnología[editar]
El funcionamiento de la pila de combustible es similar al de una batería. Se obtiene electricidad a partir de sustancias que reaccionan químicamente entre sí. Sin embargo, mientras que las baterías tienen una capacidad limitada de almacenamiento de energía, la pila de combustible está diseñada para permitir un abastecimiento continuo de los reactivos. Además, los electrodos de la pila de combustible actúan también como catalizadores de las reacciones químicas de oxidación/reducción.

Existen tipos muy distintos de pilas de combustibles. Para explicar su funcionamiento básico, se toma como ejemplo una de las más comunes, la denominada PEM (de membrana de intercambio protónico, en inglés Proton Exchange Membrane). El esquema básico de la celda unitaria de una pila PEM se muestra en la figura de la derecha. Consta de dos electrodos: el ánodo (donde se oxida el combustible) y el cátodo (donde el oxidante o comburente se reduce). El electrolito actúa simultáneamente como aislante eléctrico, conductor protónico y separador de las reacciones que tienen lugar en el cátodo respecto a las que tienen lugar en el ánodo. Debido a lo anterior, los electrones viajan desde el ánodo hasta el cátodo a través de un circuito externo, generando una corriente eléctrica, mientras que los protones lo hacen a través del electrolito. En el cátodo, los electrones, protones y el comburente se reducen, dando lugar a los productos. La reacción es exotérmica y, aunque es espontánea, suele ser muy lenta como para ser operativa sin la presencia de catalizadores. De hecho, lo más común es que los propios electrodos se utilicen como catalizadores. En este tipo de pilas se suele utilizar hidrógeno como agente reductor y oxígeno como oxidante.
Es importante mencionar que, para que los protones puedan atravesar la membrana, esta debe estar convenientemente humidificada, porque la conductividad protónica de las membranas poliméricas utilizadas en este tipo de pilas depende de la humedad de la membrana. Por lo tanto, es habitual humidificar los gases previamente al ingreso a la pila.
Además de hidrógeno puro, también se tiene el hidrógeno contenido en otras moléculas de combustibles incluyendo el diésel, metanol (véase DMFC) y los hidruros químicos. El residuo producido por este tipo de combustibles además de agua es dióxido de carbono, entre otros.
Las pilas de combustible se pueden clasificar en función del electrolito y del combustible elegido, lo que a su vez determina el tipo de reacciones que se llevarán a cabo en los electrodos y los tipos de iones que la corriente transportará a través del electrolito. Hoy en día, la mayoría de las células de combustible en desarrollo utilizan hidrógeno o gases sintéticos ricos en hidrógeno. El hidrógeno tiene una alta reactividad y puede obtenerse de formas muy diversas tanto a partir de combustibles fósiles o renovables, como a partir de un proceso electrolítico. Por razones prácticas, el oxidante más común es el oxígeno gaseoso, debido a su alta disponibilidad. Una ventaja de utilizar la combinación de hidrógeno con oxígeno, es que el único producto de la reacción es agua. Por esto, esta combinación es muy utilizada en aplicaciones espaciales. Además, oxígeno y el hidrógeno pueden almacenarse criogénicamente de forma compacta.
La diferencia de potencial generada por una sola unidad o monocelda es inferior a un voltio, por lo que hay que conectar en serie varias mono-pilas para obtener las tensiones adecuadas para las aplicaciones más comunes. Por lo tanto, en la práctica se utilizan sistemas de pilas de combustible.
Tensión[editar]
La tensión de celda depende de la corriente de carga. En circuito abierto, es de 1,2 voltios. Para crear suficiente tensión, las celdas se agrupan combinándolas en serie y en paralelo, en lo que en inglés se denomina "Fuel Cell Stack" (pila de células de combustible). Generalmente, se usan más de 45, aunque varían según el diseño.
Materiales[editar]
Los materiales usados en celdas de combustible varían según el tipo. Véase Tipos de pilas de combustible.
Las placas del electrodo/bipolar se hacen generalmente de nanotubos de metal, de níquel o de carbón, y están cubiertas por un catalizador (como el platino o el paladio) para conseguir una eficacia más alta.
El electrolito puede ser de cerámica o bien una membrana de electrolito polimérico híbrida. Ésta consta de dos polímeros distintos. Se disponen de forma que ambos constituyen una estructura donde uno de los polímeros (que es un polímero de siloxano), hace de base perforada para que el otro (un electrolito polimérico), se pueda distribuir en él las perforaciones en forma de canales.
Consideraciones de diseño en las pilas de combustible[editar]
- Costos. En 2002, las celdas típicas tenían un coste debido al catalizador de 850 € (aprox. 1000 USD) por kilovatio energía eléctrica útil; sin embargo, se espera que antes de 2007, se reduzca a unos 25 € (aprox. 30 USD) por kilovatio [3]. Gracias a un catalizador mejorado con seda de carbono (carbon silk), Ballard ha conseguido una reducción del 30% (1 mg/cm² a 0,7 mg/cm²) en la cantidad de platino, sin reducir su rendimiento (información de 2005)[4].
- Los costes MEA (del inglés Membrane Electrode Assembly, o montaje del electrodo de la membrana) del PEM (membrana intercambiadora de protones) varían según el fabricante. Así, la membrana de Nafion® de aprox. 400 €/m² utilizada en la membrana PEM de Toyota y 3M se está sustituyendo pora membrana de la ITM Power, con un precio alrededor de 4 €/m² (2004). Esta membrana nueva es un hidrocarburo-polímero. Una compañía holandesa que ha realizado grandes inversiones en este terreno está utilizando Solupor® (un film de polietileno poroso)[5].
- Gestión del agua en las PEMFC. En este tipo de celdas de combustible, la membrana debe hidratarse, requiriendo evaporar el agua exactamente en la misma medida en que se produce. Si el agua se evapora demasiado rápido, la membrana se seca, la resistencia a través suyo aumenta, y se agrietará, creando un "corto circuito" de gas donde el hidrógeno y el oxígeno se combinan directamente, generando calor que dañará la celda de combustible. Si el agua se evapora demasiado lentamente, los electrodos se inundarán, evitando que los reactivos puedan alcanzar el catalizador y se parará la reacción. Uno de los objetivos más importantes en la investigación sobre células de combustible es la adecuada gestión del agua.
- Gestión de la temperatura. Se debe mantener la misma temperatura en toda la celda para no destruir la celda por fatiga térmica.
- Control de flujo. Al igual que en un motor de combustión, hay que mantener una relación constante entre el reactivo y el oxígeno para que la celda funcione eficientemente.
- Durabilidad, vida, y requisitos especiales para ciertos tipos de celdas. Los usos estacionarios requieren normalmente más de 40.000 horas operativas fiables a una temperatura de -35 °C a 40 °C, mientras que las células de combustible para automoción requieren al menos de 5000 horas (el equivalente a unos 200.000 kilómetros) bajo temperaturas extremas. (Véase: Vehículo de hidrógeno). Además, las aplicaciones para automoción deben permitir el arranque en frío hasta -30 °C y poseer una alta potencia por unidad de volumen (típicamente 2.5 kW por litro).
- Tolerancia limitada al CO (monóxido de carbono).
Sistemas de pilas de combustible[editar]
Celda unitaria[editar]
La celda unitaria o mono-pila es el elemento básico de un sistema basado en pilas de combustible. Los elementos que la componen se describen a continuación:
- Electrolito. Es a la vez conductor iónico, aislante eléctrico y separador del cátodo y el ánodo. Atendiendo al estado de agregación en que se encuentre el electrolito, podemos encontrarnos con dos tipos de combustible. Así, según Appleby y Foulkes,[18] tenemos:
- Pilas de combustible de electrolito líquido. En este tipo, los electrodos son porosos y el electrolito está en contacto con éstos, empapando pequeñas zonas. Los reactivos gaseosos se difunden a través de una delgada capa de electrolito y reaccionan electroquímicamente en las superficies de los electrodos. La cantidad de electrolito que puede contener el electrodo es limitada. Por tanto, un exceso de líquido podría impedir el transporte de las especies gaseosas y también las reacciones necesarias para la obtención de energía.
- Pilas de combustible de electrolito sólido. Este tipo contiene un elevado número de catalizadores en la interfaz, que deben estar eléctrica y iónicamente conectados a los electrodos y al electrolito respectivamente, y que además, están eficientemente expuestos a los reactivos gaseosos.
- Electrodos. Las reacciones electroquímicas tienen lugar en la superficie de los electrodos. El combustible se oxida en el ánodo y el oxígeno se reduce en el cátodo. Los electrodos suelen ser porosos, para permitir la difusión gaseosa (aunque existen algunos no porosos[19]). De esta forma, puede establecerse un buen contacto entre las tres fases que participan en la reacción (la sólida del electrodo, la gaseosa del combustible y la líquida o sólida del electrolito). Las funciones principales de los electrodos son:
- Conducir o desalojar los iones de la interfase ternaria.
- Asegurar que los reactivos gaseosos se distribuyan uniformemente en el electrolito.
- Asegurar que los productos de la reacción se llevan de forma eficiente hacia la fase gaseosa.
Apilamientos[editar]
Dado que la diferencia de potencial generada por una única pila de combustible es pequeña (0.7 voltios aproximadamente), en la práctica se combinan varias en serie para conseguir el voltaje de salida adecuado a la aplicación deseada. Lógicamente, las interconexiones entre las pilas unitarias se realizan mediante materiales con alta conductividad eléctrica. De entre los numerosos tipos de apilamientos o "stacks" (en inglés) posibles, los más usuales son los que tienen estructura plana, aunque también los hay tubulares.


En los apilamientos de estructura plana, normalmente se incluyen unos elementos conocidos como en "platos bipolares" (ver Celdas de Combustible (animaciones)). Constan de dos platos separadores situados en los extremos del sistema. mediante los que se hacen las conexiones. Uno actúa como ánodo y otro como cátodo. Además, estos platos separan el combustible y el oxidante de las celdas adyacentes, proporcionando a su vez un excelente medio para el suministro estos reactivos. En muchos diseños, las placas incluyen canales (ver figura de la derecha) que permiten la distribución uniforme del flujo de gas sobre las celdas. Este diseño es bastante simple eléctricamente: el camino que recorre la corriente eléctrica es relativamente corto y, por tanto, ofrece poca resistencia al paso de los electrones, y por consiguiente poca caída de tensión.
Otro tipo de apilamiento, especialmente indicado para pilas de combustible que trabajen a altas temperaturas (como las de óxido sólido-SOFC), consiste en una configuración tubular (figura de la izquierda). Este tipo de pilas suelen utilitzar como electrolito un material cerámico sólido, tal como óxido de circonio estabilizado con óxido de itrio, en lugar de un líquido o de una membrana de intercambio.
Sistemas basados en pilas de combustible[editar]
Si bien la propia pila de combustible es el componente clave, un sistema basado en pilas de combustible debe incluir otros subsistemas y componentes, conocidos como balance de planta (en inglés; balance of plant o BOP). Un sistema basado en pilas de combustible está formado entonces por apilamiento de pilas de combustible y por un BOP, debidamente combinados. Existe una gran variedad de configuraciones para este tipo de sistemas. En efecto, la composición y disposición precisa de los elementos del BOP depende en gran medida del tipo de pila de combustible, de la temperatura de operación, del combustible elegido y de la aplicación para la que se utilice. Además, las condiciones de operación específicas y los requisitos de la celda individual y el diseño del apilamiento, determinan las características del BOP.

Sin embargo, aun teniendo en cuenta la diversidad y flexibilidad de estos sistemas, conviene mostrar al menos un ejemplo de cuáles son los componentes (o etapas) de los que consta un sistema basado en pilas de combustibles. En la figura se muestra un esquema de un sistema genérico basado en pilas de combustible. Como puede observarse, en la primera etapa, el combustible (hidrógeno, gas natural, metano, etc.) se introduce en el reformador en el que, mediante una transformación química, se produce un gas rico en hidrógeno conocido como "reformado" y como subproducto, monóxido de carbono con un nivel de concentración menor a 50 ppm.
La siguiente etapa se desarrolla en el sistema purificador de gas, donde se eliminan las impurezas que pudiera tener el reformado. Una vez purificado el hidrógeno, está listo para introducirse en la pila de combustible. En esta etapa se genera la energía eléctrica, mediante la reacción electroquímica con el oxígeno. El calor generado en la reacción se puede aprovechar para utilizarlo para precalentar el combustible. En el caso de pilas de combustible que operen a alta temperatura (entre 600-1000 °C), el calor generado podría invertirse en cogeneración, es decir, se puede utilizar para mover turbinas de gas y generar más electricidad, para unidades de desulfuración, generación de productos químicos, etc.[20]
Tipos de pilas de combustible[editar]
Actualmente existe una gran variedad de pilas de combustible en diferentes etapas de desarrollo. Por ello, se pueden clasificar atendiendo a numerosas características. Las más comunes son las siguientes:[21]
- Según el tipo de combinación de combustible y oxidante. Los combustibles típicos son el hidrógeno molecular y el metanol, y normalmente oxígeno o aire como oxidante. Pero como se ha visto en la figura 2.4, se pueden alimentar con una amplia variedad de combustibles, como hidrógeno, metanol, biomasa, gasolina, carbón, etc.
- Según el tipo de electrolito usado. Por ejemplo: ácido fosfórico, membrana de polímero sólido, solución alcalina, etc.
- Según la temperatura de operación. Por un lado, tenemos pilas de combustible de baja o media temperatura (con temperaturas inferiores a 200 °C), como las PEM, las AFC y las PAFC. Por otro, las de alta temperatura, que sobrepasan los 600 °C, como las MCFC y las SOFC. Según la fuente que se consulte, los rangos son ligeramente distintos, por lo que esta clasificación no es estricta.
- Según su eficiencia. En este caso, el rango es distinto dependiendo del tipo de pila y del tipo de aplicación en la que se utilice. Por ejemplo, para una PEM tiene una eficiencia en torno a un 40%[21] en aplicaciones estacionarias y en torno a un 60% en aplicaciones para el transporte.
- Según el tipo de uso. Aplicaciones portátiles, estacionarias, de transporte, militares, espaciales, etc.
- Según su potencia. Pilas de baja potencia (alrededor de 5 kW en el caso de las DMFC, por ejemplo) y de alta potencia (100 kW a 2 MW en las SOFC, por ejemplo).[22]
- Según el catalizador utilizado. Típicamente, platino, metales no preciosos o el propio material de los electrodos. También pueden ser de paladio.[23]
La forma más usual de clasificación es por el tipo de electrolito que utilizan. Se pueden entonces establecer,[21] cinco tipos principales de pilas, que se describen a continuación.
Pila de Combustible de Membrana de intercambio protónico (PEM)[editar]

- Electrolito: membrana de polímero sólido
- Catalizador: platino.
- Temperatura de operación: alrededor de los 80-95 °C
- Eficiencia eléctrica: 40-60%

Las PEM operan a temperaturas relativamente bajas, tienen una alta densidad de potencia y, además, pueden variar rápidamente su potencia de salida para adaptarse a la demanda energética. Existen PEMs con potencias que varían entre unos pocos vatios hasta varios kilovatios, por lo que se pueden utilizar en multitud de sistemas. Así, hasta 2013 la máxima potencia conseguida con una planta de energía estacionaria (instalación de energía fija) tipo PEM es de 1 MW, y fue instalada por la empresa japonesa Honda[6]
Los sistemas de pilas de combustible tipo PEM son adecuados para aplicaciones que requieran una respuesta de funcionamiento rápida. Así, se utilizan en una amplia variedad de sistemas que se centran en el mercado de las telecomunicaciones (tanto a nivel industrial como casero) y en vehículos para el transporte de materiales, como los montacargas. También se utilizan en autobuses y se espera que entre 2014-2016 se puedan comercializar vehículos de pasajeros (turismos como el mostrado en la figura) de PEM. Las PEMs pueden utilizar como combustible hidrógeno, metanol o combustibles reformados.
En las PEM, el electrolito es una membrana de polímero sólido que contiene ácidos sulfónicos perfluorados, y debe mantenerse completamente hidratada durante la operación para favorecer la conducción de los protones. Este requerimiento limita la temperatura de operación por debajo de 100 °C y es fundamental para obtener una buena eficiencia. Al ser agua el único líquido utilizado, los problemas de corrosión son mínimos.[22]
Los principales retos actuales en el desarrollo de este tipo de pilas son: disminuir el coste y aumentar la eficiencia (lo que se traduce en reducir el espesor de la capa catalítica de platino y optimizar la dispersión del catalizador); mejorar las prestaciones de la membrana polimérica (aumentar la conductividad iónica y capacidad de retención de agua); y encontrar un material alternativo al grafito para la placa bipolar que sea de alta conductividad eléctrica y térmica, resistente a la corrosión, más ligero y económico.[22]
Membrana de intercambio protónica de alta temperatura (High-temperature PEM o HT-PEM)
Las HT-PEMs son, en esencia, PEMs que pueden operar a altas temperaturas, entre 120 °C y 200 °C. Se suelen utilizar en vehículos y, menos habitualmente, para suministrar energía a edificios. A menudo, las HT-PEMs integran un reformador (es decir, un dispositivo capaz de reformar combustibles fósiles o alcoholes en gas sintético formado principalmente por hidrógeno y monóxido de carbono), lo que permite alimentarlas con una mayor variedad de combustibles.
Pila de combustible de Metanol (DMFC)[editar]

- Electrolito: membrana de polímero sólido.
- Catalizador: Platino.
- Temperatura de operación: alrededor de los 50-120 °C.
- Eficiencia eléctrica: por encima del 40%.
Al igual que las PEMs, las DMFC utilizan como electrolito una membrana de polímero. Sin embargo, en los sistemas DMFC no es necesario que el combustible pase por un reformador, ya que el propio ánodo catalizador extrae el hidrógeno del metanol líquido. Dado que la temperatura mínima de operación de este tipo de pilas es baja, las DMFC se pueden utilizar en aplicaciones de pequeño tamaño, como teléfonos móviles (ver figura de la izquierda), ordenadores portátiles y cargadores de baterías para otros productos electrónicos [7] Archivado el 14 de julio de 2014 en Wayback Machine., y también en aplicaciones de tamaño medio para alimentar la electrónica de barcos o cabañas.
En este tipo de pilas, el reto consiste en encontrar una membrana que permita trabajar a temperatura superior a los 130 °C y que no presente problemas de “crossover” (paso del reactante anódico al compartimiento catódico a través de la membrana) y en encontrar un catalizador anódico más activo para la oxidación directa de metanol.[22]
Celdas de Combustible Alcalinas (AFC)[editar]

- Electrolito: una solución de hidróxido de potasio en agua.
- Catalizador: se puede usar una gran variedad de metales no preciosos.
- Temperatura de operación: entre 105-245⁰C
- Eficiencia eléctrica: 60-70%
El combustible y el comburente que se utilizan en las AFC tienen que ser hidrógeno y oxígeno puros. En efecto, el CO2 (o el CO) reacciona con el KOH y se forma carbonato potásico, lo que reduce enormemente la eficiencia de la pila de combustible.[22] Incluso con pequeñas concentraciones (10 a 100 ppm) se produce el "envenenamiento" de la pila por monóxido o dióxido de carbono.[24] Por este motivo, se utilizan principalmente en el sector aeroespacial y ambientes submarinos, figura 2.15. La concentración del electrolito está en torno al 35-50% para temperaturas de operación inferiores a 120 °C, pudiendo operar a 250 °C cuando la concentración es del 85%.[22]
Estas pilas son las que ofrecen un mayor rendimiento. Es una de las razones por las que se utilizan en la exploración espacial, ya que hay que poner en órbita el combustible y la masa a elevar tiene que ser óptima. La NASA ha utilizado desde 1960 las AFCs alimentadas con hidrógeno en las misiones espaciales, para proporcionar electricidad y agua potable.[25]
Pila de Combustible de Ácido Fosfórico (PAFC)[editar]

- Electrolito: Ácido fosfórico líquido.
- Catalizador: Platino sobre base de carbono
- Temperatura de operación: entre 180-205⁰C
- Eficiencia eléctrica: 36-42%

Las PAFCs pueden utilizar hidrocarburos o biogás como combustible. Las reacciones en el cátodo y en el ánodo son parecidas a las que se dan en las PEMs, pero la temperatura de operación es más alta y también toleran mejor las impurezas que pueda tener el combustible. Las PAFCs se utilizan con frecuencia en cogeneración. Hoy en día, la comercialización de las PAFCs está muy extendida. Se utilizan con frecuencia para proveer de electricidad a edificios con alta demanda energética, tanto públicos como privados.
En 1991, UTC puso en el mercado la primera planta de generación de potencia basada en esta tecnología de pila de combustible. El sistema de potencia PureCell, ver figura, suministra 200 kW de potencia y unos 850 J de energía cada hora. El tiempo acumulado de operación por el conjunto de todas las unidades vendidas supera los 6 millones de horas.[22]
Pila de Combustible de Carbonato fundido (MCFC)[editar]

- Electrolito: carbonatos alcalinos sobre una matriz cerámica.
- Catalizador: de los electrodos (no platino)
- Temperatura de operación: alrededor de 650 °C
- Eficiencia eléctrica: 50-60%
En este tipo de pilas, la alta temperatura de operación permite el reformado interno del combustible, es decir, la conversión del combustible a hidrógeno se hace dentro de la propia pila. Dado que las MCFCs no son propensas a contaminarse con CO o CO2, pueden utilizar como combustible incluso óxidos de carbono, algo que las hace especialmente propicias para alimentarlas con gases procedentes del carbón. Las MCFCs se utilizan en aplicaciones estacionarias y en cogeneración, para proveer de energía a edificios públicos o privados.
Esta tecnología lleva mucho tiempo en desarrollo. En el siguiente enlace se muestra una foto de un sistema de potencia de 100 W basado en tecnología MCFC y fabricada por Texas Instruments en 1966. Los máximos exponentes en el desarrollo de esta tecnología ha sido la alemana MTU, y su socio americano, Fuel Cell Energy.[22]
Pila de Combustible de Óxido Sólido (SOFC)[editar]

- Electrolito: sólido cerámico u óxido metálico no poroso.
- Catalizador: material de los electrodos (no platino).
- Temperatura de operación: 800-1000 °C.
- Eficiencia eléctrica: 50-60%
Este tipo de pilas de alta temperatura están diseñadas para reformar hidrocarburos ligeros (como el gas natural) de manera interna. Por tanto, si se quisieran emplear hidrocarburos más pesados (como gasolina) se requeriría de un reformador externo. Su forma puede ser plana o tubular. Este tipo de pilas se utilizan en una larga lista de aplicaciones estacionarias a lo largo de todo el mundo.[26]
Dado que actualmente este tipo de pilas operan entre 800-1000 °C, el reto es bajar a 600-800 °C (IT-SOFC, "Intermediate Temperature Solid Oxide Fuel Cell"). La investigación se focaliza en disminuir el espesor de la capa de electrolito y en la búsqueda de nuevos materiales, basados en óxidos lantánidos o con estructura de perovskita, que presenten alta conductividad iónica a baja temperatura.[22]
Comparación entre los distintos tipos[editar]
A modo de resumen, la tabla siguiente compara los principales tipos de pila de combustible en estado de Comercialización / investigación.
| Tipo de Pila | Electrolito | Catalizador | Temperatura de Operación(°C) | Potencia | Eficiencia Eléctrica(%) | Usos Principales | Ventajas | Inconvenientes |
|---|---|---|---|---|---|---|---|---|
| PEMFC | polímero sólido | Platino | 80-95 | (0,1-100)kW |
|
|
|
|
| DMFC | polímero sólido | Platino | 50-120 | 1mW-100kW |
|
|
|
|
| AFC | solución de hidróxido de potasio en agua | metales no preciosos | 105-245 | (10-100)kW |
|
|
|
|
| PAFC | Ácido fosfórico líquido | platino sobre base de carbono | 180-205 | >10MW |
|
|
|
|
| MCFC | carbonatos alcalinos sobre una matriz cerámica | material de los electrodos (no platino) | 650 | 100W |
|
|
|
|
| SOFC | sólido cerámico | material de los electrodos (no platino) | 800-1000 | >100kW |
|
|
|
|
Otros tipos de pilas de combustible[editar]
En la tabla siguiente se presentan otros tipos de pilas de combustible que están basados en los tipos principales, pero que poseen características propias que las hacen interesantes tanto para aplicaciones generales como específicas.
| Tipo de pila de combustible | Electrolito | Potencia eléctrica (W) | Temperatura de trabajo (°C) | Eficiencia de la pila (%) | Eficiencia del sistema (%) | Estado |
|---|---|---|---|---|---|---|
| Pila de combustible de hidruros metálicos | solución acuosa alcalina | -20 | ||||
| Pila de combustible electro-galvánica | solución acuosa alcalina | >40 | Comercial / investigación | |||
| Pila de combustible de ácido fórmico | membrana polimérica (ionómero) | < 50 W | < 40 | Comercial / investigación | ||
| Batería de zinc-aire | solución acuosa alcalina | <40 | Producción en masa | |||
| Pila de combustible microbiana | Membrana de polímero o ácido húmico | <40 | investigación | |||
| Pila de combustible regenerativa | membrana polimérica (ionómero) | <50 | Comercial / investigación | |||
| Pila de combustible borohidruro | solución acuosa alcalina | 70 | Comercial / investigación | |||
| Pila de combustible de metanol reformado | membrana polimérica (ionómero) | 5 W – 100 kW | 125-300 | 50–60 | 25–40 | Comercial / investigación |
| Pila de combustible de etanol | membrana polimérica (ionómero) | < 140 mW/cm² | > 25 | investigación | ||
| Pila de combustible REDOX | electrolitos líquidos y membrana polimérica (ionómero) | 1 kW – 10 MW | investigación | |||
| Pila de combustible cerámica protónica | conductor de H+ de óxido cerámico | investigación | ||||
| Pila de combustible de carbono | varios diferentes | 700–850 | 80 | 70 | Comercial / investigación | |
| Bio-pilas de combustible enzimáticas | cualquiera que no desnaturalice la enzima | <40 | investigación | |||
| Pila de combustible de magnesio-aire | agua salada | (-20)-555 | 90 | Comercial / investigación |
Comportamiento[editar]
La función de Gibbs y el potencial de Nernst[editar]
En una pila de combustible se produce una reacción electroquímica a temperatura y presión constantes que nunca llegará al equilibrio. Al trabajo que se puede obtener en dichas condiciones se le llama trabajo de no expansión[27] y su valor máximo coincide con la variación de energía libre de Gibbs. En el caso de una reacción electroquímica este trabajo es la energía eléctrica necesaria para liberar los electrones, Welect, y viene dado por el cambio en la función de Gibbs, ΔGreac, de la reacción química (también se le llama energía libre de reacción):[27]
Esta expresión es particularmente útil para evaluar el trabajo eléctrico que se produce en las células de combustible y células electroquímicas. El trabajo eléctrico se obtiene teniendo en cuenta el número n de electrones son liberados por cada molécula producida en la reacción química, y la diferencia de potencial E que adquieren al ser liberados. Dicho trabajo es igual a –neE, siendo e la carga del electrón. Si queremos expresar la reacción por mol en lugar de por molécula, habrá que multiplicar n por el número de Avogadro con lo que se tendrán nNA electrones por cada mol producido. Por tanto, el trabajo asociado a la generación de nNA electrones, con una diferencia de potencial E, es:[21]
Al producto eNA, que es la carga eléctrica de un mol de electrones, se le da el nombre de constante de Faraday y se designa con la letra F. Por tanto:
siendo .[28]
El potencial E es conocido como potencial de Nernst[21] y da la tensión eléctrica que se puede obtener cuando se produce una reacción electroquímica de forma reversible. Dicho potencial también es conocido como fuerza electromotriz y es el que se obtiene en condiciones de circuito abierto, es decir, en ausencia de corriente eléctrica.
Es usual encontrar la energía libre de reacción, o bien, los datos necesarios para calcularla,(como entalpías y entropías) tabulados para el estado estándar de T=298,15 K y P = 1 atm.[29] Dicha energía de reacción en el estado estándar se denota como ΔG0. Para una reacción que no ocurra en estas condiciones estándar se puede escribir[29]
donde Q es el Cociente de reacción.
Dividiendo la ecuación anterior entre nF obtenemos la denominada Ecuación de Nernst:
donde E0 es conocido como el potencial estándar de celda, que no es más que la energía estándar de reacción de Gibbs expresada en Voltios.
Como en las pilas de combustible es normal tener los reactivos y los productos en estado gaseoso, entonces Q se obtiene a partir de las presiones parciales:[21][27]
donde νi y νj son los coeficientes estequiométricos de la reacción química. Por lo que el potencial de Nernst en este caso será:
El potencial de Nernst es el equivalente a la “fuerza electromotriz” o “potencial de celda” de una pila, que es la diferencia de potencial que se observa en una pila en circuito abierto.
Rendimiento[editar]
Se define el rendimiento o eficiencia ideal de la conversión química a eléctrica como el cociente entre la energía eléctrica obtenida en el caso en el que la corriente sea infinitamente pequeña, Welec, ideal o como vimos en el primer apartado de esta sección,ΔGreac, ideal, y la energía química puesta en juego ∆Hreac podemos escribirlo como:
Como ejemplo, puede hacerse el cálculo del rendimiento ideal en condiciones estándar (T=298,15 K y P = 1 atm), ηideal0, para una pila basada en la reacción de hidrógeno con oxígeno:
donde el agua producida es líquida. En estas condiciones:[21]
por tanto,
Para otras reacciones electroquímicas se procedería de forma análoga.
El rendimiento de las células de combustible, a diferencia de los motores de combustión (interna y externa) no está limitado por el ciclo de Carnot ya que no siguen un ciclo termodinámico. Por lo tanto, su rendimiento es muy alto en comparación, al convertir energía química en eléctrica directamente.
La diferencia de potencial en los electrodos de la pila decrece cuando existe corriente. Por conveniencia, el rendimiento de una pila de combustible se expresa a menudo en términos del cociente entre el voltaje ideal y el voltaje real (con el que opera la pila de combustible), siendo este último menor que el primero debido a las pérdidas óhmicas y a las asociadas con mecanismos de polarización dentro de la pila. La expresión de la eficiencia de la pila de combustible es la siguiente:
donde Vreal es el voltaje medido entre los electrodos en condiciones reales de funcionamiento, e I es la intensidad de corriente que circula por el circuito externo. Esta eficiencia, también se conoce como eficiencia en voltaje.[30] En esta expresión se considera que todo el combustible está siendo aprovechado, puesto que así ocurre en la mayoría de los motores de combustión. Sin embargo, en las pilas de combustible no se suele dar la conversión completa del combustible siendo necesario, para calcular la eficiencia en voltaje real, multiplicar la ecuación anterior por un factor que nos indique cuánto combustible está siendo utilizado.
Por tanto, aunque el rendimiento ideal parezca muy elevado, se ve reducido por las condiciones reales de funcionamiento.
Una célula de combustible convierte normalmente la energía química de combustible en electricidad con un rendimiento aproximadamente del 50%. El rendimiento sin embargo depende en gran medida de la corriente que circula a través de la celda de combustible: cuanto mayor es la corriente, menor el rendimiento.
Hay que considerar también las pérdidas debidas a la producción, al transporte y al almacenaje. Los vehículos con célula de combustible que funcionan con hidrógeno comprimido tienen una eficiencia del 22% si el hidrógeno se almacena como gas a alta presión, y del 17% si se almacena como hidrógeno líquido (estas cifras deberían justificar su metodología de cálculo).
Las células de combustible no pueden almacenar energía como una batería, sino que en algunos usos, como centrales eléctricas independientes basadas en fuentes "discontinuas" (solares, energía del viento), se combinan con electrolizadores y sistemas de almacenaje para formar un conjunto para almacenar esta energía. El rendimiento del proceso reversible (de electricidad al hidrógeno y de nuevo a electricidad) de tales plantas se encuentra entre el 30 y el 40%.
En "usos combinados de calor y de energía" (cogeneración), para aplicaciones donde también se requiere energía calorífica, se acepta un rendimiento más bajo de la conversión de combustible a electricidad (típicamente 15-20%), porque la mayoría de la energía no convertida en electricidad se utiliza como calor. Se pierde algo de calor con los gases que salen de la célula como ocurre en cualquier caldera convencional, por lo que con esta producción combinada de energía térmica y de energía eléctrica la eficacia sigue siendo más baja de 100%, normalmente alrededor del 80%. En términos de energía sin embargo, el proceso es ineficaz, y se obtendrían mejores resultados energéticos maximizando la electricidad generada y después usando la electricidad para hacer funcionar una bomba de calor.
Comportamiento real[editar]

Como se ha indicado en secciones anteriores, el potencial de Nernst da la “fuerza electromotriz” de la pila de combustible, es decir, la diferencia de potencial entre sus electrodos en ausencia de corriente eléctrica. Una vez que el circuito se cierra y la corriente empieza a fluir aparecen pérdidas de potencial relacionadas con la conducción de carga dentro del electrolito y con fenómenos de polarización. Como consecuencia, la diferencia de potencial que se mide entre los electrodos es menor que la ideal (potencial de Nernst) calculada en la sección anterior.
Para visualizar claramente la diferencia entre ambos potenciales se suele representar el potencial frente a la densidad de corriente, dando lugar a la llamada curva de operación, también llamada curva de polarización. Dicha curva, como muestra la figura de la derecha, presenta tres regiones principales de operación.
Como se muestra entre paréntesis, cada una de las regiones mostradas en la gráfica anterior tiene asociada una fuente de pérdida de eficiencia:[21]
- Pérdidas por activación: debidas a la baja velocidad de las reacciones en la región de polarización por activación.
- Pérdidas óhmicas(resistivas): relacionadas con el flujo de electrones a través del material de los electrodos, así como a la resistencia al flujo de iones a través del electrolito en la región de polarización óhmica.
- Pérdidas por concentración: los cambios de concentración del gas o transporte de masas región de polarización por concentración.
A continuación veremos con más detalle los tipos de pérdidas citados.
Pérdidas por activación[editar]
Este tipo de pérdidas se deben a la lentitud de las reacciones en los electrodos. Para que las reacciones electroquímicas comiencen, al igual que en las reacciones químicas comunes, los reactivos deben superar la energía de activación. En realidad, en los electrodos no ocurre una sola reacción sino varias, cada una de ellas con su propia velocidad y energía de activación. Así, las pérdidas por activación son el resultado de las pérdidas debidas a cada una de estas reacciones sucesivas.
Las pérdidas por activación se expresan matemáticamente mediante la ecuación de Tafel:[31]
R≡constante de los gases ideales medida en J/molK
T≡temperatura de operación en K
α≡coeficiente de transporte de electrones (adimensional)
n≡número de electrones por molécula (adimensional)
F≡constante de Faraday en C/mol
i≡corriente generada en A
i0≡corriente de intercambio (depende del tipo de material), medida en A
Esta ecuación es válida para valores de ΔEact≥(50-100)mV.[31]
Según Barbir[32] los factores que reducen las pérdidas por activación son:
- Incremento de la temperatura de operación.
- Catalizadores efectivos.
- Uso de oxígeno puro como agente oxidante en vez de aire.
- Incremento de la concentración de los reactivos.
- Presiones de operación más altas.
Pérdidas Óhmicas[editar]
Las pérdidas óhmicas se deben a la resistencia al flujo de iones en el electrolito y a la resistencia al flujo de electrones que viajan a través del electrodo. Los electrodos y el electrolito suelen ser materiales fundamentalmente óhmicos, es decir, materiales en los que predomina el comportamiento lineal de la tensión frente a la intensidad de corriente. Por tanto, las pérdidas óhmicas se pueden expresar a través de la ley de Ohm:
donde I es la corriente que fluye a través de la pila y R es la resistencia total, que incluye la debida a los electrones, la debida a los iones y la debida a los terminales de contacto y las conexiones:
Dependiendo de la geometría de la pila de combustible, la contribución a la resistencia total de cada una de estas resistencias varía.[32] Así en una pila de combustible tipo SOFC con una estructura plana domina la resistencia iónica, mientras que en una SOFC de tipo tubular, domina la debida al paso de los electrones.
Los factores que reducen las pérdidas óhmicas son, según Barbir:[32]
- Utilizar electrodos fabricados con un material de alta conductividad eléctrica.
- Realizar un buen diseño estructural, minimizando los caminos de paso de corriente.
- Uso de membranas iónicas delgadas.
Pérdidas por concentración[editar]
Cuando el transporte de masas ocurre a velocidad finita en el electrodo se limita la entrada de gas reactivo y la correcta evacuación de los productos, por ello, a menudo ocurre que el gas del interior se consume, diluyéndose en los productos. Como consecuencia, se crea un gradiente de concentración entre la superficie del electrodo y las entradas de suministro, que contribuye negativamente al potencial de salida.
La tasa de transporte de masa hacia la superficie de un electrodo, se puede describir a través de la ley de difusión de Fick:[33]
Donde D es el coeficiente de difusión de los reactivos, CB su concentración de máxima, CS su concentración en la superficie y δ, es el espesor de la capa de difusión. La corriente límite, IL, es una medida de la máxima velocidad con que el reactivo puede suministrarse al electrodo y esto ocurre cuando CS=0. Por tanto:
Entonces podemos expresar las concentraciones de la forma siguiente:
Por tanto, la ecuación de Nernst para las especies químicas en condiciones de equilibrio, o en circuito abierto, es:
Cuando sí hay flujo de corriente, la concentración superficial es inferior a la concentración máxima, y la ecuación de Nernst se convierte en
La diferencia de potencial que se produce por un cambio concentración en el electrodo, ΔEcon, se conoce con el nombre de polarización por concentración:
o en función de la corriente límite:
Para reducir este tipo de pérdidas Barbir[32] da las siguientes indicaciones:
- Depurar con frecuencia el contenido de agua en el cátodo para que los gases puedan difundirse adecuadamente.
- Incrementar la temperatura de operación para que el agua acumulada se evapore y se reduzca así, el bloqueo de los gases que se suministran.
Variables que afectan al funcionamiento[editar]
El potencial de salida de las pilas de combustible se ve afectado por las condiciones de operación (temperatura, presión, composición del gas, aprovechamiento de reactivos, densidad de corriente), por el diseño de la pila y por otros factores (impurezas, durabilidad del dispositivo) que hacen que se aleje del valor ideal antes calculado. Para más información sobre este tipo de pérdidas, consultar las siguientes referencias.[21][32][34][35]
Aplicaciones de las celdas de combustible[editar]
Energía[editar]
Las pilas de combustible son muy útiles como fuentes de energía en lugares remotos, como por ejemplo naves espaciales, estaciones meteorológicas alejadas, parques grandes, localizaciones rurales, y en ciertos usos militares. Un sistema con pila de combustible que funciona con hidrógeno puede ser compacto, ligero y no tiene piezas móviles importantes. Debido a que las pilas de combustible no tienen partes móviles y no implican combustión, en condiciones ideales que pueden alcanzar hasta fiabilidad 99,9999%.[36] Esto equivale a menos de un minuto de tiempo muerto en un período de seis años.[36]
Aplicaciones de cogeneración (uso combinado de calor y electricidad) para viviendas, edificios de oficinas y fábricas. Este tipo de sistema genera energía eléctrica de manera constante (vendiendo el exceso de energía a la red cuando no se consume), y al mismo tiempo produce aire y agua caliente gracias al calor que desprende. Las celdas de combustible de Ácido fosfórico (PAFC Phosphoric-Acid Fuel Cells) abarcan el segmento más grande de aplicaciones de cogeneración en todo el mundo y pueden proporcionar eficacias combinadas cercanas al 80% (45-50% eléctrico + el resto como térmica). El mayor fabricante de células de combustible de PAFC es UTC Power, una división de United Technologies Corporation. También se utilizan celdas de combustible de carbonato Fundido (MCFC Molten Carbonate Fuel Cell) con fines idénticos, y existen prototipos de celdas de óxido sólido (SOFC Solid-Oxide Fuel Cell).
Los sistemas electrolizadores no almacenan el combustible en sí mismos, por lo que necesitan de unidades de almacenamiento externas, por lo que se suelen utilizar en áreas rurales.[37] En este caso, las baterías tienen que ser de gran tamaño para satisfacer la demanda del almacenaje, pero aun así esto supone un ahorro con respecto a los dispositivos eléctricos convencionales.
Hay muchos tipos diferentes de pilas de combustible estacionarias así eficiencias varían, pero la mayoría son entre 40% y 60% de eficiencia energética.[38] Sin embargo, cuando se utiliza el calor residual de la pila de combustible para calentar un edificio en un sistema de cogeneración esta eficiencia puede aumentar a 85%,[38] es decir, casi tres veces más eficiente que las plantas de carbón tradicionales.[39] Por lo tanto, en la producción a gran escala, las pilas de combustible podrían ahorrar un 20-40% en costos de energía cuando se utiliza en sistemas de cogeneración.[40] Las pilas de combustible son mucho más limpias que las plantas energéticas tradicionales; una planta de energía basada en pila de combustible que utilice gas natural como fuente de hidrógeno podría generar menos de una onza (28, 35 gramos aproximadamente) de contaminantes (distintos al CO2), por cada kW/h producido, mientras que con los sistemas de combustión convencionales se generarían 25 onzas (708 gramos).[41]
Existe un programa experimental en Stuart Island en el estado de Washington,[42] donde la compañía Stuart Island Energy Initiative ha construido un sistema completo en el cual los paneles solares generan la corriente para hacer funcionar varios electrolizadores que producen hidrógeno. Dicho hidrógeno se almacena en un tanque de 1900 litros, a una presión de 10 a 80 bar. Este combustible finalmente se utiliza para hacer funcionar una celda de combustible de hidrógeno de 48 V marca ReliOn que proporciona suficiente energía eléctrica para fines residenciales en la isla (véase el enlace externo a SIEI. ORG). Otro sistema de este tipo se instaló en 2011 Hempstead, NY.[43]
Las pilas de combustible pueden utilizarse con gas de baja calidad de los vertederos o de las plantas de tratamiento de aguas residuales para generar energía y reducir las emisiones de metano. La planta de energía basada en pilas de combustible más grande es una planta de 2,8 MW situada en California.[44]
Protium, una banda de rock formada en la Ponaganset High School, en Glocester, fue el primer conjunto musical del mundo en utilizar celdas de combustible de hidrógeno para proveerse de energía. La banda utilizaba un Airgen Fuelcell de 1kW Ballard Power systems. El conjunto ha tocado en numerosos eventos relacionados con las celdas de combustible incluyendo el CEP de Connecticut, y el 2003 Fuel Cell Seminar en Miami beach.
Plug Power Inc. es otra compañía importante en el diseño, desarrollo y fabricación de celdas de combustible PEM para aplicaciones estacionarias, incluyendo productos dirigidos a las telecomunicaciones, energía básica, y aplicaciones de cogeneración.
Cogeneración[editar]
Los sistemas combinados de pilas de combustible para producir calor y energía (CHP), incluyendo los microsistemas combinados de calor y energía (MicroCHP), son utilizados para proporcionar calor y energía a hogares, edificios de oficinas y fábricas. Estos sistemas generan energía eléctrica constantemente (vendiendo el exceso a la red cuando no se consume) y, al mismo tiempo, produce aire y agua calientes con el calor residual. Como resultado los sistemas CHP tienen el potencial de ahorrar energía primaria ya que pueden hacer uso del calor residual, el cual es normalmente rechazado por los sistemas de conversión de energía térmica.[45] El rango de potencia típico de una célula de combustible doméstica es 1–3 kWel / 4–8 kWth.[46][47] Los sistemas CHP conectados a refrigeradores de absorción usan el calor residual para la refrigeración.[48]
El calor residual de las pilas de combustible puede ser desviado en verano directamente hacia el suelo consiguiendo enfriamiento adicional mientras que en invierno el calor residual puede ser bombeado directamente al edificio. La Universidad de Minesota posee los derechos de patente de este tipo de sistemas.[49][50]
Los sistemas de cogeneración pueden alcanzar un rendimiento del 85% (40-60 % eléctrico y el resto térmico).[38] Las pilas de ácido fosfórico (PAFC) son las más utilizadas en los productos CHP en el mundo y pueden alcanzar unas eficiencias combinadas cercanas al 90%.[51][52] Las pilas de carbonato fundido (MCFC) y de óxido sólido (SOFC) también se utilizan para sistemas combinados de producción de calor y energía y tienen una eficiencia eléctrica cercana al 60%.[53] Las desventajas de estos sistemas de cogeneración incluyen altos costos y poca duración.[54][55] Además su necesidad de tener un tanque para almacenar agua caliente para suavizar la producción de calor representa un serio problema para el mercado doméstico ya que en los hogares el espacio representa un gran coste.[56]
Vehículos de pila de combustible[editar]
Automóviles[editar]

Aunque actualmente no existen vehículos equipados con pilas de combustibles disponibles para la venta a gran escala, se han lanzado más de 20 prototipos de vehículos con pilas de combustible (FECV) y coches de demostración desde 2009. Entre los modelos de demostración se incluyen Honda FCX Clarity, Toyota FCHV, Fiat Phyllis y Mercedes-Benz F-Cell.[57] Desde 2011 los coches de demostración FECVs han recorrido más de 4.800.000 km, con más de 27.000 recargas.[58] Se ha conseguido una autonomía de 400 km entre recargas.[59] Además se pueden recargar en menos de 5 minutos.[60] El Programa de Tecnología de Células de Combustible del Departamento Estadounidense de Energía asegura que, a partir de 2011, las células de combustible están alcanzando una eficiencia entre el 53% y el 59% a un cuarto de su potencia y entre el 42% y el 53% a toda potencia[61] con una durabilidad de 120.000 km con una degradación inferior al 10%.[59] En un análisis completo “pozo-a-rueda”, que no tiene en cuenta las restricciones económicas ni de mercado, General Motors y sus socios estimaban que, por milla recorrida, un vehículo alimentado con hidrógeno gaseoso comprimido utilizaba alrededor de un 40% menos de energía y emitía un 45% menos de gases culpables del efecto invernadero que un vehículo de combustión interna.[62] Un ingeniero jefe del Departamento de Energía cuyo equipo está probando coches con células de combustible dijo en 2011 “que su atractivo potencial reside en que son vehículos completamente funcionales sin límite de recarga y por tanto son un reemplazo directo para cualquier vehículo. Por ejemplo, si se está conduciendo un SUV de tamaño máximo y se quiere arrastrar un bote hasta la montaña se puede hacer con esta tecnología y no se puede hacer con los vehículos actuales que funcionan solo con baterías, los cuales están más pensados para la conducción urbana”.[63]

Algunos expertos creen, sin embargo, que los coches de pilas de combustible nunca llegarán a ser económicamente competitivos con otras tecnologías[64][65] o que se tardarán décadas hasta que sean rentables.[66][67] En julio de 2011 el presidente y director ejecutivo de General Motors, Daniel Akerson, dijo lo siguiente: “El coche todavía es demasiado caro y no probablemente no será práctico hasta más tarde del 2020, no lo sé” aunque los precios del coche de pila de combustible de hidrógeno estaban disminuyendo.[68]
En 2012, Lux Research, Inc., publicó un artículo en el que se decía: “El sueño de una economía del hidrógeno…..no está más cerca”. Concluía diciendo: “El coste de capital… limitará su adopción a no más de 5,9 GW” en 2030 con una casi “infranqueable barrera a su adopción excepto en áreas de mercado muy limitadas” El análisis finalizaba diciendo que en 2030 el mercado estacionario de PEM alcanzaría un billón de dólares mientras que el mercado de vehículos, incluyendo montacargas, un total de dos billones.[69] Otros análisis citan la falta de una estructura del hidrógeno extensiva en Estados Unidos como un desafío para la comercialización de vehículos de pilas eléctricas de combustible. En 2006, un estudio para IEEE mostraba que, para el hidrógeno producido por la electrólisis del agua: “Aproximadamente, solo un 25% de la energía eólica, hidráulica o solar tiene uso práctico” El estudio, más adelante, mencionaba que: “parece ser que la energía obtenida a partir de pilas de combustible de hidrógeno es cuatro veces más cara que la energía obtenida de la red….Porque las altas pérdidas de energía (hidrógeno) no pueden competir con la electricidad"(95). Es más, el estudio constataba: La modificación del gas natural no es una solución sostenible”.[70] La gran cantidad de energía que se necesita para aislar el hidrógeno de otros componentes naturales (agua, gas natural, biomasa), almacenar el gas por compresión o licuefacción, transferir la energía al usuario, más la pérdida de energía cuando se convierte en energía eléctrica utilizable mediante pilas de combustible dejan alrededor de un 25% para uso práctico.[71][72][73]
A pesar de esto, varios fabricantes importantes de coches han anunciado planes para introducir la producción de un modelo de coche con pila de combustible en el 2015. En 2013, Toyota ha manifestado que planea introducir dicho vehículo por un precio inferior a 100.000 dólares.[74] Mercedes-Benz anunció que moverá la fecha de producción programada para su coche de pila de combustible de 2015 a 2014, afirmando que: “el vehículo está preparado técnicamente para el mercado….el problema es de infraestructura”.[75] En la Exposición de Coches de París en septiembre de 2012, Hyundai anunció que planeaba empezar la producción comercial de un modelo con pila de combustible (basado en el ix35) en diciembre de 2012 y que esperaba entregar 1000 unidades en 2015.[76] Otros fabricantes que planean tener listos vehículos de pilas de combustible para el 2016 o antes son General Motors,[77] Honda[78] en Japón y Nissan.[79]
La Administración del expresidente Obama redujo la financiación para el desarrollo de los vehículos de pilas de combustible, aduciendo que otras tecnologías del automóvil conseguirían una mayor reducción de las emisiones en menor tiempo.[80] Steven Chu, Secretario de Energía de los Estados Unidos, anunció en 2009, que los vehículos de hidrógeno “no serán prácticos durante los próximos 10 o 20 años”.[81][82] Sin embargo, en 2012, Chu declaró que veía los coches de pila de combustible más viables ya que los precios del gas natural habían descendido y las tecnologías de modificación del hidrógeno habían mejorado.[83][84]
Autobuses[editar]
Desde 2011 hay un total de aproximadamente 100 autobuses alimentados con pilas de combustible distribuidos por todo el mundo. La mayoría de los autobuses están fabricados por UTC Power, Toyota, Ballard, Hydrogenics, y Proton Motor. Los autobuses de UTC han recorrido desde entonces 970.000 km.[85] Los autobuses de pilas de combustible mejoran el rendimiento de combustible con respecto a los autobuses diésel y a los de gas natural en torno al 39%-141%.[86] Los autobuses con pilas de combustible se han distribuido en lugares como: Whistler, Canadá; San Francisco, Estados Unidos; Hamburgo, Alemania; Shanghái, China; Londres, Inglaterra; Sao Paulo, Brasil; y otros lugares[87] El Fuel Cell Bus Club es un esfuerzo cooperativo globar para el ensayo de autobuses de pila de combustible. Otros proyectos destacados incluyen:
- 12 autobuses se han distribuido en Oakland y en el área de la Bahía de San Francisco en California[87]
- Daimler AG, con 36 autobuses experimentales alimentados con Sistemas de Energía Ballard de pilas de combustible ha completado con éxito un ensayo de tres años en 11 ciudades en junio de 2007.[88]
El primer prototipo de autobús brasileño con pilas de combustible de hidrógeno se utilizó en Sao Paulo. Fue fabricado en Caxias do Sul y el hidrógeno produjo en Sao Bernardo do Campo a partir de agua mediante electrólisis. El programa, llamado "Ônibus Brasileiro a Hidrogênio", incluye tres autobuses adicionales.[89]
Montacargas[editar]
Un montacargas de pila de combustible (también llamado camión elevador de pila de combustible) es un montacargas industrial alimentado con una pila de combustible utilizado para elevar y transportar materiales. La mayoría de las pilas utilizadas para la manipulación de materiales son alimentadas por pilas de combustible PEM.
En 2013 se usaban más de 4.000 montacargas de este tipo en Estados Unidos,[90] de los cuales, solo 500 recibieron financiación del DOE (2012).[91] Las flotas de pilas de combustible las operan un gran número de compañías, entre ellas: Sysco Foods, Fedex Freight, GENCO (Wegmans, Coca-Cola, Kimberly Clark, y Whole Foods), y H-E-B Grocers. En Europa funcionaban 30 montacargas de pila de combustible de Hylift. Este número se elevó a 200 unidades con HyLIFT-EUROPE,[92] con proyectos en Francia[93][94] y Austria.[95] Pike Research anunció en 2011 que los montacargas alimentados con pilas de combustible serían el mayor eje impulsor de la demanda de hidrógeno en el 2020.[96]
Los montacargas que funcionan con pilas de combustible PEM tienen ventajas importantes sobre los alimentados con petróleo y baterías ya que no producen emisiones locales, pueden trabajar un turno de 8 horas seguidas con un solo tanque de hidrógeno, pueden recargarse en 3 minutos y tienen una duración de 8-10 años. Habitualmente se utilizan en almacenes refrigeraos ya que su rendimiento no se ve afectado por las bajas temperaturas. Muchas compañías no utilizan montacargas alimentados con petróleo ya que estos vehículos se utilizan en interiores donde se deben controlar las emisiones y en su lugar se están pasando a los montacargas eléctricos.[97] En el diseño las pilas de combustible se fabrican de manera que puedan ser repuestas inmediatamente.[98][99]
Motocicletas y bicicletas[editar]
En 2005, un fabricante inglés de pilas de combustible alimentadas con hidrógeno, Intelligent Energy(IE), produjo la primera motocicleta propulsada con hidrógeno, llamada la ENV (Vehículo de Emisión Neutra). La motocicleta almacena suficiente combustible como para funcionar durante 4 horas y recorrer 160 km en un área urbana, a una velocidad máxima de 80 km/h.[100] En 2004, Honda desarrolló una motocicleta basada en pila de combustible que utilizaba un apilamiento de pilas de combustible de Honda.[101][102]
Otros ejemplos de motocicletas[103] y bicicletas[104] que usan pilas de combustible de hidrógeno son la scooter de la compañía taiwanesa APFCT que usa el sistema de combustible de la italiana Acta Spa[105] y la scooter Burgman de Suzuki con una pila de combustible IE que recibió el EU Whole Vehicle Type Approval en 2011.[106] Suzuki Motor Corp e IE han anunciado una aventura empresarial conjunta para acelerar la comercialización de vehículos de emisión cero.[107]
Aviones[editar]
En 2003, el primer avión (no tripulado) enteramente propulsado mediante pilas de combustible hizo su primer vuelo. La píla de combustible era un único diseño de apilamiento FlatstackTM, que le permitía estar integrado en las superficies aerodinámicas del avión.[108]
Ha habido varios vehículos aéreos con pilas de combustible no tripulados (UAV). Un UAV Horizon Fuel Cell estableció el récord de distancia de vuelo para un UAV pequeño en 2007.[109]
Los investigadores de la empresa Boeing y otros socios empresariales en Europa llevaron a cabo vuelos de prueba en febrero de 2008 con un avión tripulado propulsado solamente por una pila de combustible y baterías ligeras. El así llamado “avión demostrador de pila de combustible, usaba un sistema híbrido compuesto por una pila de combustible PEM y una batería de ion litio para propulsar un motor eléctrico acoplado a un propulsor convencional.[110] En abril de 2008, en Toledo (España), la compañía Boeing hizo volar el primer avión propulsado por pila de hidrógeno.[111] De manera parecida Airbus está desarrollando un prototipo de avión que utiliza esta tecnología.
Los militares están interesados especialmente en esta aplicación por su ruido escaso, el poco calor que desprenden y por su capacidad para alcanzar gran altitud. En 2009 el Ion Tiger del Laboratorio de Investigación Naval (NRL con sus siglas en inglés), hizo un vuelo de 23 horas y 17 minutos utilizando una pila de combustible de hidrógeno.[112] Las pilas de combustible también se están utilizando para suministrar energía adicional en los aviones, reemplazando los generadores de combustible fósil que se utilizaban anteriormente para encender los motores y proporcional energía a bordo.[113] Los aviones propulsados por pilas de combustible pueden ayudar en la reducción de emisiones contaminantes y de ruido.[114]
Barcos[editar]
El primer barco de pila de combustible HYDRA usó un sistema AFC con una potencia de salida neta de 6.5 kW. Islandia se ha comprometido a convertir su vasta flota de barcos de pesca en barcos que usen pilas de combustible para proporcionar potencia auxiliar para el 2015 y, finalmente, para proporcionar la potencia primaria. Ámsterdam recientemente ha introducido el primer ferry de pasajeros que hace un recorrido por los famosos canales de la ciudad alimentado con pilas de combustible.[115]
Actualmente, un equipo de estudiantes universitarios llamado Energy-Quest está preparando un barco accionado por esta tecnología para hacer un viaje alrededor del mundo, así como otros proyectos usando combustibles más eficientes o renovables. Su empresa se llama Tritón.
Submarinos[editar]

Los submarinos Type 212A, un avanzado diseño alemán de submarinos no nucleares, utiliza pilas de combustible (desarrolladas por Siemens) para alimentar nueve propulsores y puede mantenerse sumergido durante semanas sin tener que subir a la superficie.[116] El sistema consiste en 9 pilas de combustible PEM, que proporcionan entre 30 kW y 50 kW cada una. Es silencioso, lo que le da ventaja en la detección de otros submarinos.[117]
Un sistema propulsor parecido de pilas de hidrógeno, aunque mejorado tienen los submarinos españoles S-80 desarrollado por Abengoa.
Estaciones de servicio[editar]
La primera estación de abastecimiento de hidrógeno como combustible fue abierta en Reikiavik, Islandia en abril de 2003. Esta estación abastece a tres autobuses construidos por DaimlerChrysler y que prestan servicio en la red de transporte público de Reykjavík. La propia estación produce el hidrógeno que necesita, gracias a una unidad electrolizadora (fabricada por Norsk Hydro), y no necesita ser abastecida externamente: los únicos suministros necesarios son electricidad y agua. Shell también participa en el proyecto. La estación no tiene cubierta, para que en caso de peligro el hidrógeno pueda escapar libremente a la atmósfera.
En 2010 había 85 hidrogeneras en Estados Unidos.[118] En 2012, California contaba con 23 hidrogeneras en funcionamiento.[118][119] Honda anunció, en marzo de 2011, que planeaba abrir la primera estacióin que generaría hidrógeno mediante electrólisis producida por energía solar. Carolina del Sur también tiene dos hidrogeneras, en Aike y Columbia respectivamente. La Universidad de Carolina del Sur, un miembro fundador de la Alianza del Hidrógeno y las Pilas de Combustible de Carolina del Sur, recibió 12.5 millones de dólares del Departamento Estadounidense de Energía para su Programa Combustibles del Futuro.[120]
Se planea que las 14 estaciones alemanas sean 50 en 2015[121] a través de su colaboración público-privada Now-GMBH.[122] Japón cuenta con una autopista de hidrógeno, como parte del Proyecto Japonés de Pilas de Combustible de Hidrógeno.
Sistemas de energía portátiles[editar]
Los sistemas de energía portátiles basados en pilas de combustible se pueden utilizar en el sector del ocio (p. ej. caravanas, cabañas, lanchas), el sector industrial (p. ej. para alimentar pozos de gas o petróleo situados en lugares remotos, torres de comunicación, seguridad, estaciones meteorológicas, etc..) y el sector militar.[123][124]
Otros posibles usos[editar]
- Sistemas Auxiliares de Energía[125]
- Proporcionar energía para estaciones de radio base[126]
- Sistemas de centralización de energía
- Sistemas de energía de emergencia, en los que se que incluyen alumbrado, generadores y otros aparatos que proporcionan apoyo en situaciones críticas o cuando los sistemas normales fallan. Se pueden utilizar en muchos lugares, desde hogares a hospitales, centros de investigación y centros de datos.[127]
- Equipo de telecomunicaciones y modernos equipamientos navales.[128]
- Sistema de alimentación ininterrumpida UPS (del inglés uninterruptible power supply), proporciona energía en caso de emergencia y, dependiendo de la topología, regula la línea además del equipo proporcionado energía desde una fuente separada cuando la otra no está disponible. A diferencia de un generador en modo de espera, proporciona protección instantánea contra una interrupción momentánea de la línea.
- Pilas de combustible de hidrógeno solares para el calentamiento de agua.[129]
- Vehículos híbridos, utilizando, por ejemplo una pila de combustible y una batería.
- Sistemas de apoyo a la red eléctrica
- Puertos portátiles para instrumentos electrónicos pequeños (p. ej., una pinza para el cinturón que carga tu móvil o PDA)
- Teléfonos inteligentes, portátiles y tabletas.
- Aparatos de calefacción pequeños[130]
- Conservación de comida, conseguida eliminando el oxígeno y automáticamente manteniendo la ausencia de oxígeno en un contenedor que contenga por ejemplo pescado fresco.
- Alcoholímetros, donde el voltaje generado por la pila se usa para determinar la concentración de combustible en la muestra (alcohol)[131]
- Detectores de monóxido de carbono, sensor electroquímico.
En la actualidad, los mayores problemas residen en los materiales de soporte y de catálisis. Según diversos autores(Venkatachalapathy, Davila et al. 1999), (Hoogers 2003), un material electrocatalizador debe satisfacer varios requisitos. Necesita, en primer lugar, alta eficiencia en la oxidación electroquímica del combustible en el ánodo, (e.g. H2 o CH4) y para la reducción del O2 en el cátodo. Una elevada durabilidad es también un requisito fundamental: se espera que las PEMFCs funcionen al menos durante 10 000 horas. Es necesario que un electrocatalizador tenga una buena conductividad eléctrica para reducir al mínimo las pérdidas por resistencia en la capa del catalizador. Ha de tener finalmente un bajo coste de producción.
Economía y Medio Ambiente[editar]
En 2012, los ingresos de la industria de las pilas de combustible superaron el billón de dólares en el mercado de valores en todo el mundo.[132] Sin embargo, todavía en octubre de 2013, ninguna compañía pública en la industria era todavía rentable.[133] Se enviaron globalmente 140.000 apilamientos de células de combustible en 2010, 11 000 más que en 2007, y desde 2011 hasta 2012 la tasa de crecimiento de envíos fue del 85%.[134] Tanaka Kikinzoku Kogyo K.K aumentó sus instalaciones para la producción de catalizadores para pilas de combustilbes a fin de dar respuesta a la demanda anticipada ya que la Japanese ENE Farm esperaba instalar 50.000 unidades en 2013[135] y la compañía está experimentando un rápido crecimiento de mercado.
Aproximadamente el 50% de los envíos de pilas de combustible en 2010 fueron pilas de combustible, en comparación con el tercio de 2009, y los cuatro productores dominantes en la Industria de las Pilas de Combustible eran los Estados Unidos, Alemania, Japón y Corea del Sur.[136] El Departamento de Energía del Estado Sólido y la Alianza de la Conversión de Energía encontraron que, en junio de 2011, las pilas de combustible fijas generaron potencia a un precio de 774 – 775 dólares por kilovatio instalado.[137] En 2011, Bloom Energy, un gran proveedor de pilas de combustible, dijo que sus pilas de combustible generaban energía a 9 -11 céntimos por kilovatio-hora, incluyendo el precio del combustible, mantenimiento y equipos.[138]
Los grupos industriales predicen que hay suficientes reservas de platino para la demanda futura,[139] y en 2007, la investigación llevada a cabo en Brookhaven National Laboratory sugirió que el platino podría ser reemplazado por un recubrimiento de oro y paladio, que podría ser menos susceptible de envenenamiento y por tanto alargar la vida de la pila de combustible.[140] Otro método podría ser la utilización de hierro y azufre en lugar de platino. Esto abarataría el coste de las pilas (ya que el platino de una pila de combustible típica cuesta alrededor de 1500 dólares americanos y el hierro necesario costaría 1,50 dólares). El concepto estaba siendo desarrollado por una coalición formada por el centro John Innes y la Universidad de Milán-Bicocca.[141] Los cátodos PEDOT son inmunes al envenenamiento por monóxido.[142]
Las pilas de combustible son muy atractivas para usos avanzados por su alta eficacia e idealmente (véase energías renovables) por ser de emisiones cero, en contraste con los combustibles actuales más comunes, como puedan ser el metano o el gas natural, que siempre generan dióxido de carbono. Casi el 50% de toda la electricidad que es producida en los Estados Unidos, es procedente del carbón, que es una fuente de energía altamente sucia. Si se utiliza electrólisis para crear el hidrógeno usando la energía procedente de las centrales eléctricas, en realidad el hidrógeno es creado a partir de carbón. Aunque la celda de combustible solo emita calor y agua como residuos, el problema de la contaminación continuará presente en las centrales eléctricas.
Un acercamiento global debe considerar los impactos provocados por el escenario completo del hidrógeno, lo que incluye la producción, el uso, la infraestructura y los conversores de energía. Las pilas de combustible hoy en día están sobredimensionadas de catalizador, para compensar su propio deterioro [8]. La limitación en las reservas minerales de platino ha provocado la búsqueda de otras soluciones, por ejemplo la síntesis de un complejo inorgánico muy similar a la base catalítica del hierro-sulfuro de las bacterias hidrogenasas [9]. Las reservas mundiales de platino serían insuficientes (una cuarta parte) del necesario para permitir una conversión total de los vehículos a células de combustible: una introducción significativa de vehículos con la actual tecnología, por lo tanto, provocaría un gran incremento del precio del platino y un descenso significativo de sus reservas. Sin embargo, trabajos recientes han logrado diseñar catalizadores de hierro y nitrógeno tan eficientes como los de platino, pero con una menor vida útil (100 horas) [10].
Glosario de términos[editar]
- Electrodo: Extremo de un cuerpo conductor en contacto con un medio del que recibe o al que transmite una corriente eléctrica[143]
- Ánodo: Electrodo en el que se produce la oxidación. Para pilas de combustible y otras pilas galvánicas el ánodo es el terminal negativo; para pilas electrolíticas(en las que se produce la electrólisis) el ánodo es el terminal positivo.[144]
- Cátodo: Electrodo en el que se produce la reducción (ganancia de electrones). Para pilas de combustible y otras pilas galvánicas el cátodo es el terminal positivo; para pilas electrolíticas el cátodo es el terminal negativo.[144]
- Electrolito: Una sustancia que conduce iones cargados de un electrodo a otro en una pila de combustible, batería, o electrolizador.[144]
- Apilamiento: Pilas de combustible individuales conectadas en serie. Las pilas de combustible se apilan para aumentar el voltaje.[144]
- Solución: A: un proceso por el que un sólido, líquido, o una sustancia gaseosa se mezcla homogéneamente con un líquido o, a veces con un gas o con un sólido; B: una mezcla homogénea formada por este proceso; C: la condición de ser disuelto[145]
- Catalizador:Una sustancia química que aumenta la velocidad de una reacción sin ser consumida.[144]
- Matriz:lugar desde el cual o en cuyo interior algo se origina, desarrolla o toma forma.[146]
- Membrana: La capa de separación en una pila de combustible que actúa como electrolito y como una película de barrera que separa los gases en los compartimientos anódico y catódico de la pila de combustible.[144]
Videos sobre pilas de combustible[editar]
En esta sección se resumirán los principales aspectos referidos a treinta y cinco videos seleccionados y se hará breve una reseña de los mismos. La selección se ha centrado en videos de carácter divulgativo y sobre todo, en los que tratan los aspectos científicos y técnicos de las pilas de combustible. Sin embargo, con el fin de complementar el rigor científico de los otros videos, también se han seleccionado videos cuyas explicaciones son escuetas pero que nos ofrecen una perspectiva visual del dispositivo que estamos tratando y de sus aplicaciones. La lista consta de 11 videos en español y 24 en inglés. El enlace directo a la lista de reproducción es el siguiente:
Videos en español[editar]
1º Las pilas de combustible.
- Enlace directo
- Autor: Universidad de Vigo, Prof. Anxo Sánchez Bermúdez
- Duración: 19:55 minutos.
- Descripción: introducción a las pilas de combustible. Define claramente este tipo de dispositivos y habla de sus distintos aspectos de forma general y sin ahondar en detalles. Sin embargo, hay que tener en cuenta que cuando habla de las características, las ventajas e inconvenientes se está refiriendo principalmente a la pila de hidrógeno. Se trata pues de un video de carácter divulgativo y muy útil para una primera aproximación a la temática.
2º Serie de videos: Energía del Hidrógeno.
- Enlace directo
- Autor: Universidad Politécnica de Madrid, realizado por alumnos.
- Duración: 1:58 horas
- Descripción: se trata de nueve de presentaciones realizadas por los alumnos de la UPM acerca de las pilas de combustible de hidrógeno y sus distintas aplicaciones; cada presentación se centra en aspecto distinto. El interés de estos videos reside en que en ellos se muestran y analizan un gran número de aplicaciones que pueden tener estos dispositivos. A pesar de que se centran en aspectos y aplicaciones concretos, generalmente pueden ser entendibles para el público no especializado puesto que no se suelen exponer detalles muy técnicos y algunas de las presentaciones comienzan con una pequeña introducción sobre las pilas de combustible. A continuación se muestra una descripción de cada uno de los videos que compone la serie:
- Aplicaciones estacionarias de los diversos tipos de pilas de combustible: Se describen las principales características de los distintos tipos de pila de combustible y sus aplicaciones en la generación de potencia estacionaria.
- Aplicaciones en automoción: Se describen los prototipos fabricados por las distintas compañías de automóviles: se expone el estado de la implantación comercial de los automóviles impulsados con pilas de combustible.
- Aplicaciones portátiles de las pilas de combustible: Se discute la elección de combustible en el caso de las pilas de combustible utilizadas en aplicaciones portátiles y se muestran algunos prototipos.
- Uso del hidrógeno en vehículos aeroespaciales 1: Se explica el ámbito de aplicación y el uso de las pilas de combustible en transbordadores espaciales y en aviones tripulados y no tripulados.
- Uso del hidrógeno en vehículos aeroespaciales 2: Continúa donde termina el video anterior complementándolo. Se explican los tipos de propulsión de vehículos aeroespaciales con uso del hidrógeno: pilas de combustible, motores de combustión interna y sistemas híbridos. Se detalla el "Proyecto Aviazor".
- Proyectos que desarrollan propulsión de vehículos aeroespaciales con hidrógeno: Se continúa la con la temática del video 5, describiendo las diferentes etapas y las características de los proyectos algunos proyectos como: "Ion Tiger", "Solareagle", "Phantom Eye" y "Global Observer".
- Aplicaciones de la pilas de combustible en el medio marino: Se da una visión general sobre qué es una pila de combustible, su clasificación y sus principales ventajas. Se ofrece una breve visión de las posibles aplicaciones de los distintos tipos de pilas de combustible en el medio marino.
- Aplicaciones de las pilas de combustible en artefactos submarinos: Se describen los submarinos existentes que cuentan en su propulsión con pilas de combustible. Se explica qué es un sistema AIP (Air Independent Propulsion). Se explica en especial el submarino S-80 que utilizará hidrógeno procedente de bioetanol reformado para alimentar pilas de combustible PEMFC. Se describen también artefactos submarinos autónomos no tripulados.
- Aplicaciones de las pilas de combustible en buques de superficie: Se describen proyectos de embarcaciones de superficie que incorporan pilas de combustible en su sistema de propulsión principal o para atender consumo eléctrico o como unidades de potencia auxiliar. Se estudia el efecto de la reducción de emisiones como consecuencia del uso de pilas de combustible en el mundo marino.
3º Pila de hidrógeno.
- Enlace directo
- Autor: Tecnópolis. Presentado por Vicente López
- Duración: 1:40 minutos.
- Descripción: Explicación breve pero concisa sobre el vehículo de pila de combustible de hidrógeno y sobre la viabilidad del hidrógeno como vector energético, destacando las ventajas medioambientales de su utilización.
- Enlace directo
4º Autobuses con pila de combustible.
- Enlace directo
- Autor: Cursos CEER.
- Duración: 1:53 minutos.
- Descripción: explicación dinámica con figuras y texto sobre el funcionamiento de una pila de combustible tipo PEM. Se describen los componentes principales y se muestra su ubicación específica en la pila. Finalmente, se ve su aplicación en un vehículo de transporte(autobús).
5º Producir electricidad mediante las plantas.
- Enlace directo
- Autor: Euronews.
- Duración: 1:58 minutos.
- Descripción: En este video se muestra como las plantas verdes generan electricidad. Se trata del proyecto Plant-e de la Universidad de Wageningen de los Países Bajos. La pila de combustible vegetal microbiana genera electricidad a partir de la interacción natural entre las raíces de las plantas y las bacterias del suelo. Funciona mediante el aprovechamiento de hasta el 70% de material orgánico producido a través de la fotosíntesis que no utiliza la planta y que se segrega por las raíces. Las bacterias que están junto a las raíces interactúan con los residuos orgánicos, liberando electrones. Y así se genera electricidad: colocando un electrodo que absorbe los electrones liberados.
6º Células de combustible.
- Enlace directo
- Autor: Universidad Politécnica de Valencia, Javier Orozco Messana.
- Duración: 11:01 minutos.
- Descripción: Se trata de una introducción a las pilas de combustible. Comienza con una breve definición. Continúa con un recorrido histórico. Posteriormente se centra en el funcionamiento tomando como ejemplo una pila de hidrógeno y luego habla de los demás tipos de pilas.
Videos en inglés[editar]
1º How does a fuel cell work?
- Enlace directo
- Autor: Naked Science Scrapbook.
- Duración: 4:01 min.
- Descripción: Introducción a las pilas de combustible. Las explicaciones se realizan mediante dibujos en un cuaderno acompañado de una voz en off. Comienza anunciándolas como la posible tecnología del futuro y hace referencia a sus posibles aplicaciones en distintos dispositivos. Explica sus principios de funcionamiento tomando como ejemplo una pila de hidrógeno y luego explica el funcionamiento y las aplicaciones de las PEMFC, de las AFC y de las SOFC. Alude en repetidas ocasiones a las ventajas que ofrecen estos dispositivos frente a los métodos de obtención de electricidad tradicionales.
2º How a fuel cell works?
- Enlace directo
- Autor: University of Waterloo Alternative Fuel Cell Team.
- Duración: 1:51 minutos.
- Descripción: explicación divulgativa sobre el funcionamiento del coche de pila de combustible de hidrógeno. Se muestra su ubicación dentro del vehículo así como la del combustible. Se explica el funcionamiento lo que ocurre dentro de una celda individual mediante una animación.
3ºBuilding a Fuel Cell Stack.
- Enlace directo
- Autor: Schatz Energy Research Center.
- Duración: 11:05 minutos.
- Descripción: en este video muestra el proceso de montaje de un apilamiento de pilas de combustible tipo PEM. Comienza exponiendo brevemente el mecanismo de funcionamiento de una pila de combustible de este tipo. Por último, se nos muestra cómo se realiza el montaje paso a paso, todo ello acompañado de las explicaciones pertinentes.
4º OWI's Salt Water Fuel Cell Car.
- Enlace directo
- Autor: ABC News.
- Duración: 1:45 minutos.
- Descripción: el video muestra un coche de juguete cuyo combustible es agua salada que puede funcionar de manera continua de 5 a 7 horas. Este automóvil da la oportunidad tanto a niños como a adultos de aprender acerca de las formas de energía limpia.
5º Toyota's Fuel Cell Vehicle: A Zero-Emission Car Coming 2015!
- Enlace directo
- Autor: DNews.
- Duración: 3:27 minutos.
- Descripción: en este video se muestra un vehículo de pila de combustible de hidrógeno que saldrá al mercado en 2015. Se entrevista al ingeniero superior de Toyota Fuel Cell Group, quien da una breve explicación de lo que es una pila de hidrógeno y describe brevemente el funcionamiento de un vehículo de hidrógeno y la diferencia que hay entre éste y los vehículos híbridos. Se hace hincapié en que se trata de una tecnología limpia. desde el punto de vista medioambiental.
6º Virtual Fuel Cell Interactive Visualization.
- Enlace directo
- Autor: NASA Glenn Graphics and Visualization Lab.
- Duración: 1:36 minutos.
- Descripción: video hecho a partir de un programa de simulación de una pila de combustible de configuración tubular. La simulación permite controlar la cantidad de impurezas del combustible, viéndose así, cómo una elevada cantidad de éstas afectan directamente al funcionamiento de la pila. También se puede controlar la velocidad de la simulación y la potencia de salida de la pila.
7º Serie de videos: Introduction to the Fuel Cell.
- Enlace directo
- Autor: Universidad Politécnica de Valencia: María Desamparados Ribes Greus.
- Duración:1:59:41 horas
- Descripción: en esta serie de videos se hace un completo análisis sobre el funcionamiento de las pilas de combustible. Se trata prácticamente toda la temática expuesta en esta memoria desde un punto de vista científico-técnico, las explicaciones están hechas de forma clara y, en la medida que la especialización de la temática lo permite, divulgativa. Se trata de una pues de una completa guía de introducción, por ello, se ha incluido la serie entera.
- Main Aspect: se dan a conocer los aspectos fundamentales y las propiedades de las pilas de combustible; se centra en su papel en el entorno de las energías renovables. Se trata a modo introductorio varios aspectos generales de las pilas de combustible: su electroquímica, su estructura básica, sus principales características y sus aplicaciones. En los videos siguientes se profundizará en los temas citados.
- Electrochemical Basis of Fuel Cells: tratan, en mayor profundidad, los fundamentos electroquímicos del funcionamiento de las pilas de combustible y baterías eléctricas y las bases para poder resolver problemas para el cálculo del potencial eléctrico.
- Main Components of a Fuel Cell: este video muestra los principales componentes (según su criterio) de una pila de combustible, el electrodo y el electrolito, y describe sus funciones. Finalmente habla de los otros componentes que se encuentran en estos dispositivos.
- General criteria for the classification of fuel cells: este video tiene un nombre distinto en la lista de reproducción: "Power Plants". Sin embargo, el nombre de la presentación en es que se ha puesto al principio. Se clasifican las pilas de combustible por su temperatura de operación y luego se habla de los tipos de electrolito que pueden utilizar.
- Fuels: como su propio nombre indica, en este video se presentan los combustibles más comúnmente utilizados en las pilas de combustible.
- Proton exchange membrane fuel cells: se exponen las características básicas de las PEMFC, sus componentes y su funcionamiento.
- Transport in PEMFC: se explican los fenómenos de transporte que tienen lugar dentro de una pila de combustible Se ve el paso del combustible por el ánodo (y del comburente por el cátodo) donde tenemos partículas de platino (catalizador) y por el electrolito. Posteriormente se describen los fenómenos que tienen lugar en la membrana polimérica.
- Fuel cell power plant: se hace un breve repaso del funcionamiento de una celda individual para luego dar paso a explicar lo que es un apilamiento y su inclusión en una planta de energía.
- Fuels. Hydrogen: describe las características principales del hidrógeno como combustible, destacando las que lo hacen medioambientalmente atractivo. También señala los inconvenientes asociados a su extracción, transporte y peligro de explosión.
- Applications of fuel cells: como su propio nombre indica, el video trata sobre las distintas aplicaciones en las que se utilizan las pilas de combustible. Comienza hablando de las características generales y luego, da paso a las aplicaciones fijas. Por último se habla de las aplicaciones portátiles.
- Deviations from ideal Behaviour: se explican los fenómenos que provocan la reducción de eficiencia que tiene lugar en las pilas de combustible en operación, comparando su funcionamiento con el ideal. Se exponen las expresiones que permiten describir y predecir su comportamiento.
- Overpotential: describe los distintos tipos de pérdidas, por activación, resistivas y por concentración, asociadas a las distintas regiones de la curva de polarización de la pila de combustible.
- Direct Methanol Fuel Cells: se presentan las pilas de combustible de metanol (DMFC) y las de etanol. Se tratan sus fundamentos y las ventajas y las limitaciones de su uso respecto a otras pilas de combustible, comparándola mayormente con la PEM.
- Alkaline Fuel Cell: describe el funcionamiento de la pila de combustible alcalina. Habla de sus ventajas e inconvenientes y las compara con otros tipos de pilas de combustible. También se presentan sus aplicaciones más comunes.
8º Compact, high-power hydrogen fuel cell for release in spring 2013
- Enlace directo
- Autor: Diginfo TV
- Duración: 2:46 minutos.
- Descripción: el video nos muestra distintos tipos de pila de combustible diseñados por la Universidad de Kioto aplicables tanto a dispositivos que con requerimientos de potencia bajos (teléfonos móviles, ordenadores portátiles, etc) como medios(televisores de plasma) e incluso con potencias altas que permiten alimentar varios aparatos la simultáneamente o generar electricidad para un hogar.
Véase también[editar]
- Hidrógeno
- Hidrogenera
- Economía de hidrógeno
- Metanol (combustible)
- Metanol
- Etanol (combustible)
- Etanol
- Biocarburante
Referencias[editar]
- ↑ [1] Manual de la técnica del automóvil. Escrito por Robert Bosch GmbH. pág 732. books.google.es
- ↑ Life cycle assessment of PEM FC applications: electric mobility and μ-CHP. Dominic A. Notter,*a Katerina Kouravelou,b Theodoros Karachalios,b Maria K. Daletouc and Nara Tudela Haberlandad; Energy Environ. Sci., 2015,8, 1969-1985 DOI: 10.1039/C5EE01082A
- ↑ Fuel Cell Hand Book. EG&G Technical Services, Inc. 2004. ISBN 9780442319267.
- ↑ Enciclopedia de los niños. Printer Latinoamérica, LTDA. 1990. ISBN ISBN 958-28-0193-X (Colección) / ISBN 958-28-0195-6 (Tomo 2)
|isbn=incorrecto (ayuda). - ↑ Prabhu, Rahul R. (13 de enero de 2013). «Stationary Fuel Cells Market size to reach 350,000 Shipments by 2022». Renew India Campaign. Archivado desde el original el 19 de enero de 2013. Consultado el 14 de enero de 2013.
- ↑ «On the Voltaic Polarization of Certain Solid and Fluid Substances». The London and Edinburgh Philosophical Magazine and Journal of Science. 1839. Archivado desde el original el 5 de octubre de 2013. Consultado el 2 de octubre de 2013.
- ↑ Pilas de combustible: una alternativa limpia de producción de energía Ricardo Escudero-Cid, Enrique Fatás, Juan Carlos Pérez-Flores y Pilar Ocón,2013
- ↑ «Mr. W. R. Grove on a new Voltaic Combination». The London and Edinburgh Philosophical Magazine and Journal of Science. 1838. Consultado el 2 de octubre de 2013.
- ↑ Grove, William Robert. "On Voltaic Series and the Combination of Gases by Platinum", Philosophical Magazine and Journal of Science vol. XIV (1839), pp. 127–130
- ↑ a b Fuel Cell Technology Handbook. CRC Press. 2002. ISBN 9781420041552.
- ↑ Bacon, F.T., Research into the properties of the hydrogen-oxygen fuel cell, BEAMA Journal, 61, 6–12, 1954.
- ↑ http://www.hydrogencarsnow.com/index.php/history/field-test-in-hydrogen-and-fuel-cell-history/
- ↑ Morrill, C.C., Apollo fuel cell system, Proceedings of the 19th Annual Power Sources Conference, New Jersey, 18–20 May, 1965, pp. 38–41.
- ↑ Howard, P. and Greenhill, C., "Ballard PEM Fuel Cell Powered ZEV Bus," SAE Technical Paper 931817, 1993, doi:10.4271/931817
- ↑ enlace
- ↑ «ACAL Energy System Breaks The 10,000 Hour Endurance Barrier». Archivado desde el original el 16 de octubre de 2013.
- ↑ http://www.acalenergy.co.uk/technology/about-flowcath FlowCath
- ↑ A.J. Appleby, F.R. Foulkes, Fuel Cell Handbook, Van Nostrand Reinhold, New York, NY,1989
- ↑ Performance of non-porous graphite and titanium-based anodes in microbial fuel cells Annemiek ter Heijne, Hubertus V.M. Hamelers, Michel Saakes, Cees J.N. Buisman. 2008
- ↑ REVIEWS ON SOLID OXIDE FUEL CELL TECHNOLOGY,Navadol Laosiripojanaa, Wisitsree Wiyaratnb,Worapon Kiatkittipongc, Arnornchai Arpornwichanopd,Apinan Soottitantawatd, and Suttichai Assabumrungratd,2009.
- ↑ a b c d e f g h i Fuel Cell HandBook, Seventh Edition, EG&G Technical Services, Inc., 2004
- ↑ a b c d e f g h i APPICE http://www.appice.es
- ↑ «http://news.brown.edu/pressreleases/2009/03/palladium».
- ↑ Gottesfeld, S. and Pafford, J., A new approach to the problem of carbon monoxide poisoning in fuel cells operating at low temperatures, Journal of the Electrochemical Society, 135, 2651–2652, 1988.
- ↑ Pilas de combustible: una alternativa limpia de producción de energía Ricardo Escudero-Cid, Enrique Fatás, Juan Carlos Pérez-Flores y Pilar Ocón,2013.
- ↑ «http://www.fuelcell.no/fuel_cell_types_sofc_es.htm».
- ↑ a b c Atkins' Physical Chemistry, Peter Atkins, Julio de Paula, Oxford University, Press, W. H. Freeman and Company New York 2010
- ↑ CODATA (2006): Faraday constant, NIST.
- ↑ a b Petrucci R. Química General,Ed.Precinte Hall.2003
- ↑ «https://www.princeton.edu/~humcomp/sophlab/ther_58.htm».
- ↑ a b S.N. Simons, R.B. King and P.R. Prokopius, in Symposium Proceedings Fuel Cells Technology Status and Applications, Figure 1, p. 46, Edited by E.H. Camara, Institute of Gas Technology, Chicago, IL, 45, 1982.
- ↑ a b c d e F. Barbir, PEM fuel cell, ELSEVIER, 2005.
- ↑ Fundamentos de transferencia de calor, Frank P.Incropera, David P. DeWitt, Pearson Educación, 1999
- ↑ Fuchs, M. and F. Barbir, Development of Advanced, Low-Cost PEM Fuel Cell Stack and System Design for Operation on Reformate Used in Vehicle Power Systems, Transportation Fuel Cell Power Systems, 2000 Annual Progress Report (U.S. Department of Energy, Office of Advanced Automotive Technologies, Washington, D.C., October 2000) pp. 79-84
- ↑ «http://mse.xjtu.edu.cn/keyan/hsmg/fc_course/fcm00r0.pdf». Archivado desde el original el 25 de julio de 2014.
- ↑ a b «Fuel Cell Basics: Benefits». Fuel Cells 2000. Archivado desde el original el 28 de septiembre de 2007. Consultado el 27 de mayo de 2007.
- ↑ "Fuel Cell Basics: Applications" Archivado el 15 de mayo de 2011 en Wayback Machine. Fuel Cells 2000. Accessed 2 August 2011.
- ↑ a b c "Types of Fuel Cells". Department of Energy EERE website, accessed 4 August 2011 http://energy.gov/eere/fuelcells/fuel-cells
- ↑ "Energy Sources: Electric Power". U.S. Department of Energy. Accessed 2 August 2011.
- ↑ "2008 Fuel Cell Technologies Market Report" Archivado el 4 de septiembre de 2012 en Wayback Machine.. Bill Vincent of the Breakthrough Technologies Institute, Jennifer Gangi, Sandra Curtin, and Elizabeth Delmont. Department of Energy Energy Efficiency and Renewable Energy. June 2010.
- ↑ U.S. Fuel Cell Council Industry Overview 2010, p. 12. U.S. Fuel Cell Council. 2010.
- ↑ «Stuart Island Energy Initiative». Siei.org. Archivado desde el original el 1 de julio de 2013. Consultado el 21 de septiembre de 2009. – gives extensive technical details
- ↑ «Town's Answer to Clean Energy is Blowin' in the Wind: New Wind Turbine Powers Hydrogen Car Fuel Station». Town of Hempstead. Archivado desde el original el 28 de enero de 2012. Consultado el 13 de enero de 2012.
- ↑ World's Largest Carbon Neutral Fuel Cell Power Plant Archivado el 28 de mayo de 2013 en Wayback Machine., 16 October 2012
- ↑ «Reduction of residential carbon dioxide emissions through the use of small cogeneration fuel cell systems – Combined heat and power systems». IEA Greenhouse Gas R&D Programme (IEAGHG). 11 de noviembre de 2008. Archivado desde el original el 3 de diciembre de 2013. Consultado el 1 de julio de 2013.
- ↑ «Reduction of residential carbon dioxide emissions through the use of small cogeneration fuel cell systems – Scenario calculations». IEA Greenhouse Gas R&D Programme (IEAGHG). 11 de noviembre de 2008. Archivado desde el original el 26 de octubre de 2013. Consultado el 1 de julio de 2013.
- ↑ «COGEN EUROPE».
- ↑ «Fuel Cells and CHP». Archivado desde el original el 18 de mayo de 2012.
- ↑ «Patent 7,334,406». Consultado el 25 de agosto de 2011.
- ↑ «Geothermal Heat, Hybrid Energy Storage System». Archivado desde el original el 5 de marzo de 2012. Consultado el 25 de agosto de 2011.
- ↑ «Reduction of residential carbon dioxide emissions through the use of small cogeneration fuel cell systems – Commercial sector». IEA Greenhouse Gas R&D Programme (IEAGHG). 11 de noviembre de 2008. Archivado desde el original el 5 de marzo de 2018. Consultado el 1 de julio de 2013.
- ↑ "PureCell Model 400: Overview". UTC Power. Accessed 2 August 2011.
- ↑ "Comparison of Fuel Cell Technologies" Archivado el 1 de marzo de 2013 en Wayback Machine.. Departement of Energy Energy Efficiency and Renewable Energy Fuel Cell Technologies Program. February 2011.
- ↑ H.I. Onovwiona and V.I. Ugursal. Residential cogeneration systems: review of the current technology. Renewable and Sustainable Energy Reviews, 10(5):389 – 431, 2006.
- ↑ AD. Hawkes, L. Exarchakos, D. Hart, MA. Leach, D. Haeseldonckx, L. Cosijns and W. D’haeseleer. EUSUSTEL work package 3: Fuell cells, 2006.
- ↑ «Reduction of residential carbon dioxide emissions through the use of small cogeneration fuel cell systems». IEA Greenhouse Gas R&D Programme (IEAGHG). 11 de noviembre de 2008. Archivado desde el original el 4 de mayo de 2018. Consultado el 1 de julio de 2013.
- ↑ "Hydrogen and Fuel Cell Vehicles Worldwide". TÜV SÜD Industrie Service GmbH, accessed on 2 August 2011
- ↑ Wipke, Keith, Sam Sprik, Jennifer Kurtz and Todd Ramsden. "Controlled Hydrogen Fleet and Infrastructure Demonstration and Validation Project" Archivado el 16 de octubre de 2011 en Wayback Machine.. National Renewable Energy Laboratory, 11 September 2009, accessed on 2 August 2011
- ↑ a b "Accomplishments and Progress" Archivado el 21 de agosto de 2011 en Wayback Machine.. Fuel Cell Technology Program, U.S. Dept. of Energy, 24 June 2011
- ↑ Wipke, Keith, Sam Sprik, Jennifer Kurtz and Todd Ramsden. "National FCEV Learning Demonstration" Archivado el 19 de octubre de 2011 en Wayback Machine.. National Renewable Energy Laboratory, April 2011, accessed 2 August 2011
- ↑ Garbak, John. "VIII.0 Technology Validation Sub-Program Overview" Archivado el 24 de septiembre de 2015 en Wayback Machine.. DOE Fuel Cell Technologies Program, FY 2010 Annual Progress Report, accessed 2 August 2011
- ↑ Brinkman, Norma, Michael Wang, Trudy Weber and Thomas Darlington. "Well-To-Wheels Analysis of Advanced Fuel/Vehicle Systems – A North American Study of Energy Use, Greenhouse Gas Emissions, and Criteria Pollutant Emissions". General Motors Corporation, Argonne National Laboratory and Air Improvement Resource, Inc., May 2005, accessed 9 August 2011
- ↑ Lammers, Heather (17 de agosto de 2011). «Low Emission Cars Under NREL's Microscope». NREL Newsroom. Archivado desde el original el 25 de septiembre de 2011. Consultado el 21 de agosto de 2011.
- ↑ «From TechnologyReview.com "Hell and Hydrogen", March 2007». Technologyreview.com. Archivado desde el original el 14 de abril de 2012. Consultado el 31 de enero de 2011.
- ↑ White, Charlie. "Hydrogen fuel cell vehicles are a fraud" Archivado el 19 de junio de 2014 en Wayback Machine. Dvice TV, 31 July 2008
- ↑ Squatriglia, Chuck. "Hydrogen Cars Won't Make a Difference for 40 Years", Wired, 12 May 2008
- ↑ Boyd, Robert S. "Hydrogen cars may be a long time coming". McClatchy Newspapers, 15 May 2007, accessed 13 August 2011
- ↑ "GM CEO: Fuel cell vehicles not yet practical", The Detroit News, 30 July 2011; and Chin, Chris. "GM's Dan Akerson: Fuel-cell vehicles aren't practical… yet". egmCarTech, 1 August 2011, accessed 27 February 2012
- ↑ Brian Warshay, Brian. "The Great Compression: the Future of the Hydrogen Economy", Lux Research, Inc. January 2013
- ↑ Bossel, Ulf. "Does a Hydrogen Economy Make Sense? Proceedings of the IEEE Vol. 94, No. 10, October 2006.
- ↑ Meyers, Jeremy P. "Getting Back Into Gear: Fuel Cell Development After the Hype". The Electrochemical Society Interface, Winter 2008, pp. 36–39, accessed 7 August 2011
- ↑ Eberle, Ulrich and Rittmar von Helmolt. "Sustainable transportation based on electric vehicle concepts: a brief overview". Energy & Environmental Science, Royal Society of Chemistry, 14 May 2010, accessed 2 August 2011
- ↑ Zyga, Lisa. "Why a hydrogen economy doesn't make sense". physorg.com, 11 December 2006, accessed 2 August 2011, citing Bossel, Ulf. "Does a Hydrogen Economy Make Sense?" Proceedings of the IEEE. Vol. 94, No. 10, October 2006
- ↑ Kubota, Yoko. "Toyota says slashes fuel cell costs by nearly $1 million for new hydrogen car". Reuters, Oct 10, 2013
- ↑ Lienert, Anita. "Mercedes-Benz Fuel-Cell Car Ready for Market in 2014". Edmunds Inside Line, 21 June 2011
- ↑ Korzeniewski, Jeremy (27 September 2012). "Hyundai ix35 lays claim to world's first production fuel cell vehicle title". autoblog.com. Retrieved 2012-10-07.
- ↑ "GM's Fuel Cell System Shrinks in Size, Weight, Cost". General Motors. 16 March 2010. Retrieved 5 March 2012.
- ↑ "Honda unveils FCX Clarity advanced fuel cell electric vehicle at motor show in US". Honda Worldwide. Retrieved 5 March 2012.
- ↑ "Environmental Activities: Nissan Green Program 2016". Nissan. Retrieved 5 March 2012.
- ↑ Chu, Steven. "Winning the Future with a Responsible Budget". U.S. Dept. of Energy, 11 February 2011
- ↑ Matthew L. Wald (7 May 2009). "U.S. Drops Research into Fuel Cells for Cars". The New York Times. Retrieved 2009-05-09.
- ↑ Bullis, Kevin. "Q & A: Steven Chu", Technology Review, 14 May 2009
- ↑ Steven Chu turns out to be a supporter of Hydrogen Technologies – on 2.10 min
- ↑ Motavalli, Jim. "Cheap Natural Gas Prompts Energy Department to Soften Its Line on Fuel Cells", The New York Times, 29 May 2012
- ↑ "Transportation Fleet Vehicles: Overview". UTC Power. Accessed 2 August 2011.
- ↑ "FY 2010 annual progress report: VIII.0 Technology Validation Sub-Program Overview".John Garbak. Department of Energy Hydrogen Program.
- ↑ a b "National Fuel Cell Bus Program Awards". Calstart. Accessed 12 August 2011
- ↑ "Fuel cell buses". Transport for London. Archived from the original on 13 May 2007. Retrieved 2007-04-01.
- ↑ "Ônibus brasileiro movido a hidrogênio começa a rodar em São Paulo" (in Portuguese). Inovação Tecnológica. 8 April 2009. Retrieved 2009-05-03.
- ↑ «http://www.fuelcells.org/pdfs/FuelCellForkliftsGainGround.pdf». Archivado desde el original el 21 de agosto de 2013.
- ↑ «http://www1.eere.energy.gov/hydrogenandfuelcells/pdfs/economic_impacts_of_arra_fc.pdf». Archivado desde el original el 3 de diciembre de 2013.
- ↑ «http://www.hylift-projects.eu/».
- ↑ «http://www.fuelcelltoday.com/news-archive/2013/may/first-hydrogen-station-for-fuel-cell-forklift-trucks-in-france,-for-ikea».
- ↑ «http://www.horizonhydrogeneenergie.com/pile-a-combustible-pour-chariot-elevateur.html». Archivado desde el original el 4 de marzo de 2015. Consultado el 9 de julio de 2014.
- ↑ «http://www.fuelcelltoday.com/news-archive/2013/october/hygear-delivers-hydrogen-system-for-fuel-cell-based-forklift-trucks».
- ↑ «http://www.environmentalleader.com/2011/07/20/hydrogen-fueling-stations-could-reach-5200-by-2020/». Archivado desde el original el 23 de julio de 2011. Consultado el 9 de julio de 2014.
- ↑ «http://www1.eere.energy.gov/hydrogenandfuelcells/pdfs/forklift_anl_esd.pdf». Archivado desde el original el 17 de febrero de 2013.
- ↑ «http://www.still.co.uk/fuel-cell-technology-uk.0.0.html». Archivado desde el original el 3 de diciembre de 2013. Consultado el 9 de julio de 2014.
- ↑ «http://graftechaet.com/getattachment/065811d2-720e-40c6-b236-0440c4d90d76/OFCC-Forklift-Case-Study.aspx». Archivado desde el original el 6 de diciembre de 2010.
- ↑ «http://ww2.envbike.com/».
- ↑ «http://world.honda.com/news/2004/2040824_03.html». Archivado desde el original el 2 de abril de 2007.
- ↑ «http://www.autoblog.com/2005/07/21/honda-to-offer-fuel-cell-motorcycle/».
- ↑ «https://www.youtube.com/watch?gl=DE&hl=de&v=B_Whbb_hlPs».
- ↑ «http://www.horizonfuelcell.com/mobility.htm». Archivado desde el original el 22 de julio de 2011.
- ↑ «http://www.apfct.com/article_cat.php?act=view&no=26». Archivado desde el original el 1 de enero de 2013.
- ↑ «http://www.fuelcelltoday.com/media/1713685/fct_review_2012.pdf».
- ↑ «http://www.globalsuzuki.com/motorcycle/history/products/products_2000s.html». Archivado desde el original el 24 de octubre de 2013.
- ↑ «http://www.horizonfuelcell.com/file/pterosoardistancerecord.pdf». Archivado desde el original el 14 de octubre de 2011.
- ↑ "«Copia archivada». Archivado desde el original el 14 de octubre de 2011. Consultado el 3 de agosto de 2011.
- ↑ «http://www.boeing.com/news/frontiers/archive/2008/may/ts_sf04.pdf».
- ↑ «Boeing presenta el primer avión de pila de hidrógeno». Archivado desde el original el 9 de febrero de 2009. Consultado el 15 de enero de 2009.
- ↑ «http://www.alternative-energy-news.info/fuel-cell-powered-uav-flight/».
- ↑ «http://www.theengineer.co.uk/sectors/aerospace/news/hydrogen-powered-unmanned-aircraft-completes-set-of-tests/1009080.article». Archivado desde el original el 15 de octubre de 2015. Consultado el 9 de julio de 2014.
- ↑ «http://www.vidasostenible.org/observatorio/f2_final.asp?idinforme=1286». Archivado desde el original el 14 de julio de 2014.
- ↑ «http://www.lovers.nl/co2zero/». Archivado desde el original el 31 de julio de 2014. Consultado el 9 de julio de 2014.
- ↑ «http://edition.cnn.com/2011/TECH/innovation/02/22/hybrid.submarine/index.html?_s=PM:TECH».
- ↑ «http://www.naval-technology.com/projects/type_212/».
- ↑ a b «http://www.afdc.energy.gov/locator/stations/».
- ↑ «http://www.greencarreports.com/news/1076699_rip-hydrogen-highway-california-takes-back-grant-dollars».
- ↑ «http://www.schydrogen.org/documents/Reports/Cluster_Successes.pdf». Archivado desde el original el 3 de marzo de 2012.
- ↑ «http://www.h2euro.org/2012/german-government-announces-support-for-50-urban-hydrogen-refuelling-stations».
- ↑ «http://www.now-gmbh.de/en/».
- ↑ «http://www.sfc.com/en».
- ↑ «http://www.ensolsystems.com/products/hybrid-light-trailer/». Archivado desde el original el 2 de diciembre de 2014. Consultado el 10 de julio de 2014.
- ↑ «http://www.hydrogenics.com/products-solutions/fuel-cell-power-systems/stationary-stand-by-power/telecom-data-centre-backup-power».
- ↑ «https://www.nttdocomo.co.jp/english/binary/pdf/corporate/technology/rd/technical_journal/bn/vol15_3/vol15_3_004en.pdf».
- ↑ «http://www.t-systems.com/publicsector/uti/767072». Archivado desde el original el 14 de julio de 2014. Consultado el 10 de julio de 2014.
- ↑ «http://www.fuelcells.org/base.cgim?template=markets». Archivado desde el original el 13 de julio de 2014. Consultado el 10 de julio de 2014.
- ↑ «http://es.scribd.com/doc/34346401/Solar-Hydrogen-Fuel-Cell-Water-Heater-Educational-Stand».
- ↑ «http://www.dvgw-cert.com/index.php?id=26». Archivado desde el original el 26 de febrero de 2021. Consultado el 10 de julio de 2014.
- ↑ «http://www.intox.com/t-fuelcellwhitepaper.aspx».
- ↑ «http://www.greencarcongress.com/2013/08/navigant-20130812-1.html».
- ↑ «http://www.greentechmedia.com/articles/read/Will-Plug-Power-Be-the-First-Profitable-Fuel-Cell-Company».
- ↑ «http://www.mmh.com/article/fuel_cell_report_highlights_continued_growth_in_material_handling_applicati».
- ↑ «http://www.fuelcelltoday.com/analysis/analyst-views/2013/13-02-27-latest-developments-in-the-ene-farm-scheme».
- ↑ «http://www.navigantresearch.com/wordpress/wp-content/uploads/2011/05/FCAR-11-Executive-Summary.pdf». Archivado desde el original el 6 de diciembre de 2013. Consultado el 10 de julio de 2014.
- ↑ «http://energy.gov/fe/science-innovation/clean-coal-research».
- ↑ «http://www.bloomenergy.com/reduce-energy-costs//».
- ↑ «http://www.ipa-news.com/pgm/faq/index.htm». Archivado desde el original el 9 de febrero de 2010.
- ↑ «http://www.eetimes.com/document.asp?doc_id=1164952».
- ↑ «http://pubs.acs.org/cen/news/83/i07/8307notw8.html».
- ↑ «http://arstechnica.com/uncategorized/2008/07/fuel-cell-improvements-raise-hopes-for-clean-cheap-energy/».
- ↑ Diccionari WordRefence http://www.wordreference.com/definicion/electrodo
- ↑ a b c d e f "Fuel Cell Technologies Program: Glossary" Archivado el 23 de febrero de 2014 en Wayback Machine.. Department of Energy Energy Efficiency and Renewable Energy Fuel Cell Technologies Program. 7 July 2011. Accessed 3 August 2011.
- ↑ "Solution". Merriam-Webster Free Online Dictionary
- ↑ "Matrix". Merriam-Webster Free Online Dictionary
Bibliografía[editar]
- Gregor Hoogers, Hoogers Hoogers - Fuel Cell Technology Handbook - Edita:CRC Press enero de 2003 - ISBN 0-8493-0877-1
- Venkatachalapathy, R., G. P. Davila, et al. (1999). "Catalytic decomposition of hydrogen peroxide in alkaline solutions." Electrochemistry Communications 1: 614-617.
Enlaces externos[editar]
 Wikimedia Commons alberga una galería multimedia sobre Pila de combustible.
Wikimedia Commons alberga una galería multimedia sobre Pila de combustible.- Celdas de Combustible (animaciones)
- Celdas de Combustible
- Célula o Pila de Combustible, Video corto del Discovery Channel
- Célula o Pila de Combustible (PEMFC), animation
- Electrocell - Celda de Combustible, Stacks, Equipamiento de Testes
- La celda de combustible
- Ballard Power Systems
- Hydrogen Fuel Cell Realm
- EERE: Fuel Cell Types
- EERE: Hydrogen, Programa de Infraestructuras y Celdas de combustible del gobierno de EE. UU.
- How Stuff Works: Celdas de Combustible
- Hydrogen Trade: Tipos de celdas de Combustible
- PhysicsWorld: Celdas de combustible
- FuelCell Energy Inc.
- UTC Power, una subsidiaria de United Technologies Corporation
- Plug Power Fuel Cell Systems
- Vehículos impulsados por hidrógeno
- Stuart Island Energy Initiative (en inglés)
- Pilas de combustible basadas en Goretex para vehículos híbridos
- Engadget
- Pirncipales componentes de las pilas de combustible
- National Geografic. Pilas de combustible
- American History
- Fuelcells.org Información sobre pilas de combustible
- Asociación Española del Hidrógeno
- DOE Fuel Cell HandBook (imágenes del libro explicadas)
- The Fuel Cell Industry Review 2012
- Tipos de pilas de combustible
- Fuel Cell Advances
- Una pila de combustible española supera la meta de potencia marcada por Estados Unidos
- Pilas de combustible: de la pila de Volta a los coches eléctricos (UNED)
- Una pila de combustible "Made in UNED"
- Raíces vegetales y bacterias: una inesperada fuente de electricidad
- "El salto al hidrógeno"
- "Everything you've always wanted to know about electricity energy storage technology options"
- "Recent DOE Break-Through with Hydrogen Fuel Cells, should make them Affordable"
- U.S. Department of Energy. Hidrogen and Fuel Cells Program.2013 Annual Progress Report
- Motorola leads charge for portable fuel cells
- Una pila de combustible podría explicar cómo surgió la vida en la Tierra
- GEI Global Energy Corp. Announces Biogas Power Generation Order
- Water management in regenerative fuel cells
- HIDRÓGENO Y PILAS DE COMBUSTIBLE: SEGURIDAD Y SOSTENIBILIDAD ENERGÉTICA























