Diferencia entre revisiones de «Metformina»
+ chemical formulae |
Indicaciones |
||
| Línea 101: | Línea 101: | ||
== Farmacocinética == |
== Farmacocinética == |
||
La metformina es un [[fármaco]] antihiperglicemiante útil en el manejo de la diabetes mellitus tipo 2. La metformina se administra por vía oral donde su absorción es lenta e incompleta y ocurre principalmente en el [[intestino delgado]].<ref name=scieloco>CUESTA GONZALEZ, Fanny, HOLGUIN MARTINEZ, Gloria, ARCHBOLD JOSEPH, Rosendo et al. Bioequivalence of two metformin formulations. iatreia.rev.fac.med.univ.antioquia. [online]. Julio/Sept. 2005, vol.18, no.3 [consultado 07 Agosto, 2009], p.289-301. Disponible en la World Wide Web: [http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0121-07932005000300003&lng=en&nrm=iso]. ISSN 0121-0793.</ref> Después de su absorción gastrointestinal, se distribuye rápidamente a los tejidos corporales periféricos y prácticamente no se une a las [[proteína]]s plasmáticas.<ref name=farmacologiahumana /> Tiene una [[biodisponibilidad]] del 50 al 60% y la Cmax se observa entre 2 y 4 horas después de la administración.<ref name=scieloco /> No es metabolizada en el [[hígado]] o el [[tracto gastrointestinal]], por lo que se excreta inalterada a través del [[riñón]] (el 90% en aproximadamente 12 horas), con una [[vida media de eliminación]] que fluctúa entre 1.5 y 4.5 horas por lo que debe administrarse 2 a 3 veces al día.<ref name=farmacologiahumana /> |
La metformina es un [[fármaco]] antihiperglicemiante útil en el manejo de la diabetes mellitus tipo 2. La metformina se administra por vía oral donde su absorción es lenta e incompleta y ocurre principalmente en el [[intestino delgado]].<ref name=scieloco>CUESTA GONZALEZ, Fanny, HOLGUIN MARTINEZ, Gloria, ARCHBOLD JOSEPH, Rosendo et al. Bioequivalence of two metformin formulations. iatreia.rev.fac.med.univ.antioquia. [online]. Julio/Sept. 2005, vol.18, no.3 [consultado 07 Agosto, 2009], p.289-301. Disponible en la World Wide Web: [http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0121-07932005000300003&lng=en&nrm=iso]. ISSN 0121-0793.</ref> Después de su absorción gastrointestinal, se distribuye rápidamente a los tejidos corporales periféricos y prácticamente no se une a las [[proteína]]s plasmáticas.<ref name=farmacologiahumana /> Tiene una [[biodisponibilidad]] del 50 al 60% y la Cmax se observa entre 2 y 4 horas después de la administración.<ref name=scieloco /> No es metabolizada en el [[hígado]] o el [[tracto gastrointestinal]], por lo que se excreta inalterada a través del [[riñón]] (el 90% en aproximadamente 12 horas), con una [[vida media de eliminación]] que fluctúa entre 1.5 y 4.5 horas por lo que debe administrarse 2 a 3 veces al día.<ref name=farmacologiahumana /> |
||
== Indicaciones clínicas == |
|||
Las [[biguanida]]s han sido prescritos fundamentalmente en pacientes cuya hiperglicemia se debe a la ineficaz acción de la insulina, es decir, el síndrome de resistencia a la insulina.<ref name=katzung>{{cita libro |apellidos= Katzung|nombre= Bertram G.|editorial= [[McGraw-Hill]]|título= Basic & Clinical Pharmacology|edición= 9|fecha= 2007|isbn= 0071451536|páginas= |capítulo= Chapter 41. Pancreatic |
|||
Hormones & Antidiabetic Drugs |URLcapítulo= |cita= }}</ref> Dado que la metformina no actúa sobre la insulina y evita el aumento de peso ni provoca hipoglucemia, ofrece evidentes ventajas sobre la insulina o [[sulfonilurea]]s en el tratamiento de la hiperglicemia en este grupo de pacientes. El grupo de estudio UKPDS (del inglés, ''United Kingdom Prospective Diabetes Study'') informó de que la terapia con metformina disminuye el riesgo de trastornos macrovasculares y microvasculares,<ref name=diabetes /> en contraste con los otros grupos de fármacos, que sólo modifican la morbilidad microvascular.<ref name=katzung /> La metformina también se indica para su uso en combinación con insulina o secretagogos [[tiazolidindiona]]s en diabéticos tipo 2 en los que monoterapia oral resulta insuficiente.<ref>{{cita publicación |apellido= Stafford|nombre= John M |enlaceautor= |coautores= Tom Elasy |año= 2007|mes= agosto|título= Treatment update: thiazolidinediones in combination with metformin for the treatment of type 2 diabetes|publicación= Vasc Health Risk Manag|volumen= 3|número= 4|páginas= 503–510|pmcid= PMC2291335 |url= http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=2291335|fechaacceso=9 de agosto de 2009 |cita= }}</ref> La metformina es útil en la prevención de la diabetes tipo 2, el «Programa de Prevención de Diabetes» llegó a la conclusión de que la metformina es eficaz en la prevención del debút de la diabetes tipo 2 en pacientes de mediana edad, los individuos obesos con intolerancia a la glucosa e hiperglucemia en ayunas. Curiosamente, la metformina no previene la diabetes en pacientes prediabéticos de mayor edad y en buenas condiciones físicas.<ref name=katzung /> |
|||
== Efectos Secundarios == |
== Efectos Secundarios == |
||
Revisión del 04:14 9 ago 2009
| Metformina | ||
|---|---|---|
 | ||
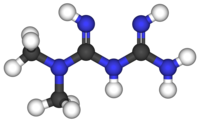 | ||
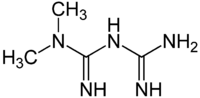
| Nombre (IUPAC) sistemático | ||
| Diamida N,N-dimetilimidodicarbonimidico | ||
| Identificadores | ||
| Número CAS | 657-24-9 | |
| Código ATC | A10BA02 | |
| PubChem | 4091 | |
| DrugBank | APRD01099 | |
| Datos químicos | ||
| Fórmula | C4H11N5 | |
| Peso mol. |
129.164 gr/mol 165.63 gr/mol (hidrocloruro) | |
| Datos físicos | ||
| Densidad | 1,41 g/cm³ | |
| P. de ebullición | 97 °C (207 °F) | |
| Solubilidad en agua | 0,285 mg/mL (20 °C) | |
| Farmacocinética | ||
| Biodisponibilidad | 50 a 60% en ayunas | |
| Unión proteica | 50 - 80%, principalmente albúmina | |
| Metabolismo | Ninguna | |
| Vida media | 6.2 horas | |
| Excreción | Excreción renal activa | |
| Datos clínicos | ||
| Cat. embarazo | C (AU) Los estudios en animales no han demostrado efectos adversos sobre el feto, pero no hay estudios clínicos adecuados y bien controlados hechos en embarazadas. Puede emplearse con vigilancia médica. (EUA) | |
| Estado legal | POM (UK) ℞-only (EUA) | |
| Vías de adm. | Oral | |
La metformina o el preparado comercial hidrocloruro de metformina es un medicamento antidiabético de aplicación oral del tipo biguánido.[1] Es comúnmente utilizado en el tratamiento y la prevención de la diabetes mellitus tipo 2, también conocida como diabetes no insulinodependiente, particularmente en pacientes con sobrepeso, así como en niños[2] y personas que presentan una función renal normal. Se indica por sí sola como adyuvante del ejercicio físico y la dieta en pacientes cuya hiperglicemia no puede ser controlada solo con modificaciones en la dieta.[1]
A diferencia de muchos otros antidiabéticos, la metformina no produce hipoglicemia si se usa a solas. La metformina también ha reducido los niveles de LDL y triglicéridos circulantes en la sangre y puede ayudar a perder peso.[3] Para el año 2009, la metformina es uno de dos antiglicemiantes orales que pertencen a la Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud, junto con la glibenclamida,[4] y es el único medicamento conocido capaz de prevenir las enfermedades cardiovasculares asociadas a la diabetes.[5]
Historia
Esta clase de medicamento antidiabético tienen su origen histórico en una planta (galega officinalis) conocida desde hace siglos por reducir los efectos de la diabetes. La Metformina fue descrita en la literatura científica en 1957 y se vendió por vez primera en Francia en 1979, aunque no fue aprobada por las autoridades pertinentes en los Estados Unidos hasta 1995.
Mecanismo de Acción
La metformina es un antihiperglicemiante pero no actúa como hipoglicemiante por lo que no produce hipoglicemia.[6] El mecanismo exacto por el cual la metformina actúa en el tratamiento de la diabetes es incierto, a pesar de sus ampliamente conocidos beneficios terapéuticos. La metformina no afecta la secreción del páncreas, sin embargo, no es activa en ausencia de la insulina.[6] Parece ser que actúa principalmente reduciendo la gluconeogénesis hepática, pero también reduce la absorción de glucosa por parte del tracto gastrointestinal a la vez de incrementar la sensibilidad a la insulina por medio del aumento en la utilización de la glucosa por parte de tejidos periféricos,[6] al aumentar la actividad IP3 quinasa del receptor insulínico.[7] El diabético promedio con diabetes tipo 2 tiene un ritmo de gluconeogénesis tres veces mayor a lo normal, y aparentemente la metformina reduce ésta situación en más de un tercio.[8] La metformina no es metabolizada, sino que se excreta en la orina con un tiempo medio de eliminación de 6.2 horas.
El consumo de este medicamento por parte de las mujeres que sufren trastornos ovulatorios, provoca una pérdida de peso, así como una mejora tanto en la ovulación como en la fertilidad, una disminución en la tasa de abortos y de diabetes gestacional.[9] En estas pacientes, la administración de metformina reduce los niveles de la hormona luteinizante, así como su liberación aguda inducida por agonistas de la hormona liberadora de gonadotropina (GnRH),[7] probablemente por disminución de la actividad del citocromo P450C17 ovárica y adrenal.
La metformina también mejora el perfil de dislipidemia característico de la mayoría de pacientes diabéticos, reduciendo los valores de triglicéridos, así como el VLDL y LDL y, en ocasiones, ha aumentado la concentración de HDL.[6]
Efecto sobre el hígado
La metformina mejora la hiperglicemia sobre todo a través de su represión de la producción hepática de glucosa, es decir, la gluconeogénesis hepática.[10] La metformina activa la proteincinasa activada por AMP (AMPK, por sus siglas en inglés), una enzima hepática que desempeña un papel importante en la señalización de la vía de la insulina, el manejo energético del cuerpo entero y el metabolismo de la glucosa y las grasas.[11] La activación de la AMPK es necesaria para el efecto inhibitorio de la metformina sobre la producción de glucosa por las células hepáticas.[12] Una investigación publicada en 2008 dilucidó con más claridad el mecanismo de acción de la metformina, demostrando que la activación de AMPK es necesaria para un aumento en la expresión del factor de transcripción «SHP», que a su vez inhibe la expresión de los genes gluconeogénicos hepáticos PEPCK y GLC-6-Pase.[13] La metformina se utiliza frecuentemente en investigaciones como agonista de la AMPK. El mecanismo por el cual las biguanidas incrementan la actividad de AMPK sigue siendo incierto, sin embargo, las investigaciones sugieren que la metformina aumenta la cantidad de AMP citosólico, en oposición a variaciones en el AMP total o de la relación AMP total/ATP.[14]
Farmacocinética
La metformina es un fármaco antihiperglicemiante útil en el manejo de la diabetes mellitus tipo 2. La metformina se administra por vía oral donde su absorción es lenta e incompleta y ocurre principalmente en el intestino delgado.[15] Después de su absorción gastrointestinal, se distribuye rápidamente a los tejidos corporales periféricos y prácticamente no se une a las proteínas plasmáticas.[6] Tiene una biodisponibilidad del 50 al 60% y la Cmax se observa entre 2 y 4 horas después de la administración.[15] No es metabolizada en el hígado o el tracto gastrointestinal, por lo que se excreta inalterada a través del riñón (el 90% en aproximadamente 12 horas), con una vida media de eliminación que fluctúa entre 1.5 y 4.5 horas por lo que debe administrarse 2 a 3 veces al día.[6]
Indicaciones clínicas
Las biguanidas han sido prescritos fundamentalmente en pacientes cuya hiperglicemia se debe a la ineficaz acción de la insulina, es decir, el síndrome de resistencia a la insulina.[16] Dado que la metformina no actúa sobre la insulina y evita el aumento de peso ni provoca hipoglucemia, ofrece evidentes ventajas sobre la insulina o sulfonilureas en el tratamiento de la hiperglicemia en este grupo de pacientes. El grupo de estudio UKPDS (del inglés, United Kingdom Prospective Diabetes Study) informó de que la terapia con metformina disminuye el riesgo de trastornos macrovasculares y microvasculares,[17] en contraste con los otros grupos de fármacos, que sólo modifican la morbilidad microvascular.[16] La metformina también se indica para su uso en combinación con insulina o secretagogos tiazolidindionas en diabéticos tipo 2 en los que monoterapia oral resulta insuficiente.[18] La metformina es útil en la prevención de la diabetes tipo 2, el «Programa de Prevención de Diabetes» llegó a la conclusión de que la metformina es eficaz en la prevención del debút de la diabetes tipo 2 en pacientes de mediana edad, los individuos obesos con intolerancia a la glucosa e hiperglucemia en ayunas. Curiosamente, la metformina no previene la diabetes en pacientes prediabéticos de mayor edad y en buenas condiciones físicas.[16]
Efectos Secundarios

Aunque se trata de un medicamento seguro y probado que rara vez se asocia a efectos secundarios graves,[2] al uso de la metformina se le conocen varios posibles efectos secundarios nocivos.
Gastrointestinales
En primera instancia la metformina puede provocar problemas gastrointestinales, tales como diarrea, náuseas, dolor estomacal, anorexia y vómitos;[6] la ingesta de la metformina junto con la comida posiblemente reduce tales problemas. Un porcentaje pequeño de personas experimentan una alteración del sentido del gusto que toma la forma de un molesto sabor metálico. De todos los medicamentos antidiabéticos la metformina es la que ha reportado el mayor número de molestias gastrointestinales.[19] En un ensayo clínico de 286 sujetos, 53,2% de los 141 que recibieron metformina de liberación inmediata (en contraste con el placebo) reportaron diarrea, frente al 11,7% para el placebo, y el 25,5% informó de náuseas / vómitos, frente al 8,3% para los de placebo.[20]
Puede causar molestias gastrointestinales que resultan graves para los pacientes, especialmente cuando se inicia la administración de la metformina, o cuando se aumenta la dosis. El malestar puede ser evitado en un principio por dosis bajas (1 a 1,7 gramos al día) y aumentar la dosis gradualmente. Las molestias gastrointestinales, después de un uso constante y prolongado de la metformina, resultan mucho menos frecuentes.
El uso a largo plazo de metformina se ha asociado con un aumento de los niveles de homocisteína[21] y a malabsorción de vitamina B12,[22][23] especialmente en personas con un aporte bajo de calcio.[17] Las dosis más altas y un uso prolongado se asocia con aumento de la incidencia de la deficiencia de vitamina B12, y algunos investigadores recomiendan el cribado o estrategias de prevención de esa deficiencia nutricional.[24]
Acidosis láctica
Otro posible efecto secundario, más raro pero más grave, es la acidosis láctica, identificable por una sensación de debilidad y malestar general asociada con la acumulación excesiva de ácido láctico en la sangre.[25] El riesgo de una acidosis láctica no se aumenta con la administración de metformina en personas que no tenga factores de riesgo conocidos, tales como la insuficiencia renal, insuficiencia cardíaca o insuficiencia hepática.[26]
Se cree que la razón de la acidosis láctica sea un aumento en la respiración anaeróbica intestinal, normalmente, el hígado podría convertir esta acumulación de lactato en glucosa a través de la gluconeogénesis, pero es esta misma vía que la metformina inhibe.[10] Cualquier condición que puede precipitar la acidosis láctica contraindica el uso de metformina.
Todo paciente en tratamiento con metformina deberá suspender el medicamento al menos 48 horas antes de someterse a una operación quirúrgica.[25] El fármaco debe ser completamente depurado después de suspender la metformina a las 48 horas que preceden la cirugía. Esta es una medida profiláctica, en un esfuerzo por reducir el riesgo de acidosis láctica que puede ser secundaria a las complicaciones de procedimientos quirúrgicos, tales como hipotensión, infarto de miocardio, o shock séptico.[27]
Contraindicaciones
La metformina está contraindicada en las personas con cualquier condición de que podría aumentar el riesgo de acidosis láctica, incluyendo trastornos renales con niveles de creatinina de más de 1.5 mg/dl en hombres y 1.4 mg/dl en mujeres[17][28][29] (aunque este es un límite arbitrario), enfermedad pulmonar y enfermedad hepática. La insuficiencia cardíaca ha sido considerada una contraindicación para el uso de metformina,[28] aunque una revisión sistemática en 2007 mostró que la metformina es el único medicamento antidiabético oral que no se asocia con daño en personas con insuficiencia cardíaca.[30] La limitación en ancianos mayores de 75 años se fundamenta en la función renal, que se espera tenga una tasa de filtrado glomerular mayor de 60 ml/min.[17]
Se recomienda que la metformina sea suspendida temporalmente antes de cualquier estudio radiográfico de contraste yodados (como en el caso de la TAC o angiografía con contraste), como colorante de contraste que afectará de manera temporal la función renal, causando de forma indirecta una acidosis láctica por retención de metformina en el cuerpo. Se recomienda que la metformina se reanuda después de dos días, suponiendo que la función renal sea normal.[31][32] En pacientes con insuficiencia renal aguda la metformina se acumula y aparece una acidosis láctica que puede ser fatal.[28]
Sobredosis
Una revisión en los Estados Unidos durante 5 años acerca de sobredosis intencionales o accidentales con metformina reportada por centros de control de envenenamientos concluyó que los efectos adversos severos en estos casos no eran frecuentes, aunque los individuos ancianos parecían tener un riesgo mayor, así como pacientes con enfermedades subyacentes graves.[33] Aunque la incidencia de casos graves suele ser menor al 1% entre los pacientes con sobredosis, la mortalidad en esos casos graves puede llegar al 50%.[28] Se ha reportado en la literatura sobredosis intecionales con hasta 63 g de metformina.[34] Las sobredosis accidentales suelen estar relacionados con la administración del fármaco en pacientes con insuficiencia renal. La peor complicación que atenta contra la vida en estos casos de sobredosis es la acidosis láctica, caracteriza por una elevada concentración de lactato sanguíneo (> 45 mg/dl o 5 mmol/l).[28]
Los principales síntomas de sobredosis son, entre otros: cansancio extremo, debilidad, vómitos y malestar o dolor estomacal, pérdida del apetito, respiración profunda y agitada, falta de aliento, mareos, frecuencia cardiaca anormalmente rápida o lenta, dolor muscular y sensación de frío.[25] El tratamiento de una sobredosis con metformina suele ser basado en medidas generales, aunque puede incluirse la administración de bicarbonato para mejorar la acidosis, así como hemodiálisis estandar o hemofiltración contínua con el fin de rapidamente remover el exceso de metformina y corregir la acidosis.[35][36]
Combinación con otros farmacos

La metformina se puede combinar con rosiglitazona y gliburida cuando el fármaco junto a la dieta y ejercicio no proporcionen un control glucémico adecuado.[25] La combinación con rosiglitazona en los Estados Unidos por la fábrica de GlaxoSmithKline fue suspendida por aproximadamente un año por violación de buenas prácticas de manufactura.[38] La indicación de ambas drogas continúa siendo recetada en forma combinada o en tomas separadas.
En los Estados Unidos, la metformina también está disponible en combinación con pioglitazona, la sulfonilurea glipizida, con la glibenclamida, con la sitagliptina, una inhibidora de la dipeptidil peptidasa-4, y con la repaglinida, una meglitinida. Las formulaciones genéricas disponibles incluyen la combinación metformina/glipizida y metformina/glibenclamida. Una formulación genérica de metformina/rosiglitazona ha recibido aprobación tentativa por la Administración de Drogas y Alimentos (FDA) estadounidense, y se espera que lleguen al mercado a principios de 2012.[39]
Interacciones
La glucosamina puede hacer descender la efectividad de la metformina y otros fármacos empleados en el tratamiento de la diabetes.[40] La hierba china para adelgazar llamada Aristolochia suele ser nefrotóxico y a menudo se encuentra contaminado con fármacos hipoglucemiantes, incluyendo la misma metformina o el análogo fenformina, por lo tanto la combinación con hipoglucemiantes no es recomendada.[41]
Se debe consultar con un especialista calificado si se va a tomar la metformina en combinación con ciertos medicamentos como los antibióticos de la familia de aminoglucósidos, un inhibidor de la enzima convertidora de angiotensina para el tratamiento de la hipertensión arterial, antiinflamatorios no esteroideos, incluyendo el ibuprofeno, diuréticos, medicamentos de quimioterapia contra el cáncer o medicamentos para tratar el virus de la inmunodeficiencia humana.[25]
El antagonista de los receptores H2 cimetidina causa un incremento en la concentración plasmática de metformina, mediante la reducción de la depuración de la metformina por los riñones.[42] Tanto la metformina como la cimetidina se eliminan del cuerpo por secreción tubular, y ambos, en particular la forma catiónica (carga positiva) de la cimetidina, pueden competir por el mismo mecanismo de transporte tubular.[43] Un pequeño estudio doble ciego, randomizado encontró que el antibiótico cefalexina también aumenta las concentraciones de metformina por un mecanismo similar. [44] Teóricamente, otros medicamentos de naturaleza catiónica pueden producir el mismo efecto.[43]
Marcas comerciales
La metformina se puede encontrar en el mercado mundial tanto como diferentes formulaciones genéricas, como en distribción bajo los nombres farmacéuticos: Glafornil, Efficib o Janumet y en otros países:
- Venezuela: Glucofage, Glafornil, Glucaminol, Diaformina
- Colombia: Dimefor, Biguax, Diglufor
- México: Fortamet, Glucophage, Riomet
- España: Diabex, Diaformin, Fortamet, Glucophage, Glumetza, Meglucon, Riomet
- Estados Unidos: Glucophage, Glucophage XR, Glumetza, Fortamet, Riomet
La metformina viene en presentaciones de 500, 850 y 1000 mg y se administra la dosis máxima de 1 gr.
Véase también
Referencias
- ↑ a b BASAK, Subal Chandra; KUMAR, Kesevan Senthil and RAMALINGAM, Murugesan. Design and release characteristics of sustained release tablet containing metformin HCl (en inglés). Rev. Bras. Cienc. Farm. [online]. 2008, vol.44, n.3 [último acceso 2009-08-06], pp. 477-483. ISSN 1516-9332. doi: 10.1590/S1516-93322008000300018.
- ↑ a b Mark A. Sperling, ed. (2005). Sperling, M.A., Clínicas Pediátricas de Norteamérica 2005, no 6: Diabetes mellitus en la infancia. Elsevier, España. p. 1691. ISBN 8445816535.
- ↑ GUIMARAES, Camila et al. Tolerability and effectiveness of fluoxetine, metformin and sibutramine in reducing anthropometric and metabolic parameters in obese patients (en inglés). Arq Bras Endocrinol Metab [online]. 2006, vol.50, n.6 [cited 2009-08-06], pp. 1020-1025. ISSN 0004-2730. doi: 10.1590/S0004-27302006000600007.
- ↑ (Marzo 2007) [Lista modelo de medicamentos esenciales de la OMS http://www.who.int/medicines/publications/08_SPANISH_FINAL_EML15.pdf] — PDF (440 KB), 15tva edición, Organización Mundial de la Salud, pág 21. Último acceso 6 de agosto de 2009.
- ↑ Metformina como reductor del riesgo de cardiovascular:
- Selvin E, Bolen S, Yeh HC, et al. (October de 2008). «Cardiovascular outcomes in trials of oral diabetes medications: a systematic review». Arch Intern Med 168 (19): 2070-80. PMID 18955635. doi:10.1001/archinte.168.19.2070.
- «Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes (UKPDS 34). UK Prospective Diabetes Study (UKPDS) Group». Lancet 352 (9131): 854-65. 1998. PMID 9742977. doi:10.1016/S0140-6736(98)07037-8.
- Rappaport J, Fonseca V, 2005 Case-Based Study: From Prediabetes to Complications—Opportunities for Prevention. PLoS Med 2(2): e40. doi:10.1371/journal.pmed.0020040. Último acceso 6 de agosto de 2009.
- ↑ a b c d e f g Flórez, Jesús; Juan Antonio Armijo y África Mediavilla (2004). Farmacología humana (4ta edición). Elsevier, España. p. 396. ISBN 84-458-1290-4.
- ↑ a b Schnettler M., Angela (diciembre de 2002). «Sindrome de ovario poliquistico, puesta al dia en resistencia insulínica y metformina». Fronteras en Obstetricia y Ginecología 2 (2): 54-63. Consultado el 8 de agosto de 2009.
- ↑ Hundal R, Krssak M, Dufour S, Laurent D, Lebon V, Chandramouli V, Inzucchi S, Schumann W, Petersen K, Landau B, Shulman G (2000). «Mechanism by which metformin reduces glucose production in type 2 diabetes» (PDF). Diabetes 49 (12): 2063-9. PMID 11118008. doi:10.2337/diabetes.49.12.2063.
- ↑ ROSA W., Guillermo; SAENS N., Paulina and QUINCHAVIL A., Hernán. Metformina en el tratamiento de la anovulación asociada a insulino-resistencia (en español). Rev. chil. obstet. ginecol. [online]. 2004, vol.69, n.4 [cited 2009-08-06], pp. 286-289. ISSN 0717-7526.
- ↑ a b Kirpichnikov D, McFarlane SI, Sowers JR (2002). «Metformin: an update» (PDF). Ann Intern Med 137 (1): 25-33. PMID 12093242. Parámetro desconocido
|fechaaceso=ignorado (se sugiere|fechaacceso=) (ayuda) - ↑ Acción de la metformina sobre la AMPK:
- Towler MC, Hardie DG (2007). «AMP-activated protein kinase in metabolic control and insulin signaling». Circ Res 100 (3): 328-41. PMID 17307971. doi:10.1161/01.RES.0000256090.42690.05.
- Kronenberg, H.M. (2004). Williams Tratado de Endocrinología (11va edición). Elsevier, España. p. 1378. ISBN 8480863773.
- Vazquez-Martin A; Oliveras-Ferraros C, del Barco S, Martin-Castillo B, Menendez JA (marzo de 2009). «The antidiabetic drug metformin: a pharmaceutical AMPK activator to overcome breast cancer resistance to HER2 inhibitors while decreasing risk of cardiomyopathy». Ann Oncol 20 (3): 592-5. PMID 19153119. Consultado el 7 de agosto de 2009.
- ↑ Zhou G, Myers R, Li Y, Chen Y, Shen X, Fenyk-Melody J, Wu M, Ventre J, Doebber T, Fujii N, Musi N, Hirshman M, Goodyear L, Moller D (2001). «Role of AMP-activated protein kinase in mechanism of metformin action». J Clin Invest 108 (8): 1167-74. PMID 11602624. doi:10.1172/JCI13505.
- ↑ Kim YD, Park KG, Lee YS, et al. (2008). «Metformin inhibits hepatic gluconeogenesis through AMP-activated protein kinase-dependent regulation of the orphan nuclear receptor SHP». Diabetes 57 (2): 306-14. PMID 17909097. doi:10.2337/db07-0381.
- ↑ Zhang L, He H, Balschi JA (2007). «Metformin and phenformin activate AMP-activated protein kinase in the heart by increasing cytosolic AMP concentration». Am J Physiol Heart Circ Physiol 293 (1): H457-66. PMID 17369473. doi:10.1152/ajpheart.00002.2007.
- ↑ a b CUESTA GONZALEZ, Fanny, HOLGUIN MARTINEZ, Gloria, ARCHBOLD JOSEPH, Rosendo et al. Bioequivalence of two metformin formulations. iatreia.rev.fac.med.univ.antioquia. [online]. Julio/Sept. 2005, vol.18, no.3 [consultado 07 Agosto, 2009], p.289-301. Disponible en la World Wide Web: [1]. ISSN 0121-0793.
- ↑ a b c Katzung, Bertram G. (2007). «Chapter 41. Pancreatic Hormones & Antidiabetic Drugs». Basic & Clinical Pharmacology (9 edición). McGraw-Hill. ISBN 0071451536.
- ↑ a b c d e Figuerola, Daniel (2003). Diabetes (4ta edición). Elsevier, España. p. 141. ISBN 8445813005.
- ↑ Stafford, John M; Tom Elasy (agosto de 2007). «Treatment update: thiazolidinediones in combination with metformin for the treatment of type 2 diabetes». Vasc Health Risk Manag 3 (4): 503-510. Consultado el 9 de agosto de 2009. Parámetro desconocido
|pmcid=ignorado (ayuda); - ↑ Bolen S, Feldman L, Vassy J, et al. (2007). «Systematic review: comparative effectiveness and safety of oral medications for type 2 diabetes mellitus». Ann Intern Med 147 (6): 386-99. PMID 17638715.
- ↑ Drug Facts and Comparisons 2005 (59th edición). Lippincott Williams & Wilkins. October de 2004. ISBN 1-57439-193-3.
- ↑ Wulffele MG, Kooy A, Lehert P, Bets D, Ogterop JC, Borger van der Burg B, Donker AJ, Stehouwer CD. (November de 2003). «Effects of short-term treatment with metformin on serum concentrations of homocysteine, folate and vitamin B12 in type 2 diabetes mellitus: a randomized, placebo-controlled trial». J Intern Med 254 (5): 455-63. PMID 14535967. doi:10.1046/j.1365-2796.2003.01213.x.
- ↑ Andrès E, Noel E, Goichot B (2002). «Metformin-associated vitamin B12 deficiency». Arch Intern Med 162 (19): 2251-2. PMID 12390080. doi:10.1001/archinte.162.19.2251-a.
- ↑ Gilligan M (2002). «Metformin and vitamin B12 deficiency». Arch Intern Med 162 (4): 484-5. PMID 11863489. doi:10.1001/archinte.162.4.484.
- ↑ Ting R, Szeto C, Chan M, Ma K, Chow K (2006). «Risk factors of vitamin B(12) deficiency in patients receiving metformin». Arch Intern Med 166 (18): 1975-9. PMID 17030830. doi:10.1001/archinte.166.18.1975.
- ↑ a b c d e [MedlinePlus] Comprueba el valor del
|enlaceautor=(ayuda) (enero de 2007). «Metformina». Enciclopedia médica en español. Consultado el 8 de agosto de 2009. - ↑ Salpeter S, Greyber E, Pasternak G, Salpeter E (2003). «Risk of fatal and nonfatal lactic acidosis with metformin use in type 2 diabetes mellitus: systematic review and meta-analysis». Arch Intern Med 163 (21): 2594-602. PMID 14638559. doi:10.1001/archinte.163.21.2594.
- ↑ Pietropaolo M, 2005 An 18-Year-Old Patient with Type 1 Diabetes Undergoing Surgery. PLoS Med 2(5): e140. doi:10.1371/journal.pmed.0020140. Último acceso 6 de Agosto de 2009.
- ↑ a b c d e ORTEGA CARNICER, J. et al. Sobredosis de metformina secundaria a insuficienciarenal aguda: A propósito de 6 observaciones. Med. Intensiva [online]. 2007, vol.31, n.9 [citado 2009-08-07], pp. 521-525 . Disponible en: [2]. ISSN 0210-5691.
- ↑ Jones G, Macklin J, Alexander W (2003). «Contraindications to the use of metformin». BMJ 326 (7379): 4-5. PMID 12511434. doi:10.1136/bmj.326.7379.4.
- ↑ Eurich DT, McAlister FA, Blackburn DF, et al. (2007). «Benefits and harms of antidiabetic agents in patients with diabetes and heart failure: systematic review». BMJ 335 (7618): 497. PMID 17761999. doi:10.1136/bmj.39314.620174.80.
- ↑ Weir J (March 19, 1999). Guidelines with Regard to Metformin-Induced Lactic Acidosis and X-ray Contrast Medium Agents. Royal College of Radiologists. Retrieved on 2007-10-26 through the Internet Archive.
- ↑ Thomsen HS, Morcos SK (2003). «Contrast media and the kidney: European Society of Urogenital Radiology (ESUR) guidelines». Br J Radiol 76 (908): 513-8. PMID 12893691. doi:10.1259/bjr/26964464.
- ↑ Spiller HA, Quadrani DA (2004). «Toxic effects from metformin exposure». The Annals of pharmacotherapy 38 (5): 776-80. PMID 15031415. doi:10.1345/aph.1D468.
- ↑ Gjedde S, Christiansen A, Pedersen SB, Rungby J (2003). «Survival following a metformin overdose of 63 g: a case report». Pharmacol. Toxicol. 93 (2): 98-9. PMID 12899672. doi:10.1034/j.1600-0773.2003.930207.x.
- ↑ Harvey B, Hickman C, Hinson G, Ralph T, Mayer A (2005). «Severe lactic acidosis complicating metformin overdose successfully treated with high-volume venovenous hemofiltration and aggressive alkalinization». Pediatr Crit Care Med 6 (5): 598-601. PMID 16148825. doi:10.1097/01.PCC.0000162451.47034.4F.
- ↑ Guo PY, Storsley LJ, Finkle SN (2006). «Severe lactic acidosis treated with prolonged hemodialysis: recovery after massive overdoses of metformin». Semin Dial 19 (1): 80-3. PMID 16423187. doi:10.1111/j.1525-139X.2006.00123.x.
- ↑ Hranjec, T; , Kovac A, Kos J, Mao W, Chen JJ, Grollman AP y Jelaković B. (febrero de 2005). «Endemic nephropathy: the case for chronic poisoning by aristolochia.». 1: Croat Med J. 46 (1): 116-25. PMID 15726685. Consultado el 8 de agosto de 2009.
- ↑ «Questions and Answers about the Seizure of Paxil CR and Avandamet». U.S. Food and Drug Administration. March 4, 2005. Consultado el 27 de diciembre de 2006.
- ↑ «Teva Pharm announces settlement of generic Avandia, Avandamet, and Avandaryl litigation with GlaxoSmithKline». Reuters. September 27, 2007. Consultado el 17 de febrero de 2009.
- ↑ The Health Professional’s Guide to Popular Dietary Supplements, 2nd Edition. Allison Sarubin Fragakis, MS, RD, The American Dietetic Association, 2003.
- ↑ McQueen, Cydney E. (2007). Pharmaceutical care with dietary supplements. American Society of Health-System Pharmacists. p. 46. ISBN 1585281433.
- ↑ Somogyi A, Stockley C, Keal J, Rolan P, Bochner F (1987). «Reduction of metformin renal tubular secretion by cimetidine in man». Br J Clin Pharmacol 23 (5): 545-51. PMID 3593625.
- ↑ a b «Glucophage Side Effects & Drug Interactions». RxList.com. 2007. Consultado el 19 de noviembre de 2007.
- ↑ Jayasagar G, Krishna Kumar M, Chandrasekhar K, Madhusudan Rao C, Madhusudan Rao Y (2002). «Effect of cephalexin on the pharmacokinetics of metformin in healthy human volunteers». Drug Metabol Drug Interact 19 (1): 41-8. PMID 12222753.
Enlaces externos
 Wikimedia Commons alberga una galería multimedia sobre Metformina.
Wikimedia Commons alberga una galería multimedia sobre Metformina.- [3]
- [4]
- [5]
- [6]
- [7]
- [8]
