Resveratrol
| Resveratrol | ||
|---|---|---|
  | ||
| Nombre IUPAC | ||
| 5-[(E)-2-(4-hydroxyphenyl)ethenyl]benzene-1,3-diol | ||
| General | ||
| Otros nombres |
trans-3,5,4'-trihidroxistilbeno 3,4',5-stilbenetriol trans-resveratrol (E)-5-(p-hidroxistiril)resorcinol (E)-5-(4-hidroxiestiril)benceno-1,3-diol | |
| Fórmula estructural |
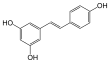 | |
| Fórmula molecular | C14H12O3 | |
| Identificadores | ||
| Número CAS | 501-36-0[1] | |
| Número RTECS | CZ8987000 | |
| ChEBI | 45713 | |
| ChEMBL | CHEMBL165 | |
| ChemSpider | 392875 | |
| DrugBank | 02709 | |
| PubChem | 445154 | |
| UNII | Q369O8926L | |
| KEGG | C03582 | |
| Propiedades físicas | ||
| Apariencia |
polvo blanco con un leve tono amarillo | |
| Masa molar | 228,25 g/mol | |
| Propiedades químicas | ||
| Solubilidad en agua | 0,03 g/L | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El resveratrol (3, 5, 4'-trihidroxi-trans-estilbeno) es un estilbenoide, un tipo de fenol natural, y una fitoalexina que se produce de manera natural en varias plantas como respuesta a una lesión o cuando se encuentran bajo el ataque de patógenos, tales como bacterias u hongos.[2] Las fuentes alimenticias del resveratrol incluyen la piel de las uvas, arándanos, frambuesas y moras.[3]
Efectos en la salud[editar]
Enfermedades del corazón[editar]
Existe muy poca evidencia acerca de los beneficios del resveratrol en las personas que ya padecen una enfermedad cardíaca.[4] En un meta-análisis de 2014, se encontró que el suplemento de resveratrol en dosis habituales no tiene ningún efecto sobre la presión arterial, pero puede ayudar a la misma si se utiliza en dosis altas. Los efectos secundarios todavía están en investigación.[5]
Cáncer[editar]
A partir de 2014, la evidencia de los efectos del resveratrol sobre el cáncer ha sido inconsistente por el momento .[6]
Metabolismo[editar]
Existe muy poca evidencia de que el resveratrol tenga un efecto en el metabolismo de los humanos.[7] Algunos datos tentativos apoyan que existe un beneficio potencial en el control de algunos biomarcadores en diabetes, pero se necesita más evidencia antes de que este tratamiento pueda ser recomendado.[8]
Esperanza de vida[editar]
En 2011, el efecto del resveratrol sobre la vida de los seres humanos no era claro.[9] En octubre de 2017 se obtuvo alguna evidencia de su efecto en la disminución de algunas características de la senescencia replicativa en células, tales como el aumento de factores de empalme de ARNm y alargamiento de telómeros[10]
Neuroprotección[editar]
Se ha observado que puede reducir la patología de tipo Alzheimer en cultivos celulares y en roedores. El resveratrol potencia los mecanismos protectores que degradan las proteínas anormales, como la β-amiloide y la tau hiperfosforilada. En el experimento, realizado con ratones transgénicos de Alzheimer, los científicos añadieron resveratrol a la dieta de dos grupos de roedores, un grupo de control y otro con patología de Alzheimer. En ambos casos, se observó una respuesta mejorada en el aprendizaje. En el caso de los afectados de Alzheimer, se vio un efecto de protección contra la pérdida de memoria y contra la patología. Además, el resveratrol activa la vía molecular de neuroprotección y longevidad de SIRT1.[11]
Un estudio del Institut de Investigacions Biomèdiques de Barcelona apoya el uso del resveratrol como agente nutracéutico contra la neurodegeneración y la enfermedad de Alzheimer.
Desencadenamiento y progresión de la patología de la enfermedad de Alzheimer inducida por una dieta alta en grasas[editar]
El resveratrol protegió contra la pérdida de memoria inducida por una dieta alta en grasas en ratones y previno la pérdida de memoria en ratones modificados genéticamente que modelan la enfermedad de Alzheimer. También redujo la manifestación de las características distintivas de la enfermedad de Alzheimer: placas amiloides y ovillos neurofibrilares.[12]
Efectos adversos[editar]
Los efectos adversos son desconocidos, pero un número de estudios clínicos han demostrado una buena tolerancia.[5][8]
Descubrimiento y nombre[editar]
El resveratrol fue mencionado por primera vez en un artículo de Japón en 1939 por Michio Takaoka, quien lo aisló de la venenosa pero medicinal, Veratrum álbum, una variedad de glandiflorum.[13] El nombre probablemente proviene del hecho de que es un derivado del resorcinol que proviene de una especie de Veratrum.[14] En 2003, David Sinclar de la escuela de medicina de Harvard reportó en la revista Nature que el resveratrol activa las sirtuinas en las células de levaduras. Este descubrimiento fue seguido por el lanzamiento de los farmacéuticos Sirtris. Mientras que los efectos farmacológicos de resveratrol no resultaron ser comercialmente viables, su descubrimiento condujo a grandes esfuerzos para desarrollar otro tipo de activadores de genes SIRT.
Farmacocinética[editar]
Una forma de administración del resveratrol para humanos es por vía oral, que consiste en la absorción directa a través de los tejidos en el interior de la boca. Al retener por un minuto un miligramo de resveratrol disuelto en alcohol en la boca, se logra medir dos minutos más tarde 37 ng/mL de resveratrol libre en el plasma. Este nivel de resveratrol sin cambios en la sangre sólo se puede lograr con 250 mg de resveratrol tomados en forma de comprimidos.[15] Sin embargo, la viabilidad de un método de administración oral se pone en duda debido a la baja solubilidad acuosa de la molécula. Para que un medicamento sea absorbido vía transmucosa debe estar en forma libre o disuelta.[16][17] El resveratrol se ajusta a los criterios de dosificación oral transmucosa, aunque vale la pena mencionar que la baja solubilidad acuosa, limita en gran medida la cantidad que puede ser absorbida a través de la mucosa bucal. Se esperaba que el resveratrol tomado por vía oral[18] pasara a través de la membrana mucosa de la boca y se absorbiera al igual que una dosis oral común, sin embargo, se demostró la necesidad de explorar el suministro oral en formulaciones farmacéuticas futuras.[17][19]
Mientras que el 70% del resveratrol administrado por vía oral se absorbe, su biodisponibilidad es de aproximadamente 0.5% debido a la glucuronidación hepática y sulfatación del mismo.[20] El rastro sin cambios de resveratrol por debajo de 5ng/ml puede ser detectado en sangre después de una dosis oral de 25 mg.[20] Incluso cuando una dosis muy grande (2,5 y 5 g) se administra en forma de pastilla no recubierta, la concentración de resveratrol en la sangre no logra alcanzar el nivel que se afirma es necesario para la prevención del cáncer sistémico.[21] Actualmente, se encuentra en producción una formulación de resveratrol en forma de goma de mascar, y se espera que proporcione concentraciones a nivel sanguíneo mucho más altas que las formulaciones orales. El resveratrol en su formulación patentada SRT-501 (3 o 5 g), desarrollada por Sirtris Pharmaceuticals, alcanzó niveles en sangre cinco a ocho veces mayores. Estos niveles se acercaron a la concentración necesaria para ejercer los efectos observados en modelos animales y en experimentos in vitro.[22] Sin embargo, el 5 de mayo de 2010, GlaxoSmithKline (GSK) aseveró que había suspendido un ensayo clínico de SRT501, la forma patentada de resveratrol, por cuestiones de seguridad, y terminó el estudio el 2 de diciembre de 2010.[23]
En ratas se observó menos del 5% de la dosis oral de resveratrol se encontraba libre en el plasma sanguíneo.[20][21][24][25][26] Los metabolitos más abundantes de resveratrol en los seres humanos, ratas y ratones son el trans-resveratrol-3-O-glucurónido y trans-resveratrol-3-sulfato. Walle sugiere que los sulfatos conjugados son la principal fuente de actividad,[20] por otro lado, Wang et al. afirman que son los glucurónidos, y Boocock[27] et al. hizo hincapié en la necesidad de un mayor estudio de los efectos de los metabolitos, incluyendo la posibilidad de desconjugación para liberar el resveratrol en las células. Goldberg, quien estudió la farmacocinética del resveratrol, catequinas y la quercetina en los seres humanos, concluyó "parece que los beneficios potenciales para la salud de estos compuestos, basados en las actividades in vitro de los compuestos no conjugados no son realistas y se han exagerado mucho. De hecho, la profusión de documentos que describen dichas actividades legítimamente pueden ser descritos como irrelevantes y engañosos. A partir de entonces, las investigaciones de esta naturaleza se concentran en los potenciales beneficios para la salud de sus conjugados glucurónidos y sulfatos”.[28]
La hipótesis de que el resveratrol del vino podría tener mayor biodisponibilidad que el de una píldora,[29][30] ha sido refutada por varios datos experimentales.[28][31] Por ejemplo, después de que cinco hombres tomaron 600 ml de vino tinto con un contenido de 3.2 mg/l de resveratrol antes del desayuno, se detectó resveratrol sin cambios en la sangre sólo en dos de ellos, y esto solo en cantidades traza (por debajo de 2,5 ng/ml). Los niveles de resveratrol parecían ser ligeramente mayores con el vino tinto (600 ml de vino tinto contienen 0.6 mg/ml; resveratrol dosis total de 0.5 mg) tomado con una comida: pequeñas cantidades (1-6 ng/ml) fueron encontradas en cuatro de diez sujetos.[31] En otro estudio, la farmacocinética del resveratrol (25 mg) no cambiaba si se tomaba con jugo de verduras, vino blanco o jugo de uva blanca. El nivel más alto de resveratrol sin cambios en el suero sanguíneo (7-9 ng/ml) se logró después de 30 minutos, y desapareció por completo de la sangre después de cuatro horas.[28] Los autores de ambos estudios concluyeron que las cantidades de resveratrol alcanzadas en la sangre son insuficientes para explicar la paradoja francesa. Los efectos benéficos del vino aparentemente podrían explicarse por los efectos del alcohol[28] o todo el complejo de sustancias que el vino contiene;[31] por ejemplo, los beneficios cardiovasculares del vino parecen estar correlacionados con el contenido de procianidinas.[32]
Mecanismos de acción[editar]
Algunos estudios han indicado que el resveratrol activa a SIRT1[33] y PGC-1α, además mejora el funcionamiento de las mitocondrias.[34] La capacidad directa del resveratrol de activar SIRT1 ha sido puesta en cuestión,[35][36][37] aunque muchos nuevos intentos tratan de volver a confirmar este vínculo,[38] una investigación más reciente ha demostrado que el resveratrol se una a TyrRS para potenciar una señalización en cascada de PARP1/NAD+ y a su vez activar p53 y AMPK por medio de la inhibición de SIRT1.[39]
En células tratadas con resveratrol se observa que la acción de la MnSOD (SOD2) aumenta catorce veces.[40] El MnSOD reduce el superóxido a peróxido de hidrógeno (H2O2), pero este no se incrementa debido a otra actividad celular. El superóxido O2- es un subproducto de la respiración en los complejos 1 y 3 de la cadena de transporte de electrones. No es "altamente tóxico, [pero] es capaz de extraer un electrón de la membrana biológica y otros componentes de las células, provocando reacciones en cadena de radicales libres. Por lo tanto, es esencial para mantener aniones superóxido en control dentro de la célula."[41] El MnSOD reduce al superóxido, y por lo tanto, confiere resistencia a la disfunción mitocondrial, transición de permeabilidad, y a la muerte por apoptosis en varias enfermedades. Se ha implicado en la extensión de la vida útil, inhibe el cáncer, (por ejemplo, cáncer de páncreas),[42][43] proporciona resistencia a la lesión por reperfusión y daño por irradiación.[44][45][46] Estos efectos también se han observado con el resveratrol. Robb et al. proponen que el MnSOD se incrementa por la vía RESV → SIRT1 / NAD + → FOXO3a → MnSOD. Se ha demostrado que el resveratrol causa que SIRT1 provoque la migración de los factores de transcripción FOXO al núcleo,[47] lo cual, estimula la actividad transcripcional de FOXO3a[48] y además mejora la desacetilación catalizada (actividad) de FOXO3a.[49] Se sabe que el MnSOD es un objetivo de FOXO3a, y la expresión de MnSOD está fuertemente inducida en células que sobre expresan FOXO3a. También se ha informado que la regulación desproporcionada de la expresión del superóxido dismutasa (SOD), catalasa (CAT) y de la glutatión peroxidasa (GPX) y su actividad enzimática en células de cáncer da como resultado la acumulación mitocondrial de H2O2, que a su vez induce la apoptosis de células cáncerigenas.[50]
El resveratrol interfiere con las tres etapas de la carcinogénesis-iniciación, promoción y progresión. Experimentos en cultivos celulares in vitro de varios tipos de sistemas subcelulares implican bastantes mecanismos relacionados con la actividad farmacológica del resveratrol. Estos mecanismos incluyen la modulación del factor de transcripción NF-kB,[51] la inhibición de la CYP1A1[52] de la isoenzima citocromo P450 (aunque esto puede no ser relevante para la bioactivación del CYP1A1 mediada por el procarcinógeno benzopireno),[53] alteraciones en acciones androgénicas,[54] en la expresión y actividad de la enzima ciclooxigenasa (COX). De manera in vitro, el resveratrol "inhibe la proliferación de líneas celulares de cáncer de páncreas humano." En algunos linajes de cultivo de células de cáncer, se ha demostrado que el resveratrol induce apoptosis, lo que significa que mata a las células, y por lo tanto, puede destruir células cancerosas.[54][55][56][57][58][59] Se ha presentado que el resveratrol induce al ligando Fas/Fas mediador de apoptosis, a p53 y a las ciclinas A, B1, y cinasas dependientes de ciclina CDK 1 y 2. El resveratrol también posee propiedades antioxidantes y anti-angiogénicos.[60][61]
Se informó que el resveratrol es eficaz combatiendo la disfunción neuronal y la muerte celular, y en teoría, podría ser eficaz contra enfermedades tales como la enfermedad de Huntington y Alzheimer.[62][63] De nuevo, esto aún no se ha probado para ninguna enfermedad de los seres humanos.
El resveratrol tiene acción inhibidora directa sobre el cultivo de tejido de fibroblastos cardíacos de rata y puede inhibir la progresión de la fibrosis cardíaca.[64]
El resveratrol también aumenta significativamente la producción natural de testosterona de modo que actúa tanto como un modulador selectivo del receptor de estrógeno[65] y un inhibidor de la aromatasa. También se ha encontrado que puede funcionar como agonista de la GPER (GPER 30).[66]
El resveratrol aumenta los niveles del glutatión intracelular a través de la regulación positiva Nrf2 dependiente de glutamilcistina gama ligasa en las células epiteliales del pulmón, lo que les protege contra el extracto de estrés oxidativo inducido del humo del cigarrillo.[67]
Otro mecanismo potencialmente importante que es común tanto en resveratrol como en la restricción calórica es la regulación de autofagia.[68] SIRT1 es un objetivo hipotético de ambos y se ha demostrado que facilita la autofagia a través de la inhibición de mTOR, que a su vez regula de manera negativa la autofagia.[69]
En 2012, se demostró que el resveratrol es capaz de inhibir de manera competitiva varias fosfodiesterasas, lo cual da como resultado un incremento en la concentración de AMPc en el citosol, esto actúa como un mensajero secundario para la activación de la vía Epac1/CaMKKβ/AMPK/SIRT1/PGC-1α. Este incremento en la concentración de AMPc permite aumentar la oxidación de los ácidos grasos, la biogénesis mitocondrial, la respiración mitocondrial y la gluconeogénesis.[70][71]
Propiedades químicas y físicas[editar]
Resveratrol (3,5,4’-trihidroxiestilbeno) es un estilbenoide, un derivado del estilbeno.[72]
Existe como dos isómeros geométricos: cis-(Z) y trans-(E), el isómero trans se muestra en la imagen superior. El resveratrol trans y cis puede estar libre o unido a la glucosa.
La forma trans puede sufrir isomerización a la forma cis cuando se expone a irradiación UV,[73] proceso llamado fotoisomerización:[74]
Recientemente, se ha observado que la irradiación ultravioleta en la forma cis del resveratrol induce más reacción fotoquímica, lo cual produce una molécula fluorescente llamada “Resveratrone”.[75]
Se encontró que el trans-resveratrol en polvo es estable en condiciones “de estabilidad acelerada” es decir, a 75% de humedad y 40 °C en presencia de aire.[76] El isómero trans también se estabiliza con la presencia de las proteínas de transporte.[77] El contenido de resveratrol también se mantuvo estable por un largo período en las pieles de las uvas durante la fermentación y almacenado.[78] Los datos de las formas más comunes IH y 13C del resveratrol se pueden encontrar en la literatura.[72]
Metabolismo[editar]
El resveratrol se metaboliza ampliamente en el cuerpo. Los principales sitios de su metabolismo son el hígado y el intestino, aunque los pulmones también están involucrados, pero con una diferencia entre las especies del metabolismo pulmonar.[79]
Biosíntesis
El resveratrol es producido en las plantas por medio de la acción de la enzima resveratrol sintetasa.[80]
Biotransformación
El patógeno fúngico Botrytis cinérea es capaz de oxidar el resveratrol en metabolitos que demuestran una atenuación en su actividad antifúngica. Entre ellos se incluyen los dímeros de resveratrol restritisol A, B y C, el resveratrol transdehidrodímero, leachinol F y palidol.[81] La bacteria del suelo Bacillus cereuscan puede ser utilizado para transformar resveratrol en piceído (resveratrol 3-O-beta-D-glucósido).[82]
Conceptos[editar]
Plantas[editar]
El resveratrol fue aislado originalmente por Takaoka, a partir de las raíces de eléboro en 1940, y más tarde, en 1963, de las raíces del centidonia japonés. Sin embargo, atrajo una mayor atención en 1992, cuando su presencia en el vino fue sugerido como explicación de los efectos cardioprotectores del mismo.[29]
En las uvas, el trans-resveratrol es una fitoalexina producida como protección contra el crecimiento de hongos patógenos tales como Botrytis cinerea.[83] Su presencia en la uva Vitis vinifera también es constitutivo, con la acumulación de resveratroles unidos y libres en las bayas maduras de diferentes niveles, de acuerdo con el genotipo.[84] En las uvas, el resveratrol se encuentra principalmente en la piel,[85] y en la uva moscatel, también en las semillas.[86] La cantidad que se encuentra en la piel de la uva también varía con el cultivar de esta, su origen geográfico, y la exposición a la infección por hongos. La cantidad de tiempo de fermentación de un vino que permanece en contacto con la piel de la uva es un determinante importante de su contenido de resveratrol.[72][85]
También se encuentra en Pinus strobus, el pino blanco del este.
Alimentos[editar]
Los niveles de resveratrol que se encuentran en los alimentos son muy variables. El vino tinto contiene entre 0,2 y 5,8 mg/l,[87] en función de la variedad de uva, mientras que el vino blanco tiene mucho menos, ya que el vino tinto se fermenta con las pieles, permitiendo que el vino extraiga el resveratrol, mientras que el vino blanco se fermenta después de que la piel se ha eliminado.[85][88] La composición del vino es diferente a la de las uvas, ya que la extracción de resveratrol de la uva depende de la duración del contacto con la piel, y los resveratrol 3-glucósidos están parcialmente hidrolizados, produciendo tanto trans- como cis- resveratrol.[72] Varios informes han indicado que la uva moscatel puede contener altas concentraciones de resveratrol, y que los vinos producidos a partir de estas uvas, tanto rojos como blancos, pueden contener más de 40 mg/l,[86][89] Sin embargo, estudios posteriores han encontrado poco o nada de resveratrol en las diferentes variedades de uva moscatel.[90][91]
Una de las fuentes más prometedoras son los cacahuates, especialmente germinados donde mismo que el contenido rival de las uvas. Antes de la germinación, en el rango de 2.3 a 4.5 mg/g, y después de la germinación, en el intervalo de 11,7 a 25,7 mg/g dependiendo del cultivo de maní.[92]
El fruto de la morera (esp. De la piel)[93] también es una fuente, y se vende como un suplemento nutricional.
El cacao en polvo, el chocolate para hornear y el chocolate negro también aportan bajos niveles de resveratrol en cantidades normales de consumo (0,35 a 1,85 mg/kg).[94]
Vino y jugo de uvas[editar]
La concentración de trans-resveratrol medido en 40 vinos de la Toscana osciló entre 0,3 a 2,1 mg/l en los 32 vinos tintos probados y tenía un máximo de 0,1 mg/l en los 8 vinos blancos de la prueba. En las muestras analizadas se detectaron los isómeros de resveratrol cis- y trans-. Los niveles de cis-resveratrol fueron comparables a los del isómero trans. Se extienden de 0,5 mg/l a 1,9 mg/l en los vinos tintos y tenían un máximo de 0,2 mg/l en los vinos blancos.[95] Los informes sugieren algunos aspectos del proceso de elaboración del vino que convierte piceído a resveratrol en el vino, este parece tener el doble de la concentración media de resveratrol en los zumos comerciales equivalentes.[86] En general, los vinos elaborados a partir de uvas de las variedades Pinot Noir y St. Laurent mostraron el nivel más alto de trans-resveratrol, aunque sin vino o región aún no se puede decir que produce que estos vinos tengan concentraciones significativamente más altas que cualquier otro vino o región.[96]Alimentos seleccionados[editar]
| Alimento | Porción | Resveratrol total (mg)[94][97] |
|---|---|---|
| Cacahuates (crudo) | 1 c (146 g) | 0.01 – 0.26 |
| Cacahuates (hervidos) | 1 c (180 g) | 0.32 – 1.28 |
| Mantequilla de maní | 1 c (258 g) | 0.04 – 0.13 |
| Uvas rojas | 1 c (160 g) | 0.24 – 1.25 |
| Polvo de cacao | 1 c (200 g) | 0.28 – 0.46 |
Suplementos[editar]
Como resultado de la extensa cobertura de noticias,[98][99] se dio un aumento en las ventas de estos suplementos, en 2006.[100] Esto a pesar de la existencia de estudios que advierten que los beneficios para los seres humanos no han sido probados.[100][101][102]
Los suplementos varían en pureza y pueden contener desde un 50% hasta un 99% de resveratrol. Muchas marcas consisten en un extracto purificado de centidonia japonés (Polygonum cuspidatum), una especie introducida en muchos países. Estos contienen aproximadamente 50% en peso de resveratrol, así como emodina, que puede tener un efecto laxante en altas cantidades.[103] El resveratrol puede ser producido a partir del piceído glucósido del centidonia japonés fermentado por Aspergillus oryzae.[104]
David Sinclair, científico y profesor de la Universidad de Harvard es citado a menudo en los anuncios en línea para los suplementos de resveratrol, muchos de los cuales implican la aprobación del producto anunciado; sin embargo, Sinclair, quien ha estudiado ampliamente el resveratrol, asevera que él nunca pronunció muchas de las declaraciones que se le atribuyen en estos sitios.[105]
Investigación[editar]
Están surgiendo una gran serie de estudios prometedores en animales y algunos datos de ensayos clínicos en humanos.[106][107] Sin embargo, no hay pruebas suficientes para recomendar el consumo de resveratrol más allá de la cantidad que se puede obtener a través de fuentes dietéticas, y aún son necesarios más ensayos clínicos en humanos.[108]
Cáncer[editar]
Los resultados de los ensayos clínicos en humanos acerca de los efectos del resveratrol sobre el cáncer son inconsistentes. Las pruebas de resveratrol en modelos animales de cáncer también han mostrado resultados mixtos.[6] Existe evidencia fuerte sobre la acción anticancerígena del resveratrol en tumores que pueden estar en contacto directo con el compuesto, tales como los de la piel y tumores del tracto gastrointestinal. Para otros tipos de cáncer, la evidencia es incierta, incluso si se utilizan dosis masivas de resveratrol.[109] El tratamiento con resveratrol aparenta la prevención del desarrollo de tumores en la mama en modelos animales; sin embargo, no tuvo efecto sobre el crecimiento de tumores ya existentes. El tratamiento con altas dosis de resveratrol en ratones prepúberes mejora la formación de tumores. Inyectado en dosis altas en ratones, el resveratrol reduce el crecimiento de los neuroblastomas.[109]
Efectos cardioprotectores[editar]
El consumo moderado del vino tinto se asocia con la disminución del riesgo de padecer enfermedades cardíacas.[110] Más conocido como "la paradoja francesa".[111][112] Los estudios sugieren que el resveratrol en el vino tinto puede jugar un papel importante en este fenómeno.[113] Parece estimular la actividad[114] de la óxido nítrico sintasa endotelial (eNOS) e inhibición de la agregación plaquetaria.[115]
Efectos antidiabéticos[editar]
Los estudios del resveratrol en animales han demostrado efectos antidiabéticos.[34][116] Se comprobó que este compuesto puede actuar como agonista de PPAR gamma, receptor nuclear que es un objetivo farmacológico actual para el tratamiento de la diabetes tipo 2.[117] Un meta-análisis de estudios humanos basados en las observaciones en 283 participantes determinó que el tratamiento con resveratrol resultaba en una mejora en los valores de glucosa en ayunas ( -0.29 mmol/l, 95% CI: -0.51, -0.06, p < 0.01) y los niveles de insulina (-0.64 U/mL, 95% CI: -0.95, -0.32, p < 0.0001). El tratamiento también mejoraba el índice HOMA-IR así también como la presión sistólica y diastólica en pacientes con diabetes tipo 2. Los cambios en valores de hemoglobina A1c (HbA1C), LDL y HDL no eran estadísticamente significativos.[118]
Rejuvenecimiento visual[editar]
El estrés oxidativo inducido por la radiación ultravioleta es una de las principales causas de envejecimiento prematuro al traspasar la mácula por el cristalino en la absorción de la luz que se dispersa por la curvatura de la córnea como arco iris refractando dentro del ojo por lo cual daña el mismo por variables de intensidad y exposición. En investigaciones se aplicó clorhidroxidocarbofitosodico RESVERATROLina en gotas oftálmicas en más de 800 pacientes. Estos colirios oftalmológicos investigados por el Dr. Hector Damian Brzostowski fueron nombrados en la investigación "Prevention of eyes". Se colocó el producto en perros con cataratas por vejez o cataratas por diabetes y los resultados fueron que en 7 días se logró la limpieza total de la cataratas de estos caninos, por lo tanto pasamos a seres humanos y los separamos en 400 pacientes de diferentes patologías obteniendo resultados clínicos favorables. Al ingresar el Resveratrol a la mácula es absorbida por las células oculares de la cual se activa por la glutamina intracelular y al ingresar los rayos ultravioletas activa la Resveratrola fluorescente dentro de la membrana plasmática tomando velocidad de traspaso de la membrana gracias al clorhidroxidocarbofitosodico regenerando las células dañadas. La concentración "ResveratrolINA" debido a su efecto sobre la vía mesolímbica del cerebro, activa la regeneración general de la mácula y cura enfermedades como miopía, astigmatismo y 10 patologías más referentes a la vista. Actualmente se produce en una empresa brasilera de manipulados bajopPatente y responsabilidad del Dr. Hector Damian Brzostowski creador del activo, el cual produce este producto que se comercializa hace más de 20 años. El activo fue comparado a resultados anteriores en genes SIRT.
Protección de la piel[editar]
El estrés oxidativo inducido por la radiación ultravioleta es una de las principales causas de envejecimiento prematuro de la piel. Los efectos fotoprotectores de varios polifenoles conocidos por sus propiedades antioxidantes, incluyendo el resveratrol, se han investigado in silico y en condiciones de aplicación tópica.[119][120]
Psicológico[editar]
En varios modelos animales el resveratrol ha tenido un efecto antidepresivo,[119] pero aún no está claro si existe o no un efecto en los seres humanos.[120]
Compuestos relacionados[editar]
- Pallidol, dímero del resveratrol
- Piceatannol, metabolito activo del resveratrol que se encuentra en el vino
Véase también[editar]
Referencias[editar]
- ↑ Número CAS
- ↑ Fremont, Lucie (January 2000). «Biological Effects of Resveratrol». Life Sciences 66: 663-673. PMID 10680575. doi:10.1016/S0024-3205(99)00410-5. Consultado el 6 de junio de 2014.
- ↑ Jasiński M, Jasińska L, Ogrodowczyk M; Jasińska; Ogrodowczyk (August 2013). «Resveratrol in prostate diseases - a short review». Cent European J Urol 66 (2): 144-9. PMC 3936154. PMID 24579014. doi:10.5173/ceju.2013.02.art8 (inactivo 2015-02-01).
- ↑ Tomé-Carneiro J, Gonzálvez M, Larrosa M, Yáñez-Gascón MJ, García-Almagro FJ, Ruiz-Ros JA, Tomás-Barberán FA, García-Conesa MT, Espín JC; Gonzálvez; Larrosa; Yáñez-Gascón; García-Almagro; Ruiz-Ros; Tomás-Barberán; García-Conesa et al. (Jul 2013). «Resveratrol in primary and secondary prevention of cardiovascular disease: a dietary and clinical perspective». Annals of the New York Academy of Sciences 1290: 37-51. Bibcode:2013NYASA1290...37T. PMID 23855464. doi:10.1111/nyas.12150.
- ↑ a b Liu Y, Ma W, Zhang P, He S, Huang D; Ma; Zhang; He; Huang (March 2014). «Effect of resveratrol on blood pressure: A meta-analysis of randomized controlled trials». Clinical Nutrition 34 (1): 27-34. PMID 24731650. doi:10.1016/j.clnu.2014.03.009.
- ↑ a b Carter LG, D'Orazio JA, Pearson KJ; d'Orazio; Pearson (June 2014). «Resveratrol and cancer: focus on in vivo evidence». Endocr. Relat. Cancer 21 (3): R209-25. PMC 4013237. PMID 24500760. doi:10.1530/ERC-13-0171.
- ↑ Poulsen MM, Jørgensen JO, Jessen N, Richelsen B, Pedersen SB; Jørgensen; Jessen; Richelsen; Pedersen (Jul 2013). «Resveratrol in metabolic health: an overview of the current evidence and perspectives». Annals of the New York Academy of Sciences 1290: 74-82. Bibcode:2013NYASA1290...74P. PMID 23855468. doi:10.1111/nyas.12141.
- ↑ a b Hausenblas HA, Schoulda JA, Smoliga JM; Schoulda; Smoliga (19 de agosto de 2014). «Resveratrol treatment as an adjunct to pharmacological management in type 2 diabetes mellitus-systematic review and meta-analysis». Molecular nutrition & food research 59 (1): 147-59. PMID 25138371. doi:10.1002/mnfr.201400173.
- ↑ Fernández AF, Fraga MF; Fraga (Jul 2011). «The effects of the dietary polyphenol resveratrol on human healthy aging and lifespan». Epigenetics : official journal of the DNA Methylation Society 6 (7): 870-4. PMID 21613817. doi:10.4161/epi.6.7.16499.
- ↑ Eva Latorre ,Vishal C. Birar ,Angela N. Sheerin ,J. Charles C. Jeynes ,Amy Hooper ,Helen R. Dawe ,David Melzer ,Lynne S. Cox ,Richard G. A. Faragher ,Elizabeth L. OstlerAutor, Lorna W. HarriesAutor (Oct 2017). «Small molecule modulation of splicing factor expression is associated with rescue from cellular senescence». BMC Cell Biology 18 (31). doi:10.1186/s12860-017-0147-7.
- ↑ Resveratrol Induces Brain Resilience Against Alzheimer Neurodegeneration Through Proteostasis EnhancementCorpas R, Griñán-Ferré C, Rodríguez-Farré E, Pallàs M, Sanfeliu C. (Feb 2019). «Resveratrol Induces Brain Resilience Against Alzheimer Neurodegeneration Through Proteostasis Enhancement». Mol Neurobiol 56 (2). doi:10.1007/s12035-018-1157-y.
- ↑ «Resveratrol Protects Cognition in Alzheimer’s Mice Fed High-Fat Diets». www.nmn.com. Consultado el 21 de enero de 2021.
- ↑ Resveratrol, a new phenolic compound, from Veratrum grandiflorum. M Takaoka, Journal of the Chemical Society of Japan, 1939, volume 60, pages 1090-1100 (abstract)
- ↑ Schröder, Joachim (6 de marzo de 2010). «Discovery of resveratrol». Resveratrol. Archivado desde el original el 26 de agosto de 2014. Consultado el 18 de marzo de 2016.
- ↑ Asensi M, Medina I, Ortega A, Carretero J, Baño MC, Obrador E, Estrela JM; Medina; Ortega; Carretero; Baño; Obrador; Estrela (August 2002). «Inhibition of cancer growth by resveratrol is related to its low bioavailability». Free Radic. Biol. Med. 33 (3): 387-98. PMID 12126761. doi:10.1016/S0891-5849(02)00911-5.
- ↑ Madhav NV, Shakya AK, Shakya P, Singh K; Shakya; Shakya; Singh (November 2009). «Orotransmucosal drug delivery systems: a review». J Control Release 140 (1): 2-11. PMID 19665039. doi:10.1016/j.jconrel.2009.07.016.
- ↑ a b Ansari KA, Vavia PR, Trotta F, Cavalli R; Vavia; Trotta; Cavalli (March 2011). «Cyclodextrin-based nanosponges for delivery of resveratrol: in vitro characterisation, stability, cytotoxicity and permeation study». AAPS PharmSciTech 12 (1): 279-86. PMC 3066340. PMID 21240574. doi:10.1208/s12249-011-9584-3.
- ↑ Shojaei AH (1998). «Buccal mucosa as a route for systemic drug delivery: a review». J Pharm Pharm Sci 1 (1): 15-30. PMID 10942969.
- ↑ Santos AC, Veiga F, Ribeiro AJ; Veiga; Ribeiro (August 2011). «New delivery systems to improve the bioavailability of resveratrol». Expert Opin Drug Deliv 8 (8): 973-90. PMID 21668403. doi:10.1517/17425247.2011.581655.
- ↑ a b c d Walle T, Hsieh F, DeLegge MH, Oatis JE, Walle UK; Hsieh; Delegge; Oatis Jr; Walle (December 2004). «High absorption but very low bioavailability of oral resveratrol in humans». Drug Metab. Dispos. 32 (12): 1377-82. PMID 15333514. doi:10.1124/dmd.104.000885.
- ↑ a b Boocock DJ, Faust GE, Patel KR, Schinas AM, Brown VA, Ducharme MP, Booth TD, Crowell JA, Perloff M, Gescher AJ, Steward WP, Brenner DE; Faust; Patel; Schinas; Brown; Ducharme; Booth; Crowell; Perloff; Gescher; Steward; Brenner (June 2007). «Phase I dose escalation pharmacokinetic study in healthy volunteers of resveratrol, a potential cancer chemopreventive agent». Cancer Epidemiol. Biomarkers Prev. 16 (6): 1246-52. PMID 17548692. doi:10.1158/1055-9965.EPI-07-0022.
- ↑ Elliott PJ, Jirousek M; Jirousek (April 2008). «Sirtuins: novel targets for metabolic disease». Current Opinion in Investigational Drugs 9 (4): 371-8. PMID 18393104.
- ↑ «A Clinical Study to Assess the Safety and Activity of SRT501 Alone or in Combination With Bortezomib in Patients With Multiple Myeloma». NIH. Consultado el 18 de marzo de 2016.
- ↑ Wenzel E, Soldo T, Erbersdobler H, Somoza V; Soldo; Erbersdobler; Somoza (May 2005). «Bioactivity and metabolism of trans-resveratrol orally administered to Wistar rats». Mol Nutr Food Res 49 (5): 482-94. PMID 15779067. doi:10.1002/mnfr.200500003.
- ↑ Marier JF, Vachon P, Gritsas A, Zhang J, Moreau JP, Ducharme MP; Vachon; Gritsas; Zhang; Moreau; Ducharme (July 2002). «Metabolism and disposition of resveratrol in rats: extent of absorption, glucuronidation, and enterohepatic recirculation evidenced by a linked-rat model». J. Pharmacol. Exp. Ther. 302 (1): 369-73. PMID 12065739. doi:10.1124/jpet.102.033340.
- ↑ Abd El-Mohsen M, Bayele H, Kuhnle G, Gibson G, Debnam E, Kaila Srai S, Rice-Evans C, Spencer JP; Bayele; Kuhnle; Gibson; Debnam; Kaila Srai; Rice-Evans; Spencer (July 2006). «Distribution of [3H]trans-resveratrol in rat tissues following oral administration». Br. J. Nutr. 96 (1): 62-70. PMID 16869992. doi:10.1079/BJN20061810.
- ↑ Wang LX, Heredia A, Song H, Zhang Z, Yu B, Davis C, Redfield R; Heredia; Song; Zhang; Yu; Davis; Redfield (October 2004). «Resveratrol glucuronides as the metabolites of resveratrol in humans: characterization, synthesis, and anti-HIV activity». J Pharm Sci 93 (10): 2448-57. PMID 15349955. doi:10.1002/jps.20156.
- ↑ a b c d Goldberg DM, Yan J, Soleas GJ; Yan; Soleas (February 2003). «Absorption of three wine-related polyphenols in three different matrices by healthy subjects». Clin. Biochem. 36 (1): 79-87. PMID 12554065. doi:10.1016/S0009-9120(02)00397-1.
- ↑ a b Baur JA, Sinclair DA; Sinclair (June 2006). «Therapeutic potential of resveratrol: the in vivo evidence». Nature Reviews Drug Discovery 5 (6): 493-506. PMID 16732220. doi:10.1038/nrd2060.
- ↑ Wenzel E, Somoza V; Somoza (May 2005). «Metabolism and bioavailability of trans-resveratrol». Mol Nutr Food Res 49 (5): 472-81. PMID 15779070. doi:10.1002/mnfr.200500010.
- ↑ a b c Vitaglione P, Sforza S, Galaverna G, Ghidini C, Caporaso N, Vescovi PP, Fogliano V, Marchelli R; Sforza; Galaverna; Ghidini; Caporaso; Vescovi; Fogliano; Marchelli (May 2005). «Bioavailability of trans-resveratrol from red wine in humans». Mol Nutr Food Res 49 (5): 495-504. PMID 15830336. doi:10.1002/mnfr.200500002.
- ↑ Corder R, Mullen W, Khan NQ, Marks SC, Wood EG, Carrier MJ, Crozier A; Mullen; Khan; Marks; Wood; Carrier; Crozier (November 2006). «Oenology: red wine procyanidins and vascular health». Nature 444 (7119): 566. Bibcode:2006Natur.444..566C. PMID 17136085. doi:10.1038/444566a.
- ↑ Alcaín FJ, Villalba JM; Villalba (April 2009). «Sirtuin activators». Expert Opin Ther Pat 19 (4): 403-14. PMID 19441923. doi:10.1517/13543770902762893.
- ↑ a b Lagouge M, Argmann C, Gerhart-Hines Z, Meziane H, Lerin C, Daussin F, Messadeq N, Milne J, Lambert P, Elliott P, Geny B, Laakso M, Puigserver P, Auwerx J; Argmann; Gerhart-Hines; Meziane; Lerin; Daussin; Messadeq; Milne; Lambert; Elliott; Geny; Laakso; Puigserver; Auwerx (December 2006). «Resveratrol improves mitochondrial function and protects against metabolic disease by activating SIRT1 and PGC-1alpha». Cell 127 (6): 1109-22. PMID 17112576. doi:10.1016/j.cell.2006.11.013.
- ↑ Kaeberlein M, McDonagh T, Heltweg B, Hixon J, Westman EA, Caldwell SD, Napper A, Curtis R, DiStefano PS, Fields S, Bedalov A, Kennedy BK; McDonagh; Heltweg; Hixon; Westman; Caldwell; Napper; Curtis; Distefano; Fields; Bedalov; Kennedy (April 2005). «Substrate-specific activation of sirtuins by resveratrol». J. Biol. Chem. 280 (17): 17038-45. PMID 15684413. doi:10.1074/jbc.M500655200.
- ↑ Beher D, Wu J, Cumine S, Kim KW, Lu SC, Atangan L, Wang M; Wu; Cumine; Kim; Lu; Atangan; Wang (December 2009). «Resveratrol is not a direct activator of SIRT1 enzyme activity». Chem Biol Drug Des 74 (6): 619-24. PMID 19843076. doi:10.1111/j.1747-0285.2009.00901.x.
- ↑ Pacholec M, Bleasdale JE, Chrunyk B, Cunningham D, Flynn D, Garofalo RS, Griffith D, Griffor M, Loulakis P, Pabst B, Qiu X, Stockman B, Thanabal V, Varghese A, Ward J, Withka J, Ahn K; Bleasdale; Chrunyk; Cunningham; Flynn; Garofalo; Griffith; Griffor; Loulakis; Pabst; Qiu; Stockman; Thanabal; Varghese; Ward; Withka; Ahn (March 2010). «SRT1720, SRT2183, SRT1460, and resveratrol are not direct activators of SIRT1». J. Biol. Chem. 285 (11): 8340-51. PMC 2832984. PMID 20061378. doi:10.1074/jbc.M109.088682.
- ↑ «Fortifying the Link between SIRT1, Resveratrol, and Mitochondrial Function». Cell Metabolism 15: 566-567. doi:10.1016/j.cmet.2012.04.016.
- ↑ http://www.nature.com/nature/journal/vaop/ncurrent/full/nature14028.html
- ↑ Robb EL, Page MM, Wiens BE, Stuart JA; Page; Wiens; Stuart (March 2008). «Molecular mechanisms of oxidative stress resistance induced by resveratrol: Specific and progressive induction of MnSOD». Biochem. Biophys. Res. Commun. 367 (2): 406-12. PMID 18167310. doi:10.1016/j.bbrc.2007.12.138.
- ↑ Radák, Zsolt (2000). Free radicals in exercise and aging. Champaign, IL: Human Kinetics. p. 39. ISBN 978-0-88011-881-1.
- ↑ Cullen JJ, Weydert C, Hinkhouse MM, Ritchie J, Domann FE, Spitz D, Oberley LW; Weydert; Hinkhouse; Ritchie; Domann; Spitz; Oberley (March 2003). «The role of manganese superoxide dismutase in the growth of pancreatic adenocarcinoma». Cancer Res. 63 (6): 1297-303. PMID 12649190.
- ↑ «Mounting evidence shows red wine antioxidant kills cancer». University of Rochester Medical Center. 26 de marzo de 2008. Consultado el 10 de agosto de 2010.
- ↑ Sun J, Folk D, Bradley TJ, Tower J; Folk; Bradley; Tower (June 2002). «Induced overexpression of mitochondrial Mn-superoxide dismutase extends the life span of adult Drosophila melanogaster». Genetics 161 (2): 661-72. PMC 1462135. PMID 12072463.
- ↑ Hu D, Cao P, Thiels E, Chu CT, Wu GY, Oury TD, Klann E; Cao; Thiels; Chu; Wu; Oury; Klann (March 2007). «Hippocampal long-term potentiation, memory, and longevity in mice that overexpress mitochondrial superoxide dismutase». Neurobiol Learn Mem 87 (3): 372-84. PMC 1847321. PMID 17129739. doi:10.1016/j.nlm.2006.10.003.
- ↑ Wong GH (May 1995). «Protective roles of cytokines against radiation: induction of mitochondrial MnSOD». Biochim. Biophys. Acta 1271 (1): 205-9. PMID 7599209. doi:10.1016/0925-4439(95)00029-4.
- ↑ Stefani M, Markus MA, Lin RC, Pinese M, Dawes IW, Morris BJ; Markus; Lin; Pinese; Dawes; Morris (October 2007). «The effect of resveratrol on a cell model of human aging». Annals of the New York Academy of Sciences 1114: 407-18. Bibcode:2007NYASA1114..407S. PMID 17804521. doi:10.1196/annals.1396.001.
- ↑ Brunet A, Sweeney LB, Sturgill JF, Chua KF, Greer PL, Lin Y, Tran H, Ross SE, Mostoslavsky R, Cohen HY, Hu LS, Cheng HL, Jedrychowski MP, Gygi SP, Sinclair DA, Alt FW, Greenberg ME; Sweeney; Sturgill; Chua; Greer; Lin; Tran; Ross; Mostoslavsky; Cohen; Hu; Cheng; Jedrychowski; Gygi; Sinclair; Alt; Greenberg (March 2004). «Stress-dependent regulation of FOXO transcription factors by the SIRT1 deacetylase». Science 303 (5666): 2011-5. Bibcode:2004Sci...303.2011B. PMID 14976264. doi:10.1126/science.1094637.
- ↑ Kops GJ, Dansen TB, Polderman PE, Saarloos I, Wirtz KW, Coffer PJ, Huang TT, Bos JL, Medema RH, Burgering BM; Dansen; Polderman; Saarloos; Wirtz; Coffer; Huang; Bos; Medema; Burgering (September 2002). «Forkhead transcription factor FOXO3a protects quiescent cells from oxidative stress». Nature 419 (6904): 316-21. Bibcode:2002Natur.419..316K. PMID 12239572. doi:10.1038/nature01036.
- ↑ Khan MA, Chen HC, Wan XX, Tania M, Xu AH, Chen FZ, Zhang DZ; Chen; Wan; Tania; Xu; Chen; Zhang (March 2013). «Regulatory effects of resveratrol on antioxidant enzymes: a mechanism of growth inhibition and apoptosis induction in cancer cells». Mol Cells 35 (3): 219-25. PMC 3887918. PMID 23456297. doi:10.1007/s10059-013-2259-z.
- ↑ Leiro J, Arranz JA, Fraiz N, Sanmartín ML, Quezada E, Orallo F; Arranz; Fraiz; Sanmartín; Quezada; Orallo (February 2005). «Effect of cis-resveratrol on genes involved in nuclear factor kappa B signaling». Int. Immunopharmacol. 5 (2): 393-406. PMID 15652768. doi:10.1016/j.intimp.2004.10.006.
- ↑ Chun YJ, Kim MY, Guengerich FP; Kim; Guengerich (August 1999). «Resveratrol is a selective human cytochrome P450 1A1 inhibitor». Biochem. Biophys. Res. Commun. 262 (1): 20-4. PMID 10448061. doi:10.1006/bbrc.1999.1152.
- ↑ Schwarz D, Roots I; Roots (April 2003). «In vitro assessment of inhibition by natural polyphenols of metabolic activation of procarcinogens by human CYP1A1». Biochem. Biophys. Res. Commun. 303 (3): 902-7. PMID 12670496. doi:10.1016/S0006-291X(03)00435-2.
- ↑ a b Benitez DA, Pozo-Guisado E, Alvarez-Barrientos A, Fernandez-Salguero PM, Castellón EA; Pozo-Guisado; Alvarez-Barrientos; Fernandez-Salguero; Castellón (2007). «Mechanisms involved in resveratrol-induced apoptosis and cell cycle arrest in prostate cancer-derived cell lines». J. Androl. 28 (2): 282-93. PMID 17050787. doi:10.2164/jandrol.106.000968.
- ↑ Faber AC, Chiles TC; Chiles (December 2006). «Resveratrol induces apoptosis in transformed follicular lymphoma OCI-LY8 cells: evidence for a novel mechanism involving inhibition of BCL6 signaling». Int. J. Oncol. 29 (6): 1561-6. PMID 17088997. doi:10.3892/ijo.29.6.1561.
- ↑ Riles WL, Erickson J, Nayyar S, Atten MJ, Attar BM, Holian O; Erickson; Nayyar; Atten; Attar; Holian (September 2006). «Resveratrol engages selective apoptotic signals in gastric adenocarcinoma cells». World J. Gastroenterol. 12 (35): 5628-34. PMC 4088162. PMID 17007014.
- ↑ Sareen D, van Ginkel PR, Takach JC, Mohiuddin A, Darjatmoko SR, Albert DM, Polans AS; Van Ginkel; Takach; Mohiuddin; Darjatmoko; Albert; Polans (September 2006). «Mitochondria as the primary target of resveratrol-induced apoptosis in human retinoblastoma cells». Invest. Ophthalmol. Vis. Sci. 47 (9): 3708-16. PMID 16936077. doi:10.1167/iovs.06-0119.
- ↑ Tang HY, Shih A, Cao HJ, Davis FB, Davis PJ, Lin HY; Shih; Cao; Davis; Davis; Lin (August 2006). «Resveratrol-induced cyclooxygenase-2 facilitates p53-dependent apoptosis in human breast cancer cells». Mol. Cancer Ther. 5 (8): 2034-42. PMID 16928824. doi:10.1158/1535-7163.MCT-06-0216.
- ↑ Aziz MH, Nihal M, Fu VX, Jarrard DF, Ahmad N; Nihal; Fu; Jarrard; Ahmad (May 2006). «Resveratrol-caused apoptosis of human prostate carcinoma LNCaP cells is mediated via modulation of phosphatidylinositol 3'-kinase/Akt pathway and Bcl-2 family proteins». Mol. Cancer Ther. 5 (5): 1335-41. PMID 16731767. doi:10.1158/1535-7163.MCT-05-0526.
- ↑ Cao Y, Fu ZD, Wang F, Liu HY, Han R; Fu; Wang; Liu; Han (June 2005). «Anti-angiogenic activity of resveratrol, a natural compound from medicinal plants». J Asian Nat Prod Res 7 (3): 205-13. PMID 15621628. doi:10.1080/10286020410001690190.
- ↑ Hung LM, Chen JK, Huang SS, Lee RS, Su MJ; Chen; Huang; Lee; Su (August 2000). «Cardioprotective effect of resveratrol, a natural antioxidant derived from grapes». Cardiovasc. Res. 47 (3): 549-55. PMID 10963727. doi:10.1016/S0008-6363(00)00102-4.
- ↑ Marambaud P, Zhao H, Davies P; Zhao; Davies (November 2005). «Resveratrol promotes clearance of Alzheimer's disease amyloid-beta peptides». J. Biol. Chem. 280 (45): 37377-82. PMID 16162502. doi:10.1074/jbc.M508246200.
- ↑ Parker JA, Arango M, Abderrahmane S, Lambert E, Tourette C, Catoire H, Néri C; Arango; Abderrahmane; Lambert; Tourette; Catoire; Néri (April 2005). «Resveratrol rescues mutant polyglutamine cytotoxicity in nematode and mammalian neurons». Nat. Genet. 37 (4): 349-50. PMID 15793589. doi:10.1038/ng1534.
- ↑ Olson ER, Naugle JE, Zhang X, Bomser JA, Meszaros JG; Naugle; Zhang; Bomser; Meszaros (March 2005). «Inhibition of cardiac fibroblast proliferation and myofibroblast differentiation by resveratrol». Am. J. Physiol. Heart Circ. Physiol. 288 (3): H1131-8. PMID 15498824. doi:10.1152/ajpheart.00763.2004.
- ↑ Bhat KP, Lantvit D, Christov K, Mehta RG, Moon RC, Pezzuto JM; Lantvit; Christov; Mehta; Moon; Pezzuto (October 2001). «Estrogenic and antiestrogenic properties of resveratrol in mammary tumor models». Cancer Res. 61 (20): 7456-63. PMID 11606380.
- ↑ Prossnitz, Eric R.; Barton, Matthias (2014). «Estrogen biology: New insights into GPER function and clinical opportunities». Molecular and Cellular Endocrinology 389 (1-2): 71-83. ISSN 0303-7207. doi:10.1016/j.mce.2014.02.002.
- ↑ Kode A, Rajendrasozhan S, Caito S, Yang SR, Megson IL, Rahman I; Rajendrasozhan; Caito; Yang; Megson; Rahman (March 2008). «Resveratrol induces glutathione synthesis by activation of Nrf2 and protects against cigarette smoke-mediated oxidative stress in human lung epithelial cells». Am. J. Physiol. Lung Cell Mol. Physiol. 294 (3): L478-88. PMID 18162601. doi:10.1152/ajplung.00361.2007.
- ↑ Ghosh HS, McBurney M, Robbins PD; McBurney; Robbins (2010). «SIRT1 negatively regulates the mammalian target of rapamycin». PLoS ONE 5 (2): e9199. Bibcode:2010PLoSO...5.9199G. PMC 2821410. PMID 20169165. doi:10.1371/journal.pone.0009199.
- ↑ Morselli E, Galluzzi L, Kepp O, Criollo A, Maiuri MC, Tavernarakis N, Madeo F, Kroemer G; Galluzzi; Kepp; Criollo; Maiuri; Tavernarakis; Madeo; Kroemer (December 2009). «Autophagy mediates pharmacological lifespan extension by spermidine and resveratrol». Aging (Albany NY) 1 (12): 961-70. PMC 2815753. PMID 20157579.
- ↑ Tennen RI, Michishita-Kioi E, Chua KF; Michishita-Kioi; Chua (February 2012). «Finding a target for resveratrol». Cell 148 (3): 387-9. PMID 22304906. doi:10.1016/j.cell.2012.01.032.
- ↑ Park SJ, Ahmad F, Philp A, Baar K, Williams T, Luo H, Ke H, Rehmann H, Taussig R, Brown AL, Kim MK, Beaven MA, Burgin AB, Manganiello V, Chung JH; Ahmad; Philp; Baar; Williams; Luo; Ke; Rehmann; Taussig; Brown; Kim; Beaven; Burgin; Manganiello; Chung (February 2012). «Resveratrol ameliorates aging-related metabolic phenotypes by inhibiting cAMP phosphodiesterases». Cell 148 (3): 421-33. PMC 3431801. PMID 22304913. doi:10.1016/j.cell.2012.01.017.
- ↑ a b c d Mattivi F, Reniero F, Korhammer S; Reniero; Korhammer (1995). «Isolation, characterization, and evolution in red wine vinification of resveratrol monomers». Journal of Agricultural and Food Chemistry 43 (7): 1820-3. doi:10.1021/jf00055a013.
- ↑ Lamuela-Raventos RM, Romero-Perez AI, Waterhouse AL, de la Torre-Boronat MC; Romero-Perez; Waterhouse; de la Torre-Boronat (1995). «Direct HPLC Analysis of cis- and trans-Resveratrol and Piceid Isomers in Spanish Red Vitis vinifera Wines». Journal of Agricultural and Food Chemistry 43 (2): 281-283. doi:10.1021/jf00050a003.
- ↑ Resveratrol Photoisomerization: An Integrative Guided-Inquiry Experiment Elyse Bernard, Philip Britz-McKibbin, Nicholas Gernigon Vol. 84 No. 7 July 2007 Journal of Chemical Education 1159.
- ↑ Yang I, Kim E, Kang J, Han H, Sul S, Park SB, Kim SK; Kim; Kang; Han; Sul; Park; Kim (2012). «Photochemical generation of a new, highly fluorescent compound from non-fluorescent resveratrol». Chemical Communications 48 (32): 3839-41. PMID 22436889. doi:10.1039/C2CC30940H.
- ↑ Prokop J, Abrman P, Seligson AL, Sovak M; Abrman; Seligson; Sovak (2006). «Resveratrol and its glycon piceid are stable polyphenols». J Med Food 9 (1): 11-4. PMID 16579722. doi:10.1089/jmf.2006.9.11.
- ↑ Pantusa M, Bartucci R, Rizzuti B; Bartucci; Rizzuti (2014). «Stability of trans-resveratrol associated with transport proteins». J Agric Food Chem 62 (19): 4384-91. PMID 24773207. doi:10.1021/jf405584a.
- ↑ Bertelli AA, Gozzini A, Stradi R, Stella S, Bertelli A; Gozzini; Stradi; Stella; Bertelli (1998). «Stability of resveratrol over time and in the various stages of grape transformation». Drugs Exp Clin Res 24 (4): 207-11. PMID 10051967.
- ↑ Sharan S, Nagar S; Nagar (2013). «Pulmonary Metabolism of Resveratrol: In Vitro and in Vivo Evidence». Drug Metabolism and Disposition 41 (5): 1163-9. PMC 3629805. PMID 23474649. doi:10.1124/dmd.113.051326.
- ↑ Schröder G, Brown JW, Schröder J; Brown; Schröder (February 1988). «Molecular analysis of resveratrol synthase. cDNA, genomic clones and relationship with chalcone synthase». Eur. J. Biochem. 172 (1): 161-9. PMID 2450022. doi:10.1111/j.1432-1033.1988.tb13868.x.
- ↑ Cichewicz RH, Kouzi SA, Hamann MT; Kouzi; Hamann (January 2000). «Dimerization of resveratrol by the grapevine pathogen Botrytis cinerea». J. Nat. Prod. 63 (1): 29-33. PMID 10650073. doi:10.1021/np990266n.
- ↑ Cichewicz RH, Kouzi SA; Kouzi (October 1998). «Biotransformation of resveratrol to piceid by Bacillus cereus». J. Nat. Prod. 61 (10): 1313-4. PMID 9784180. doi:10.1021/np980139b.
- ↑ Favaron, F.; Lucchetta, M.; Odorizzi, S.; Pais da Cunha, A.T.; Sella, L. (2009). «The role of grape polyphenols on trans-resveratrol activity against Botrytis cinerea and of fungal laccase on the solubility of putative grape PR proteins». Journal of Plant Pathology 91 (3): 579-88. doi:10.4454/jpp.v91i3.549 (inactivo 2015-02-01).
- ↑ Gatto P, Vrhovsek U, Muth J, Segala C, Romualdi C, Fontana P, Pruefer D, Stefanini M, Moser C, Mattivi F, Velasco R; Vrhovsek; Muth; Segala; Romualdi; Fontana; Pruefer; Stefanini; Moser; Mattivi; Velasco (December 2008). «Ripening and genotype control stilbene accumulation in healthy grapes». Journal of Agricultural and Food Chemistry 56 (24): 11773-85. PMID 19032022. doi:10.1021/jf8017707.
- ↑ a b c Roy, H., Lundy, S., Resveratrol Archivado el 28 de marzo de 2016 en Wayback Machine., Pennington Nutrition Series, 2005 No. 7
- ↑ a b c LeBlanc, Mark Rene (13 de diciembre de 2005). «Cultivar, Juice Extraction, Ultra Violet Irradiation and Storage Influence the Stilbene Content of Muscadine Grapes (Vitis Rotundifolia Michx.)». Archivado desde el original el 12 de octubre de 2007. Consultado el 15 de agosto de 2007.
- ↑ Gu X, Creasy L, Kester A, Zeece M; Creasy; Kester; Zeece (August 1999). «Capillary electrophoretic determination of resveratrol in wines». Journal of Agricultural and Food Chemistry 47 (8): 3223-7. PMID 10552635. doi:10.1021/jf981211e.
- ↑ Mattivi F (June 1993). «Solid phase extraction of trans-resveratrol from wines for HPLC analysis». Z Lebensm Unters Forsch 196 (6): 522-5. PMID 8328217. doi:10.1007/BF01201331.
- ↑ Ector BJ, Magee JB, Hegwood CP, Coign MJ (1996). «Resveratrol Concentration in Muscadine Berries, Juice, Pomace, Purees, Seeds, and Wines». American Journal of Enology and Viticulture 47 (1): 57-62.
- ↑ Pastrana-Bonilla E, Akoh CC, Sellappan S, Krewer G; Akoh; Sellappan; Krewer (August 2003). «Phenolic content and antioxidant capacity of muscadine grapes». Journal of Agricultural and Food Chemistry 51 (18): 5497-503. PMID 12926904. doi:10.1021/jf030113c. «Contrary to previous results, ellagic acid and not resveratrol was the major phenolic in muscadine grapes. The HPLC solvent system used coupled with fluorescence detection allowed separation of ellagic acid from resveratrol and detection of resveratrol." "[T]rans-resveratrol had the lowest concentrations of the detected phenolics, ranging from not detected in two varieties to 0.2 mg/ 100 g of FW (Tables 1 and 2). Our result for resveratrol differed from previous results [Ector et al., 1996] indicating high concentrations. These researchers apparently were not able to separate ellagic acid from resveratrol with UV detection alone.»
- ↑ Hudson TS, Hartle DK, Hursting SD, Nunez NP, Wang TT, Young HA, Arany P, Green JE; Hartle; Hursting; Nunez; Wang; Young; Arany; Green (September 2007). «Inhibition of prostate cancer growth by muscadine grape skin extract and resveratrol through distinct mechanisms». Cancer Res. 67 (17): 8396-405. PMID 17804756. doi:10.1158/0008-5472.CAN-06-4069. «MSKE [muscadine grape skin extract] does not contain significant quantities of resveratrol and differs from MSEE. To determine whether MSKE contains significant levels of resveratrol and to compare the chemical content of MSKE (skin) with MSEE (seed), HPLC analyses were done. As depicted in Supplementary Fig. S1A and B, MSKE does not contain significant amounts of resveratrol (<1 ?g/g by limit of detection).»
- ↑ Wang KH, Lai YH, Chang JC, Ko TF, Shyu SL, Chiou RY; Lai; Chang; Ko; Shyu; Chiou (January 2005). «Germination of peanut kernels to enhance resveratrol biosynthesis and prepare sprouts as a functional vegetable». Journal of Agricultural and Food Chemistry 53 (2): 242-6. PMID 15656656. doi:10.1021/jf048804b.
- ↑ Stewart JR, Artime MC, O'Brian CA; Artime; O'Brian (July 2003). «Resveratrol: a candidate nutritional substance for prostate cancer prevention». J. Nutr. 133 (7 Suppl): 2440S-2443S. PMID 12840221.
- ↑ a b Hurst WJ, Glinski JA, Miller KB, Apgar J, Davey MH, Stuart DA; Glinski; Miller; Apgar; Davey; Stuart (September 2008). «Survey of the trans-resveratrol and trans-piceid content of cocoa-containing and chocolate products». Journal of Agricultural and Food Chemistry 56 (18): 8374-8. PMID 18759443. doi:10.1021/jf801297w.
- ↑ Mozzon M (1996). «Resveratrol content in some Tuscan wines». Ital. J. Food Sci. (Chiriotti, Pinerolo, ITALIE) 8 (2): 145-52.
- ↑ Stervbo U, Vang O, Bonnesen C; Vang; Bonnesen (2007). «A review of the content of the putative chemopreventive phytoalexin resveratrol in red wine». Food Chemistry 101 (2): 449-57. doi:10.1016/j.foodchem.2006.01.047.
- ↑ Higdon J, Drake VJ, Steward WP (May 2008). «Resveratrol». Micronutrient Information Center. Linus Pauling Institute.
- ↑ Rimas A (11 de diciembre de 2006). «His research targets the aging process». The Boston Globe.
- ↑ Stipp D (19 de enero de 2007). «Can red wine help you live forever?». Fortune magazine.
- ↑ a b Seward ZM (30 de noviembre de 2006). «Quest for youth drives craze for 'wine' pills». The Wall Street Journal.
- ↑ «Caution urged with resveratrol». United Press International. 30 de noviembre de 2006.
- ↑ Aleccia J (22 de abril de 2008). «Longevity quest moves slowly from lab to life». MSNBC.
- ↑ Gocze T (8 de septiembre de 2008). «Japanese Knotweed a Resilient Invader». Bangor Daily News.
- ↑ Wang H, Liu L, Guo YX, Dong YS, Zhang DJ, Xiu ZL; Liu; Guo; Dong; Zhang; Xiu (June 2007). «Biotransformation of piceid in Polygonum cuspidatum to resveratrol by Aspergillus oryzae». Appl. Microbiol. Biotechnol. 75 (4): 763-8. PMID 17333175. doi:10.1007/s00253-007-0874-3.
- ↑ Weintraub A (29 de julio de 2009). «Resveratrol: The Hard Sell on Anti-Aging». Bloomberg Businessweek.
- ↑ Pangeni R, Sahni JK, Ali J, Sharma S, Baboota S; Sahni; Ali; Sharma; Baboota (2014). «Resveratrol: review on therapeutic potential and recent advances in drug delivery». Expert Opinion on Drug Delivery 11 (8): 1285-1298. ISSN 1742-5247. PMID 24830814. doi:10.1517/17425247.2014.919253.
- ↑ Tomé-Carneiro J, Larrosa M, González-Sarrías A, Tomás-Barberán FA, García-Conesa MT, Espín JC; Larrosa; González-Sarrías; Tomás-Barberán; García-Conesa; Espín (2013). «Resveratrol and clinical trials: the crossroad from in vitro studies to human evidence». Curr. Pharm. Des. 19 (34): 6064-93. PMC 3782695. PMID 23448440. doi:10.2174/13816128113199990407.
- ↑ Vang O, Ahmad N, Baile CA, Baur JA, Brown K, Csiszar A, Das DK, Delmas D, Gottfried C, Lin HY, Ma QY, Mukhopadhyay P, Nalini N, Pezzuto JM, Richard T, Shukla Y, Surh YJ, Szekeres T, Szkudelski T, Walle T, Wu JM (2011). «What is new for an old molecule? Systematic review and recommendations on the use of resveratrol». PLoS ONE 6 (6): e19881. PMC 3116821. PMID 21698226. doi:10.1371/journal.pone.0019881.
- ↑ a b Athar M, Back JH, Tang X, Kim KH, Kopelovich L, Bickers DR, Kim AL; Back; Tang; Kim; Kopelovich; Bickers; Kim (November 2007). «Resveratrol: a review of preclinical studies for human cancer prevention». Toxicol. Appl. Pharmacol. 224 (3): 274-83. PMC 2083123. PMID 17306316. doi:10.1016/j.taap.2006.12.025.
- ↑ Szmitko PE, Verma S; Verma (January 2005). «Cardiology patient pages. Red wine and your heart». Circulation 111 (2): e10-1. PMID 15657377. doi:10.1161/01.CIR.0000151608.29217.62.
- ↑ Ferrières J (January 2004). «The French paradox: lessons for other countries». Heart 90 (1): 107-11. PMC 1768013. PMID 14676260. doi:10.1136/heart.90.1.107.
- ↑ Simini B (January 2000). «Serge Renaud: from French paradox to Cretan miracle». Lancet 355 (9197): 48. PMID 10615898. doi:10.1016/S0140-6736(05)71990-5.
- ↑ Kopp P (June 1998). «Resveratrol, a phytoestrogen found in red wine. A possible explanation for the conundrum of the 'French paradox'?». Eur. J. Endocrinol. 138 (6): 619-20. PMID 9678525. doi:10.1530/eje.0.1380619.
- ↑ Duffy SJ, Vita JA; Vita (2003). «Effects of phenolics on vascular endothelial function». Current Opinion in Lipidology 14 (1): 21-7. PMID 12544657. doi:10.1097/01.mol.0000052857.26236.f2 (inactivo 2015-02-01).
- ↑ Olas B, Wachowicz B; Wachowicz (August 2005). «Resveratrol, a phenolic antioxidant with effects on blood platelet functions». Platelets 16 (5): 251-60. PMID 16011975. doi:10.1080/09537100400020591.
- ↑
- ↑ Wang L, Waltenberger B, Pferschy-Wenzig EM, Blunder M, Liu X, Malainer C, Blazevic T, Schwaiger S, Rollinger JM, Heiss EH, Schuster D, Kopp B, Bauer R, Stuppner H, Dirsch VM, Atanasov AG; Waltenberger; Pferschy-Wenzig; Blunder; Liu; Malainer; Blazevic; Schwaiger; Rollinger; Heiss; Schuster; Kopp; Bauer; Stuppner; Dirsch; Atanasov (2014). «Natural product agonists of peroxisome proliferator-activated receptor gamma (PPARγ): a review». Biochem Pharmacol 92 (1): 73-89. PMC 4212005. PMID 25083916. doi:10.1016/j.bcp.2014.07.018.
- ↑ «Effects of resveratrol on glucose control and insulin sensitivity in subjects with type 2 diabetes: systematic review and meta-analysis.».
- ↑ a b Afaq F, Mukhtar H; Mukhtar (2006). «Botanical antioxidants in the prevention of photocarcinogenesis and photoaging». Experimental Dermatology 15 (9): 678-84. PMID 16881964. doi:10.1111/j.1600-0625.2006.00466.x.
- ↑ a b Baliga MS, Katiyar SK; Katiyar (2006). «Chemoprevention of photocarcinogenesis by selected dietary botanicals». Photochemical & Photobiological Sciences 5 (2): 243-53. PMID 16465310. doi:10.1039/b505311k.
Enlaces externos[editar]
- Félicien Breton (2008). «Resveratrol and polyphenols in wines».
- CTD's Resveratrol page desde la Base de datos comparativa Toxicogenómica
- U.S. National Library of Medicine: Drug Information Portal – Resveratrol
- Detailed Micro-Nutrient information on Resveratrol desde el Instituto Linus Pauling
- Aspolvit Care+ Antiox Forte con Resveratrol
- Resveratrol: Don't Buy the Hype
- Stay young on red wine drugs? Think again
- Ver Producción de Resveratrol Página 5 del Dr. Hector Damian Brzostowski Publicado 2008 INPI Patente Industrial. Investigaciones file:///C:/Users/CASA/Desktop/Eye%20Prevention%20IBF.pdf https://drive.google.com/file/d/1TWEFWkQt6YUmxoXueOGTcJc509Ks6Jad/view?usp=drivesdk

