Bioquímica del arsénico

La bioquímica del arsénico se refiere a los procesos por los que los seres vivos pueden modificar químicamente el arsénico o sus compuestos, como el arseniato. El arsénico es un elemento moderadamente abundante en la corteza terrestre, y a pesar de que muchos de sus compuestos son tóxicos, existen numerosos organismos capaces de metabolizar compuestos orgánicos e inorgánicos de arsénico y de producir una amplia variedad de compuestos organoarsénicos; otros elementos, como el selenio, combinan también un papel biológico y efectos nocivos. La bioquímica del arsénico es objeto de interés debido a la presencia de muchos compuestos tóxicos de arsénico en algunos acuíferos,[1] con efectos potenciales en la salud de millones de personas.[2]
Fuentes de arsénico
[editar]Compuestos de organoarsénico en la naturaleza
[editar]
La posibilidad de que el arsénico sea un nutriente benéfico por debajo de los niveles normales de exposición de los organismos vivos está sujeta a investigación.[3] Los lagos que contienen una cantidad sustancial de arsénico inorgánico disuelto albergan biota tolerante al arsénico y existen bacterias y hongos capaces de metabolizar el arsénico inorgánico.[4]
Entre los compuestos organoarsenicales encontrados en la naturaleza están la arsenobetaína y la arsenocolina,[5] presentes en muchos organismos marinos.[2] Estos compuestos pueden formar parte de nucleósidos que contienen las base adenina y adenosina.[6] Varias de las moléculas organoarsenicales surgen por medio de los procesos de metilación. Por ejemplo, el moho Scopulariopsis brevicaulis y otros microorganismos producen la trimetilarsina o gas de Gosio, intensamente maloliente, en presencia de compuestos inorgánico del arsénico.[7][4]
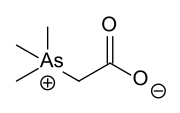
La arsenobetaína puede encontrarse en mariscos y algas, y, en mayores concentraciones, en hongos. La ingesta promedio de arsenobetaína en el ser humano varía entre 10 y 50 µg por día, pero puede alcanzar los 1000 µg después del consumo de pescado u hongos; sin embargo este compuesto del arsénico no es tóxico.[8]
- Compuestos organoarsénicos representativos encontrados en la naturaleza
-
Arsenobetaína, uno de los compuestos del arsénico más comunes en la naturaleza. La arsenocolina, otro compuesto abundante, contiene un grupo CH2OH en lugar de CO2H.
-
Trimetilarsina, producida por la acción microbiana en los pigmentos derivados del arseniato.
-
Derivados de la ribosa con arsénico.
Vida basada en el arsénico
[editar]En un estudio de la bacteria GFAJ-1 se postuló la teoría de que el arsénico podría reemplazar al fósforo en el ADN o en el ARN. Sin embargo, no se ha podido hallar ningún indicio de que esto ocurra en la naturaleza, a pesar de la similitud estructural del arseniato y el fosfato y la teoría se considera refutada.[9][10][11]
Compuestos de arsénico antropogénicos
[editar]Los principales compuestos de arsénico antropogénicos (generados por el hombre) se encuentran en los deshechos del tratamiento de minerales y de vertidos de granjas de ganado porcino y avícola, que acaban infiltrándose en los acuíferos.[12] Por ejemplo, muchos minerales, especialmente los minerales sulfuros, están contaminados con arsénico, que se desprende durante el proceso de tostado al convertirse el ion de arseniuro en trióxido de arsénico, el cual es volátil a temperaturas altas y se incorpora a la atmósfera. Las granjas de cerdos y de aves de corral hacen uso de los organoarsénicos ácido ureidofenil arsónico, el ácido p-arsanílico y la roxarsona, un derivado del ácido fenilarsónico (CH3AsO(OH)2 como suplemento alimenticio para los animales en Estados Unidos.[13][14]
Otros compuestos encontrados en la naturaleza como resultado de las actividades humanas son el arsenato de cobre, empleado a veces como preservativo para tratar la madera, y el ácido metanoarsónico (CH3AsO(OH)2), precursor de algunos fungicidas empleados en los cultivos de arroz y algodón. Los pigmentos verdes que fueron populares en los papeles tapiz, ej. verde París están basados en el acetoarsenito de cobre, también usado como insecticida.[15] Los mecanismos por los cuales estas sustancias afectan a los organismos acuáticos no se conocen totalmente pero son probablemente muy diversos. Un mecanismo comúnmente citado es la metilación.[16]
Medicamentos a base de arsénico
[editar]A pesar, o posiblemente a causa de la bien conocida toxicidad del arsénico, los medicamentos y brebajes que lo contienen como ingrediente tienen una larga historia en la medicina y el curanderismo que continúa en el siglo XXI.[17][18] La solución de Fowler, un brebaje tóxico a base de arsenito de sodio, se podía vender desde principios del siglo XIX hasta el XX. La arsfenamina, un compuesto organoarsénico descubierto por Paul Ehrlich, fue el primer agente sintético para la quimioterapia;[18] sin embargo, el tratamiento provocaba muchas complicaciones de salud de larga duración.[19] Un medicamento relacionado, el Melarsoprol, se sigue usando contra la Tripanosomiasis africana (enfermedad del sueño), a pesar de su alta toxicidad y posibles efectos secundarios mortales.
Estudios in vitro sugieren que el trióxido de arsénico (As2O3) inhibe la proliferación de las células del mieloma múltiple por medio de la detención del ciclo celular así como la muerte celular inducida,[20] por lo que este compuesto podría ser clínicamente útil para tratar pacientes con esta dolencia[20] o leucemia.[21]
Metilación del arsénico
[editar]Tras su incorporación a un organismo vivo, el arsénico inorgánico y sus compuestos experimentan un proceso metabólico de biometilación. Aunque la metilación del arsénico se ha considerado durante mucho tiempo una forma de reducir su toxicidad,[16] los experimentos llevados a cabo en los años 2000 apuntan a lo contrario.[2][22] En los vertebrados, la biometilación tiene lugar en el hígado.
El arsénico que entra en el cuerpo se encuentra generalmente en el estado de oxidación As(III) o As(V).[23] El trióxido de arsénico entra en las células a través de las acuaporinas 7 y 9, mientras que el óxido de arsénico(V) usa transportadores de fosfato para entrar en las células.[23] El arsénico (V) puede convertirse en arsénico (III) por la enzima purina nucleósido fosforilasa,[23] en lo que se considera un proceso de bioactivación.[24]
En los mamíferos, la metilación es mediada por metiltransferasas, mediante dos rutas diferentes.[25] La primera ruta usa la metiltransferasa Cyt19, también deominada AS3MT. El cofactor S-adenosil metionina (SAM) es el donante del grupo metilo al trióxido de arsénico en este proceso.[26] El compuesto resultante puede experimentar una segunda metilación; el arsénico(V) de la molécula metilada o dimetilada se convierte a arsénico(III) mediante la enzima Glutatión S-Transferasa Omega-1 (GSTO1).[23] En la segunda ruta de metilación, el glutatión (GHS) se conjuga con el trióxido de arsénico para formar un complejo de arsénico, sobre el que actúa la metiltransferasa del arsénico Cyt19 para metilarlo.[23]
Los complejos del arsénico, monometilado y dimetilo, pueden excretarse fácilmente en la orina.[24] No obstante, el compuesto monometilado puede ser más reactivo y más tóxico que los compuestos inorgánicos del arsénico cuando interactúa con los hepatocitos, los queratinocitos de la piel, y las células bronquiales epiteliales de los pulmones.[27]

En las bacterias existe una enzima análoga a la metiltranferasa Cyt19, llamada CmArsM. Esta enzima ha sido estudiada en tres estados: libre, ligada al arsénico (III) y ligada a SAM. El arsénico se une generalmente a los grupos tiol de la cisteínas Cys72, Cys174, y Cys224 de la enzima. En una reacción SN2, el átomo de sulfuro de la SAM incorpora ul electrón del carbono del grupo metil, el cual interactúa con el par libre del arsénico para formar el enlace As-C.[28]
Estudios experimentales en animales y humanos muestran que los compuestos de arsénico inorgánicos y los metabolitos metilados cruzan la placenta hacia el feto; hay indicios de que la metilación se incrementa durante el embarazo, lo que se ha interpretado como un mecanismo de protección para el desarrollo del organismo.[29]
Excreción
[editar]En humanos, la ruta mayor de excreción de la mayoría de los compuestos del arsénico es la orina. La vida media biológica del arsénico inorgánico es de cuatro días, pero es ligeramente más corta si se trata de un arseniato en lugar de un arsenito. Los principales compuestos del arsénico excretados en la orina humana son el ácido arsénico monometilado o dimetilado y compuestos inorgánicos del arsénico sin metabolizar.[26]
La biotransformación del arsénico previa a la excreción, se lleva a cabo primordialmente por la ruta del factor Nrf2, que regula la expresión de enzimas destoxificantesy antioxidantes.[30] En condiciones normales el Nrf2 está vinculado a la forma inactiva de la proteína Keap1.[31] Tras la absorción del arsénico en las células y la producción de especies reactivas de oxígeno (ROS) durante las reacciones metabólicas subsecuentes, Keap1 forma enlaces tiol con las ROS o con moléculas electrófilas del arsénico, como el trióxido de arsénico monometilado, y libera el Nrf2, el cual se desplaza al núcleo celular.[30] Allí activa las secuencias de ADN conocidas como elemento de respuesta antioxidante y elemento de respuesta a electrófilos (EpRE) que contribuyen en el aumento de proteínas antioxidantes,[32] como la hemo oxigenasa 1 (HO-1), la AD(P)H quinona oxidoreductasa 1 (NQO1), y la γ-glutamil cisteina sintetasa (γGCS); estas actúan en conjunto para reducir el estrés oxidativo de la célula. El incremento de γGCS causa un aumento en la producción de arsenito de glutatión (As(SG)3), un importante aducto digerido por las proteínas de farmacorresistencia múltiple 1 o 2 (MRP1 o MRP2) las cuales retiran el arsénico de la célula a la bilis para excreción.[30] El arsenito de glutatión puede descomponerse en arsénico inorgánico de nuevo.
Toxicidad del arsénico
[editar]El arsénico causa muchas muertes alrededor del mundo; los problemas asociados a su ingestión incluyen enfermedades del corazón, hígado, páncreas, respiratorias, gastrointestinales y nerviosas.[2][26]
Los compuestos de arsénico dañan la célula por una inhibición alostérica de un complejo enzimático metabólico esencial llamado piruvato deshidrogenasa (PDH), el cual cataliza la oxidación de piruvato en acetil-CoA por medio del NAD+. Como consecuencia, la generación de energía del sistema celular se interrumpe y se inicia el proceso de apoptosis celular. Bioquímicamente hablando, el arsénico impide el uso de la tiamina lo que da como resultado, en un marco clínico, la deficiencia de tiamina. El envenenamiento con arsénico puede aumentar los niveles de lactato y dar lugar a una acidosis láctica. El arsénico es también genotóxico, capaz de inhibir la reparación y metilación del ADN. El arsénico induce el estrés oxidativo, responsable de efectos carcinógeno.
Por su alta toxicidad, varios compuestos del arsénico son potenciales armas químicas, como por ejemplo, el cloruro de dimetil arsénico. Algunos compuestos se emplearon con este uso en la Primera Guerra Mundial.[cita requerida] Debido a esta amenaza, se han realizado muchos estudios de antídotos y se han ampliado los conocimientos de los efectos de los compuestos del arsénico en los seres vivos. El desarrollo de antídotos como el dimercaprol es el resultado de estas investigaciones. Muchos de los antídotos estudiados se basan en la afinidad de As(III) para formar tiolatos, derivados organoarsénicos de menor toxicidad.
En el caso del óxido de arsénico, el efecto tóxico puede usarse con fines quimoterapéuticos para el tratamiento de leucemia promielocítica aguda (APL).[3]
Toxicidad de los compuestos arsenicales pentavalentes
[editar]Los metabolitos de los compuestos arsenicales pentavalentes son capaces de reemplazar a los grupos fosfato, claves en el metabolismo celular, debido a las similares propiedades químicas y características estructurales de ambas moléculas.[33] Cuando el arseniato reacciona con la glucosa y el gluconato in vitro se generan glucosa-6-arseniato y 6-arsenogluconato, los cuales actúan como análogos de la glucosa-6-fosfato y 6-fosfogluconato. Durante la glucólisis, la glucosa-6-arseniato se enlaza como sustrato a la glucosa-6-fosfato deshidrogenasa; a diferencia del fosfato, la presencia del arseniato impide la generación de ATP debido a la formación de un producto anhídrido (el 1-arsenato-3-fosfo-D-glicerato) por la reacción con D-gliceroaldehído-3-fosfato; Este anhídrido es inestable y se hidroliza fácilmente por la mayor longitud del enlace As-O comparado con el P-O.[33]
A nivel mitocondrial, el arseniato interrumpe la síntesis de ATP por formar un compuesto inestable al enlazarse con el ADP en presencia del succinato, lo que reduce la ganancia neta de ATP.[33]
Toxicidad de los compuestos arsenicales trivalentes
[editar]Las enzimas y receptores que contienen grupos tiol o sulfhidrilo —normalmente el glutatión y la cisteína— son susceptibles a unirse a los metabolitos del arsenito (III), con una afinidad mayor que a los metabolitos de arseniato. Estos enlaces restringen la actividad de algunos mecanismos metabólicos: por ejemplo, la piruvato deshidrogenasa (PDH) se inhibe cuando el ácido monometilarsénico (MMAIII) ataca el grupo tiol del cofactor del ácido lipoico.[33] El PHD es un precursor del acetil-CoA, por lo tanto la inhibición del PHD limita la producción de ATP en la cadena de transporte de electrones, así como la producción de los intermediarios de la gluconeogénesis.[33]
Estrés oxidativo
[editar]El arsénico puede causar estrés oxidativo a través de la formación de especies reactivas de oxígeno (ROS), y de especies reactivas de nitrógeno (RNS).[25] Las especies reactivas de oxígeno aparecen cuando la enzima NADPH oxidasa transfiere electrones del NADPH al oxígeno para sintetizar un radical libre reactivo conocido como superóxido, que genera peróxido de hidrógeno y las especies reactivas de oxígeno. La enzima NADPH oxidasa es capaz de generar más especies reactivas de oxígeno en presencia del arsénico, por promover este la transferencia de electrones.[25] Las especies reactivas de oxígeno pueden desencadenar una respuesta a proteínas desplegadas, inflamación, proliferación celular, y eventualmente a la muerte celular.[25] Las especies reactivas de oxígeno también pueden reestructurar el citoesqueleto, lo cual afecta a las proteínas contráctiles y puede conllevar también la muerta celular.[25] Una vez que las especies reactivas de oxígeno destruyen las mitocondrias, se produce la reacción entre los superóxidos y el óxido nítrico para formar peroxinitrito, responsable de los daños al ADN en el envenenamiento con arsénico.[25]
Daño al ADN
[editar]Hay pruebas de que el arsénico causa modificaciones en el ADN como aneuploidía, formación de micronúcleos, mutaciones cromosómicas, deleciones, intercambio de cromátidas hermanas y reticulación de ADN-proteína.[34] Se ha demostrado que el arsénico no interactúa directamente con el ADN y es considerado un mutágeno débil, pero contribuye a la mutagenicidad de otros carcinógenos.[35] Por ejemplo, en células humanas y de otras especies animales se da un incremento sinérgico en la actividad mutagénica del arsénico en presencia de luz UV.[36][37] Varias observaciones experimentales sugieren que la genotoxicidad del arsénico está relacionada con la generación de especies reactivas de oxígeno (ROS) durante su biotransformación.[38][39][40] La producción de ROS puede tener como resultado la formación de aductos de ADN, la rotura de las cadenas de ADN, reticulaciones y mutaciones cromosómicas.[41][42][43][44] El daño tiene lugar por la modificación de las bases nitrogenadas del ADN, en particular la 8-oxoguanina (8-OHdG), que causa mutaciones.[45] El arsénico inorgánico puede romper la cadena de ADN incluso en concentraciones bajas.[46]
Inhibición de la reparación de ADN
[editar]La inhibición de la reparación del ADN es considerada uno de los principales mecanismos de la genotoxicidad del arsénico inorgánico. Tras sufrir daños el ADN se activan los procesos de reparación por escisión de nucleótidos (REN) y la reparación por escisión de bases (REB). La REN es el mecanismo principal para reparar distorsiones voluminosas en la doble cadena del ADN, mientras que la REB tiene lugar cuando se rompe una sola cadena;[47][48][49][50] este último proceso es el que puede reprimir el arsénico inorgánico.[47][51][52]
Disfunción inmune
[editar]La exposición al arsénico en niños pequeños distorsiona la razón de linfocitos T CD4 a linfocitos T CD8, los cuales son responsables por ocasionar inmunodepresión.[53] El arsénico incrementa el número de moléculas responsables de la inflamación secretadas a través de macrófagos.[53] La cantidad en exceso de granulocitos y monocitos conducen a un estado crónico de inflamación, lo que puede ocasionar el desarrollo de cáncer.[53]
Tratamiento al envenenamiento con arsénico
[editar]La intoxicación por arsénico se trata con agentes quelantes, moléculas que se unen al arsénico e impiden que participe en otras reacciones nocivas para el metabolismo. Entre estas moléculas se cuentan el dimercaprol, el succímero (ácido dimercaptosuccínico) y el unitiol (ácido dimercapto-propano sulfónico); el succímero y el unitiol tienen un mayor índice terapéutico que el dimecarprol. Otros agentes quelantes capaces de inactivar el arsénico presentan más efectos secundarios y se usan menos.[54] Estos agentes capturan el arsénico inorgánico mediante los átomos de un grupo tiol, hacia el que el arsénico tiene una alta afinidad. El compuesto orgánico resultante puede excretarse, eliminando el arsénico inorgánico del cuerpo.
Los agentes quelantes son eficaces para tratar casos de envenenamiento agudo con arsénico, cuando se presentan síntomas como dolores de cabeza, vómitos o sudoración excesiva. Por contra, cuando aparecen efectos crónicos del envenenamiento, como daños a órganos, suele ser demasiado tarde para utilizar estos medicamentos.[55]
Véase también
[editar]Referencias
[editar]- ↑ Pearce, Fred (2006). When the Rivers Run Dry: Journeys Into the Heart of the World's Water Crisis. Toronto: Key Porter. ISBN 978-1-55263-741-8.
- ↑ a b c d Elke Dopp, Andrew D. Kligerman and Roland A. Diaz-Bone Organoarsenicals. Uptake, Metabolism, and Toxicity 2010, Royal Society of Chemistry. ISBN 978-1-84973-082-2. doi 10.1039/9781849730822-00231
- ↑ a b Wilcox, Dean E. (2013). «Chapter 15. Arsenic. Can This Toxic Metalloid Sustain Life?». En Astrid Sigel, Helmut Sigel and Roland K. O. Sigel, ed. Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences 13. Springer. pp. 475-498. doi:10.1007/978-94-007-7500-8_15.
- ↑ a b Cullen, William R.; Reimer, Kenneth J. (1989). «Arsenic speciation in the environment». Chemical Reviews 89: 713-764. doi:10.1021/cr00094a002.
- ↑ Arsenocholine - Structure and Data
- ↑ Francesconi, Kevin A.; Edmonds, John S.; Stick, Robert V. (1992). «Arsenic compounds from the kidney of the giant clam Tridacna maxima: Isolation and identification of an arsenic-containing nucleoside». Journal of the Chemical Society, Perkin Transactions 1 (11): 1349. doi:10.1039/P19920001349.
- ↑ Bentley, Ronald; Chasteen, TG (2002). «Microbial Methylation of Metalloids: Arsenic, Antimony, and Bismuth». Microbiology and Molecular Biology Reviews 66 (2): 250-271. PMC 120786. PMID 12040126. doi:10.1128/MMBR.66.2.250-271.2002.
- ↑ Cullen, William R; Reimer, Kenneth J. (1989). «Arsenic speciation in the environment». Chemical Reviews 89 (4): 713-764. doi:10.1021/cr00094a002.
- ↑ Erb, T. J.; Kiefer, P.; Hattendorf, B.; Gunther, D.; Vorholt, J. A. (2012). «GFAJ-1 is an Arsenate-Resistant, Phosphate-Dependent Organism». Science 337 (6093): 467-70. Bibcode:2012Sci...337..467E. PMID 22773139. doi:10.1126/science.1218455.
- ↑ Reaves, M. L.; Sinha, S.; Rabinowitz, J. D.; Kruglyak, L.; Redfield, R. J. (2012). «Absence of Detectable Arsenate in DNA from Arsenate-Grown GFAJ-1 Cells». Science 337 (6093): 470-3. Bibcode:2012Sci...337..470R. PMC 3845625. PMID 22773140. arXiv:1201.6643. doi:10.1126/science.1219861.
- ↑ Westheimer, F.H. (6 de junio de 1987). «Why nature chose phosphates». Science 235 (4793): 1173-1178 (see pp. 1175-1176). Bibcode:1987Sci...235.1173W. doi:10.1126/science.2434996. Archivado desde el original el 16 de junio de 2011.
- ↑ Nordstrom DK (2002). «Worldwide occurrences of arsenic in ground water». Science 296 (5576): 2143-2145. doi:10.1126/science.1072375.
- ↑ Hileman, B (9 de abril de 2007). «Arsenic in Chicken Production». Chemical and Engineering News. pp. 34-35.
- ↑ Bottemiller, Helena (26 de septiembre de 2009). «Bill Introduced to Ban Arsenic Antibiotics in Feed». Food Safety News. Consultado el 10 de enero de 2011.
- ↑ Ronald Bentley and Thomas G. Chasteen (2002). «Microbial Methylation of Metalloids: Arsenic, Antimony, and Bismuth». Microbiology and Molecular Biology Reviews 66 (2): 250-271. PMC 120786. PMID 12040126. doi:10.1128/MMBR.66.2.250-271.2002.
- ↑ a b Sakurai T (2003). «Biomethylation of Arsenic is Essentially Detoxicating Event». Journal of Health Science 49 (3): 171-178. doi:10.1248/jhs.49.171. Consultado el 10 de enero de 2011.
- ↑ Jun Zhu; Zhu Chen; Valérie Lallemand-Breitenbach; Hugues de Thé (2002). «How Acute Promyelocytic Leukaemia Revived Arsenic». Nature Reviews Cancer 2 (9): 705-714. PMID 12209159. doi:10.1038/nrc887. Consultado el 27 de septiembre de 2013.
- ↑ a b Gibaud, Stéphane; Jaouen, Gérard (2010). «Arsenic - based drugs: from Fowler's solution to modern anticancer chemotherapy». Topics in Organometallic Chemistry. Topics in Organometallic Chemistry 32: 1-20. ISBN 978-3-642-13184-4. doi:10.1007/978-3-642-13185-1_1.
- ↑ Elschenbroich, C. ”Organometallics” (2006) Wiley-VCH: Weinheim. ISBN 978-3-527-29390-2
- ↑ a b Park, Woo H. Park; Jae G. Seol; Eun S. Kim; Jung M. Hyun; Chul W. Jung; Chung C. Lee; Byoung K. Kim; Young Y. Lee (6 de junio de 2000). «Arsenic Trioxide-mediated Growth Inhibition in MC/CAR Myeloma Cells via Cell Cycle Arrest in Association with Induction of Cyclin-dependent Kinase Inhibitor, p21, and Apoptosis». Cancer Research 60 (3065): 3065-71. PMID 10850458. Consultado el 15 de diciembre de 2010.
- ↑ Lunghi, Paolo Lunghi; Antonio Costanzo; Massimo Levrero; Antonio Bonati (15 de julio de 2004). «Treatment with arsenic trioxide (ATO) and MEK1 inhibitor activates the p73-p53AIP1 apoptotic pathway in leukemia cells». Blood 104 (2): 519-525. PMID 15031205. doi:10.1182/blood-2003-08-2743. Consultado el 15 de diciembre de 2010.
- ↑ Stýblo, M.; Drobná, Z.; Jaspers, I.; Lin, S.; Thomas, D. J. (2002). «The role of biomethylation in toxicity and carcinogenicity of arsenic: A research update». Environmental Health Perspectives 110 (Suppl 5): 767-771. PMC 1241242. PMID 12426129. doi:10.1289/ehp2110s5767.
- ↑ a b c d e Kumagai, Yoshito; Sumi, Daigo (2007). «Arsenic: Signal Transduction, Transcription Factor, and Biotransformation Involved in Cellular Response and Toxicity». Annual Review of Pharmacology and Toxicology 47: 243-62. PMID 17002598. doi:10.1146/annurev.pharmtox.47.120505.105144.
- ↑ a b Vahter, Marie (2002). «Mechanisms of arsenic biotransformation». Toxicology. 181-182: 211-7. PMID 12505313. doi:10.1016/S0300-483X(02)00285-8.
- ↑ a b c d e f Hunt, Katherine M.; Srivastava, Ritesh K.; Elmets, Craig A.; Athar, Mohammad (2014). «The mechanistic basis of arsenicosis: Pathogenesis of skin cancer». Cancer Letters 354 (2): 211-9. PMID 25173797. doi:10.1016/j.canlet.2014.08.016.
- ↑ a b c «Arsenic in Drinking Water - Review article». IARC Monographs - World Health Organization 84. Consultado el 10 de enero de 2011.
- ↑ Petrick, Jay S.; Ayala-Fierro, Felix; Cullen, William R.; Carter, Dean E.; Vasken Aposhian, H. (2000). «Monomethylarsonous Acid (MMAIII) is More Toxic Than Arsenite in Chang Human Hepatocytes». Toxicology and Applied Pharmacology 163 (2): 203-7. PMID 10698679. doi:10.1006/taap.1999.8872.
- ↑ Ajees, A.A. (10 de julio de 2012). «Structure of an As(III) S-Adenosylmethionine Methyltransferase: insights into the Mechanism of Arsenic Biotransformation». Biochemistry 51: 5476-5485. doi:10.1021/bi3004632.
- ↑ «Arsenic in Drinking Water - Review article». IARC Monographs - World Health Organization 84: 138. Consultado el 10 de enero de 2011.
- ↑ a b c Kumagai, Yoshito; Sumi, Daigo Sumi (2007). «Arsenic: Signal Transduction, Transcription Factor, and Biotransformation Involved in Cellular Response and Toxicity». Annual Review of Pharmacology and Toxicology 47: 243-62. PMID 17002598. doi:10.1146/annurev.pharmtox.47.120505.105144.
- ↑ Itoh, K.; Wakabayashi, N.; Katoh, Y.; Ishii, T.; Igarashi, K.; Engel, J. D.; Yamamoto, M (1999). «Keap1 represses nuclear activation of antioxidant responsive elements by Nrf2 through binding to the amino-terminal Neh2 domain». Genes Dev 13 (1): 76-86. PMC 316370. PMID 9887101. doi:10.1101/gad.13.1.76.
- ↑ Pi, J; Waalkes, MP; Kumagai, Y; Reece, JM; Qu, W (2003). «Transcription factor Nrf2 activation by inorganic arsenic in cultured keratinocytes: involvement of hydrogen peroxide». Exp. Cell Res 290 (2): 234-45. PMID 14567983. doi:10.1016/s0014-4827(03)00341-0.
- ↑ a b c d e Hughes, Michael F (2002). «Arsenic toxicity and potential mechanisms of action». Toxicology Letters 133 (1): 1-16. PMID 12076506. doi:10.1016/S0378-4274(02)00084-X.
- ↑ Rossman, T.G (2003). «Mechanism of arsenic carcinogenesis: An integrated approach». Mutation Research/Fundamental and Molecular Mechanisms of Mutagenesis 533: 37-65. doi:10.1016/j.mrfmmm.2003.07.009.
- ↑ Pierce, B.L; Kibriya, M.G (2012). «Genome-wide association study identifies chromosome 10q24.32 variants associated with arsenic metabolism and toxicity phenotypes in Bangladesh». PLoS Genetics 8: e1002522. doi:10.1371/journal.pgen.1002522.
- ↑ Li, J.H; Rossman, T.G (1991). «Comutagenesis of sodium arsenite with ultraviolet radiation in Chinese hamster V79 cells». Biology of Metals 4: 197-200. doi:10.1007/BF01141180.
- ↑ Lee, T.C; Oshimura, M (1985). «Comparison of arsenic-induced cell transformation, cytotoxicity, mutation and cytogenetic effects in Syrian hamster embryo cells in culture». Carcinogenesis 6: 1421-1426. doi:10.1093/carcin/6.10.1421.
- ↑ Kessel, M; Liu, S.X (2002). «Arsenic induces oxidative DNA damage in mammalian cells». Molecular and Cellular Biochemistry. 234/235: 234-235:301-308. doi:10.1023/A:1015927406142.
- ↑ Nesnow, S; Roop, B.C (2002). «DNA damage induced by methylated trivalent arsenicals is mediated by reactive oxygen species». Chemical Research in Toxicology 15: 1627-1634. doi:10.1021/tx025598y.
- ↑ Jomova, K; Jenisova, Z (2011). «Arsenic: Toxicity, oxidative stress and human disease». Journal of Applied Toxicology 31: 95-107. doi:10.1002/jat.1649.
- ↑ Kitchin, K.T; Wallace, K (2008). Evidence against the nuclear in situ binding of arsenicals—Oxidative stress theory of arsenic carcinogenesis 232. pp. 252-257. doi:10.1016/j.taap.2008.06.02.
- ↑ Bau, D.T; Wang, T.S (2002). «Oxidative DNA adducts and DNA-protein cross-links are the major DNA lesions induced by arsenite». Environmental Health Perspectives 110: 753-756. PMC 1241239. PMID 12426126. doi:10.1289/ehp.02110s5753.
- ↑ Hwang, E.S; Kim, G.H (2007). «Biomarkers for oxidative stress status of DNA, lipids, and proteins in vitro and in vivo cancer research». Toxicology 229: 1-10. doi:10.1016/j.tox.2006.10.013.
- ↑ Liu, Su X. (December 2000). «Induction of oxyradicals by arsenic: Implication for mechanism of genotoxicity». Proceedings of the National Academy of Sciences of the United States of America. Consultado el 4 de abril de 2013.
- ↑ Grollman, A.P; Moriya, M (1993). «Mutagenesis by 8-oxoguanine: An enemy within». Trends in Genetics 9: 246-249. doi:10.1016/0168-9525(93)90089-Z.
- ↑ Martinez, V.D; Vucic, E.A (2011). «Arsenic biotransformation as a cancer promoting factor by inducing DNA damage and disruption of repair mechanisms». Molecular Biology International 2011: 1-11. doi:10.4061/2011/718974.
- ↑ a b Lai, Y; Zhao, W (2011). «Role of DNA polymerase beta in the genotoxicity of arsenic». Environmental and Molecular Mutagenesis 52: 460-468. doi:10.1002/em.20643.
- ↑ Hartwig, A; Groblinghoff, U.D (1997). «Interaction of arsenic(III) with nucleotide excision repair in UV-irradiated human fibroblasts». Carcinogenesis 18: 399-405. PMID 9054635. doi:10.1093/carcin/18.2.399.
- ↑ Curnow, A; Salter, L (2001). «A preliminary investigation of the effects of arsenate on irradiation-induced DNA damage in cultured human lung fibroblasts». Journal of Toxicology and Environmental Health, Part A 63: 605-616. doi:10.1080/152873901316857789.
- ↑ Schwerdtle, T; Walter, I (2003). «Induction of oxidative DNA damage by arsenite and its trivalent and pentavalent methylated metabolites in cultured human cells and isolated DNA». Carcinogenesis 24: 967-974. doi:10.1093/carcin/bgg018.
- ↑ Ebert, F; Weiss, A (2011). «Arsenicals affect base excision repair by several mechanisms». Mutat Res 715: 32-41. PMID 21782832. doi:10.1016/j.mrfmmm.2011.07.004.
- ↑ Sykora, P; Snow, E.T (2008). «Modulation of DNA polymerase beta-dependent base excision repair in cultured human cells after low dose exposure to arsenite». Toxicology and Applied Pharmacology 228: 385-394. doi:10.1016/j.taap.2007.12.019.
- ↑ a b c Vega, L. Environmental Health Risks. Nova Science Publishers. pp157-159. ISBN 978-1-60741-781-1
- ↑ Kosnett, M. J. (2013). «The Role of Chelation in the Treatment of arsenic and Mercury Poisoning». Journal of medical toxicology 4: 347-357. doi:10.1007/s13181-013-0344-5.
- ↑ «Acute & Chronic Poisoning Affects». medtox. Archivado desde el original el 16 de agosto de 2015. Consultado el 30 de marzo de 2015.