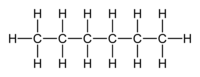
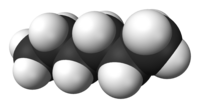
Hexano
| Hexano | ||
|---|---|---|
 | ||
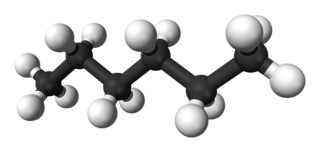 | ||
| Nombre IUPAC | ||
| Hexano | ||
| General | ||
| Otros nombres | n-hexano | |
| Fórmula semidesarrollada | CH3CH2CH2CH2CH2CH3 | |
| Fórmula molecular | C6H14 | |
| Identificadores | ||
| Número CAS | 110-54-3[1] | |
| Número RTECS | MN9275000 | |
| ChEBI | 29021 | |
| ChEMBL | CHEMBL15939 | |
| ChemSpider | 7767 | |
| PubChem | 8058 | |
| UNII | 2DDG612ED8 | |
| KEGG | C11271 | |
| Propiedades físicas | ||
| Apariencia | incoloro | |
| Densidad | 654,8 kg/m³; 0,6548 g/cm³ | |
| Masa molar | 86,18 g/mol | |
| Punto de fusión | 178 K (−95 °C) | |
| Punto de ebullición | 342 K (69 °C) | |
| Temperatura crítica | 507,6 K (234 °C) | |
| Viscosidad | 0,294 cP a 25 °C | |
| Índice de refracción (nD) | 1.375 (20 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | 6,1 mg/L | |
| Momento dipolar | 0 D | |
| Termoquímica | ||
| ΔfH0gas | -167.1 kJ/mol | |
| ΔfH0líquido | -198.321(3) kJ/mol | |
| S0gas, 1 bar | 388.82 J·mol–1·K | |
| S0líquido, 1 bar | -726.694(3) J·mol–1·K–1 | |
| Peligrosidad | ||
| NFPA 704 |
3
1
0
| |
| Temperatura de autoignición | 497 K (224 °C) | |
| Frases R | R11, R38, R48/20, R51,53, R62, R65, R67, | |
| Frases S | (S2), S9, S16, S29, S33, S36/37, S61, S62 | |
| Límites de explosividad | 1.2% - 7.7% | |
| Compuestos relacionados | ||
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El hexano o n-hexano es un hidrocarburo alifático alcano con seis átomos de carbono. Su forma química es C6H14.
Existen varios isómeros de esta sustancia, siendo la más conocida e importante la del n-hexano:
- CH3 - CH2 - CH2 - CH2 - CH2 - CH3
Otros isómeros son: 2-metilpentano (o isohexano), 3-metilpentano, 2,2-dimetilbutano (o neohexano) y 2,3-dimetilbutano
Se trata de un líquido incoloro, fácilmente inflamable y con un olor característico a disolvente. Es poco soluble en agua, pero se mezcla bien con los disolventes orgánicos apolares como, el éter o el benceno. Es muy poco polar por lo que su momento dipolar es casi nulo y su fuerza de elución es muy baja (εº=0,01).
Obtención
El hexano y sus isómeros forman parte de los derivados del petróleos y se obtiene mediante destilación fraccionada. A menudo no hace falta separar el n-hexano si no se emplea directamente la mezcla obtenida cuyo intervalo de ebullición coincide aproximadamente con el punto de ebullición del hexano.
Uso
El hexano es utilizado como disolvente para algunas pinturas y procesos químicos y para quitar etiquetas de precios ya que disuelve el pegamento con que se adhieren. También fue muy utilizado en la industria del calzado y la marroquinería, aunque su uso en industrias controladas está más restringido. También se usa para disolver las pepitas de la uva y extraer aceite de orujo. De igual manera es empleado en análisis de laboratorios siendo un solvente eficaz para la obtención de Hidrocarburos Fracción pesada en suelo y agua.
Toxicología
El n-hexano es uno de los pocos alcanos tóxicos. El efecto fisiológico no se debe a la misma sustancia sino a los productos de su metabolización, especialmente la 2,5-hexadiona. Este compuesto reacciona con algunas aminas esenciales para el funcionamiento de las células nerviosas. Por lo tanto, es neurotóxico. Además, posee un potencial adictivo y peligroso.
Véase también
Referencias
- ↑ Número CAS
- ↑ Rojas Pérez, Orlando (6 de junio de 2010). «Trabajadores chinos que fabrican el iPhone 4G alertan que fueron envenenados». Evaluamos.com. Archivado desde el original el 19 de noviembre de 2015. Consultado el 5 de enero de 2011.
3| Plyasunov, A.V., Shock, E.L., Correlation strategy for determining the parameters of the revised Helgeson-Kirkham-Flowers model for aqueous nonelectrolytes, Geochimica et Cosmochimica Acta, Vol. 65, No. 21, pp. 3879-3900, 2001.
Enlaces externos
 Wikimedia Commons alberga una galería multimedia sobre Hexano.
Wikimedia Commons alberga una galería multimedia sobre Hexano.- ATSDR en español - ToxFAQs™: n-hexano
- Instituto nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del hexano.