Receptor acoplado a proteínas G
| GPCR | ||
|---|---|---|
 Rodopsina bovina, un ejemplo de Receptor acoplado a proteínas G, con sus 7 dominios. | ||
| Identificadores | ||
| Símbolo | 7tm_1 | |
| Pfam | PF00001 | |
| InterPro | IPR000276 | |
| PROSITE | PDOC00210 | |
| Familia OPM | 6 | |
| Proteína OPM | 1gzm | |
Los receptores acoplados a proteínas G (GPCR: G protein-coupled receptors en inglés ), también conocidos como receptores transmembrana de siete dominios, receptores 7TM, receptores heptahelicoidales, receptor serpentina, comprenden una gran familia de proteínas de receptores transmembrana que responden a una variedad de estímulos extracelulares que van desde fotones y pequeñas moléculas hasta péptidos y proteínas, tales como hormonas, neurotransmisores y agentes paracrinos los cuales activan las vías de transducción de señales y, finalmente, dan origen a las respuestas celulares específicas. En el ser humano existen más de 800 RAPG diferentes, ubicados en distintos sistemas, que participan en funciones tan variadas como la visión, el olfato, el gusto; funciones neurológicas, cardiovasculares, endocrinas y reproductivas. Esta ubicuidad convierte a los RAPG en un objetivo principal del desarrollo farmacológico siendo el blanco de aproximadamente el 40% de todos los fármacos modernos.[1][2][3][4][5][6]
Los receptores acoplados a proteínas G GPCR solo se encuentran en eukaryotas, incluyendo la levadura, choanomonadas y animales.[7]
Hay dos vías de transducción de señales principales que involucran a los receptores acoplados a proteínas G: la vía de señal cAMP (Adenosín monofosfato cíclico) y la vía de señal fosfatidilinositol.[8] Cuando un ligando se liga al RAPG, este provoca un cambio conformacional en el RAPG, lo que le permite actuar como un factor intercambiador de nucleótido de guanina (GEF). El RAPG puede entonces activar una proteína G asociada mediante el intercambio de su GDP (Guanosín difosfato) enlazado por un GTP (Guanosín trifosfato).
Clasificación[editar]
Los receptores acoplados a proteínas G son una superfamilia que incluye las siguientes familias:[2][4][9][10]
- Familia de la rodopsina o Clase A, es la familia más grande y representa el 80% de los RAPG de los seres humanos.
- Grupo α, incluye la familia de los receptores aminérgicos.[11]
- Receptores adrenérgicos.
- Receptores muscarínicos.
- Receptores dopaminérgicos.
- Receptores histaminérgicos.
- Receptores serotoninérgicos.
- Receptores de trazas de aminas.
- Grupo β.
- Grupo γ.
- Grupo δ.
- Grupo κ.
- Grupo μ.
- Grupo α, incluye la familia de los receptores aminérgicos.[11]
- Familia de la secretina o Clase B. Se caracterizan por su gran dominio N-terminal extracelular. Incluye el receptor de la CRH.
- Familia de los receptores metabotrópicos de glutamato o «Clase C». Se caracterizan por su conformación de venus atrapamoscas.
- Receptores de feromonas fúngicas o «Clase D», no presentes en vertebrados.
- Receptores de AMP cíclico o «Clase E».
- Familia atípica de Frizzled o «Clase F».
- Familia adhesIón.
Estructura[editar]
Todos los receptores acoplados a proteínas G tienen siete hélices alfa transmembrana, un N-terminal y tres bucles extra celulares, un C-terminal y tres bucles intracelulares. No son estructuras rígidas que alternen sólo dos estados: una conformación activada (unido al ligando) y otra desactivada (sin el ligando); por el contrario, pueden adoptar una serie de conformaciones fugaces que son determinadas por el ligando, otros receptores, proteínas reguladoras y señales, modificaciones translacionales y condiciones ambientales. Estas innumerables conformaciones pueden agruparse en «estados conformacionales».[1][3][4][10]
También son conocidos como receptores 7TM (transmembrana) o "en serpentina", debido a la región incluida en la membrana, que asoma siete veces.
A esta clase de receptores pertenecen los receptores adrenérgicos, que se dividen en receptores α y receptores β.
Función[editar]
El receptor acoplado a proteínas G es activado por una señal externa en forma de un ligando u otro mediador de señal. Esto crea un cambio conformacional en el receptor, que a nivel intracelular se acompaña de la unión o aclopamiento de una proteína G. El efecto intracelular depende del tipo de proteína G.[1]
La subunidad α de la proteína G, junto con el GTP enlazado, puede entonces disociarse de las subunidades β y γ para afectar aún más las proteínas de señalización intracelular o dirigirse directamente a las proteínas funcionales dependiendo del tipo de subunidad α (Gαs, Gαi/o, Gαq/11, Gα12/13).[12]
En primer lugar, el ligando se une al receptor en su región N-terminal. Luego, el receptor se une a proteínas G en las regiones internas (la región C-terminal desempeña un papel en el reconocimiento de esta proteína G). Así, se activa el mecanismo efector y se varían los niveles de segundo mensajero.
La enzima efectora activa al segundo mensajero, el AMPc, que a su vez activa a la protein quinasa A, la cual fosforila proteínas con aminoácidos con grupos hidroxilo, Serina, Treonina y Tirosina. Esto provoca un cambio en la célula y a su vez la respuesta.
Unión del ligando[editar]
Los RAPG incluyen receptores de mediadores de señales sensoriales (por ejemplo, moléculas estimuladoras de luz y olfativas); adenosina, bombesina, bradicinina, endotelina, ácido γ-aminobutírico (GABA), factor de crecimiento de hepatocitos (HGF), melanocortinas, neuropéptido Y, péptidos opioides, opsinas, somatostatina, GH, kisspeptinas, taquicininas, miembros de la familia péptido vasoactivo intestinal, y vasopresina; aminas biogénicas (por ejemplo, dopamina, epinefrina, norepinefrina, histamina, glutamato (efecto metabotrópico), glucagón, acetilcolina (efecto muscarínico), y serotonina); quimiocinas; mediadores lipídicos de inflamación (por ejemplo, prostaglandinas, prostanoides, factor activador de plaquetas, y leucotrienos); y hormonas peptídicas (por ejemplo, calcitonina, C5a anafilatoxina, hormona foliculoestimulante (FSH), hormona liberadora de gonadotropina (GnRH), neuroquinina, hormona liberadora de tirotropina (TRH), cannabinoides, y oxitocina). Los RAPGs que actúan como receptores para estímulos que aún no han sido identificados se conocen como receptores huérfano.
Considerando que, en otros tipos de receptores que han sido estudiados, en donde los ligandos se unen externamente a la membrana, los ligandos de los RAPGs típicamente se unen dentro del dominio transmembranal. Sin embargo, los receptores activados por proteasa son activados por escisión de una parte de sus dominios extracelulares.[14]
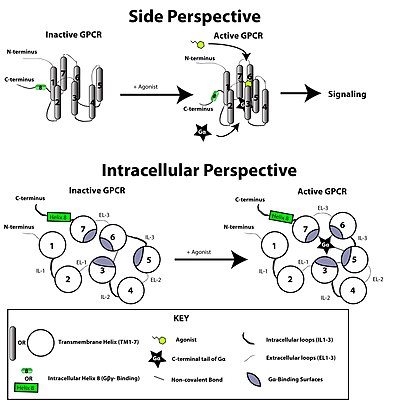
Cambio conformacional[editar]

La transducción de la señal a través de la membrana por el receptor no se conoce completamente. Se sabe que la proteína G inactiva está enlazada al receptor en su estado inactivo. Una vez que el ligando es reconocido, el receptor cambia de conformación, y así activa mecánicamente a la proteína G, que se separa del receptor. El receptor ahora puede activar otra proteína G o volver a su estado inactivo. El proceso real es mucho más complejo, pero esta descripción permite comprenderlo someramente.
Se cree que una molécula de receptor existe en un equilibrio entre los estados conformacionales biofísicos activos e inactivos.[15] La unión de un ligando en un receptor podría desplazar el equilibrio hacia los estados activos del receptor.[16] Existen tres tipos de ligandos:
- los agonistas son ligandos que desplazan el equilibrio en favor de los estados activos;
- los agonistas inversos son ligandos que desplazan el equilibrio en favor de los estados inactivos;
- y los antagonistas neutrales son ligandos que no afectan el equilibrio.
Aún no se sabe exactamente cómo los estados activos e inactivos difieren entre sí.
Ciclo de activación/desactivación de la proteína G[editar]

Cuando el receptor está inactivo, el dominio GEF podría estar enlazado a una también inactiva subunidad α de una proteína G heterotrimérica. Estas "proteínas G" son un trímero de subunidades α, β, y γ (conocidas como Gα, Gβ, y Gγ respectivamente) que se vuelven inactivas cuando se enlazan reversiblemente a un guanosín difosfato (GDP) (o alternativamente, a ningún nucleótidos de guanina) pero se vuelven activas cuando se unen a un guanosín trifosfato (GTP). Tras la activación del receptor, el dominio GEF, a su vez, activa alostéricamente la proteína G al facilitar el intercambio de una molécula de GDP por una de GTP en la subunidad α de la proteína G. La célula mantiene una relación 10:1 de GTP:GDP cíclico, así el intercambio por un GTP está asegurado. En este punto, las subunidades de laproteína G se disocian del receptor, así como entre ellos, para producir un monómero Gα-GTP y un dímero Gβγ, que ahora son libres para modular la actividad de otras proteínas intracelulares. El grado en que puede difundirse, sin embargo, es limitado debido a la palmitoilación del Gα y la presencia de una molécula de glicophosfatidilinositol (GPI) que ha sido covalentemente añadido al terminal C del Gγ. La mitad fosfatidilinositol del enlace GPI contiene dos grupos acilo hidrófobos que anclan cualquier proteína enlazada con GPI (por ejemplo, Gβγ) con la membrana plasmática, y también, en cierta medida, a las balsas lipídicas locales (compare esto con el efecto de palmitoilación en la localización del RAPG discutida anteriormente).
Debido a la lenta capacidad de hidrólisis GTP→GDP del Gα, la forma inactiva de la subunidad α (Gα-GDP) es eventualmente regenerada, permitiendo la reasociación con el dímero Gβγ para formar una proteína G "inactiva", que a su vez puede nuevamente unirse a un RAPG y esperar la activación. La velocidad de hidrólisis de GTP es generalmente muy rápida. Esto es debido a la acción de otra familia de proteínas moduladoras alostéricas llamadas reguladoras de la señalización de la proteína G, o proteínas RGS. Estas proteínas RGS que son un tipo de proteínas activadoras de GTPasa, con un dominio GAP que tiene la capacidad de acelerar la hidrólisis del GTP. De hecho, muchas de las principales proteínas efectoras (por ejemplo adenilil ciclasa) que se activan/desactivan ante la interacción con Gα-GTP también tienen actividad GAP. Así, incluso en esta etapa temprana del proceso, la señalización iniciada por RAPG tiene la capacidad de auto-terminación.
Véase también[editar]
Referencias[editar]
- ↑ a b c Latorraca, Naomi R.; Venkatakrishnan, A. J.; Dror, Ron O. (septiembre de 2016). «GPCR Dynamics: Structures in Motion» [Dinámica RAPG: estructuras en movimiento]. Chem. Rev. (en inglés) (American Chemical Society) 117: 139−155. doi:10.1021/acs.chemrev.6b00177. Consultado el 16 de mayo de 2017.
- ↑ a b Hanlon, Caitlin D.; Andrew, Deborah J. (2015). «Outside-in signaling – a brief review of GPCR signaling with a focus on the Drosophila GPCR family» [Señalización afuera y adentro – una revisión breve de la señalización de GPRC con foco en la familia RAPG de la Drosophila]. J Cell Sci (en inglés) 128: 3533-3542. doi:10.1242/jcs.175158. Consultado el 15 de mayo de 2017.
- ↑ a b Geppetti, Pierangelo; Veldhuis, Nicholas A.; Lieu, TinaMarie; Bunnett, Nigel W. (noviembre de 2015). «G Protein-Coupled Receptors: Dynamic Machines for Signaling Pain and Itch» [Receptor acoplado a proteínas G: Máquinas dinámicas para señalizar dolor y picor]. Neuron (en inglés) (Elsevier Inc) 88: 635-649. doi:10.1016/j.neuron.2015.11.001. Consultado el 15 de mayo de 2017.
- ↑ a b c Zhang, Dandan; Zhao, Qiang; Wu, Beili (octubre de 2015). «Structural Studies of G Protein-Coupled Receptors» [Estudios estructurales de los receptores acoplados a proteína G]. Mol Cells (en inglés) (Korean Society for Molecular and Cellular Biology) 38 (10): 836-842. PMID 26467290. doi:10.14348/molcells.2015.0263. Consultado el 16 de mayo de 2017.
- ↑ Katritch, Vsevolod; Cherezov, Vadim; Stevens, Raymond C. (enero de 2013). «Structure-Function of the G-protein-Coupled Receptor Superfamily» [Estructura-función de la superfamilia de receptores acoplado a proteína G]. Annu Rev Pharmacol Toxicol (en inglés) 53: 531-556. PMID 23140243. doi:10.1146/annurev-pharmtox-032112-135923. Consultado el 15 de mayo de 2017.
- ↑ Filmore, David (noviembre de 2004). «It's a GPCR world. Cell-based screening assays and structural studies are fueling G-protein coupled receptors as one of the most popular classes of investigational drug targets» [Es un mundo RAPG. Estudios estructurales y ensayos de tamizaje basado en células están posicionando a los receptores acoplados a proteínas G como una de las clases más populares de blanco para las drogas de investigación]. Modern Drug Discovery (American Chemical Society) 7 (11): 24-28. ISSN 1532-4486.
- ↑ King N, Hittinger CT, Carroll SB (2003). «Evolution of key cell signaling and adhesion protein families predates animal origins». Science 301 (5631): 361-363. PMID 12869759. doi:10.1126/science.1083853.
- ↑ Gilman A.G. (1987). «G Proteins: Transducers of Receptor-Generated Signals». Annual Review of Biochemistry 56: 615-649. PMID 3113327. doi:10.1146/annurev.bi.56.070187.003151.
- ↑ Alexander, S. P. H.; Davenport, A. P.; Kelly, E.; Marrion, N.; Peters, J. A.; Benson, H. E. (2015). «The Concise Guide to PHARMACOLOGY 2015/16: G protein-coupled receptors» [La guía concisa de farmacología 2015/16: receptores acoplados a proteínas G]. Br J Pharmacol (en inglés) 172: 5744-5869. Consultado el 17 de mayo de 2017.
- ↑ a b Rosenbaum, Daniel M.; Rasmussen, Søren G. F.; Kobilka, Brian K. (mayo de 2009). «The structure and function of G-protein-coupled receptors» [La estructura y función de los receptores acoplados a proteínas G]. Nature (en inglés) 459 (7245): 356-363. PMID 19458711. doi:10.1038/nature08144. Consultado el 17 de mayo de 2017.
- ↑ Michino, Mayako; Beuming, Thijs; Donthamsetti, Prashant; Newman, Amy Hauck; Javitch, Jonathan A.; Shi, Lei (enero de 2015). «What Can Crystal Structures of Aminergic Receptors Tell Us about Designing Subtype-Selective Ligands?» [¿Qué nos pueden decir la estructuras cristalinas de los receptores aminérgicos acerca del diseño de ligandos selectivos de subtipos?]. Pharmacological Reviews (en inglés) (American Society for Pharmacology and Experimental Therapeutics) 67 (1): 198-213. ISSN 1521-0081. doi:10.1124/pr.114.009944. Consultado el 16 de mayo de 2017.
- ↑ Wettschureck N, Offermanns S (octubre de 2005). «Mammalian G proteins and their cell type specific functions». Physiol. Rev. 85 (4): 1159-204. PMID 16183910. doi:10.1152/physrev.00003.2005.
- ↑ Millar RP, Newton CL (enero de 2010). «The year in G protein-coupled receptor research». Mol. Endocrinol. 24 (1): 261-74. PMID 20019124. doi:10.1210/me.2009-0473.
- ↑ Brass LF (septiembre de 2003). «Thrombin and platelet activation». Chest 124 (3 Suppl): 18S-25S. PMID 12970120. doi:10.1378/chest.124.3_suppl.18S.
- ↑ Rubenstein, Lester A. and Lanzara, Richard G. (1998). «Activation of G protein-coupled receptors entails cysteine modulation of agonist binding». Journal of Molecular Structure (Theochem) 430: 57-71. doi:10.1016/S0166-1280(98)90217-2.
- ↑ http://www.bio-balance.com/
