Ribosoma

1. Nucléolo, 2. Núcleo celular, 3. Ribosomas (pequeños puntos) 4. Vesículas, 5. Retículo endoplásmico rugoso, 6. Aparato de Golgi,
7. Microtúbulo (citoesqueleto), 8. Retículo endoplásmico liso, 9. Mitocondrias,10. Vacuolas,
11. Citosol, 12. Lisosoma, 13. Centríolos,
14. Membrana celular
Los ribosoma y polisomas son orgánulos citoplasmáticos no delimitados por una membrana, formados por el ácido ribonucleico ribosómico (ARNr) y proteínas ribosómicas,[1] que constituyen una máquina molecular presente en todas las células (excepto en los espermatozoides).[2] Son los centros celulares de traducción que hacen posible la expresión de los genes. Es decir, son los encargados de la síntesis de proteínas a partir de la información contenida en el ADN, que llega transcrita a los ribosomas en forma de ARN mensajero (ARNm).
Para todo lo perteneciente o relativo a los ribosomas, se utiliza propiamente en español el adjetivo «ribosómico», siendo «ribosomal» un anglicismo.
Función[editar]
Los ribosomas son responsables de la síntesis de proteínas,[3] en un proceso conocido como traducción. La información necesaria para esa síntesis se encuentra en el ARN mensajero (ARN), cuya secuencia de nucleótidos, determina la secuencia de aminoácidos de la proteína. A su vez, la secuencia del ARN proviene de la transcripción de un gen que se encuentra en el ADN. El ARN de transferencia lleva los aminoácidos a los ribosomas donde se incorporan al polipéptido en crecimiento.
Traducción[editar]


El ribosoma lee el ARN mensajero y ensambla los aminoácidos suministrados por los ARN de transferencia a la proteína en crecimiento, proceso conocido como traducción o síntesis de proteínas.
Todas las proteínas están formadas por aminoácidos. Entre los seres vivos se han descubierto hasta ahora 20 aminoácidos. En el código genético, cada uno de los aminoácidos está codificado por uno o varios codones. En total hay 64 codones que codifican 20 aminoácidos y 3 señales de parada de la traducción. Esto hace que el código sea degenerado y que haya varios codones diferentes para un mismo aminoácido.
La traducción comienza, en general, con el codón AUG que codifica el aminoácido metionina. Al final de la secuencia se ubica un codón que indica el final de la proteína; es el codón de terminación. El código genético es universal porque cada codón codifica el mismo aminoácido para la mayoría de los organismos (no todos).
El ribosoma consta de dos partes, la subunidad mayor y una menor, estas salen del núcleo celular por separado. Las subunidades se mantienen unidas por cargas. Al disminuir experimentalmente la concentración de Mg2+, las subunidades tienden a separarse.
Por ejemplo, en el citoplasma de una célula eucariota, el proceso con la secuencia de ARN mensajero que se indica sería este:[4]
- AUG le indica que tiene que empezar a ensamblar la proteína. Es un codón de iniciación. Ensambla una metionina.
- GCC es alanina. Toma una alanina y la une a la metionina.
- AAC es asparagina, lo une con la alanina.
- GGC es glicina, lo ensambla a la asparagina.
- AUG era el símbolo de iniciación, pero el proceso ya ha comenzado. Une una metionina con la glicina anterior.
- CCU es prolina. Ensambla la prolina a la metionina.
- ACU es treonina. Ensambla la treonina con la prolina.
- UAG es el codon de terminación. Deja de ensamblar la proteína.
Por tanto, la cadena polipeptídica ensamblada ha sido: Alanina-Asparagina-Glicina-Metionina-Prolina-Treonina.

Estructura y localización[editar]
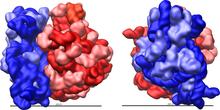
Los ribosomas se encuentran en el citosol, en las mitocondrias, en el retículo endoplasmático rugoso y en los cloroplastos. Solo son visibles al microscopio electrónico, debido a su reducido tamaño (29 nanómetros en células procariotas y 32 nm en eucariotas). Bajo el microscopio electrónico se observan como estructuras redondeadas, densas a los electrones. Bajo el microscopio óptico se observa que son los responsables de la basofilia que presentan algunas células. Los ribosomas están considerados en muchos textos como orgánulos no membranosos, ya que no existen endomembranas en su estructura,[5] aunque otros biólogos no los consideran orgánulos propiamente por esta misma razón.[6]
Están formados por ARN ribosómico (ARNr) y por proteínas ribosómicas. Estructuralmente, tienen siempre dos subunidades: la mayor o grande y la menor o pequeña. En las células, estas macromoléculas aparecen en diferentes estados de disociación. Cuando están completas, pueden estar aisladas o formando grupos (polisomas). En células eucariotas, los ribosomas se elaboran en el núcleo pero desempeñan su función de síntesis en el citosol. Las proteínas sintetizadas por los ribosomas actúan principalmente en el citosol; también pueden aparecer asociados al retículo endoplasmático rugoso o a la membrana nuclear externa, y las proteínas que sintetizan son sobre todo para la secreción.
Tanto el ARNr como las subunidades de los ribosomas se suelen nombrar por su coeficiente de sedimentación en unidades Svedberg. En las células eucariotas, los ribosomas del citoplasma alcanzan 80 S. En plastos de eucariotas, así como en procariotas, son 70 S. Los ribosomas mitocondriales son de tamaño variado, entre 55 y 70 S.[7]
Ribosoma procariota[editar]
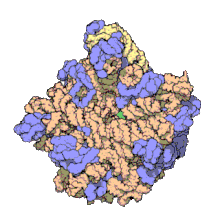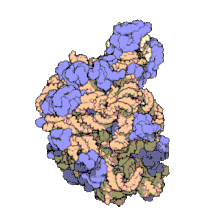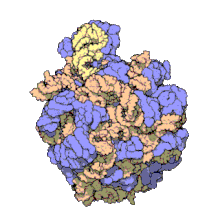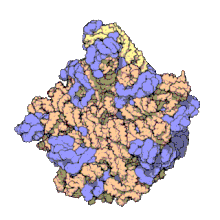
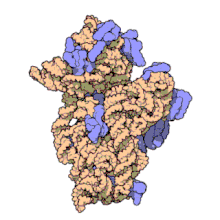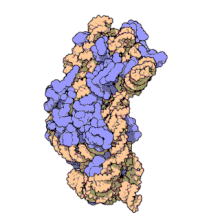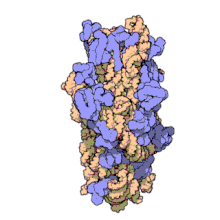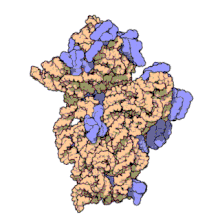
En la célula procariota, tanto de bacterias como de arqueas,[10] los ribosomas tienen un coeficiente de sedimentación de 70 S. Contienen un 66 % de ARNr y se dividen en dos subunidades de distinto tamaño:
- Subunidad mayor: Su coeficiente de sedimentación es 50 S. Tiene dos tipos de ARNr: 5 S (con 120 nucleótidos) y 23 S (2.904 nt), y tiene 31 proteínas ribosómicas como promedio.
- Subunidad menor: Su coeficiente de sedimentación es 30 S. Tiene una sola molécula de ARNr 16 S con 1.542 nucleótidos y contiene 21 proteínas.[11]
La función más importante del ribosoma es la síntesis de las proteínas, elemento esencial para el funcionamiento general de todos los seres vivos.[12]
Ribosoma eucariota[editar]
En la célula eucariota, los ribosomas tienen un coeficiente de sedimentación de 80 S. Su peso molecular es de 4.194 Kd. Contienen un 40 % de ARNr y 60 % de proteínas. Al igual que los procariotas se dividen en dos subunidades de diferentes tamaños.
Subunidad mayor[editar]
Coeficiente de sedimentación de 60 S. Tres tipos de ARNr: 5 S, 28 S y 5,8 S y tiene 49 proteínas, todas ellas distintas a las de la subunidad menor.
Subunidad menor[editar]
Coeficiente de sedimentación es 40 S. Tiene una sola molécula de ARNr 18 S y contiene 33 proteínas. Dependiendo del organismo eucariota, este ARNr 18 S puede presentar variaciones.
Ribosoma mitocondrial[editar]
Los ribosomas mitocondriales o «mitorribosomas» junto con ARNt y ARNm, son parte del aparato propio de síntesis proteica que tienen las mitocondrias. Son de tamaño variable, desde los 50S de Leishmania[13] hasta 72S en Candida.[14] Los mitorribosomas de las células animales son 55S y sus dos tipos de ARN ribosómicos, el 12S y 16S, se transcriben a partir de genes del ADN mitocondrial, y son transcritos por una ARN polimerasa mitocondrial específica. Todas las proteínas que forman parte de los ribosomas mitocondriales están codificadas por genes del núcleo celular, que son traducidos en el citosol y transportados hasta las mitocondrias.[15]
Ribosoma plastidial[editar]

Los ribosomas que aparecen en plastos o «plastorribosomas» son similares a los ribosomas procariotas. Son, al igual que los procariotas, de 70 S, pero en la subunidad mayor hay un ARNr de 4 S que es equivalente al 5 S procariota.
La subunidad mayor 50S tiene unas 33 proteínas y la subunidad menor 30S tiene unas 25 proteínas. La gran mayoría de estas proteínas son homólogas (ortólogas) a las proteínas ribosómicas bacterianas y unas pocas son específicas de los cloroplastos.[16]
Origen[editar]
El ribosoma podría haber aparecido en un mundo de ARN, primero como un complejo autorreplicante que después evolucionó con la habilidad para encadenar aminoácidos.[17] Estudios sugieren que un ribosoma compuesto únicamente de ARNr sería capaz de propiciar la formación de enlaces peptídicos.[18][19][20] Adicionalmente, otras evidencias aducen la autosuficiencia genética de los ribosomas, característica ausente en el complejo aparato de replicación del ADN. Presumiblemente, el ARNr surgió como catalizador de su propia replicación, haciendo uso de su capacidad para luego codificar y sintetizar ARNt y proteínas para llevarla a cabo.[21] Conforme fueron apareciendo aminoácidos en las condiciones prebióticas del mundo de ARN,[22][23] sus interacciones con el ARN autocatalítico habrían conferido a este último un mayor alcance y eficiencia.[17] Bajo esta rúbrica, la fuerza motora para la evolución del ribosoma actual a partir de una máquina autorreplicante arcaica podría haber sido la presión selectiva por incorporar proteínas a la maquinaria, de manera que aumentara su capacidad de autorreplicación.[21]
Descubrimiento[editar]
Los ribosomas fueron observados por primera vez a mediados de la década de 1950 por el biólogo celular rumano-estadounidense George Emil Palade, usando un microscopio electrónico, como partículas densas o gránulos.[2][24] El término «ribosoma» fue propuesto por el científico Haguenau a fines de 1958:
Durante el transcurso del simposio se hizo evidente una dificultad semántica. Para algunos de los participantes, «microsomas» significa las partículas de ribonucleoproteína de la fracción de microsomas contaminadas por otras proteínas y material lipídico; para otros, los microsomas consisten en proteínas y lípidos contaminados por partículas. La frase «partículas microsómica» no parece adecuada, y «partículas de ribonucleoproteínas de la fracción microsómica» es demasiado incómoda. Durante la reunión se sugirió la palabra «ribosoma», que tiene un nombre muy satisfactorio y un sonido agradable. La confusión actual se eliminaría si se adoptara «ribosoma» para designar partículas de ribonucleoproteína en tamaños que oscilan entre 35 y 100S.During the course of the symposium a semantic difficulty became apparent. To some of the participants, "microsomes" mean the ribonucleoprotein particles of the microsome fraction contaminated by other protein and lipid material; to others, the microsomes consist of protein and lipid contaminated by particles. The phrase "microsomal particles" does not seem adequate, and "ribonucleoprotein particles of the microsome fraction" is much too awkward. During the meeting, the word "ribosome" was suggested, which has a very satisfactory name and a pleasant sound. The present confusion would be eliminated if "ribosome" were adopted to designate ribonucleoprotein particles in sizes ranging from 35 to 100S.Microsomal Particles and Protein Synthesis[25]
Albert Claude, Christian de Duve y George Emil Palade recibieron conjuntamente el Premio Nobel de Fisiología o Medicina en 1974 por el descubrimiento del ribosoma.[26] El Premio Nobel de Química 2009 fue otorgado a Venkatraman Ramakrishnan, Thomas A. Steitz y Ada E. Yonath por determinar la estructura detallada y el mecanismo del ribosoma.[27]
Véase también[editar]
Referencias[editar]
- ↑ «ribosoma». Real Academia Nacional de Medicina de España.
- ↑ a b Mollejo, Verónica (14 de agosto de 2017). «Ribosomas: ¿Qué son y para qué sirve este complejo supramolecular?». OKDIARIO (España). Consultado el 24 de junio de 2018.
- ↑ «ribosoma». RAE.
- ↑ Nelson, David L.; Cox, Michael M. (2006). Lehninger. Principios de bioquímica. Omega. pp. 1038-1058. ISBN 8428214107.
- ↑ F. Jiménez y H. Merchant 2003. Biología Celular y Molecular. Parte II Estructuras celulares. Cap.13 Ribosomas. Pearson Educación, México
- ↑ lberts, Bruce et al. (2002). The Molecular Biology of the Cell, 4th ed., Garland Science.
- ↑ MITORIBOSOMES TERMIUM Plus®, el banco de datos terminológicos y lingüísticos del Gobierno de Canadá
- ↑ Ban N, Nissen P, Hansen J, Moore P, Steitz T (2000). «The complete atomic structure of the large ribosomal subunit at 2.4 Ångström resolution». Science (en inglés) 289 (5481): 905-20. PMID 10937989. doi:10.1126/science.289.5481.905.
- ↑ Wimberly BT, Brodersen DE, Clemons WM Jr, Morgan-Warren RJ, Carter AP, Vonrhein C, Hartsch T, Ramakrishnan V (septiembre de 2000). «Structure of the 30S ribosomal subunit». Nature 407 (6802): 327-39. PMID 11014182. doi:10.1038/35030006.
- ↑ W. S. Vincent Yip, Nicholas G. Vincent and Susan J. Baserga, 2013. Ribonucleoproteins in Archaeal Pre-rRNA Processing and Modification. Archaea, 2013.
- ↑ Reginald Garrett, Charles Grisham 2009-2013. Biochemistry. Cap.10 Nucleotides an Nucleic Acids. 10.5. Differents classes. Books/Cole CA USA
- ↑ «Significado de Ribosomas». Significados. com. 2013. Consultado el 8 de noviembre de 2020.
- ↑ D. Maslov & R. Agrawal 2012. Mitochondrial Translation in Trypanosomatids Nucleic Acids and Molecular Biology Volume 28, 2012, pp 215-236
- ↑ Pierre V. Vignais et al 1972. MITORIBOSOMES FROM CANDIDA UTILIS J Cell Biol. 1972 September 1; 54(3): 468–492.
- ↑ Devlin, T. M. 2004. Bioquímica, 4.ª edición. Reverté, Barcelona. ISBN 84-291-7208-4
- ↑ Yamaguchi K & Subramanian AR 2000. The plastid ribosomal proteins. Identification of all the proteins in the 50 S subunit of an organelle ribosome (chloroplast). J Biol Chem. 2000 Sep 15;275(37):28466-82.
- ↑ a b Noller, H. F. (2012). «Evolution of protein synthesis from an RNA world». Cold Spring Harbor Perspectives in Biology 4: 1-U20.
- ↑ Dabbs, E.R. (1986). Mutant studies on the prokaryotic ribosome. Springer-Verlag, N.Y.
- ↑ Noller, H. F.; Hoffarth, V.; Zimniak, L. (1992). «Unusual resistance of peptidyl transferase to protein extraction procedures». Science 256: 1416-1419. PMID 1604315. doi:10.1126/science.1604315.
- ↑ Nomura, M.; Mizushima, S.; Ozaki, M.; Trau, P.; Lowry, C. V. (1969). «Structure and function of ribosomes and their molecular components». Cold Spring Harbor Symposium of Quantitative Biology 34: 49-61. doi:10.1101/sqb.1969.034.01.009.
- ↑ a b Root-Bernstein, M.; Root-Bernstein, R. (2015). «The ribosome as a missing link in the evolution of life». Journal of Theoretical Biology 367: 130-158. PMID 25500179. doi:10.1016/j.jtbi.2014.11.025.
- ↑ Caetano-Anolles, G.; Seufferheld, M. J. (2013). «The coevolutionary roots of biochemistry and cellular organization challenge the RNA world paradigm». Journal of Molecular Microbiology and Biotechnology 23: 152-177. doi:10.1159/000346551.
- ↑ Saladino, R.; Botta, G.; Pino, S.; Costanzo, G.; Mauro, E. Di (2012). «Genetics first or metabolism first? The formamide clue». Chemical Society Reviews 41: 5526-5565. doi:10.1039/c2cs35066a.
- ↑ «A small particulate component of the cytoplasm». The Journal of Biophysical and Biochemical Cytology 1 (1): 59-68. January 1955. PMC 2223592. PMID 14381428. doi:10.1083/jcb.1.1.59. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ «Introduction». Microsomal Particles and Protein Synthesis. New York: Pergamon Press, Inc. 1958. Parámetro desconocido
|veditors=ignorado (ayuda) - ↑ «The Nobel Prize in Physiology or Medicine 1974». Nobelprize.org. The Nobel Foundation. Archivado desde el original el 26 de enero de 2013. Consultado el 10 de diciembre de 2012.
- ↑ «2009 Nobel Prize in Chemistry». The Nobel Foundation. Archivado desde el original el 28 de abril de 2012. Consultado el 10 de diciembre de 2012.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Ribosomas.
Wikimedia Commons alberga una categoría multimedia sobre Ribosomas. Wikcionario tiene definiciones y otra información sobre ribosoma.
Wikcionario tiene definiciones y otra información sobre ribosoma.
