Nucléolo
En biología celular, el nucléolo o nucleolo[1] es una región del núcleo que se considera una estructura supra-macromolecular,[2][3] que no posee membrana que lo limite.[4] La función principal del nucléolo es la transcripción del ARN ribosomal por la polimerasa I, y el posterior procesamiento y ensamblaje de los pre-componentes que formarán los ribosomas.
La biogénesis del ribosoma es un proceso nucleolar muy dinámico, que involucra: la síntesis y maduración de ARNr, sus interacciones transitorias con proteínas no-ribosomales y RNP y también el ensamblaje con proteínas ribosomales.[5]
Además, el nucléolo tiene roles en otras funciones celulares tales como la regulación del ciclo celular, las respuestas de estrés celular, la actividad de la telomerasa y el envejecimiento.
Estos hechos muestran la naturaleza multifuncional del nucléolo, que se refleja en la complejidad de su composición de proteína y de ARN, y se refleja también en los cambios dinámicos que su composición molecular presenta en respuesta a las condiciones celulares variables.[6]
Historia[editar]
A principios del siglo XVII pocos tenían un microscopio simple, y tal vez alguno de ellos pudo ver un nucléolo. Si lo hicieron, fue examinando cortes finos de tejidos, con el modo de iluminación hoy conocido como de campo claro.
La descripción realizada por Felice Fontana en 1781 fue la de una mota en el centro de un núcleo oviforme "...on observe un corps oviforme, ayant une tache dans son milieu.", posiblemente lo que él vio fue el nucléolo.[7]
El término nucléolo fue introducido por Gabriel Valentin en 1836. La palabra nucléolo viene a ser un diminutivo . Núcleo proviene del latín nux y significa nuececilla o semilla. Entonces, el nucléolo sería como la pequeña nuececilla del núcleo celular.[8] En esa época los nucléolos se mencionan de pasada, incluidos en algunos trabajos citológicos.
Las primeras revisiones documentadas del nucléolo las realizaron Rudolph Wagner en 1835[9]
y Gabriel Gustav Valentin en 1836.[10]
Luego una monografía sobre el nucléolo fue publicada por Montgomery en 1898,[11] con figuras de núcleos y nucléolos en color dibujadas a mano, tomadas de diversos materiales biológicos.
Estructura[editar]
El nucléolo ha sido denominado como: estructura, orgánulo, región, agrupamiento o compartimiento según los métodos de estudio utilizados. Un estudio morfológico lo definiría como estructura o región; en tanto que un estudio bioquímico diría que es un compartimiento o un agrupamiento macromolecular.
La genética definiría al nucléolo como una entidad citogenética,[12] que determina un compartimiento subnuclear;[13] este compartimiento deja dentro los dominios moleculares funcionales, necesarios para su actividad.

El nucléolo se organiza en torno a cromosomas específicos, que contienen segmentos de DNA repetidos y son llamados regiones organizadoras nucleolares (en inglés NORs).
Las NOR se localizan solamente en aquellos cromosomas que presentan una constricción secundaria, ésta determina que el extremo adopte una forma similar a la de un satélite. Por tanto se denominan cromosomas SAT a aquellos donde se encuentran las NORs. El número de cromosomas SAT varía dependiendo de la especie.
- En el humano las NOR aparecen ocupando una posición subterminal en los brazos cortos de 5 cromosomas acrocéntricos (13,14,15,21 y 22), donde se localizan entre 30 y 40 repeticiones en tándem de una unidad de transcripción de 13 kilobases y un espaciador no transcrito de 27 kb, donde residen los elementos reguladores.
Durante la interfase, estas porciones del genoma se encuentran desenrolladas y localizadas en un dominio del nucléolo y sobre ellas de forma continua se produce la transcripción de los genes ribosomales.
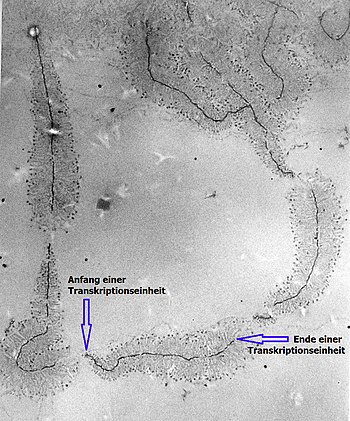
Cada uno de los genes que tiene la información para el ARNribosomal está repetido en racimos (clusters) distales y colocado en serie (tandem) en estos cinco cromosomas y se encuentra rodeado de cadenas de ARNr en crecimiento.
El complejo que realiza la síntesis de ARNribosomal, se coloca sobre una hebra del ADN y se va desplazando sobre el gen, creando una cadena de nucleótidos. Mediante una técnica especial, que provoca un extendido de cromatina nucleolar, se puede visualizar este proceso. Una micrografía electrónica tomada durante el proceso de síntesis, muestra cadenas de pre-ARNr en diferentes etapas de crecimiento sucesivo y por tanto con longitudes progresivamente crecientes, dando una imagen denominada “árbol de navidad” por Miller,[14][15] donde el tronco es el gen dentro de la fibra del ADN y las ramas son las cadenas de nucleótidos o transcritos primarios.
A partir de los genes (ADNr), la enzima ARN polimerasa I (polimerasa I o pol I) sintetiza una molécula larga llamada precursor de ARNribosomal (pre-ARNr).
Este pre-ARNr nucleolar, transcrito por la polimerasa I, tiene un coeficiente de sedimentacion de 45S en los eucariotas y 47S en mamíferos. El transcripto primario contiene: los tres ARNr, dos espaciadores externos (ETS) que también son transcritos, localizados en los extremos 5´ y 3´ del pre-ARN y dos espaciadores internos (ITS) que se sitúan entre las secuencias de los ARNr 18s, 5.8S y 28s. Entonces la fórmula de la estructura del pre-ARNr es la siguiente: 5´-ETS-18S-ITS-5.8S-ITS-28S-3´.
Luego de procesado el pre-ARNr da lugar al ARNr 18S de la subunidad ribosómica 40S (pequeña) y a los ARNr 5,8S y 28S de la subunidad ribosómica 60S (grande).
La alta densidad de las cadenas de ARNr en crecimiento es debida a la gran cantidad de moléculas de ARN polimerasa I presentes, con una densidad máxima de una polimerasa por cada cien pares de bases del ADN molde.
Morfología[editar]
El nucléolo es la estructura más prominente dentro del núcleo. Debido a la diferencia de densidad con la cromatina en la que está inmerso, se observa fácilmente en las células estudiadas con microscopio de luz.
Tanto el tamaño, como el número de los nucléolos son utilizados como método diagnóstico del estado funcional normal o de patología de la célula.
Forma[editar]
En general posee una forma aproximadamente esférica, pero varía en diferentes tipos de células eucariotas. En las preparaciones histológicas, luego de ser cortado, el nucléolo se observa como oval o redondeado y aparenta tener límites netos, pero en realidad no existe una membrana que separe el nucléolo del nucleoplasma en el que está inmerso. En las células vivas estudiadas con el microscopio de contraste de fases es posible observarlo de una forma más natural y cambiante.
Es fácilmente visible, debido a que su viscosidad y su refringencia son mayores que las del resto del núcleo. Los nucléolos son alrededor de dos veces más densos ópticamente que la cromatina que los circunda.[16]
Los medios más refringentes son aquellos en los que la luz se propaga a menor velocidad; se dice también que tienen una mayor densidad óptica. Por regla general, la refringencia de un medio va ligada a su densidad de materia, pues la luz encontrará más dificultades para propagarse cuanta mayor cantidad de materia haya de atravesar para una misma distancia. Las lentes de la mayor parte de los microscopios ópticos basan su funcionamiento en este fenómeno físico.
Localización[editar]
Los nucléolos suelen encontrarse en el centro del núcleo o ligeramente desplazados hacia la periferia. En núcleos polilobulados se los encuentra en un determinado lóbulo.
El nucléolo se encuentra en todas las células eucariotas con excepción de los espermatozoides y de los núcleos de segmentación de los anfibios.
A partir de la demostración de los territorios cromosómicos es posible asegurar que la cromatina, durante la interfase, tiene una disposición que no es aleatoria. Debido a que los cromosomas durante la interfase ocupan zonas exclusivas y limitadas en el núcleo, podemos anticipar la localización del nucléolo.[17] En un mismo tipo celular específico, se encontrarán los cromosomas portadores de las NOR en lugares determinados.
Tamaño[editar]
El tamaño de un nucléolo puede ser muy variable entre especies animales y vegetales, pero un promedio global suele oscilar entre 1 micrómetro (µm) y 2µm. El tamaño nucleolar usualmente refleja su actividad metabólica habitual dentro la célula, que es la biogénesis del ribosoma.

El tamaño de los nucléolos de las células germinales, ovocitos, y células intestinales en el gusano C. elegans es relativamente grande, con diámetros que van de 3 a 7µm. Las células germinales en el brazo distal (inicio) de las gónadas tienen los nucléolos más grandes de todos, que ocupan el 80 a 90% del volumen del núcleo. Mientras que los nucléolos de los ovocitos (en el final de la gónada) son indetectables. Los nucléolos de las neuronas son los más pequeños de todos con menos que 1 µm de diámetro. Los nucléolos son más grandes porque las células germinales y las células intestinales muestran mayor actividad de producción de ribosomas que las neuronas, ya que la función neuronal tiene menos necesidad de traducción de proteínas.[18]
Número[editar]
El número de nucléolos por núcleo celular es bastante variable, dependiendo del tipo de célula estudiado. Incluso en un mismo tipo celular, podemos encontrar importantes variaciones en cuanto a cantidad de nucléolos. La mayoría de las células tienen uno o dos nucléolos.
Los ovocitos de muchas especies de anfibios, peces, moluscos, insectos y gusanos, necesitan una activa síntesis proteica para acumular sustancias de reserva. Una síntesis proteica activa solamente se logra con un gran número de ribosomas y estos se construyen con ARN ribosómico. Los genes que codifican el ARN ribosómico se encuentran en las regiones organizadoras nucleolares (NOR). EL ADN de las NOR, se replica muchas veces y a este proceso se le llama amplificación génica. Estas dobles hélices replicadas emigran hacia la periferia nuclear donde formarán numerosos nucléolos.[19]
Se pueden llegar a observar muchos nucléolos en los ovocitos de Xenopus laevis, donde se han contado entre 500 y 2500 nucléolos.[20][21]
A medida que el ovocito de la rana Pelophylax perezi madura, en su núcleo (clásicamente denominado vesícula germinal) se produce un fenómeno denominado amplificación génica, en el cual se transcriben masivamente los cistrones ribosomales, por lo que se pueden observar gran cantidad de nucléolos extracromosómicos dispersos por el núcleo[22]
El nucléolo está rodeado por una capa de cromatina condensada. El nucléolo es la región heterocromática más destacada del núcleo. Los nucléolos están formados por proteínas y ADN ribosomal (ADNr). El ADNr es un componente fundamental ya que es utilizado como molde para la transcripción del ARN ribosómico(ARNr), que será incorporado a nuevos ribosomas. La mayor parte de las células tanto animales como vegetales, tienen uno o más nucléolos, aunque existen ciertos tipos celulares que no los tienen. En el nucléolo además tiene lugar la producción y maduración de los ribosomas, y una parte de los pre-ribosomas se encuentran dentro de él. Se cree que el nucléolo tiene otras funciones en la biogénesis de los ribosomas.
El nucléolo desaparece durante la división celular. Tras la separación de las células hijas mediante citocinesis, los fragmentos del nucléolo se fusionan de nuevo alrededor de las regiones organizadoras nucleolares de los cromosomas. Puede observarse que en la anafase las células carecen de nucléolos. En la telofase aparecen de nuevo y en la interfase es cuando ya son visibles.
En el nucléolo se distinguen dos partes: la zona central de tipo fibrilar, constituida por filamentos de cromatina y que se corresponde con el organizador nucleolar; la zona externa o granulosa, constituida por gránulos de ribonucleoproteínas que son parecidas a los ribosomas. Dentro del componente fibrilar del nucléolo de las plantas, se describe el nucleolonema. El Nucleolonema, aunque no siempre es un dominio nucleolar que se distinga inequívocamente, ha sido descrito como un elemento morfológico bien fundamentado, especialmente en los nucléolos de plantas.[23] También se pueden observar una o más zonas formadas por pequeños gránulos densos. Estas zonas no presentan conductos y constituyen una zona amorfa.
En la célula existen unas estructuras nucleares permanentes en los eucariotas verdaderos que son los cariosomas o cuerpos centrales. En la metafase se dividen en dos. Se sospecha que puedan ser nucléolos permanentes encontrándose en algas, protozoos y ciertos hongos.
Mediante estudios con el microscopio electrónico, se ha podido comprobar en el interior de los nucléolos, estructuras funcionales similares a "conductos" y "vacuolas".
Función[editar]
La función principal del nucléolo es la biosíntesis de ribosomas desde sus componentes de ADN para formar ARN ribosómico (ARNr). Está relacionado con la síntesis de proteínas y en células con una síntesis proteica intensa hay muchos nucléolos.[19]
Se ha comprobado que si se destruye o se extrae el nucléolo, al cabo de un cierto tiempo empiezan a escasear los ribosomas en el citoplasma.
Además, investigaciones recientes, han descrito al nucléolo como el responsable del tráfico de pequeños segmentos de ARN. El nucléolo además, interviene en la maduración y el transporte del ARN hasta su destino final en la célula.
Aunque el nucléolo no sea visible durante la división, algunos estudios actuales aseguran que regula el ciclo celular.
La estructura granular homogénea de los nucléolos puede ser observada con microscopia electrónica.
Ciclo del nucléolo[editar]
El nucléolo no se ve a lo largo de todo el ciclo celular. Al igual que los cromosomas, sufre una serie de cambios según se encuentre en interfase o en división. En interfase no sufre cambios morfológicos significativos (se puede dar un aumento o una fusión de varios). Sin embargo en división se dan cambios que determinan el ciclo del nucléolo. En este ciclo hay tres etapas:
- Desorganización profásica: el nucléolo disminuye de tamaño y se hace bastante irregular. Aparecen pequeñas masas de material nucleolar que se disponen entre los cromosomas profásicos que se están condensando.
- Transporte metafásico y anafásico: el nucléolo pierde su individualidad y sus componentes se incorporan a los cromosomas metafásicos.
- Organización telofásica: en la primera mitad de la telofase, los cromosomas se descondensan y aparecen los cuerpos laminares y cuerpos prenucleolares (de mayor tamaño y resultado de la fusión de los primeros). Estos cuerpos son estructuras esféricas con características citoquímicas y estructurales del núcleo interfase. Los cuerpos prenucleolares aumentan de tamaño y empiezan a formar un nucléolo alrededor de la región de los organizadores nucleolares. La cantidad de nucléolos depende del número de organizadores nucleolares
Referencias[editar]
- ↑ OMS,OPS (ed.). «Nucléolo». Descriptores en Ciencias de la Salud, Biblioteca Virtual en Salud.
- ↑ Facultad de Ciencias Médicas Dr Salvador Allende (ed.). «Modelos Celulares, Célula eucariota en el organismo humano, un subsistema compartimentado». Diplomado en Morfofisiología. Encuentro No.4. pp. 1-2.
- ↑ Complejidad y estructura supra-macromolecular del DNA en el genoma, Lección 23,. Colombia: Universidad Nacional Abierta.
- ↑ Real Academia Española. «nucléolo». Diccionario de la lengua española (23.ª edición). Consultado el 5 de marzo de 2015.
- ↑ Ivan Raška, Karel Koberna, Jan Malínský, Helena Fidlerová, Martin Mašata 2004; El nucleolo y la transcripción de genes ribosomales, Biology of the Cell 96 (2004) 579–594
- ↑ Boisvert, Francois-Michel (2007). «The Multifunctional nucleolus». Nature Reviews Molecular Cell Biology (Revisión). Vol.8: 574-583.
- ↑ Fontana, Felice. (1781). «Traité sur le vénin de la vipere, avec des observations sur la structure primitive du corps animale.». citado por Mosgoeller: Nucleolar Ultrastructure in Vertebrates, en The Nucleolus; 2003; editor Mark Olson (Florencia).
- ↑ Giménez, Gonzalo (2001). «Reiniciación de la transcripción en el ciclo celular: Núcleo lo génesis». Anal. Real Acad. Farm. (España): 67.
- ↑ Wagner, Rudolph (1835). «Einige Bemerkungen und Fragen über das Keimbläschen (vesicular germinativa).». Müller’s Archiv Anat Physiol Wissenschaft Med (Berlin): 373-377.
- ↑ Valentin, Gabriel (1836). Verlag von Veit und Comp., ed. Repertorium für Anatomie und Physiologie.. Berlin. pp. 1: 1-293.
- ↑ Montgomery, TH. (1898). 15. «Comparative cytological studies, with special regard to the morphology of the nucleolus.». J Morph: 265-282.
- ↑ Pederson, Thoru (2010). «The Nucleolus.». Perspectives in Biology, csh (Cold Spring Harbor). Consultado el 24 de junio de 2019.
- ↑ Németh, A (2010). «Initial Genomics of the Human Nucleolus.». PLoS Genet (Public Library of Science) 6 (3). doi:10.1371/journal.pgen.1000889. Consultado el 14 de noviembre de 2013.
- ↑ Miller, Oscar; Beatty, B (1969). «Visualization of nucleolar genes.». Science 164: 955-957.
- ↑ McKnight, Steven (2012). «Oscar Miller (1925–2012) Retrospective». Science 335 (1457). doi:10.1126/science.1220681.
- ↑ Mello, María Luiza (2007). Barueri, San Paulo, ed. Nucléolo Cap 12 (en portugués). en A célula. Carvalho (2a edición). Manole. pp. 144-154.
- ↑ Tiang, Choon-Lin (2012). «Chromosome Organization and Dynamics during Interphase, Mitosis, and Meiosis in Plants». Plant Physiology. vol. 158 (no. 1): 26-34.
- ↑ Lee, Li-Wei; Lee, Chi-Chang; Huang, Chi-Ruei; Lo, Szecheng. (2012). «The Nucleolus of Caenorhabditis elegans». Journal of Biomedicine and Biotechnology (Hindawi Publishing Corporation) 2012 ((4)).
- ↑ a b «Tema 26: El Nucleolo. 2.1. Amplificación genética.» (pdf). Configuración de los seres vivos. Departamento de Histología Universidad Miguel Hernández Facultad de Ciencias Experimentales, Campus de Elche.
- ↑ Thiébaud, Charles (1979). «Quantitative determination of amplified rDNA and its distribution during oogenesis in Xenopus». Chromosome (Berlin). vol. 73: 37-44.
- ↑ Mais, Christine; Scheer, Ulrich (2001). «Molecular architecture of the amplified nucleoli of Xenopus oocytes». Journal of Cell Science 114 ((4)): 709-718.
- ↑ «Ovogénesis en invertebrados (ortópteros) y vertebrados (anfibios) (I) Práctica 3» (pdf). Embriología básica. Citología, Departamento de Biología, Facultad de Ciencias, U Auton Madrid. p. 5.
- ↑ Stępiński, Dariusz (2014). «Functional ultrastructure of the plant nucleolus.». Protoplasma. Vol.251 (6): 1285-1306.
Bibliografía[editar]
Cheng D. , Huang S. Nucleolar components involved in ribosome biogenesis cycle between the nucleolus and nucleoplasm in interphase cells. (2001) https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2185520/
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Nucléolo.
Wikimedia Commons alberga una categoría multimedia sobre Nucléolo.

