Inmunología de la reproducción
La inmunología de la reproducción es parte de la ciencia de la inmunología y estudia la participación del sistema inmune en la reproducción sexual animal, en especial humana. Debido a que el feto produce elementos antigénicos potencialmente reactivos en la madre, es de especial interés que las reacciones inmunológicas en contra del producto de la gestación sean virtualmente inexistentes y que el intercambio de fluidos sexuales y el subsecuente embarazo se completen sin la activación patológica de la inmunidad materna.
Generalidades[editar]
El proceso de reproducción en el humano implica el contacto entre células que son alogénicas entre sí. Durante el coito, el tracto genital femenino se expone a diferentes antígenos presentes en el semen. Los espermatozoides y algunas de las proteínas secretadas por la glándula prostática o por las vesículas seminales son potencialmente antigénicas. Después de la fecundación, en el embarazo, el feto comienza a expresar antígenos procedentes del padre que son antigenicamente diferentes a los de la contribución materna.
El recién nacido, amamantado por la madre, está a su vez sometido a células maternas con la posibilidad de reaccionar contra las proteínas presentes en su mucosa intestinal por razón de anticuerpos generados por genes heredados del padre.
Es lógico, por lo tanto, que para que los procesos de la reproducción sexual, el embarazo y la lactancia transcurran sin eventualidades inmunogénicas, se requiera un control especial de los mecanismos normales de dicha respuesta inmune.
Inmunidad e infertilidad[editar]
Estudios epidemiológicos demuestran que 10 a 15% de las parejas son infértiles.[1] De éstas, en una cuarta parte no se detecta una causa orgánica que explique la infertilidad. Un 2 a 3% de las parejas en las cuales se descarta toda explicación orgánica, hormonal o autoinmune para la infertilidad, parecen ser infértiles por mecanismos inmunitarios.
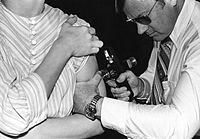
La espermatogénesis se inicia en la pubertad cuando el sistema inmune está completamente maduro, y en consecuencia este podría reaccionar contra las nuevas proteínas que se expresan en los espermatozoides. Esto no ocurre gracias a la existencia de una barrera hematotesticular, formada por unión entre las células de Sértoli y componentes inmunosupresores peritubular y que previenen el ingreso de linfocitos.[2] Esta barrera se puede romper por trauma, orquitis o ligadura del epidídimo como medida de control de fecundación. En estas circunstancias se puede generar anticuerpos contra los espermatozoides, los cuales pueden interferir en el tránsito de estos por las vías genitales del hombre o de la mujer y ocasionar infertilidad.[2] Un 3% de los hombres infértiles han demostrado tener anticuerpos contra su propio esperma en títulos mayores al 1/32.
Reacciones anafilácticas contra el semen[editar]
La mujer puede formar igualmente anticuerpos contra el espermatozoide, interfiriendo con el paso de ellos por el cuello uterino, su tránsito por el útero o las trompas de Falopio o con su aproximación y penetración al óvulo. Los espermatozoides colocados en la vagina, son en parte fagocitados por macrófagos y sus antígenos llevados a los ganglios linfáticos de la pelvis, en donde se pueden generar anticuerpos contra ellos.
Con procedimientos de aglutinación, inmovilización de los espermatozoides o pruebas de inmunofluorescencia, es posible demostrar en algunas mujeres infértiles la producción de anticuerpos contra los espermatozoides del marido. Estos anticuerpos secretados a nivel del moco cervical, pueden, por aglutinación de los espermatozoides, impedir su ingreso al útero. Estos anticuerpos pueden estar dirigidos contra diferentes sistemas antigénicos del espermatozoide, presentes en la cabeza, en la región ecuatorial, subnuclear, en la cola, o contra los antígenos del sistema sanguíneo ABO. La colocación del esperma intrauterinamente para evitar que los anticuerpos aglutinen los espermatozoides en el cuello, puede facilitar el embarazo.
Se han descrito varios casos, adecuadamente documentados en la literatura médica, de mujeres que se sensibilizan alérgicamente contra componentes del esperma del hombre y, en consecuencia, van a presentar reacciones mediadas por IgE contra las proteínas presentes en el esperma. Estas reacciones pueden dar lugar a procesos de inflamación local y, en algunos casos, a reacciones sistémicas con la producción de estados asmáticos y aun del choque anafiláctico con pérdida del conocimiento, manifestaciones que tienen lugar después de una relación sexual.[3]
Inmunidad celular y esterilidad[editar]
La atención sobre causas inmunológicas de esterilidad ha estado centrada en la producción de anticuerpos. No obstante, se empiezan a describir mecanismos de inmunidad celular que atacan el espermatozoide o el fruto de la fecundación.
Aquellos óvulos lavados, procedentes de mujeres con anticuerpos anti-espermatozoides, pueden ser fecundados in vitro y dar origen a embarazos normales después de ser implantados.
Deficiencia ovárica prematura[editar]
La menopausia prematura o precoz es la desaparición de la menstruación antes de los 40 años de edad y se presenta en 1% de las mujeres en edad reproductiva.[4] Se debe, en muchos casos, a problemas autoinmunes en los cuales hay auto-anticuerpos contra receptores para LH o FSH en el ovario.[5] Se caracteriza por niveles altos de estas hormonas y niveles bajos de estrógeno. Es frecuente la asociación con otras endocrinopatías, bien sea de tiroides o glándula suprarrenal. El fumar cigarrillos tiende a producir como secuela, la menopausia precoz. En algunos casos tratamientos inmunosupresores logran restablecer la función ovárica.
Vacunas contra la fertilidad[editar]
En ensayos de laboratorio se ha logrado producir “vacunas” o anticuerpos monoclonales contra una serie de antígenos que, obrando a distintos niveles del sistema reproductor, teóricamente evitan la fecundación o la anidación del huevo, o inducen alteraciones placentarias encaminadas al desprendimiento del embrión implantado.[6]
Los antígenos contra los cuales ha sido posible producir anticuerpos efectivos son principalmente hormonas de la reproducción: Gonadotropina coriónica humana (hCG), factor liberador de la hormona luteinizante, hormona luteinizante; así como antígenos presentes en el semen y antígenos del óvulo. Durante la maduración del óvulo se presentan nuevos antígenos de membrana celular, entre los cuales sobresale una glucoproteína de la zona pelúcida, que es gelatinosa e importante en el “atrapamiento” del espermatozoide. Ciertos anticuerpos dirigidos contra esta glucoproteína impiden la fijación de los espermatozoides y su eventual penetración en el óvulo. La producción de anticuerpos contra el trofoblasto o trofoectodermo podría desencadenar aborto inmunitario.
Inmunología del embarazo[editar]
Es debido a mecanismos inmunorreguladores de la respuesta materna, que el feto sobrevive en el medio intrauterino a pesar de poseer antígenos paternos que difieren de los de la madre.
La placenta está constituida por una serie de células trofoblásticas, que logran obtener de la madre los factores de nutrición que dan vida al desarrollo fetal. Simultáneamente establecen una marcada separación entre la circulación materna y la fetal, lo que hace que el feto no sea un verdadero injerto. Es decir, desde el punto de vista inmunológico no hay paso de células. Únicamente las inmunoglobulinas de clase IgG logran pasar la barrera placentaria, gracias a un mecanismo activo de transcitosis constituido básicamente por la interacción de receptores para la fracción Fc de la inmunoglobulina. Estos receptores se encuentran presentes en los trofoblastos y permiten captar los anticuerpos de la circulación materna, pasarlos al interior del citoplasma de las células trofoblásticas, y de ahí secretarlos a la circulación fetal.
Respuesta inmune del feto[editar]
Ha habido una acelerada evolución en el esclarecimiento de los mecanismos que permiten que un embarazo, como mecanismo inmunogénico, llegue a término, no obstante las diferencias antigénicas entre el feto —aquellos heredados por el padre— y la madre.[7] Inicialmente se creyó que el útero era un lugar inmunoprivilegiado, posteriormente que la placenta era una barrera infranqueable, luego que el sistema inmune de la madre se deprimía notablemente durante el embarazo por lo cual no podía reconocer o atacar los antígenos fetales de origen paterno.[8]
Los conceptos han cambiado radicalmente y se acepta que la inmunodepresión materna es muy discreta o se limita al sistema inmune específico, mientras que el sistema inmune innato se incrementa para garantizar una adecuada defensa de la madre frente a microorganismos patógenos. Así parece demostrarlo el incremento en la circulación materna de macrófagos y neutrófilos con fenotipo de activación, a partir del segundo trimestre del embarazo. El éxito del embarazo se debe primordialmente a un proceso de defensa activa del feto contra la respuesta inmune de la madre.
La interfase madre feto la constituyen el trofoblasto por lado del feto y la decidua por el de la madre. El trofoblasto con los eritrocitos representan las únicas células que no expresan antígenos de histocompatibilidad HLA-I, el trofoblasto expresa antígenos no clásicos HLA-G y HLA-E que permiten el contacto entre el trofoblasto y las células asesinas (células NK, del inglés Natural Killer), contacto que no solo impide la acción citotóxica de las últimas, sino que estimula en el trofoblasto la producción de factores estimuladores del crecimiento de la placenta.[8] La falta o pobre expresión de estos antígenos HLA-G y HLA-E se acompaña de aborto.
Por otra parte, la circulación fetal y materna están totalmente separadas lo que implica que el feto no puede ser considerado como un trasplante.[7] De igual manera a lo que ocurre en el ojo, el eventual ingreso de linfocitos T de la madre a la circulación materna, se acompaña de la inmediata producción del Factor de crecimiento transformante (TGF) que desactiva a estos linfocitos. El trofoblasto expresa ligando para las moléculas FAS presentes en algunas subpoblaciones de células T (TH1), que al interactuar inducen la apoptosis de estas células.[8]
Adicionalmente se produce un mediador liberado por los trofoblastos, no totalmente caracterizado y que inhibe el crecimiento de macrófagos y la respuesta de los linfocitos T a estímulos antigénicos.
Inmunosupresión materna[editar]
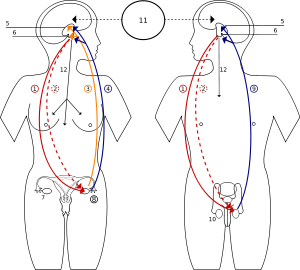
Durante el embarazo parece existir una disminución discreta de la capacidad inmunológica de la madre para reaccionar, no solo contra antígenos fetales sino contra otros con los cuales ha estado previamente en contacto.
Las hormonas producidas por la madre durante el embarazo, como los corticoesteroides, los estrógenos, la progesterona y la gonadotropina coriónica, pueden desempeñar un papel importante en cuanto a la depresión de la respuesta inmune por parte de la madre. Es sabido que los esteroides tienen efecto inmunosupresor, debido al cual se emplean en el tratamiento de enfermedades autoinmunes y en los pacientes a los cuales se les hace un trasplante de órganos. Los estrógenos cuando se emplean en dosis altas, (en el embarazo las concentraciones a nivel placentario pueden llegar hasta de 10 veces los valores normales), producen una supresión de la respuesta de inflamación y una disminución de la blastogénesis inducida por la producción de estímulos antigénicos.[9] La progesterona aumenta considerablemente durante el embarazo, alcanzando niveles que, in vitro, disminuyen la actividad linfática. La progesterona reduce en cierta forma la capacidad reactiva de la madre contra los antígenos fetales.[10] Si se colocan pellets o preparados con progesterona de liberación lenta, en forma subdérmica y en su proximidad se hace un trasplante de piel. Éste sobrevivirá meses, hasta cuando se agote la progesterona, indicando el poder inmunosupresor local de esta hormona.
La gonadotropina coriónica suprime la actividad de poblaciones de linfocitos T. Experimentalmente se logra prolongar con ella la supervivencia de un trasplante. Por lo tanto, es posible que a nivel del lugar de su mayor concentración, la placenta, desempeñe un papel inmunorregulador que deprima la respuesta inmunológica de la madre.
Anticuerpos de bloqueo[editar]
En la sangre de las mujeres multigrávidas se puede detectar una proteína ausente en las abortadoras crónicas que ha sido motivo de mucho estudio y análisis, y ha servido de base a la hipótesis de la tolerancia al tejido placentario. Igualmente es frecuente detectar anticuerpos que bloquean algunos receptores de los trofoblastos.
Parece, por lo tanto, que la tolerancia al embarazo se debe primordialmente a un proceso activo del sistema inmune del feto, reforzado por algún sistema de inmunosupresión de la madre y un mecanismo de facilitación inmunológica, producido por anticuerpos de bloqueo, y la actividad hormonal que disminuye la respuesta inmunológica de rechazo a nivel de la placenta.
La supervivencia del feto en los embarazos ectópicos está a favor de la existencia de mecanismos de tolerancia diferentes a la posible existencia de una barrera inmunológica localizada a nivel del útero.
En los sueros de multíparas es muy conocida la presencia de una serie de anticuerpos contra las proteínas fetales distintas de la madre. La obtención de sueros que permiten la tipificación de los antígenos de histocompatibilidad se logra la precisamente de mujeres multíparas. Luego, la presencia de anticuerpos está demostrando que existe una respuesta inmunológicamente de la madre contra las proteínas extrañas del feto pero que afortunadamente esta no es suficiente para producir un rechazo. La eritroblastosis fetal es otra demostración de la potencialidad reactiva del sistema inmunitario del a madre contra las proteínas del feto.
El feto tiene un sistema inmune, que pasados los primeros cuatro o cinco meses es capaz de responder a estímulos antigénicos. Si una infección materna pasa al feto, éste empieza a fabricar sus propios anticuerpos, no solo de la clase IgG sino también de la IgM. Por lo tanto, la presencia de esta clase de inmunoglobulinas en el cordón umbilical es una indicación de que durante la vida intrauterina el feto tuvo un proceso infeccioso bacteriano.
Pruebas de inmunodiagnóstico de embarazo[editar]
Las pruebas inmunológicas han remplazado a los otros procedimientos biológicos de diagnóstico de embarazo. La gonadotropina coriónica humana, inyectada en animales de laboratorio, induce la producción de anticuerpos específicos que sirven de base para las distintas pruebas inmunológicas de detección del embarazo.[cita requerida] Las pruebas más recientes de radioinmunoensayo tienen una gran sensibilidad, y en ocasiones permiten hacer el diagnóstico antes de que haya ocurrido la primera falla menstrual.[11]
Patología obstétrica[editar]
Aborto[editar]
Se estima que un 50% de las concepciones fallan por una u otra razón. El aborto espontáneo recurrente se debe en el 50% de los casos a aberraciones cromosómicas, alteraciones anatómicas o alteraciones hormonales. La mitad de los restantes se debe a anormalidades inmunológicas y el resto no tiene explicación satisfactoria.[12]
El aborto puede originarse por falta de la respuesta aloinmune normal en todo el embarazo, o por reacciones anormales en contra de granulocitos, plaquetas y otros componentes celulares.[13] Durante varios años se creyó que la inoculación de linfocitos del padre en la madre, lograba inducirla respuesta aloinmune necesaria y permitir embarazos normales. No obstante, meta-análisis recientes no logran confirmar la eficacia de este procedimiento.
Las reacciones inmunológicas responsables de abortos son de dos clases: anticuerpos antifosfolípidos[14] y reacciones autoinmunes. Los fosfolípidos de membrana del trofoblasto, son moléculas electronegativas esenciales en la adherencia del trofoblasto al endometrio. Los más comunes son cardiolipina, fosfatidil serina, fosfatidil inositol, fosfatidil etanolamina, fosfatidil glicerol y ácido fosfatídico.[8] Por razones no esclarecidas, la mujer puede desarrollar anticuerpos contra uno o varios de ellos, con lo que se compromete la adherencia de la placenta ocasionando infertilidad o abortos. Otro factor presente en la sangre materna es el anticoagulante lúpico, un anticuerpo dirigido contra la cardiolipina que interfiere con la coagulación in vitro y de ahí su nombre, por promover artificialmente el desarrollo de trombosis vasculares, especialmente frecuentes durante el embarazo y que por infartos de placenta, induce aborto.[15]
En otros casos se producen anticuerpo antinucleares, tipo antihistona, que reflejan una reacción autoinmune, que puede desencadenar un aborto.
La ausencia de una de las tres proteínas de membrana que protegen de la acción del complemento a las células normales, DAF (CD55), MCP (CD40) y CD59, permite que el complemento se active sobre la placenta y puede generar un aborto.[7][8]
Coriocarcinoma[editar]
Se trata de un tumor en el útero, rápidamente creciente, de origen placentario, que aparece después del embarazo o un aborto. Es un tipo de cáncer poco común y por lo general curable, aunque produce metástasis por vía vascular en el organismo materno.[16] Las metástasis que ocurren a nivel de pulmón son muy características dentro del cuadro clínico del coriocarcinoma. El tumor aparece como consecuencia de una alteración en la respuesta inmune madre-placenta, y parece caracterizarse por una tolerancia mayor a la que normalmente debería existir por parte de la madre hacia antígenos paternos del trofoblasto en el tejido placentario.[17] Estas pacientes muestran un retardo en el rechazo del trasplante a la piel del padre del bebé, lo que implica una inmunosupresión selectiva contra las proteínas paternas. La respuesta inmunológica contra los demás antígenos suele ser normal.
Este incremento en la tolerancia de la madre contra las proteínas originadas en el esposo, a través de un embarazo, explica el crecimiento sin control del tejido trofoblástico, primero a nivel uterino y posteriormente en forma sistémica.
Eclampsia[editar]
Se trata de un cuadro clínico complejo, caracterizado por la aparición de convulsiones durante el embarazo, en el cual parece que hay en el sistema inmune anormalidades que pueden desempeñar un papel importante en el desarrollo del síndrome. Adicionalmente, los genes de la persona, su circulación sanguínea y factores neurológicos puede que sean de importancia en el desarrollo del trastorno.[18] Los complejos inmunes formados por anticuerpos producidos por la madre contra antígenos placentarios, pueden precipitarse a nivel de la placenta y activar el complemento, evidenciado por la pronta resolución de la enfermedad al inducir el parto.[19] Este proceso inflamatorio local produce un daño en el endotelio vascular, con el desencadenamiento de trombosis y la formación de zonas isquémicas dentro de la placenta, que pueden convertirse en verdaderos infartos placentarios. De estas zonas se desprenden émbolos trofoblásticos que entran en la circulación materna.[20] Por otra parte, cierta inmunidad cruzada entre antígenos placentarios y antígenos renales puede dar lugar a daño renal, responsable de la proteinuria y de la hipertensión arterial, características de la ecplampsia.[19]
Durante las relaciones sexuales previas a un embarazo, las proteínas de los grupos HLA presentes en células epiteliales amnióticas,[21] diferentes a los de la madre, desencadenan la producción de anticuerpos de bloqueo que inducen tolerancia hacia las proteínas del padre, con anterioridad al embarazo.[22] La impresión clínica es que la eclampsia se presenta con mayor frecuencia en aquellas mujeres en las cuales el embarazo ocurre rápidamente después de los primeros contactos sexuales con el padre del bebé, sin que haya habido tiempo suficiente para la inducción de anticuerpos de bloqueo.[23] Otros factores de riesgo de contraer la enfermedad son: ser primigrávida, edad materna en los extremos bajos y altos, previa hipertensión, diabetes, y una historia familiar de preeclampsia.[24]
Cuando se presenta en embarazos posteriores, obedece por lo general a embarazos originados dentro de un segundo matrimonio, donde, nuevamente, la falta de “sensibilización” previa a las proteínas del sistema HLA seminal del nuevo esposo, puede dar lugar al desencadenamiento de una respuesta con formación de complejos inmunes a nivel placentario.[25]
Alimentación al pecho[editar]

La leche materna proporciona al niño todos los componentes esenciales desde el punto de vista calórico, proteico y vitanímico; pero además, y en forma muy especial, es rica en células y en componentes específicos de defensa. El calostro tiene un gran contenido en linfocitos, PMNs y macrófagos, células que decrecen en cantidad durante las dos primeras semanas, permaneciendo en niveles bajos durante toda la lactancia. El calostro tiene de 10 a 100 millones de leucocitos por mm³, en tanto que la leche tiene 100.000 por mm³.
Gracias a la permeabilidad de la mucosa intestinal del niño, durante las primeras semanas de vida, estos linfocitos pueden entrar en su circulación y como han sido programados en la madre, cumplir funciones especiales de defensa. Los fagocitos que llegan en el calostro y en la leche lo defenderán a nivel digestivo de muchas de las bacterias que le lleguen vía oral. La defensa del niño recién nacido contra bacterias como estreptococo, eumococo u enterobacterias, se debe en gran parte a la cantidad de anticuerpos tipos IgA e IgG que existen en el calostro. La leche es igualmente rica en anticuerpos IgA, pero muy pobre IgG. Por lo tanto, el calostro parece dar un aporte de defensa mediado por anticuerpos, que resulta invaluable en las primeras horas de la vida del niño. En el calostro, pasan de la madre al niño de cinco a seis gramos de IgA en las primeras 24 horas y, en la leche, de uno a dos gramos diarios. Esta IgA protege no solo contra infecciones a nivel digestivo sino también respiratorio y urinario.
La leche materna tiene una alta concentración de moléculas solubles de CD14, que hace parte de los mecanismos de inmunidad innata y que protegen al niño de las endotoxinas producidas por bacterias Gram negativos.
Entre elementos no específicos que llegan al calostro y leche están: factores del complemento, que complementan la acción de los Acs; monosacáridos, que pueden bloquear receptores de bacterias impidiendo su adherencia a l as mucosas; ácidos grasos, que son bactericidas, lactoferrina, que fija el hierro impidiendo que las bacterias puedan utilizarlo; lisozima, que es bactericida, y factores antioxidantes.
Los estudios prospectivos han demostrado, sin lugar a dudas, que la morbilidad, en cuanto a enfermedades infecciosas se refiere, es muchas veces mayor en niños alimentados artificialmente si se compara con los alimentados al pecho. Por otra parte, la presenciade estos anticuerpos en el calostro y en la leche parece ser un mecanismo de defensa o protección contra el eventual desarrollo de enfermedades alérgicas, especialmente las producidas por alimentos. Así, los hijos de madres que los alimentan al pecho, muestran una menos incidencia de enfermedades alérgicas de todo tipo y especialmente de las gastrointestinales.
En la población normal de niños alimentados al pecho, la incidencia de eczema es de 11%, del asma alérgica el 3% y la presencia de Acs contra la lactoferrina se da en el 8%. En cambio, en aquellos niños sometidos a alimentación artificial, la incidencia de eczema alcanza el 57%, el asma al 22% y los anticuerpos contra la lactoferrina alcanza al 84%.
Esta cifra denota claramente la importancia de la alimentación al pecho, como protectora del eventual desarrollo de enfermedades alérgicas.
Lactancia en sida[editar]

Cada año, más de 700.000 niños se infectan con VIH de madres con sida, durante el embarazo o el parto. Adicionalmente, una tercera parte de los niños infectados por sus progenitoras lo hacen a través del calostro, que es muy rico en linfocitos.[26] Es aconsejable que niños VIH negativos no sean alimentados por madres VIH positivas.
Otros factores de defensa presentes en la leche materna lactoferrina, lactoperoxidasa, lisozima y algunos lípidos constituyen factores no específicos de defensa igualmente contra infecciones virales.
Referencias[editar]
- ↑ “Frequently Asked Questions About Infertility” (2006). American Society for Reproductive Medicine.
- ↑ a b VIVAS-A, Giovanny, LOZANO-H, Jesús e VELASCO, Judith. Regulación inmuno-testicular y citocinas. Invest. clín. [online]. mar. 2007, vol.48, no.1 [citado 15 Dezembro 2007], p.107-121. Disponível na World Wide Web: [1]. ISSN 0535-5133.
- ↑ 20 minutos (15 de noviembre de 2006). «La alergia al semen que padecen algunas mujeres podría tener cura con una nueva terapia». Consultado el 15 de diciembre de 2007. «Son pocas las que la sufren, pero la alergia al semen es una dolencia que le puede arruinar las relaciones de pareja a una mujer. Muchas confunden sus síntomas (desde picores hasta un potencialmente mortal choque anafiláctico) con enfermedades de trasmisión sexual.»
- ↑ Mayo Foundation for Medical Education and Research (1 de febrero de 2007). «Controlar la menopausia de aparición precoz». Consultado el 17 de diciembre de 2007. «Aproximadamente el uno por ciento de mujeres estadounidenses presentan insuficiencia ovárica prematura, y la edad promedio de aparición es de 27 años.»
- ↑ Manual Merck - Capítulo 235: Problemas de Salud de la Mujer (2005). «Hemorragia uterina ausente o anormal». Archivado desde el original el 9 de diciembre de 2007. Consultado el 13 de diciembre de 2007. «La menopausia prematura (precoz) es un trastorno en el que los ovarios dejan de funcionar y la menstruación cesa antes de los 40 años. En la menopausia prematura, los valores de estrógenos son bajos. Sin embargo, la concentración de las hormonas hipofisarias que estimulan los ovarios (gonadotropinas), sobre todo la hormona foliculoestimulante, son altos porque intentan estimular los ovarios.»
- ↑ Indian Journal of Medical Ethics. «Investigación sobre vacunas anti-fertilidad». Métodos anticonceptivos. Consultado el 15 de diciembre de 2007.
- ↑ a b c Carmen Torres. Inmunología del embarazo. Ginecol Obstet. (Perú) 1997; 43 (2):93-5. Citado el 17 de diciembre de 2007. [2]
- ↑ a b c d e Melitza Iglesias, et al. Inmunología de la Reproducción. Acta Médica Colombiana. Número 3, volumen 27 (Mayo - Junio de 2002). Citado 17 de diciembre de 2007. Disponible en la World Wide Web: [3] Archivado el 23 de julio de 2007 en Wayback Machine.
- ↑ RODRIGUEZ CHALA, Hilda Elia y LOPEZ SANTANA, Melvis. El embarazo: Su relación con la salud bucal. Rev Cubana Estomatol. [online]. Mayo-ago. 2003, vol.40, no.2 [citado 25 diciembre de 2007], p.0-0. Disponible en la World Wide Web: [4]. ISSN 0034-7507.
- ↑ BARRERA, David, AVILA, Euclides y DIAZ, Lorenza. Papel inmunitario de la progesterona en el mantenimiento del embarazo. Rev. invest. clín. [online]. 2007, vol. 59, no. 2 [citado 2007-12-25], pp. 139-145. Disponible en: <http://scielo.unam.mx/scielo.php?script=sci_arttext&pid=S0034-83762007000200008&lng=es&nrm=iso>. ISSN 0034-8376.
- ↑ Allen J. Wilcox, Donna Day Baird, Clarice R. Weinberg. Time of Implantation of the Conceptus and Loss of Pregnancy. N Engl J Med. 1999 Jun 10;340(23):1796-9. [5]
- ↑ Medlineplus (mayo de 2005). «Aborto espontáneo». Enciclopedia médica en español. Consultado el 17 de diciembre de 2007. «Se estima que hasta un 50% del total de los óvulos fecundados mueren y se pierden (son abortados) en forma espontánea, usualmente antes de que la mujer se percate de que está embarazada. Entre los embarazos conocidos, la tasa de aborto espontáneo es alrededor del 10% y generalmente se presenta entre las 7 y las 12 semanas de embarazo.»
- ↑ ALFONSO VALDES, María Elena, EDUARDO, Muñiz, BENCOMO HERNANDEZ, Antonio et al. Alloimmunization against blood cells in the first trimester of pregnancy. Rev Cubana Hematol Inmunol Hemoter. [online]. May-Aug. 2006, vol.22, no.2 [citado 17 de diciembre de 2007], p.0-0. Disponible en la World Wide Web: [6]. ISSN 0864-0289.
- ↑ CERVERA MIGUEL, J. I., NAVARRO IBANEZ, V., CALABUIG MUNOZ, E. et al. Síndrome antifosfolípido: Utilidad de la ecocardiografía transesofágica. An. Med. Interna (Madrid). [online]. 2003, vol. 20, no. 10 [citado 2007-12-17], pp. 40-41. Disponible en: [7]. ISSN 0212-7199.
- ↑ Empson M, Lassere M, Craig J, Scott J. Prevención del aborto espontáneo recurrente en mujeres con anticuerpos antifosfolípidos o anticoagulante lúpico (Revisión Cochrane traducida). En: La Biblioteca Cochrane Plus, número 4, 2007. Oxford, Update Software Ltd. Disponible en: [8]. (Traducida de The Cochrane Library, 2007 Issue 4. Chichester, UK: John Wiley & Sons, Ltd.).
- ↑ MedlinePlus (noviembre de 2007). «Enfermedad trofoblástica gestacional». Enciclopedia médica en español. Consultado el 17 de diciembre de 2007. «Es una forma de cáncer rápidamente creciente que ocurre en el útero después de un embarazo, un aborto espontáneo o un aborto provocado. Esta afección usualmente hace metástasis, lo que significa que se disemina a otros lugares en el cuerpo. El coriocarcinoma sigue siendo un tipo de cáncer poco común, aunque casi siempre curable, que puede estar asociado con el embarazo.»
- ↑ José María Ezpeleta, Alfredo López Cousillas. Enfermedad trofoblástica gestacional. Aspectos clínicos y morfológicos. Revista Española de Patología. Vol. 35, n.º 2, 2002. [9]
- ↑ Medline Plus (mayo de 2005). «Eclampsia». Enciclopedia médica en español. Consultado el 17 de diciembre de 2007. «Aún no se comprenden bien las causas de la eclampsia. Los investigadores creen que los genes de una persona, la dieta, los vasos sanguíneos y factores neurológicos pueden jugar un papel en su manifestación; sin embargo, aún no se ha comprobado ninguna teoría.»
- ↑ a b Stephanie R Fugate; Gregory E Chow (5 de octubre de 2005). «Eclampsia» (en inglés). eMedicine.com. Consultado el 17 de diciembre de 2007.
- ↑ Amit Sengupta: «Preeclampsia y la dificultad de medir el flujo uteroplacentario - El intento de una mirada profunda». Archivado el 28 de diciembre de 2007 en Wayback Machine. Consultado el 17 de diciembre de 2007.
- ↑ Gert Datema, Claudia A. van Meir, Humphrey H. H. Kanhai, Peter J. van den Elsen. Pre-term Birth and Severe Pre-eclampsia are not Associated with Altered Expression of HLA on Human Trophoblasts. American Journal of Reproductive Immunology. Volume 49 Issue 4 Page 193-201, April 2003. [10]
- ↑ D M Jenkins, J Need, and S M Kajah. Deficienty of specific HLA antibodies in severe pregnancy pre-eclampsia/eclampsia. Clin Exp Immunol. 1977 March; 27(3): 485–486. Citado 17 de diciembre de 2007. [11]
- ↑ Einarsson, Jon I. MD; Sangi-Haghpeykar, Haleh PhD; Gardner, Michael O. MD, MPH (2003). «Sperm exposure and development of preeclampsia». Journal of Obstetrics and Gynecology 188 (5): 1241-1243.
- ↑ Stephen C Morris; Michael B Brooks (28 de septiembre de 2006). «Pregnancy, Eclampsia» (en inglés). eMedicine.com. Consultado el 17 de diciembre de 2007.
- ↑ Sex Primes Women for Sperm. BBC News. 2002-02-06. Consultado el 19 de noviembre de 2007.
- ↑ UNICEF (2002). «Prevención de la transmisión de VIH/SIDA de progenitores a hijos». VIH/SIDA y la infancia. Archivado desde el original el 14 de diciembre de 2007. Consultado el 15 de diciembre de 2007.
