Aparato de Golgi


3 Retículo endoplasmático rugoso (RER). 4 Retículo endoplasmático liso (REL). 7 Vesícula transportadora. 8 Aparato de Golgi (AG). 9 Cara-Cis del AG. 10 Cara-Trans del AG. 11 Cisterna de AG. 12 Vesícula secretora.
El complejo de Golgi o aparato de Golgi[1]
es un orgánulo presente en todas las células eucariotas que forma parte del sistema de endomembranas. El Golgi está formado principalmente por 4-6 sáculos aplanados o cisternas (dictiosomas) que se encuentran apilados unos encima de otros, y cuya función es completar el procesamiento y eventual secreción de algunas macromoléculas.[2] Funciona como una planta empaquetadora, modificando vesículas del retículo endoplasmático rugoso, el material nuevo de las membranas se forma en varias cisternas del aparato de Golgi.
Dentro de las funciones que posee el aparato de Golgi se encuentran la glucosilación de proteínas, selección, destinación y glucosilación de lípidos, y la síntesis de polisacáridos de la matriz extracelular. Almacenamiento y distribución de lisosomas, al igual que los peroxisomas, que son vesículas de secreción de sustancias.[3]
El aparato de Golgi de las células de mamíferos, también contribuye a la regulación de numerosos procesos en la célula incluyendo: la mitosis, la reparación del ADN, las respuestas al estrés, la autofagia, la apoptosis y la inflamación.[4]
Historia
[editar]El aparato fue descrito en gran detalle por el científico italiano Camillo Golgi en 1889, como aparato reticular interno en células de Purkinje del cerebelo de búho, mediante una tinción llamada reazione nera.[5]
Fuera de Italia fue observado luego por otros investigadores: Holmgrem, Retzius, Kopsch, Misch, Bergen y Weigl.
Desde 1903 Cajal utilizaba su método del nitrato de plata reducido, con el cual consiguió impregnar el aparato reticular de los invertebrados y el de algunas células epiteliales de los mamíferos jóvenes.
Con el empleo del reactivo de nitrato de urano, consigue corrientemente la coloración en todos los tejidos.
A continuación, Golgi modificó la fórmula argéntica con la adición del ácido arsenioso como fijador y la reacción parda consecuente recaía entonces en las trabéculas de dicho aparato.[6]
En 1913 Cajal lo nombra en sus trabajos habitualmente como «el aparato de Golgi» por haber sido descrito por ese investigador.[5]
Camillo Golgi recibió el Premio Nobel de Medicina en 1906 junto a Santiago Ramón y Cajal.
Estructura
[editar]La morfología del complejo de Golgi (GC en inglés), es específica del tipo de célula y depende del estado de actividad de la misma.[7]
Arquitectura microscópica
[editar]
Con el microscopio óptico el aparato de Golgi no es visible en la célula sin teñir, debido a que su índice de refracción es similar al del citoplasma que lo circunda.[5]
El investigador Camillo Golgi desarrolló un método de tinción que se basa en una solución de plata, que pone en evidencia la estructura localizada y multicapa de este complejo. Se generan depósitos opacos intracelulares de sales argénticas, producto de la reacción entre el bicromato de potasio y el nitrato de plata llamada 'reacción negra'.[8][9]

El aparato de Golgi teñido, se muestra como una estructura morfológica densa, con forma algo cambiante y mal definida. Su forma varía mucho en diferentes tipos de células y en la misma célula dependiendo del estado de actividad de esta. Se ha descrito con microscopía óptica, como un retículo filamentoso o en forma de placa, una red de diversos grados de complejidad, una disposición de canales claros, vacuolas de tamaño variable y cuerpos en forma de media luna, copa o con forma de disco.[10]
Ultraestructura
[editar]


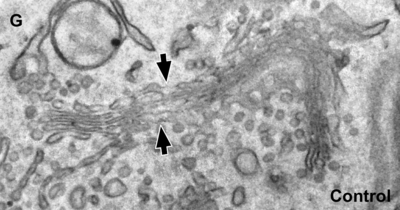
Con el microscopio electrónico se confirmó el concepto clásico del aparato de Golgi y se mostró claramente su naturaleza compleja.
El aspecto ultraestructural es de vacuolas de tamaño variable en forma de media luna, de copa o de disco.[10]
El aparato de Golgi es una estructura de membrana, y está compuesto por la agrupación estrecha de sáculos planos llamados cisternas y de túbulos.
La cisterna es la unidad básica del dictiosoma. Tiene forma discoidea y consta de una sola membrana continua de superficie lisa. Muestra una región central plana, denominada sáculo de 15-20 nm de espesor (lumen) y en sus extremos aumenta a 60-80 nm.[11]
La cisterna típica tiene un diámetro de 500-1000 nm y están separadas entre sí por una distancia de unos 15 nm.[12][7]
Estas cisternas se agrupan en número variable, en condiciones normales se observan desde 5-8 pilas hasta 60 dictiosomas en algunas especies.[13]
El número de cisternas por pila, el número de fenestraciones y la complejidad de los túbulos y vesículas asociados, son específicas del tipo de célula y dependen de su estado de actividad.[7]
Los invertebrados, las plantas y algunos hongos, tienen pilas de Golgi individuales o en pares, distribuidas por el citoplasma.
Las células de los vertebrados contienen una cinta de Golgi, que consta de numerosas pilas de cisternas, conectadas por redes tubulares, conformando un orgánulo único.[14]
- Plantas
Hay numerosas estructuras similares a los dictiosomas del Golgi, son más pequeñas, poco desarrolladas, o bien cisternas individuales y dispersas por el citoplasma, su número puede variar entre decenas y cien.[12] Cada dictiosoma presenta una pila de 5-7 cisternas.[15]
En algunos flagelados unicelulares como Euglena, se pueden combinar desde 12 hasta 60 cisternas para formar el aparato de Golgi. E. pailasensis tiene varios apilamientos distribuidos, con una longitud de 0,5-1, 0 milímetros (mm) cada uno.[16]
- Animales
Las células animales generalmente contienen entre diez y veinte pilas de Golgi por célula.[17] Las cisternas presentan conexiones tubulares que permiten el paso de sustancias entre las cisternas. Los sáculos son aplanados y curvados, con su cara convexa (cis) orientada hacia el retículo endoplasmático y el núcleo.[18] Alrededor de la cisterna principal se disponen las vesículas esféricas recién exocitadas.
Los invertebrados tienen pilas de Golgi individuales o en pares, distribuidas por el citoplasma, cerca del retículo endoplasmático (ER) y los sitios de salida del ER (ERES).
Los vertebrados muestran el mayor nivel de complejidad, ya que contienen una cinta de Golgi, que consta de numerosas pilas de cisternas, conectadas por redes tubulares no compactas, conformando así un orgánulo único.[14]
Regiones del Golgi
[editar]


El aparato de Golgi se puede dividir en tres regiones funcionales: cis, intermedia y trans.
Región cis-Golgi
[editar]La región cis-Golgi es la más interna y próxima al retículo endoplásmico. Las cisternas cis-Golgi, reciben las vesículas de transición, que son sáculos con proteínas, que han sido sintetizadas en la membrana del retículo rugoso (RER), introducidas en sus cavidades y transportadas por el lumen hasta la parte más externa del retículo.
Región medial o intermedia
[editar]La Región medial o intermedia es una zona de transición, con cisternas de número y volumen variable.
Región trans-Golgi
[editar]La región trans-Golgi es la que se encuentra más cerca de la membrana plasmática, más alejada del RER.[3][19]
Las vesículas provenientes del retículo endoplásmico se fusionan con el cis-Golgi, atravesando todos los dictiosomas hasta el trans-Golgi, donde son empaquetadas y enviadas al lugar que les corresponda. Cada una de estas tres regiones contiene diferentes enzimas, que modifican selectivamente las vesículas según donde estén destinadas.[20][21]
Funciones
[editar]El aparato de Golgi se encarga de la modificación, distribución y envío de un gran número de macromoléculas, sintetizadas en la célula, necesarias para la vida. Modifica proteínas y lípidos (grasas) que han sido sintetizados previamente tanto en el retículo endoplasmático rugoso como en el retículo endoplasmático liso y los «etiqueta» para enviarlos donde corresponda, fuera o dentro de la célula.
El aparato de Golgi de las células de mamíferos contribuye a la regulación de una variedad de procesos celulares, incluida la mitosis, la reparación del ADN, las respuestas al estrés, la autofagia, la apoptosis y la inflamación.[4]
Algunas de las principales funciones del aparato de Golgi son las siguientes:
- Modificación de sustancias sintetizadas en el RER: En el aparato de Golgi se transforman las sustancias procedentes del RER.[3]
Estas transformaciones pueden ser agregaciones de restos de carbohidratos para conseguir la estructura definitiva o para ser proteolizados y así adquirir su conformación activa. Por ejemplo, en el RER de las células de los islotes del páncreas se sintetiza la proinsulina que debido a las transformaciones que sufre en el aparato de Golgi, adquirirá la forma o conformación definitiva de la insulina. Las enzimas que se encuentran en el interior de los dictiosomas son capaces de modificar las macromoléculas mediante glicosilación (adición de carbohidratos) y fosforilación (adición de fosfatos). Para ello, el aparato de Golgi transporta ciertas sustancias como nucleótidos y azúcares al interior del orgánulo desde el citoplasma. Las proteínas también son marcadas con secuencias señal que determinan su destino final, como por ejemplo, la manosa-6-fosfato que se añade a las proteínas destinadas a los lisosomas. Para llevar a cabo el proceso de fosforilación el aparato de Golgi importa moléculas de ATP al interior del lumen,[22] donde las kinasas catalizan la reacción. Algunas de las moléculas fosforiladas en el aparato de Golgi son las apolipoproteínas que dan lugar a las conocidas VLDL que se encuentran en el plasma sanguíneo. Parece ser que la fosforilación de estas moléculas es necesaria para favorecer la secreción de las mismas al torrente sanguíneo.[23]
- Metales pesados: En las células de los vertebrados las metalotioneínas (MT) tiene la capacidad de unirse a metales pesados tanto fisiológicos (zinc y cobre) como xenobióticos (como cadmio, mercurio, aluminio y plata), a través de los grupos tiol (-SH) de sus residuos de cisteína, que representan casi el 30% de aminoácidos.[24]
- Secreción celular: Las sustancias atraviesan todos los sáculos del aparato de Golgi y cuando llegan a la cara trans del dictiosoma, en forma de vesículas de secreción, son transportadas a su destino fuera de la célula, atravesando la membrana citoplasmática por exocitosis. Un ejemplo de esto son los proteoglicanos que conforman la matriz extracelular de los animales. El aparato de Golgi es el orgánulo de mayor síntesis de carbohidratos.[25] Esto incluye la producción de glicosaminoglicanos (GAGs), largos polisacáridos que son anclados a las proteínas sintetizadas en el RE para dar lugar a los proteoglicanos. De esto se encargarán las enzimas del Golgi por medio de un residuo de xilosa. Otra forma de marcar una proteína puede ser por medio de la sulfatación de una sulfotransferasa, que gana una molécula de azufre de un donador denominado PAPS. Este proceso tiene lugar en los GAGs de los proteoglicanos así como en los núcleos de las proteínas. Este nivel de sulfatación es muy importante para los proteoglicanos etiquetando funciones y dando una carga neta negativa al proteoglicano.[25]
- Producción de membrana plasmática: Los gránulos de secreción cuando se unen a la membrana en la exocitosis pasan a formar parte de esta, aumentando el volumen y la superficie de la célula.
- Formación de los lisosomas primarios.
- Formación del acrosoma de los espermios.
Vesículas de transporte
[editar]Las vesículas generadas en el retículo endoplasmático liso forman, uniéndose entre ellas, agregados tubulo-vesiculares, los cuales son transportados hasta la región Cis-Golgi (CGN) por proteínas motoras guiadas por microtúbulos donde se fusionan con la membrana de este, vaciando su contenido en el interior del lumen. Una vez dentro, las moléculas son modificadas, marcadas y dirigidas hacia su destino final.[26]
El aparato de Golgi tiende a ser mayor y más numeroso en aquellas células que sintetizan y secretan continuamente sustancias, como pueden ser los linfocitos B y las células secretoras de anticuerpos.
Aquellas proteínas destinadas a zonas alejadas del aparato de Golgi son desplazadas hacia la región trans, internándose en una compleja red de membranas y vesículas asociadas denominadas región Trans-Golgi (TGN).[20] Esta región es donde muchas proteínas son marcadas y enviadas hacia sus correspondientes destinos por medio de alguno de estos 3 tipos diferentes de vesículas, según el marcador que presenten:[20]
| Tipo | Descripción | Ejemplo |
| Vesículas de exocitosis (constitutivas) |
Este tipo de vesículas contienen proteínas que deben ser liberadas al medio extracelular. Después de internalizarse las proteínas, la vesícula se cierra y se dirige inmediatamente hacia la membrana plasmática, con la que se fusiona, liberando así su contenido al medio extracelular. Este proceso es denominado secreción constitutiva. | Los anticuerpos liberados por linfocitos B activados. |
| Vesículas de secreción (reguladas) |
Este tipo de vesículas contienen también proteínas destinadas a ser liberadas al medio extracelular. Sin embargo, en este caso, la formación de las vesículas va seguida de su almacenamiento en la célula, donde se mantendrán a la espera de su correspondiente señal para activarse. Cuando esto ocurre, se dirigen hacia la membrana plasmática y liberan su contenido como en el caso anterior. Este proceso es secreción regulada. | Liberación de neurotransmisores desde las neuronas. |
| Vesículas lisosomales | Este tipo de vesículas transportan proteínas destinadas a los lisosomas, unos pequeños orgánulos de degradación en cuyo interior albergan multitud de hidrolasas ácidas, lisosomas de almacenamiento. Estas proteínas pueden ser tanto enzimas digestivas como proteínas de membrana. La vesícula se fusiona con un endosoma tardío y transfiere así su contenido al lisosoma por mecanismos aún desconocidos. | Proteasas digestivas destinadas a los lisosomas. |
Mecanismo de transporte
[editar]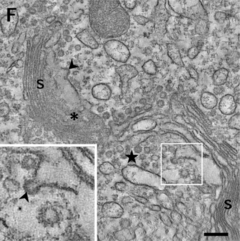
Los mecanismos de transporte que utilizan las proteínas para trasladarse a través del aparato de Golgi no estaban claros en 1994, por lo que existen diversas hipótesis para explicar dicho desplazamiento.[27]
Se plantean dos modelos predominantes que no son excluyentes entre sí, hasta el punto de ser referidos a veces como el modelo combinado:
- Modelo de maduración de las cisternas: las cisternas del aparato de Golgi llevan a cabo un movimiento unidireccional desde la región cis, donde se forman, hasta la región trans, donde son destruidas. Las vesículas del retículo endoplasmático se fusionan con los dictiosomas de la región cis para dar lugar a nuevas cisternas, lo que podría generar el movimiento de las cisternas a través del aparato de Golgi a medida que se van formando nuevas cisternas en la región cis. Este modelo se apoya en el hecho de que se han observado al microscopio estructuras mayores que las vesículas de transporte, tales como las fibras de colágeno, desplazándose a través del aparato de Golgi.[25][28] Además, existen evidencias de movimientos retrógrados (en dirección cis) de cierto tipo de vesículas (COP1), que transportan proteínas del retículo endoplasmático mediante el reconocimiento de péptidos señales.[29]

- Modelo del transporte vesicular: el transporte vesicular asume que el aparato de Golgi es un orgánulo muy estable y estático, dividido en compartimentos que se disponen en dirección cis → trans. Las vesículas son las encargadas de transportar el material entre el retículo endoplasmático y el aparato de Golgi y entre los diferentes compartimentos de este.[30] Las evidencias experimentales que apoyan esta hipótesis se basan en la gran abundancia de vesículas pequeñas (conocidas técnicamente como vesículas lanzadera) localizadas en las proximidades del aparato de Golgi. La direccionalidad vendría dada por las proteínas trasportadas en el interior de las vesículas, cuyo destino determinaría el movimiento de avance o de retroceso a través del aparato de Golgi, aunque también podría suceder que la direccionalidad no fuera necesaria y el destino de las proteínas viniera ya determinado desde el retículo endoplasmático. Al margen de esto, es probable que el transporte de vesículas se encuentre asociado al citoesqueleto por medio de filamentos de actina, encargados de asegurar la fusión de las vesículas con sus correspondientes compartimentos.[25]
Véase también
[editar]Sinónimos
[editar]Referencias
[editar]- ↑ OMS, OPS (ed.). «Aparato de Golgi». Descriptores en Ciencias de la Salud, Biblioteca virtual de salud.
- ↑ Cerezo García, Miguel (1 de marzo de 2013). Fundamentos de biología básica.. Publicacions de la Universitat Jaume I. ISBN 9788480218948. Consultado el 7 de febrero de 2018.
- ↑ a b c Welsch, Ulrich (2008). Histología Sobotta (2a. edición). Médica Panamericana. ISBN 9788498351781. Consultado el 7 de febrero de 2018.
- ↑ a b Kulkarni-Gosavi P.; Makhoul C.; Gleeson P.A. (2019). «Form and function of the Golgi apparatus: scaffolds, cytoskeleton and signaling». Epub (Revisión) (FEBS). doi:10.1002/1873-3468.13567. Consultado el 10 de agosto de 2021.

- ↑ a b c Jiménez L.F; Merchant H. (2003). «Reseña histórica y función del aparato de Golgi». Biología Celular y Molecular. Pearson Educación. p. 445. ISBN 9789702603870. Consultado el 7 de febrero de 2018.
- ↑ Cajal S. (1913). XXV: Continúa la exposición de los trabajos de 1912 a 1917. Algunos métodos nuevos de investigación: el del formol-urano para la coloración del aparato endocelular de Golgi. «Recuerdos de mi vida». Instituto Cervantes.
- ↑ a b c Martínez-Alonso E.; Tomás M.; Martínez-Menárguez J.A. (2013). «Morpho-functional architecture of the Golgi complex of neuroendocrine cells». Front. Endocrinol. (Revisión). Neuroendocrine science. doi:10.3389/fendo.2013.00041. Consultado el 11 de agosto de 2021.

- ↑ Torres-Fernández O. (2006). «La técnica de impregnación argéntica de Golgi. Conmemoración del centenario del premio nobel de Medicina (1906) compartido por Camillo Golgi y Santiago Ramón y Cajal». Biomédica (Bogotá) 26 (4).
- ↑ Grant G. (oct de 2007). «How the 1906 Nobel Prize in Physiology or Medicine was shared between Golgi and Cajal». Brain Res Rev 55 (2): 490-498. PMID 17306375. doi:10.1016/j.brainresrev.2006.11.004.
- ↑ a b Beams H.W.; Kessel R.G. (1968). «The Golgi Apparatus: Structure and Function». International Review of Cytology 23: 209-276. Consultado el 5 de agosto de 2021.
- ↑ «Tema 12: Aparato de Golgi.». Organización general de las células (PDF). Universidad Miguel Hernández. p. 1.
- ↑ a b Megías M.; Molist P.; Pombal MA. (2019). «5:Tráfico vesicular. Aparato de Golgi». Atlas de histología vegetal y animal. La célula.
- ↑ «Molecular Expressions Cell Biology: The Golgi Apparatus». Archivado desde el original el 7 de noviembre de 2006. Consultado el 8 de noviembre de 2006.
- ↑ a b Saraste J.; Prydz K. (2019). «A New Look at the Functional Organization of the Golgi Ribbon». Front. Cell Dev. Biol. doi:10.3389/fcell.2019.00171. Consultado el 13 de agosto de 2021.
- ↑ Roshchina V.V.; Roshchina V.D. (2012). «1:Cellular aspects of secretory activity in plants». The Excretory Function of Higher Plants. Springer Science & Business Media. p. 8.
- ↑ Sánchez E.; Vargas M.; Mora M.; Ortega J.M.; Serrano A.; Freer E.; Sittenfeld A. (2004). «Descripción ultraestructural de Euglena pailasensis (Euglenozoa) del Volcán Rincón de la Vieja, Guanacaste, Costa Rica». Rev. biol. trop 52 (1).
- ↑ «El aparato de Golgi.». Molecular Expressions. Florida State University.
- ↑ Jiménez (2006). Conocimientos Fundamentales de Biologia. vol.I. Pearson Educación. p. 79.
- ↑ Cediel, Juan Fernando; Cárdenas, María Helena; García, Ananías (2009). Manual de histología: Tejidos fundamentales. Bogotá, Colombia: Universidad del Rosario. ISBN 9789588378893. Consultado el 7 de febrero de 2018.
- ↑ a b c Lodish; et al. (2004). Molecular Cell Biology (5a. edición). W.H. Freeman and Company. P0-7167-4366-3.
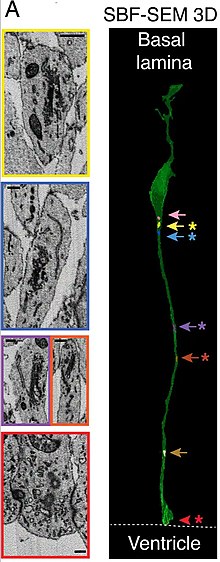
- ↑ Taverna E.; Mora-Bermúdez F.; Strzyz P.J.; Florido M.; Icha J.; Haffner C.; Norden C., Wilsch-Bräuninger M., Huttner W.B. (2016). «Non-canonical features of the Golgi apparatus in bipolar epithelial neural stem cells». Scientific Reports 6 (21206). Consultado el 2020.

- ↑ Capasso, J., et al., «Mechanism of phosphorylation in the lumen of the Golgi apparatus. Translocation of adenosine 5'-triphosphate into Golgi vesicles from rat liver and mammary gland.» Journal of Biological Chemistry, 1989. 264(9): pp. 5233-5240.
- ↑ Swift, L. L., «Role of the Golgi Apparatus in the Phosphorylation of Apolipoprotein B.» Journal of Biological Chemistry, 1996. 271(49): pp. 31491-31495.
- ↑ Sigel, A.; Sigel, H.; Sigel, R.K.O., ed. (2009). Metallothioneins and Related Chelators. Metal Ions in Life Sciences 5. Cambridge: RSC Publishing. ISBN 978-1-84755-899-2.
- ↑ a b c d Alberts, Bruce; et al. (1994). Molecular Biology of the Cell (3a. edición). Garland Publishing.
- ↑ «Un viaje en tren por el interior de la célula: el Aparato de Golgi». Ciencias Biológicas. Ciencia al Día Internacional. Ciencias Biológicas. 2001.
- ↑ Bruce Alberts; Dennis Bray; Karen Hopkin; Alexander Johnson; Julian Lewis; Martin Raff; Keith Roberts; Peter Walter (2006). «15:Compartimientos y transporte intracelular. Vías secretorias.». Introducción a la biología celular. Médica Panamericana. p. 519.
- ↑ Glick B.S.; Malhotra V. (1998). Articles «The curious status of the Golgi apparatus». Cell 95: 883-889.
- ↑ Pelham, H. R. B. y J. E. Rothman, «The Debate about Transport in the Golgi - Two Sides of the Same Coin?» Cell, 2000. 102: pp. 713-719.
- ↑ Glick, B. S., «Organisation of the Golgi apparatus.» Current Opinión in Cell Biology, 2000. 12: pp. 450-456.
Enlaces externos
[editar]- Galería de Imágenes 3D de microscopía electrónica de barrido SEM. Universidad de Keele.
- Imágenes de microscopía electrónica de barrido SEM (1999).
- Imágenes 2D con el microscopio electrónico de transmisión (TEM). Universidad de Alcalá.
- Aparato de Golgi: Estructura y Función (en inglés). Universidad de Texas.
- Aparato de Golgi. (en inglés).
- Animación de dictiosoma
- Aparato de golgi: Significado, Función, Partes e Importancia