Bicapa lipídica


La bicapa lipídica es una delgada membrana polar formada por dos capas de moléculas de lípidos, estas membranas son láminas planas que forman una barrera continua alrededor de las células y sus estructuras. Las membranas celulares de todos los organismos celulares y algunos virus están compuestas por una bicapa lipídica, así como lo son las membranas que rodean el núcleo de la célula y otras estructuras subcelulares. La bicapa lipídica es la barrera que mantiene a iones, proteínas y otras moléculas donde se necesitan evitando su dispersión. Contiene nanómetros de espesor,[1] son impermeables a la mayoría de las moléculas solubles en agua (moléculas hidrofílicas), son impermeables a los iones permitiendo que las células regulen las concentraciones de sal y pH mediante el transporte de iones a través de sus membranas de proteínas llamadas bombas iónicas o canales iónicos.
Las bicapas biológicas están compuestas por fosfolípidos anfifílicos, tienen una cabeza fosfato hidrofílica y una cola hidrofóbica que consiste en dos cadenas de ácidos grasos. Los fosfolípidos con ciertos grupos en su cabeza pueden alterar la superficie química de una bicapa y pueden servir como señales "anclas" para otras moléculas en las membranas celulares.[2]
Así como las cabezas, las colas de los lípidos también pueden afectar las propiedades de la membrana que determina la fase de la bicapa. La bicapa puede adoptar un estado de fase de gel sólido a temperaturas bajas, pero se puede someter a una transición de fase de un estado fluido a temperaturas más altas, las propiedades químicas de las colas de los lípidos influencian a qué temperatura ocurre esto. El empaquetamiento de los lípidos dentro de la bicapa afecta a sus propiedades mecánicas, incluyendo la resistencia al estiramiento y flexión. Muchas de las propiedades han sido estudiadas con bicapas artificiales "modelo" producidas en un laboratorio. Las vesículas hechas por bicapas artificiales también se utilizan clínicamente para suministrar fármacos.
Las membranas biológicas incluyen a varios tipos de moléculas distintas de fosfolípidos, un ejemplo particularmente importante en células animales es el colesterol, ya que ayuda a fortalecer la bicapa disminuyendo su permeabilidad y regular la actividad de ciertas proteínas integrales de membrana. Proteínas integrales de la membrana funcionan cuando se incorporan en una bicapa lipídica, y están sujetas fuertemente a la bicapa lipídica con la ayuda de una cáscara de lípidos anular. Debido a que las bicapas definen los límites de la célula y sus compartimentos, estas proteínas de membrana están involucradas en muchos procesos de señalización intra e inter celulares. Ciertos tipos de proteínas de membrana están involucrados en procesos de fusión de dos bicapas. Esta fusión permite la unión de dos estructuras distintas como en la fertilización de un óvulo por el espermatozoide o la entrada de un virus en una célula. Debido a que las bicapas lipídicas son bastante frágiles e invisibles en un microscopio tradicional, es difícil estudiarlas es por esto que los experimentos requieren técnicas avanzadas como la microscopía electrónica y microscopía de fuerza atómica.
Estructura y organización[editar]
Cuando los fosfolípidos se exponen al agua, se auto-ensamblan en una lámina de dos capas con las colas hidrofóbicas apuntando hacia el centro de la lámina. Ésta disposición resulta en dos "hojuelas" que son una capa molecular individual, el centro de esta bicapa casi no contiene agua y excluye moléculas como azúcares o sales que se disuelven en agua. El proceso de montaje es conducido por las interacciones entre las moléculas hidrofóbicas (también llamado el efecto hidrofóbico), un aumento en las interacciones entre moléculas hidrofóbicas (que causa la agrupación de regiones hidrofóbicas) permite que las moléculas de agua se unan más libremente entre sí, aumentando la entropía del sistema. Este complejo proceso incluye las interacciones no covalentes, tales como Van der Waals, enlaces electrostáticos y puentes de hidrógeno.

Análisis de sección transversal[editar]
La bicapa lipídica es muy delgada en comparación con sus dimensiones laterales, si una célula típica de mamífero (diámetro ~ 10 micrómetros) se magnifica con el tamaño de una sandía (~ 1 pie / 30 cm), forma la membrana de plasma aproximadamente del tamaño de una hoja de papel de oficina. A pesar de ser solo unos pocos nanómetros de espesor, la bicapa se compone de regiones químicas a través de su sección transversal, estas regiones y sus interacciones con el agua circundante se caracterizan con reflectometría de rayos x,[4] dispersión de neutrones[5] y técnicas de resonancia magnética nuclear.
La primera región de ambos lados de la bicapa es el grupo de la cabeza hidrofílica, está completamente hidratada y tiene típicamente alrededor de 0.8-0.9 nm de espesor. En las bicapas de fosfolípidos, el grupo fosfato se encuentra dentro de la región hidratada, aproximadamente 0.5 nm fuera del núcleo hidrofóbico.[6] En algunos casos, la región hidratada puede extenderse mucho más, por ejemplo, en los lípidos con una proteína grande o una cadena larga de azúcar injertada en la cabeza. Un ejemplo común de tal modificación en la naturaleza es la capa de lipopolisacáridos en una membrana externa bacteriana,[7] que ayuda a retener una capa de agua alrededor de la bacteria para prevenir la deshidratación.
Junto a la región hidratada hay una región intermedia parcialmente hidratada, esta capa límite es de aproximadamente 0.3 nm de espesor. Dentro de esta corta distancia, la concentración de gotas de agua baja de 2M en el lado del grupo de la cabeza a casi cero en el lado de la cola (región intermedia).

.[8][9] La región intermedia hidrofóbica de la bicapa es típicamente de 3-4 nm de espesor, pero este valor varía con el largo de la cadena y la química.[4][10] El espesor de la región intermedia también varía significativamente con la temperatura, en particular en una transición de fase.[11]
Asimetría[editar]
La mayoría de las bicapas de origen natural tienen distintas composiciones de las capas de la membrana interior y exterior. En las células rojas humanas de la sangre, la capa interior (citoplásmica) está compuesta principalmente de fosfatidiletanolamina, fosfatidilserina y fosfatidilinositol y sus derivados fosforilados. Por el contrario, la capa exterior (extracelular) se basa en fosfatidilcolina, esfingomielina y glicolípidos.[12][13] En algunos casos, la asimetría está basada en dónde se crean los lípidos en la célula y refleja su orientación inicial.[14] Las funciones biológicas de la asimetría de los lípidos se diferencian imperfectamente, aunque está claro que se utilizan en situaciones diferentes. Por ejemplo, cuando una célula se somete a la apoptosis, la fosfatidilserina localizada en la capa citoplasmática se transfiere a la superficie exterior: Ahí, se reconoce por un macrófago que entonces neutraliza activamente la célula que muere.
La asimetría de lípidos surge de que la mayoría de los fosfolípidos son sintetizados e inicialmente insertados en la monocapa interna: los que constituyen la monocapa externa se transportan a continuación de la monocapa interna por una clase de enzimas llamadas flipasas.[15][16] Otros lípidos, tales como la esfingomielina, parecen ser sintetizados en la capa externa. Las flipasas son miembros de una familia de moléculas grandes transportadoras de lípidos que incluye flopasas que transfieren lípidos en la dirección opuesta, y escramblasas, que aleatorizan la distribución de lípidos a través de las bicapas de lípidos (como en células apoptóticas). En cualquier caso, una vez que se establece la asimetría de los lípidos, que normalmente no se disipan rápidamente porque el proceso espontáneo de flip-flop de los lípidos entre las hojas es extremadamente lento.[17]
Es posible imitar la asimetría en el laboratorio en sistemas de modelo de dos capas. Ciertos tipos de vesículas artificiales muy pequeñas automáticamente se hacen ligeramente asimétricas, aunque el mecanismo por el cual se genera esta asimetría es muy diferente de la de las células.[18]
Mediante la utilización de dos monocapas diferentes en la deposición de Langmuir-Blodgett[19] o una combinación de Langmuir-Blodgett y la deposición de la ruptura de vesículas[20] también es posible sintetizar una bicapa planar asimétrica. Esta asimetría puede perderse con el tiempo así como los lípidos en las bicapas soportadas pueden ser propensos al proceso de flip-flop.[21]
Fases y transiciones de fase[editar]

A una temperatura dada una bicapa lipídica puede existir en forma líquida o una fase de gel (sólido). Todos los lípidos tienen una temperatura característica a la que se transforma (derrite) de gel a fase líquida. En ambas fases se evita que las moléculas de lípidos pasen por el proceso de flip-flop través de la bicapa, pero en bicapas de fase líquida un lípido dado intercambiará lugares con su vecino millones de veces por segundo. Este intercambio de paseo aleatorio permite que los lípidos se difundan y por lo tanto paseen a través de la superficie de la membrana.[22] A diferencia de las bicapas en fase líquida, los lípidos en una bicapa de fase de gel se bloquean en su lugar.
El comportamiento de fase de las bicapas lipídicas se determina en gran parte por la fuerza de las interacciones atractivas de Van der Waals entre las moléculas lipídicas adyacentes. Los lípidos de mayor largo de cola tienen más área sobre la que interactuar, aumentando la fuerza de esta interacción y, como consecuencia, la disminución de la movilidad de los lípidos. Por lo tanto, a una temperatura dada, un lípido de cola corta será más fluido que un lípido idéntico de cola larga.[10]
La temperatura de transición también puede verse afectada por el grado de insaturación de las colas de lípidos. Un doble enlace insaturado puede producir un estrechamiento en la cadena del alcano, lo que altera el empaque de los lípidos. Esta interrupción crea un espacio libre extra dentro de la bicapa que permite una mayor flexibilidad en las cadenas adyacentes.[10] Un ejemplo de este efecto puede observarse en la vida cotidiana como la mantequilla, que tiene un gran porcentaje de grasas saturadas, es sólida a temperatura ambiente, mientras que el aceite vegetal, el cual es sobre todo insaturado, es líquido.
La mayoría de las membranas naturales son una mezcla compleja de diferentes moléculas de lípidos. Si algunos de los componentes son líquidos a una temperatura dada, mientras que otros están en la fase de gel, las dos fases pueden coexistir en regiones separadas en el espacio, como un iceberg flotando en el océano. Esta separación de fases desempeña un papel fundamental en los fenómenos bioquímicos debido a que los componentes de la membrana, tales como las proteínas pueden repartirse en una u otra fase[23] y por lo tanto están concentradas o activadas a nivel local. Un componente particularmente importante de muchos sistemas de fase mixta es el colesterol, que modula la permeabilidad de la bicapa, resistencia mecánica, y las interacciones bioquímicas.
Química de superficie[editar]
Mientras que las colas de lípidos modulan principalmente el comportamiento de fase de la bicapa, es el grupo de cabeza que determina la química de la superficie de la bicapa. La mayoría de las bicapas naturales se componen principalmente de fosfolípidos, aunque los esfingolípidos tales como esfingomielina y esteroles como el colesterol son también componentes importantes. De los fosfolípidos, el grupo de cabeza más común es la fosfatidilcolina (PC), que representa alrededor de la mitad de los fosfolípidos en la mayoría de las células de mamíferos.[24] PC es un grupo de cabeza de ion híbrido, ya que tiene una carga negativa en el grupo fosfato y una carga positiva en la amina, pero, debido al balance de cargas locales, sin carga neta.
Otros grupos de cabeza también están presentes en diversos grados y pueden incluir la fosfatidilserina (PS) fosfatidiletanolamina (PE) y fosfatidilglicerol (PG). Estos grupos de cabeza alternos a menudo confieren funcionalidad biológica específica que es altamente dependiente del contexto. Por ejemplo, la presencia de PS en la cara de la membrana extracelular de los eritrocitos es un marcador de la apoptosis,[25] mientras que PS en las vesículas de la placa de crecimiento es necesaria para la nucleación de cristales de hidroxiapatita y la mineralización ósea subsiguiente.[26][27] A diferencia de la PC, algunos de los otros grupos de cabeza llevan una carga neta, que puede alterar las interacciones electrostáticas de las pequeñas moléculas con la bicapa.[28]
Roles biológicos[editar]
Contención y separación[editar]
La función principal de la bicapa lipídica en la Biología es separar compartimentos acuosos de su entorno. Sin alguna forma de delimitación entre "yo mismo" y "algo más", es difícil de definir incluso el concepto de un organismo o de la vida. Esta barrera adopta la forma de una bicapa lipídica en todas las formas de vida conocidas a excepción de unas pocas especies de arqueas que utilizan una monocapa lipídica especialmente adaptada.[7] Incluso se ha propuesto que la primera forma de vida pudo haber sido una vesícula lipídica sencilla su capacidad biosintética siendo la producción de más fosfolípidos.[29] La capacidad de partición de la bicapa lipídica se basa en el hecho de que las moléculas hidrofílicas no pueden cruzar fácilmente el núcleo de la bicapa hidrofóbica, como se discute en el transporte a través de la bicapa a continuación. El núcleo, las mitocondrias y los cloroplastos tienen dos bicapas lipídicas, mientras que otras estructuras subcelulares están rodeados por una única bicapa lipídica (tal como la membrana plasmática, retículo endoplásmico, aparato de Golgi y lisosomas). Ver Organelos.[30]
Los procariontes solo tienen una bicapa lipídica- la membrana celular (también conocida como la membrana plasmática). Muchos procariontes también tienen una pared celular, pero la pared celular está compuesta de proteínas o carbohidratos de cadena larga, no lípidos. En contraste, los eucariontes tienen una gama de organelos, incluyendo el núcleo, mitocondrias, lisosomas y retículo endoplasmático. Todos estos compartimentos subcelulares están rodeados por una o más bicapas lipídicas y, juntos, comprenden típicamente la mayoría de la zona de bicapa presente en la célula. En los hepatocitos del hígado, por ejemplo, la membrana plasmática representa solo el dos por ciento de la superficie total de dos capas de la célula, mientras que el retículo endoplásmico contiene más del cincuenta por ciento y la mitocondria un treinta por ciento más.[31]

Señalización[editar]
Probablemente, la forma más familiar de la señalización celular es la transmisión sináptica, en el que un impulso nervioso que ha llegado al final de una neurona se transporta a una neurona adyacente a través de la liberación de neurotransmisores. Esta transmisión se hace posible por la acción de las vesículas sinápticas cargadas con los neurotransmisores que se liberan. Estas vesículas se fusionan con la membrana celular en la terminal pre-sináptica y liberan su contenido al exterior de la célula. El contenido a continuación se difunde a través de la sinapsis a la terminal post-sináptica.
Las bicapas lipídicas también están implicadas en la transducción de señales a través de su papel como el hogar de las proteínas integrales de membrana. Esta es una clase extremadamente amplia e importante de la biomolécula. Se estima que hasta un tercio del proteoma humano pueden ser proteínas de membrana.[32] Algunas de estas proteínas están relacionadas con el exterior de la membrana celular. Un ejemplo de esto es la proteína CD59, que identifica células como "auto" y por lo tanto inhibe su destrucción por el sistema inmune. El virus del VIH evade el sistema inmunitario, en parte, mediante el injerto de estas proteínas de la membrana hospedera en su propia superficie.[31] Alternativamente, algunas proteínas de membrana penetran todo el camino a través de la bicapa, y sirven para transmitir eventos de señal individuales desde el exterior al interior de la célula. La clase más común de este tipo de proteína es el receptor acoplado a proteínas G (GPCR siglas en inglés). Los GPCR son responsables de gran parte de la capacidad de la célula para percibir su entorno y, debido a esta importante función, aproximadamente el 40% de todos los medicamentos modernos están dirigidos a los GPCRs.[33]
Además de proteínas y procesos de solución mediada, también es posible que las bicapas lipídicas participen directamente en la señalización. Un ejemplo clásico de esto es la fagocitosis fosfatidilserina por alarma. Normalmente, la fosfatidilserina se distribuye de manera asimétrica en la membrana celular y está presente solo en el lado interior. Durante la muerte celular programada, una proteína llamada escramblasa equilibra esta distribución, se presenta fosfatidilserina en la cara extracelular bicapa. La presencia de fosfatidilserina a continuación, desencadena la fagocitosis para eliminar las células muertas o las que están por morir.
Métodos de caracterización[editar]

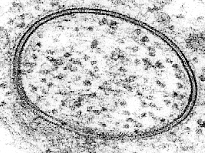
La bicapa lipídica es una estructura muy difícil de estudiar debido a que es muy delgada y frágil. A pesar de estas limitaciones docenas de técnicas se han desarrollado durante los últimos setenta años para permitir la investigación de su estructura y función.
Las mediciones eléctricas son una forma directa de caracterizar una función importante de una bicapa: su capacidad para separar y prevenir el flujo de iones en solución. Mediante la aplicación de un voltaje a través de la bicapa y la medición de la corriente resultante, se determina la resistencia de la bicapa. Esta resistencia suele ser bastante alta (108 Ohm-cm^2 o más)[34] ya que el núcleo hidrofóbico es impermeable a especies cargadas. La presencia de incluso unos pocos agujeros de escala nanométrica resulta en un aumento dramático en la corriente.[35] La sensibilidad de este sistema es tal que incluso la actividad de canales de iones individuales se puede resolver.[36]
Las mediciones eléctricas no proporcionan una imagen real como la formación de imágenes con una lata microscopio. Las bicapas lipídicas no se pueden ver en un microscopio tradicional, ya que son demasiado delgadas. Con el fin de observar las bicapas, los investigadores suelen utilizar microscopía de fluorescencia. Una muestra se excita con una longitud de onda de la luz y se observa en una longitud de onda diferente, por lo que se verán solo las moléculas fluorescentes con una excitación a juego y perfil de emisión. Las bicapas lipídicas naturales no son fluorescentes, por lo que se usa un colorante que se une a las moléculas deseadas en la bicapa. La resolución se limita generalmente a unos pocos cientos de nanómetros, mucho más pequeños que una célula típica pero mucho más grande que el espesor de una bicapa lipídica.


La microscopía electrónica ofrece una imagen de mayor resolución. En un microscopio electrónico, un haz de electrones enfocados interactúa con la muestra en lugar de un haz de luz como en la microscopía tradicional. En combinación con técnicas de congelación rápida, la microscopía electrónica también se ha utilizado para estudiar los mecanismos de transporte inter e intracelular, por ejemplo en lo que demuestra que las vesículas exocitóticas son los medios de liberación química en la sinapsis.[38]
31P-NMR (resonancia magnética nuclear) espectroscopía es ampliamente utilizada para estudios de las bicapas de fosfolípidos y las membranas biológicas en condiciones nativas.
El análisis[39] de 31P-NMR de los lípidos podría proporcionar una amplia gama de información acerca del empaquetamiento de la bicapa lipídica, transiciones de fase (fase de gel, fase de cristal líquido fisiológico, las fases de la ondulación, fases de no bicapa), orientación del grupo de cabeza de lípidos/dinámica, y las propiedades elásticas de la bicapa lipídica pura y como resultado de la unión de las proteínas y otras biomoléculas.
Un nuevo método para estudiar las bicapas lipídicas es la microscopía de fuerza atómica (AFM). En lugar de utilizar un haz de luz o partículas, una pequeña punta afilada explora la superficie al hacer contacto físico con la bicapa y moviéndose a través de ella, como un jugador de la aguja. AFM es una técnica prometedora, ya que tiene el potencial de imagen con una resolución nanométrica a temperatura ambiente e incluso bajo el agua o tampón fisiológico, condiciones necesarias para el comportamiento bicapa natural. Utilizando esta capacidad, AFM se ha utilizado para examinar el comportamiento dinámico de la bicapa incluyendo la formación de poros transmembranales (agujeros)[37] y las transiciones de fase en bicapas soportadas.[40] Otra ventaja es que AFM no requiere de una etiqueta fluorescente o isotópica de los lípidos, puesto que la punta de la sonda interactúa mecánicamente con la superficie bicapa. Debido a esto, la misma imagen puede escanear ambos lípidos y proteínas asociadas, a veces incluso con una resolución de una sola molécula.[37][41] AFM también puede sondear la mecánica natural de las bicapas lipídicas.[42]
Las bicapas lipídicas exhiben altos niveles de birrefringencia en el que el índice de refracción en el plano de la bicapa difiere de la perpendicular por 0.1 unidades de índice de refracción. Esto ha sido utilizado para caracterizar el grado de orden y la interrupción en bicapas utilizando interferometría polarización dual para entender los mecanismos de interacción de proteínas.
Las bicapas lipídicas son sistemas moleculares complicados con muchos grados de libertad. Así la simulación atomística de la membrana y, en particular, los cálculos ab initio de sus propiedades es difícil y computacionalmente costoso. Se han realizado recientemente cálculos de química cuántica exitosamente se ha para estimar momentos dipolares y cuadrupolares de las membranas lipídicas.[43]
Transporte a través de la bicapa[editar]
Difusión pasiva[editar]
La mayoría de moléculas polares tienen una baja solubilidad en el núcleo del hidrocarburo de una bicapa lipídica y, como consecuencia, tienen bajos coeficientes de permeabilidad a través de la bicapa. Este efecto es particularmente pronunciado para las especies cargadas, que tienen aún más bajos coeficientes de permeabilidad que las moléculas polares neutras.[44] Los aniones típicamente tienen un mayor rango de difusión a través de las bicapas que los cationes.[45][46]
En comparación con los iones, las moléculas de agua tienen en realidad una relativamente grande permeabilidad a través de la bicapa, como se evidencia en la hinchazón osmótica. Cuando una célula o vesícula con una alta concentración de sal en el interior se coloca en una solución con una baja concentración de sal se hinchará y, finalmente, estallará. Tal resultado no se observará a menos que el agua fuera capaz de pasar a través de la bicapa con relativa facilidad. La anómalamente gran permeabilidad del agua a través de bicapas todavía no se entiende por completo y sigue siendo objeto de debate activo.[47]
Pequeñas moléculas apolares sin carga difunden a través de las bicapas lipídicas muchos órdenes de magnitud más rápido que los iones o agua. Esto aplica tanto a las grasas y disolventes orgánicos como cloroformo y éter. Independientemente de su carácter polar, moléculas más grandes se difunden más lento a través de las bicapas lipídicas que las moléculas pequeñas.[48]
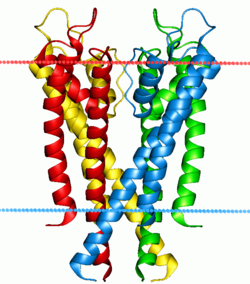
Bombas y canales de iones[editar]
Dos clases especiales de proteínas con los gradientes iónicos encontrados a través de las membranas celulares y subcelulares en los canales iónicos de naturaleza y bombas de iones. Ambas bombas y canales son proteínas integrales de membrana que pasan a través de la bicapa, pero sus funciones son muy diferentes. Las bombas de iones son las proteínas que construyen y mantienen los gradientes químicos mediante la utilización de una fuente de energía externa para mover iones contra el gradiente de concentración a un área de mayor potencial químico. La fuente de energía puede ser de ATP, como es el caso de la Na + -K + ATPasa. Alternativamente, la fuente de energía puede ser otro gradiente químico ya en el lugar, como en el antiportador Ca2 + / Na +. Es a través de la acción de bombas de iones que las células son capaces de regular el pH por medio del bombeo de protones.
En contraste con las bombas de iones, los canales iónicos no construyen gradientes químicos, sino más bien ellos se disipan con el fin de realizar un trabajo o enviar una señal. Probablemente el ejemplo más conocido y mejor estudiado es el canal de Na+ dependiente de voltaje, lo que permite la conducción del potencial de acción a lo largo de las neuronas. Todas las bombas de iones tienen algún tipo de mecanismo de disparo o "gating". En el ejemplo anterior era polarización eléctrica, pero otros canales pueden ser activados por la unión de un agonista molecular o a través de un cambio conformacional en otra proteína cercana.[49]

Endocitosis y exocitosis[editar]
Algunas moléculas o partículas son demasiado grandes o demasiado hidrófilas para pasar a través de una bicapa lipídica. Otras moléculas podrían pasar a través de la bicapa, pero deben ser transportadas rápidamente en un número tan grande que el transporte del tipo de canal es poco práctico. En ambos casos, estos tipos de carga pueden moverse a través de la membrana celular por medio de la fusión o en ciernes de vesículas. Cuando una vesícula se produce dentro de la célula y se fusiona con la membrana plasmática para liberar su contenido en el espacio extracelular, este proceso se conoce como exocitosis. En el proceso inverso, una región de la membrana celular se hará un hoyuelo hacia el interior y, finalmente se pinchará, encerrando una parte del fluido extracelular para transportarlo en la célula. La Endocitosis y exocitosis se basan en maquinaria molecular muy diferente a la función, pero los dos procesos están íntimamente vinculados y no podrían trabajar sin la otra. El mecanismo primario de esta interdependencia es la gran cantidad de material lipídico involucrados.[50] En una célula típica, el área de la bicapa equivalente a la membrana plasmática entera viajará a través del ciclo de endocitosis/exocitosis en una media hora.[51] Si estos dos procesos no se equilibran entre sí, la célula se haría un globo hacia el exterior en un tamaño difícil de manejar o se agotaría por completo su membrana plasmática en cuestión de minutos.

Exocitosis en procariontes: La exocitosis de membrana vesicular, popularmente conocida como el tráfico de vesículas de membrana, ganador del premio Nobel (año 2013) es tradicionalmente considerado como una prerrogativa de las células eucariontes.[52] Sin embargo, este mito se rompió con la revelación de que nanovesículas, popularmente conocidas como vesículas de membrana externa bacteriana, dadas a conocer por los microorganismos gram negativas, trasladan moléculas de señal bacterianas para hospedar u objetivar a células[53] para llevar a cabo múltiples procesos a favor del microbio segregador, por ejemplo, en la invasión de la célula huésped[54] y en las interacciones microbio-medio ambiente, en general.[55]
Electroporación[editar]
La electroporación es el rápido aumento de la permeabilidad en la bicapa inducida por la aplicación de un gran campo eléctrico artificial a través de la membrana. Experimentalmente, la electroporación se utiliza para introducir moléculas hidrofílicas en las células. Es una técnica particularmente útil para grandes moléculas altamente cargadas tales como ADN, que nunca se difundiría pasivamente a través del núcleo de la bicapa hidrofóbica.[56] Debido a esto, la electroporación es uno de los principales métodos de transfección, así como de la transformación bacteriana. Incluso se ha propuesto que la electroporación resultante de tormentas eléctricas podría ser un mecanismo natural de transferencia horizontal de genes.[57]
Este aumento de la permeabilidad afecta principalmente el transporte de iones y otras especies hidratadas, lo que indica que el mecanismo es la creación de agujeros llenos de agua en escala-nm en la membrana. Aunque la electroporación y la ruptura dieléctrica resultan de la aplicación de un campo eléctrico, los mecanismos implicados son fundamentalmente diferentes. En la ruptura dieléctrica se ioniza el material de barrera, creando una vía conductora. La alteración material es por lo tanto de naturaleza química. En contraste, durante la electroporación las moléculas de lípidos no se alteran químicamente sino simplemente cambian de posición, abriendo un poro que actúa como la vía conductora a través de la bicapa, ya que se llena de agua.
Mecánica[editar]

Las bicapas lipídicas son estructuras bastante grandes para tener algunas de las propiedades mecánicas de líquidos o sólidos. El módulo de compresión de área Ka, Kb módulo de flexión, y la energía borde , se puede utilizar para describirlos. Las bicapas lipídicas sólidas también tienen un módulo de corte, pero al igual que cualquier líquido, el módulo de corte es cero para bicapas de fluidos. Estas propiedades mecánicas afectan en el funcionamiento de la membrana. Ka y Kb afectan a la capacidad de las proteínas y moléculas pequeñas para insertar en la bicapa,[58][59] y las propiedades mecánicas de la bicapa se han demostrado que alteran la función de los canales iónicos activados mecánicamente.[60] Las propiedades mecánicas de la bicapa también establecen qué tipos de estrés una célula puede soportar sin que se rompa. Aunque las bicapas lipídicas pueden doblarse fácilmente, la mayoría no puede estirarse más que un pequeño tanto por ciento antes de romperse.[61]
Como se discutió en la sección Estructura y organización, la atracción hidrófoba de colas de lípidos en el agua es la fuerza primaria que contiene a las bicapas lipídicas juntas. Por lo tanto, el módulo elástico de la bicapa está determinada principalmente por la cantidad de área adicional que se expone al agua en las que las moléculas de lípidos se estiran aparte.[62] No es sorprendente, dada esta comprensión de las fuerzas involucradas que los estudios han demostrado que el Ka varía fuertemente con la presión osmótica[63] pero débilmente con el largo de la cola y la insaturación.[10] Debido a que las fuerzas implicadas son tan pequeñas, es difícil de determinar experimentalmente la Ka. La mayoría de las técnicas de microscopía requieren equipos sofisticados de medición muy sensibles.[42][64]
En contraste con Ka, que es una medida de cantidad de energía que se necesita para estirar la bicapa, Kb es una medida de la cantidad de energía que se necesita para doblar o flexionar la bicapa. Formalmente, un módulo de flexión se define como la energía necesaria para deformar una membrana de su curvatura intrínseca a alguna otra curvatura. La curvatura intrínseca se define por la relación del diámetro del grupo de cabeza a la del grupo de cola. Para los lípidos PC de dos colas, esta relación es casi uno, por lo que la curvatura intrínseca es casi cero. Si un lípido particular, tiene una desviación demasiado grande de curvatura intrínseca de cero, no se formará una bicapa y en su lugar se formarán otras fases tales como micela o micelas invertidas. La adición de pequeñas moléculas hidrofílicas como la sacarosa en liposomas laminares de lípidos mixtos a base de membranas ricas en tilacoides y galactolípidos desestabilizan las bicapas en una fase micelar.[65] Típicamente Kb no se mide experimentalmente sino se calcula a partir de medidas de Ka y el espesor de la bicapa, ya que los tres parámetros están relacionados.
es una medida de la cantidad de energía que se necesita para exponer un borde de la bicapa al agua rasgando la bicapa o la creando un agujero en ella. El origen de esta energía es el hecho de que, al crear tal interfaz, expone algunas de las colas de lípidos al agua, pero la orientación exacta de estos lípidos del borde es desconocida. Existe alguna evidencia de que tantos poros hidrofóbicos (colas rectas) e hidrofílicos (cabezas curvadas alrededor de) pueden coexistir.[66]
Fusión[editar]

La fusión es el proceso por el cual dos bicapas lipídicas se funden, lo que resulta en una estructura conectada. Si esta fusión procede completamente a través de ambas hojas de ambas bicapas, un puente lleno de agua se forma y las soluciones contenidas por las bicapas se pueden mezclar. Alternativamente, si solo una hoja de cada bicapa está involucrada en el proceso de fusión, se dice que están las bicapas están hemifusionadas. La fusión está implicada en muchos procesos celulares, en particular, en eucariontes, ya que la célula eucariota es ampliamente subdividida por bicapas lipídicas de membrana. La exocitosis, fertilización de un óvulo por el espermatozoide y el transporte de los productos de desecho al lisosoma son algunos de los muchos procesos eucariontes que dependen de alguna forma de fusión. Incluso la entrada de patógenos puede ser gobernado por fusión, ya que muchos virus recubiertos de bicapa han dedicado proteínas de fusión para poder entrar en la célula huésped.
Hay cuatro pasos fundamentales en el proceso de fusión.[24] En primer lugar, las membranas implicadas deben agregarse, acercándose entre sí dentro de varios nanómetros. En segundo lugar, las dos bicapas deben entrar en contacto muy cercano (dentro de unos pocos angstroms). Para lograr este contacto, las dos superficies deben llegar a ser al menos parcialmente deshidratadas, ya que el agua de la superficie límite normalmente presente, causa bicapas para repeler con fuerza. La presencia de iones, en particular, cationes divalentes tales como magnesio y calcio, afecta fuertemente a este paso.[67][68] Uno de los papeles críticos de calcio en el cuerpo es la regulación de la fusión de membranas. En tercer lugar, una desestabilización se debe formar en un punto entre las dos bicapas, distorsionando sus estructuras. La naturaleza exacta de esta distorsión no se conoce. Una teoría es que un "tallo" altamente curvado se debe formar entre las dos bicapas.[69] Los defensores de esta teoría creen que se explica por qué la fosfatidiletanolamina, un lípido muy curvado, promueve la fusión.[70] Finalmente, en la última etapa de la fusión, este defecto punto crece y los componentes de las dos bicapas se mezclan y se difunden lejos del sitio de contacto.


La situación se complica aún más cuando se considera fusión in vivo ya que la fusión biológica es casi siempre regulada por la acción de las proteínas asociadas a la membrana. Las primeras de estas proteínas para ser estudiadas fueron las proteínas de fusión virales, que permiten que un virus con envoltura inserte su material genético en la célula huésped (los virus envueltos son aquellos rodeados de una bicapa lipídica, y algunos otros solo tienen una capa de proteína). Las células eucariontes también utilizan proteínas de fusión, la mejor estudiada son las proteínas SNARE que se utilizan para dirigir todo el tráfico vesicular intracelular. A pesar de años de estudio, queda mucho por descubrir acerca de la función de esta clase de proteínas. De hecho, todavía hay un debate activo sobre si las SNAREs están vinculadas a acoplamiento temprano o participan más tarde en el proceso de fusión, facilitando la hemifusion.[72]
En los estudios de biología molecular y celular a menudo es deseable inducir artificialmente la fusión. La adición de polietilenglicol (PEG) provoca la fusión sin agregación significativa o la interrupción bioquímica. Este procedimiento se usa ahora ampliamente, por ejemplo mediante la fusión de las células B con células de melanoma.[73] El "hibridismo" resultante de esta combinación expresa un anticuerpo deseado tal como se determina por las células B involucradas, pero se inmortaliza debido al componente de melanoma. La fusión también puede inducirse artificialmente por medio de electroporación en un proceso conocido como electrofusión. Se cree que este fenómeno resulta de los bordes con energía activos formados durante la electroporación, que pueden actuar como el punto de defecto local para nuclear el crecimiento del tallo entre dos bicapas.[74]
Sistemas modelo[editar]
Las bicapas lipídicas pueden ser creadas artificialmente en el laboratorio para permitir que los investigadores realicen experimentos que no se pueden hacer en bicapas naturales. Existen muchos tipos de bicapas modelo, cada una con ventajas y desventajas experimentales. Se pueden hacer con lípidos ya sea sintéticos o lípidos naturales. Entre los sistemas modelo más comunes se encuentran:
- Membranas lipídicas negras
- Capas lipídicas soportadas
- Membranas de bicapas lipídicas tethered (tBLM)
- Vesículas
Aplicaciones comerciales[editar]
Hasta la fecha, la aplicación comercial más exitosa de bicapas lipídicas ha sido el uso de liposomas para la administración de fármacos, especialmente para el tratamiento del cáncer. (Nota-el término "liposoma" es, en esencia, sinónimo de "vesícula", excepto que la vesícula es un término general para la estructura, mientras que los liposomas se refieren a solamente vesículas artificiales, no naturales) La idea básica de la administración de fármacos liposomal es que el fármaco esté encapsulado en solución dentro del liposoma y luego se inyecta en el paciente. Estos liposomas cargados con el fármaco viajan a través del sistema hasta que se unen en el sitio objetivo y la rotura, liberando el fármaco. En teoría, los liposomas deben hacer un sistema de suministro de fármaco ideal ya que pueden aislar casi cualquier fármaco hidrofílico, se pueden injertar con las moléculas a los tejidos objetivo específicos y pueden ser relativamente no tóxicos ya que el cuerpo posee rutas bioquímicas para degradar lípidos.[75]
La primera generación de liposomas de administración de fármacos tuvo una composición lipídica simple y sufrió de varias limitaciones. La circulación en el torrente sanguíneo era extremadamente limitado debido tanto a compensación renal y a la fagocitosis. El refinamiento de la composición de lípidos a la fluidez tono, densidad de carga superficial, y la hidratación de superficie resultó en vesículas que se absorben menos proteínas del suero y por lo tanto son menos fácilmente reconocidos por el sistema inmune.[76] El avance más significativo en esta área fue el injerto de polietilenglicol (PEG) sobre la superficie del liposoma para producir vesículas "ocultas", que circulan durante tiempos largos sin la eliminación inmune o renal.[77]
Los primeros liposomas ocultos fueron atacados de forma pasiva en los tejidos tumorales. Debido a que los tumores inducen la angiogénesis rápida e incontrolada que son especialmente "fugas" y permiten que los liposomas salgan de la sangre a un ritmo mucho más alto que el tejido normal lo haría.[78] Más recientemente cuando el trabajo se ha realizó con los anticuerpos de injerto u otros marcadores moleculares en la superficie del liposoma con la esperanza de que se unieran activamente a ellos un tipo de célula o tejido específico.[79] Algunos ejemplos de este enfoque ya están en ensayos clínicos.[80]
Otra aplicación potencial de las bicapas lipídicas es en el campo de los biosensores. Ya que no solo la bicapa lipídica es la barrera entre el interior y el exterior de la célula, sino que también es el sitio de una extensa transducción de señales. Los investigadores en los últimos años han tratado de aprovechar este potencial para desarrollar un dispositivo basado en la bicapa para el diagnóstico clínico o la detección de bioterrorismo. El progreso ha sido lento en esta área y, aunque algunas empresas han desarrollado sistemas de detección basados en lípidos automatizados, están siendo dirigidos a la comunidad de investigación. Estos incluyen Biacore (ahora GE Healthcare Life Sciences), que ofrece un chip desechable para la utilización de bicapas de lípidos en los estudios de cinética de unión[81] y Nanion Inc., que ha desarrollado un sistema de sujeción de parches automatizado.[82] Otras aplicaciones, más exóticas también se persiguen, tales como el uso de poros de la membrana bicapa lipídica para la secuenciación de ADN por Oxford Nanolabs. Hasta la fecha, esta tecnología no ha demostrado ser comercialmente viable
Una bicapa lipídica soportada (SLB) como se describió anteriormente ha logrado un éxito comercial como una técnica de cribado para medir la permeabilidad de los fármacos. Este ensayo de permeabilidad de la membrana artificial paralela PAMPA, mide la permeabilidad a través del cóctel de lípidos específicamente formulados, en donde se ha encontrado una alta correlación con cultivos Caco-2,[83][84] el tracto gastrointestinal,[85] barrera sangre-cerebro[86] y la piel.[87]
Historia[editar]
A principios del siglo XX, los científicos habían llegado a creer que las células están rodeadas por una delgada barrera similar al aceite,[88] pero la naturaleza estructural de esta membrana no se conocía. Dos experimentos en 1925 sentaron las bases para llenar este vacío. Mediante la medición de la capacitancia de soluciones de eritrocitos, Hugo Fricke determinó que la membrana de la célula fue de 3.3 nm de espesor.[89]
Aunque los resultados de este experimento fueron exactos, Fricke malinterpretó los datos en el sentido de que la membrana celular es una capa molecular individual. El Prof. Dr. Evert Gorter[90] (1881–1954) y F. Grendel de la Universidad de Leiden abordaron el problema desde una perspectiva diferente, la difusión de los lípidos de eritrocitos como una monocapa sobre una artesa de Langmuir-Blodgett. Cuando compararon el área de la monocapa a la zona de superficie de las células, se encontraron con una relación de dos a uno.[91] Análisis posteriores mostraron varios errores y suposiciones incorrectas con este experimento, pero, casualmente, estos errores anulados y desde estos datos defectuosos Gorter y Grendel señalaron a la conclusión correcta, que la membrana celular es una bicapa lipídica.[24]
Esta teoría se confirmó mediante el uso de microscopía electrónica a finales de 1950. A pesar de que no publicó el primer estudio de microscopía electrónica de bicapas lipídicas[92] J. David Robertson fue el primero en afirmar que las dos bandas obscuras de electrones de alta densidad eran los grupos de cabeza y las proteínas asociadas de dos monocapas de lípidos que se oponen.[93][94] En este cuerpo de trabajo, Robertson propuso el concepto de la "unidad de membrana." Esta fue la primera vez que la estructura bicapa había sido asignado universalmente a todas las membranas celulares, así como las membranas de los organelos.
Casi al mismo tiempo, el desarrollo de membranas modelo confirmó que la bicapa lipídica es una estructura estable que puede existir independientemente de las proteínas. Por "pintar" una solución de lípidos en un disolvente orgánico a través de una abertura, Mueller y Rudin fueron capaces de crear una bicapa artificial y determinar que esto exhibe fluidez lateral, alta resistencia eléctrica y la auto-curación en respuesta a la perforación,[95] todas las cuales son propiedades de una membrana celular natural. Unos años más tarde, Alec Bangham mostró que bicapas, en forma de vesículas lipídicas, podrían también formarse simplemente mediante la exposición de una muestra seca de lípido a agua.[96] Este fue un avance importante, ya que se demostró que las bicapas lipídicas se forman espontáneamente a través de un autoensamblaje y no requieren una estructura de soporte diseñada.
Véase también[editar]
- Categoría: Surfactantes
- Proteína de membrana
- Cáscara anular de lípidos
- Tráfico de vesículas de membrana
- Exocitosis
- Vesículas de membrana externa bacteriana
- Biofísica de membrana
- Polimorfismo de lípidos
- Comportamiento de fase bicapa lipídica
- Liposoma
- Lipidómica
Referencias[editar]
- ↑ Andersen, Olaf S.; Koeppe, II, Roger E. (June 2007). «Bilayer Thickness and Membrane Protein Function: An Energetic Perspective». Annual Review of Biophysics and Biomolecular Structure 36 (1): 107-130. doi:10.1146/annurev.biophys.36.040306.132643. Consultado el 12 de diciembre de 2014.
- ↑ Divecha, Nullin; Irvine, Robin F (27 de enero de 1995). «Phospholipid signaling» (PDF, 0.04 MB). Cell 80 (2): 269-278. PMID 7834746. doi:10.1016/0092-8674(95)90409-3.
- ↑ Mashaghi et al. Hydration strongly affects the molecular and electronic structure of membrane phospholipids. 136, 114709 (2012)«Copia archivada». Archivado desde el original el 15 de mayo de 2016. Consultado el 17 de mayo de 2012.
- ↑ a b Lewis BA; Engelman DM (May 1983). «Lipid bilayer thickness varies linearly with acyl chain length in fluid phosphatidylcholine vesicles». J. Mol. Biol. 166 (2): 211-7. PMID 6854644. doi:10.1016/S0022-2836(83)80007-2.
- ↑ Zaccai G; Blasie JK; Schoenborn BP (January 1975). «Neutron Diffraction Studies on the Location of Water in Lecithin Bilayer Model Membranes». Proc. Natl. Acad. Sci. U.S.A. 72 (1): 376-380. Bibcode:1975PNAS...72..376Z. PMC 432308. PMID 16592215. doi:10.1073/pnas.72.1.376.
- ↑ Nagle JF; Tristram-Nagle S (November 2000). «Structure of lipid bilayers». Biochim. Biophys. Acta 1469 (3): 159-95. PMC 2747654. PMID 11063882. doi:10.1016/S0304-4157(00)00016-2.
- ↑ a b Parker J; Madigan MT; Brock TD; Martinko JM (2003). Brock biology of microorganisms (10th edición). Englewood Cliffs, N.J: Prentice Hall. ISBN 0-13-049147-0.
- ↑ Marsh D (July 2001). «Polarity and permeation profiles in lipid membranes». Proc. Natl. Acad. Sci. U.S.A. 98 (14): 7777-82. Bibcode:2001PNAS...98.7777M. PMC 35418. PMID 11438731. doi:10.1073/pnas.131023798.
- ↑ Marsh D (December 2002). «Membrane water-penetration profiles from spin labels». Eur. Biophys. J. 31 (7): 559-62. PMID 12602343. doi:10.1007/s00249-002-0245-z.
- ↑ a b c d Rawicz W; Olbrich KC; McIntosh T; Needham D; Evans E (July 2000). «Effect of chain length and unsaturation on elasticity of lipid bilayers». Biophys. J. 79 (1): 328-39. Bibcode:2000BpJ....79..328R. PMC 1300937. PMID 10866959. doi:10.1016/S0006-3495(00)76295-3.
- ↑ Trauble H; Haynes DH (1971). «The volume change in lipid bilayer lamellae at the crystalline-liquid crystalline phase transition». Chem. Phys. Lipids. 7 (4): 324-35. doi:10.1016/0009-3084(71)90010-7.
- ↑ Bretscher MS (1 de marzo de 1972). «Asymmetrical Lipid Bilayer Structure for Biological Membranes». Nature New Biology 236 (61): 11-12. PMID 4502419. doi:10.1038/newbio236011a0.
- ↑ Verkleij AJ; Zwaal RF; Roelofsen B; Comfurius P; van Deenen LL (October 1973). «The asymmetric distribution of phospholipids in the human red cell membrane. A combined study using phospholipases and freeze-etch electron microscopy». Biochim. Biophys. Acta 323 (2): 178-93. PMID 4356540. doi:10.1016/0005-2736(73)90143-0.
- ↑ Bell RM; Ballas LM; Coleman RA (1 de marzo de 1981). «Lipid topogenesis». J. Lipid Res. 22 (3): 391-403. PMID 7017050. Archivado desde el original el 17 de octubre de 2019. Consultado el 14 de junio de 2016.
- ↑ Bretscher MS (August 1973). «Membrane structure: some general principles». Science 181 (4100): 622-629. Bibcode:1973Sci...181..622B. PMID 4724478. doi:10.1126/science.181.4100.622.
- ↑ Rothman JE; Kennedy EP (May 1977). «Rapid transmembrane movement of newly synthesized phospholipids during membrane assembly». Proc. Natl. Acad. Sci. U.S.A. 74 (5): 1821-5. Bibcode:1977PNAS...74.1821R. PMC 431015. PMID 405668. doi:10.1073/pnas.74.5.1821.
- ↑ Kornberg RD; McConnell HM (March 1971). «Inside-outside transitions of phospholipids in vesicle membranes». Biochemistry 10 (7): 1111-20. PMID 4324203. doi:10.1021/bi00783a003.
- ↑ Litman BJ (July 1974). «Determination of molecular asymmetry in the phosphatidylethanolamine surface distribution in mixed phospholipid vesicles». Biochemistry 13 (14): 2844-8. PMID 4407872. doi:10.1021/bi00711a010.
- ↑ Crane JM; Kiessling V; Tamm LK (February 2005). «Measuring lipid asymmetry in planar supported bilayers by fluorescence interference contrast microscopy». Langmuir 21 (4): 1377-88. PMID 15697284. doi:10.1021/la047654w.
- ↑ Kalb E; Frey S; Tamm LK (January 1992). «Formation of supported planar bilayers by fusion of vesicles to supported phospholipid monolayers». Biochim. Biophys. Acta 1103 (2): 307-16. PMID 1311950. doi:10.1016/0005-2736(92)90101-Q.
- ↑ Lin WC; Blanchette CD; Longo ML (January 2006). «Lipid asymmetry in DLPC/DSPC-supported lipid bilayers: a combined AFM and fluorescence microscopy study». Biophys. J. 90 (1): 228-37. Bibcode:2006BpJ....90..228L. PMC 1367021. PMID 16214871. doi:10.1529/biophysj.105.067066.
- ↑ Berg, Howard C. (1993). Random walks in biology (Extended Paperback edición). Princeton, N.J: Princeton University Press. ISBN 0-691-00064-6.
- ↑ Dietrich C; Volovyk ZN; Levi M; Thompson NL; Jacobson K (September 2001). «Partitioning of Thy-1, GM1, and cross-linked phospholipid analogs into lipid rafts reconstituted in supported model membrane monolayers». Proc. Natl. Acad. Sci. U.S.A. 98 (19): 10642-7. Bibcode:2001PNAS...9810642D. PMC 58519. PMID 11535814. doi:10.1073/pnas.191168698.
- ↑ a b c Yeagle, Philip (1993). The membranes of cells (2nd edición). Boston: Academic Press. ISBN 0-12-769041-7.
- ↑ Fadok VA; Bratton DL; Frasch SC; Warner ML; Henson PM (July 1998). «The role of phosphatidylserine in recognition of apoptotic cells by phagocytes». Cell Death Differ. 5 (7): 551-62. PMID 10200509. doi:10.1038/sj.cdd.4400404.
- ↑ Anderson HC; Garimella R; Tague SE (January 2005). «The role of matrix vesicles in growth plate development and biomineralization». Front. Biosci. 10 (1–3): 822-37. PMID 15569622. doi:10.2741/1576.
- ↑ Eanes ED; Hailer AW (January 1987). «Calcium phosphate precipitation in aqueous suspensions of phosphatidylserine-containing anionic liposomes». Calcif. Tissue Int. 40 (1): 43-8. PMID 3103899. doi:10.1007/BF02555727.
- ↑ Kim J; Mosior M; Chung LA; Wu H; McLaughlin S (July 1991). «Binding of peptides with basic residues to membranes containing acidic phospholipids». Biophys. J. 60 (1): 135-48. Bibcode:1991BpJ....60..135K. PMC 1260045. PMID 1883932. doi:10.1016/S0006-3495(91)82037-9.
- ↑ Koch AL (1984). «Primeval cells: possible energy-generating and cell-division mechanisms». J. Mol. Evol. 21 (3): 270-7. PMID 6242168. doi:10.1007/BF02102359.
- ↑ «5.1 Cell Membrane Structure | Life Science | University of Tokyo». Archivado desde el original el 22 de febrero de 2014. Consultado el 14 de junio de 2016.
- ↑ a b Alberts, Bruce (2002). Molecular biology of the cell (4th edición). New York: Garland Science. ISBN 0-8153-4072-9.
- ↑ Martelli PL; Fariselli P; Casadio R (2003). «An ENSEMBLE machine learning approach for the prediction of all-alpha membrane proteins». Bioinformatics 19 (Suppl 1): i205-11. PMID 12855459. doi:10.1093/bioinformatics/btg1027.
- ↑ Filmore D (2004). «It's A GPCR World». Modern Drug Discovery 11: 24-9.
- ↑ Montal M; Mueller P (December 1972). «Formation of bimolecular membranes from lipid monolayers and a study of their electrical properties». Proc. Nat. Acad. Sci. 69 (12): 3561-6. PMID 4509315. doi:10.1073/pnas.69.12.3561.
- ↑ Melikov KC; Frolov VA; Shcherbakov A; Samsonov AV; Chizmadzhev YA; Chernomordik LV (April 2001). «Voltage-induced nonconductive pre-pores and metastable single pores in unmodified planar lipid bilayer». Biophys. J. 80 (4): 1829-36. Bibcode:2001BpJ....80.1829M. PMC 1301372. PMID 11259296. doi:10.1016/S0006-3495(01)76153-X.
- ↑ Neher E; Sakmann B (April 1976). «Single-channel currents recorded from membrane of denervated frog muscle fibres». Nature 260 (5554): 799-802. Bibcode:1976Natur.260..799N. PMID 1083489. doi:10.1038/260799a0.
- ↑ a b c Y. Roiter, M. Ornatska, A. R. Rammohan, J. Balakrishnan, D. R. Heine, and S. Minko, Interaction of Nanoparticles with Lipid Membrane, Nano Letters, vol. 8, iss. 3, pp. 941–944 (2008).
- ↑ Heuser JE; Reese TS; Dennis MJ; Jan Y; Evans L (May 1979). «Synaptic vesicle exocytosis captured by quick freezing and correlated with quantal transmitter release». J. Cell Biol. 81 (2): 275-300. PMC 2110310. PMID 38256. doi:10.1083/jcb.81.2.275.
- ↑ Dubinnyi MA; Lesovoy DM; Dubovskii PV; Chupin VV; Arseniev AS (Jun 2006). «Modeling of 31P-NMR spectra of magnetically oriented phospholipid liposomes: A new analytical solution». Solid State Nucl Magn Reson. 29 (4): 305-311. PMID 16298110. doi:10.1016/j.ssnmr.2005.10.009.
- ↑ Tokumasu F; Jin AJ; Dvorak JA (2002). «Lipid membrane phase behavior elucidated in real time by controlled environment atomic force microscopy». J. Electron Micros. 51 (1): 1-9. PMID 12003236. doi:10.1093/jmicro/51.1.1.
- ↑ Richter RP; Brisson A (2003). «Characterization of lipid bilayers and protein assemblies supported on rough surfaces by atomic force microscopy». Langmuir 19 (5): 1632-40. doi:10.1021/la026427w.
- ↑ a b Steltenkamp S; Müller MM; Deserno M; Hennesthal C; Steinem C; Janshoff A (July 2006). «Mechanical properties of pore-spanning lipid bilayers probed by atomic force microscopy». Biophys. J. 91 (1): 217-26. Bibcode:2006BpJ....91..217S. PMC 1479081. PMID 16617084. doi:10.1529/biophysj.106.081398.
- ↑ Alireza Mashaghi et al., Hydration strongly affects the molecular and electronic structure of membrane phospholipids. J. Chem. Phys. 136, 114709 (2012) «Copia archivada». Archivado desde el original el 15 de mayo de 2016. Consultado el 17 de mayo de 2012.
- ↑ Chakrabarti AC (1994). «Permeability of membranes to amino acids and modified amino acids: mechanisms involved in translocation». Amino Acids 6 (3): 213-29. PMID 11543596. doi:10.1007/BF00813743.
- ↑ Hauser H; Phillips MC; Stubbs M (October 1972). «Ion permeability of phospholipid bilayers». Nature 239 (5371): 342-4. Bibcode:1972Natur.239..342H. PMID 12635233. doi:10.1038/239342a0.
- ↑ Papahadjopoulos D; Watkins JC (September 1967). «Phospholipid model membranes. II. Permeability properties of hydrated liquid crystals». Biochim. Biophys. Acta 135 (4): 639-52. PMID 6048247. doi:10.1016/0005-2736(67)90095-8.
- ↑ Paula S; Volkov AG; Van Hoek AN; Haines TH; Deamer DW (January 1996). «Permeation of protons, potassium ions, and small polar molecules through phospholipid bilayers as a function of membrane thickness». Biophys. J. 70 (1): 339-48. Bibcode:1996BpJ....70..339P. PMC 1224932. PMID 8770210. doi:10.1016/S0006-3495(96)79575-9.
- ↑ Xiang TX; Anderson BD (June 1994). «The relationship between permeant size and permeability in lipid bilayer membranes». J. Membr. Biol. 140 (2): 111-22. PMID 7932645. doi:10.1007/bf00232899.
- ↑ Gouaux E; Mackinnon R (December 2005). «Principles of selective ion transport in channels and pumps». Science 310 (5753): 1461-5. Bibcode:2005Sci...310.1461G. PMID 16322449. doi:10.1126/science.1113666.
- ↑ Gundelfinger ED; Kessels MM; Qualmann B (February 2003). «Temporal and spatial coordination of exocytosis and endocytosis». Nat. Rev. Mol. Cell Biol. 4 (2): 127-39. PMID 12563290. doi:10.1038/nrm1016.
- ↑ Steinman RM; Brodie SE; Cohn ZA (March 1976). «Membrane flow during pinocytosis. A stereologic analysis». J. Cell Biol. 68 (3): 665-87. PMC 2109655. PMID 1030706. doi:10.1083/jcb.68.3.665.
- ↑ YashRoy R.C. (1999) 'Exocytosis in prokaryotes' and its role in salmonella invasion. ICAR NEWS - A Science and Technology Newsletter, (Oct-Dec) vol. 5(4), page 18.https://www.researchgate.net/publication/230822402_'Exocytosis_in_prokaryotes'_and_its_role_in_Salmonella_invasion?ev=prf_pub
- ↑ YashRoy R C (1993) Electron microscope studies of surface pili and vesicles of Salmonella 3,10:r:- organisms. Ind Jl of Anim Sci 63, 99-102.https://www.researchgate.net/publication/230817087_Electron_microscope_studies_of_surface_pilli_and_vesicles_of_Salmonella_310r-_organisms?ev=prf_pub
- ↑ YashRoy R.C. (1998) Discovery of vesicular exocytosis in prokaryotes and its role in Salmonella invasion. Current Science, vol. 75(10), pp. 1062-1066.https://www.researchgate.net/publication/230793568_Discovery_of_vesicular_exocytosis_in_prokaryotes_and_its_role_in_Salmonella_invasion?ev=prf_pub
- ↑ YashRoy R.C. (1998) Exocytosis from gram negative bacteria for Salmonella invasion of chicken ileal epithelium. Indian Journal of Poultry Science, vol. 33(2), pp. 119–123. https://www.researchgate.net/publication/230856738_Exocytosis_from_gram-negative_bacteria_for_Salmonella_invasion_of_chicken_ileal_epithelium?ev=prf_pub
- ↑ Neumann E; Schaefer-Ridder M; Wang Y; Hofschneider PH (1982). «Gene transfer into mouse lyoma cells by electroporation in high electric fields». EMBO J. 1 (7): 841-5. PMC 553119. PMID 6329708.
- ↑ Demanèche S; Bertolla F; Buret F; etal (August 2001). «Laboratory-scale evidence for lightning-mediated gene transfer in soil». Appl. Environ. Microbiol. 67 (8): 3440-4. PMC 93040. PMID 11472916. doi:10.1128/AEM.67.8.3440-3444.2001.
- ↑ Garcia ML (July 2004). «Ion channels: gate expectations». Nature 430 (6996): 153-5. Bibcode:2004Natur.430..153G. PMID 15241399. doi:10.1038/430153a.
- ↑ McIntosh TJ; Simon SA (2006). «Roles of Bilayer Material Properties in Function and Distribution of Membrane Proteins». Annu. Rev. Biophys. Biomol. Struct. 35 (1): 177-98. PMID 16689633. doi:10.1146/annurev.biophys.35.040405.102022.
- ↑ Suchyna TM; Tape SE; Koeppe RE; Andersen OS; Sachs F; Gottlieb PA (July 2004). «Bilayer-dependent inhibition of mechanosensitive channels by neuroactive peptide enantiomers». Nature 430 (6996): 235-40. Bibcode:2004Natur.430..235S. PMID 15241420. doi:10.1038/nature02743.
- ↑ Hallett FR; Marsh J; Nickel BG; Wood JM (February 1993). «Mechanical properties of vesicles. II. A model for osmotic swelling and lysis». Biophys. J. 64 (2): 435-42. Bibcode:1993BpJ....64..435H. PMC 1262346. PMID 8457669. doi:10.1016/S0006-3495(93)81384-5.
- ↑ Boal, David H. (2001). Mechanics of the cell. Cambridge, UK: Cambridge University Press. ISBN 0-521-79681-4.
- ↑ Rutkowski CA; Williams LM; Haines TH; Cummins HZ (June 1991). «The elasticity of synthetic phospholipid vesicles obtained by photon correlation spectroscopy». Biochemistry 30 (23): 5688-96. PMID 2043611. doi:10.1021/bi00237a008.
- ↑ Evans E; Heinrich V; Ludwig F; Rawicz W (October 2003). «Dynamic tension spectroscopy and strength of biomembranes». Biophys. J. 85 (4): 2342-50. Bibcode:2003BpJ....85.2342E. PMC 1303459. PMID 14507698. doi:10.1016/S0006-3495(03)74658-X.
- ↑ YashRoy R.C. (1994) Destabilisation of lamellar dispersion of thylakoid membrane lipids by sucrose. Biochimica et Biophysica Acta, vol. 1212, pp. 129-133.https://www.researchgate.net/publication/15042978_Destabilisation_of_lamellar_dispersion_of_thylakoid_membrane_lipids_by_sucrose?ev=prf_pub
- ↑ Weaver JC; Chizmadzhev YA (1996). «Theory of electroporation: A review». Biochemistry and Bioenergetics 41 (2): 135-60. doi:10.1016/S0302-4598(96)05062-3.
- ↑ Papahadjopoulos D; Nir S; Düzgünes N (April 1990). «Molecular mechanisms of calcium-induced membrane fusion». J. Bioenerg. Biomembr. 22 (2): 157-79. PMID 2139437. doi:10.1007/BF00762944.
- ↑ Leventis R; Gagné J; Fuller N; Rand RP; Silvius JR (November 1986). «Divalent cation induced fusion and lipid lateral segregation in phosphatidylcholine-phosphatidic acid vesicles». Biochemistry 25 (22): 6978-87. PMID 3801406. doi:10.1021/bi00370a600.
- ↑ Markin VS; Kozlov MM; Borovjagin VL (October 1984). «On the theory of membrane fusion. The stalk mechanism». Gen. Physiol. Biophys. 3 (5): 361-77. PMID 6510702.
- ↑ Chernomordik LV; Kozlov MM (2003). «Protein-lipid interplay in fusion and fission of biological membranes». Annu. Rev. Biochem. 72 (1): 175-207. PMID 14527322. doi:10.1146/annurev.biochem.72.121801.161504.
- ↑ Georgiev, Danko D .; James F . Glazebrook (2007). «Subneuronal processing of information by solitary waves and stochastic processes». En Lyshevski, Sergey Edward, ed. Nano and Molecular Electronics Handbook. Nano and Microengineering Series. CRC Press. pp. 17-1-17-41. ISBN 978-0-8493-8528-5. Archivado desde el original el 16 de enero de 2016. Consultado el 14 de junio de 2016.
- ↑ Chen YA; Scheller RH (February 2001). «SNARE-mediated membrane fusion». Nat. Rev. Mol. Cell Biol. 2 (2): 98-106. PMID 11252968. doi:10.1038/35052017.
- ↑ Köhler G; Milstein C (August 1975). «Continuous cultures of fused cells secreting antibody of predefined specificity». Nature 256 (5517): 495-7. Bibcode:1975Natur.256..495K. PMID 1172191. doi:10.1038/256495a0.
- ↑ Jordan, Carol A.; Neumann, Eberhard; Sowershi mason, Arthur E. (1989). Electroporation and electrofusion in cell biology. New York: Plenum Press. ISBN 0-306-43043-6.
- ↑ Immordino ML; Dosio F; Cattel L (2006). «Stealth liposomes: review of the basic science, rationale, and clinical applications, existing and potential». Int J Nanomedicine 1 (3): 297-315. PMC 2426795. PMID 17717971. doi:10.2217/17435889.1.3.297.
- ↑ Chonn A; Semple SC; Cullis PR (15 de septiembre de 1992). «Association of blood proteins with large unilamellar liposomes in vivo. Relation to circulation lifetimes». J. Biol. Chem. 267 (26): 18759-65. PMID 1527006. Archivado desde el original el 17 de octubre de 2019. Consultado el 14 de junio de 2016.
- ↑ Boris EH; Winterhalter M; Frederik PM; Vallner JJ; Lasic DD (1997). «Stealth liposomes: from theory to product». Advanced Drug Delivery Reviews 24 (2–3): 165-77. doi:10.1016/S0169-409X(96)00456-5.
- ↑ Maeda H; Sawa T; Konno T (July 2001). «Mechanism of tumor-targeted delivery of macromolecular drugs, including the EPR effect in solid tumor and clinical overview of the prototype polymeric drug SMANCS». J Control Release 74 (1–3): 47-61. PMID 11489482. doi:10.1016/S0168-3659(01)00309-1.
- ↑ Lopes DE; Menezes DE; Kirchmeier MJ; Gagne JF (1999). «Cellular trafficking and cytotoxicity of anti-CD19-targeted liposomal doxorubicin in B lymphoma cells». Journal of Liposome Research 9 (2): 199-228. doi:10.3109/08982109909024786.
- ↑ Matsumura Y; Gotoh M; Muro K; etal (March 2004). «Phase I and pharmacokinetic study of MCC-465, a doxorubicin (DXR) encapsulated in PEG immunoliposome, in patients with metastatic stomach cancer». Ann. Oncol. 15 (3): 517-25. PMID 14998859. doi:10.1093/annonc/mdh092.
- ↑ [1]. Biacore Inc. Retrieved Feb 12, 2009.
- ↑ Nanion Technologies. Automated Patch Clamp Archivado el 31 de marzo de 2010 en Wayback Machine.. Retrieved Feb 28, 2010. (PDF)
- ↑ Bermejo, M. et al. (2004). PAMPA – a drug absorption in vitro model 7. Comparing rat in situ, Caco-2, and PAMPA permeability of fluoroquinolones. Pharm. Sci., 21: 429-441.
- ↑ Avdeef, A. et al. (2005). Caco-2 permeability of weakly basic drugs predicted with the Double-Sink PAMPA pKaflux method. Pharm. Sci., 24: 333-349.
- ↑ Avdeef, A. et al. (2004). PAMPA – a drug absorption in vitro model 11. Matching the in vivo unstirred water layer thickness by individual-well stirring in microtitre plates. Pharm. Sci., 22: 365-374.
- ↑ Dagenais, C. et al. (2009). P-glycoprotein deficient mouse in situ blood–brain barrier permeability and its prediction using an in combo PAMPA model. Eur. J. Phar. Sci., 38(2): 121-137.
- ↑ Sinkó, B. et al. (2009). A PAMPA Study of the Permeability-Enhancing Effect of New Ceramide Analogues. Chemistry & Biodiversity, 6: 1867-1874.
- ↑ Loeb J (December 1904). «The recent development of Biology». Science 20 (519): 777-786. Bibcode:1904Sci....20..777L. PMID 17730464. doi:10.1126/science.20.519.777.
- ↑ Fricke H (1925). «The electrical capacity of suspensions with special reference to blood». Journal of General Physiology 9 (2): 137-52. PMC 2140799. PMID 19872238. doi:10.1085/jgp.9.2.137.
- ↑ Dooren LJ; Wiedemann LR (1986). «On bimolecular layers of lipids on the chromocytes of the blood». Journal of European Journal of Pediatrics 145 (5): 329. doi:10.1007/BF00439232.
- ↑ Gorter E; Grendel F (1925). «On bimolecular layers of lipids on the chromocytes of the blood». Journal of Experimental Medicine 41 (4): 439-43. PMC 2130960. PMID 19868999. doi:10.1084/jem.41.4.439.
- ↑ Sjöstrand FS; Andersson-Cedergren E; Dewey MM (April 1958). «The ultrastructure of the intercalated discs of frog, mouse and guinea pig cardiac muscle». J. Ultrastruct. Res. 1 (3): 271-87. PMID 13550367. doi:10.1016/S0022-5320(58)80008-8.
- ↑ Robertson JD (1960). «The molecular structure and contact relationships of cell membranes». Prog. Biophys. Mol. Biol. 10: 343-418. PMID 13742209.
- ↑ Robertson JD (1959). «The ultrastructure of cell membranes and their derivatives». Biochem. Soc. Symp. 16: 3-43. PMID 13651159.
- ↑ Mueller P; Rudin DO; Tien HT; Wescott WC (June 1962). «Reconstitution of cell membrane structure in vitro and its transformation into an excitable system». Nature 194 (4832): 979-80. Bibcode:1962Natur.194..979M. PMID 14476933. doi:10.1038/194979a0.
- ↑ Bangham, A. D.; Horne, R. W. (1964). «Negative Staining of Phospholipids and Their Structural Modification by Surface-Active Agents As Observed in the Electron Microscope». Journal of Molecular Biology 8 (5): 660-668. PMID 14187392. doi:10.1016/S0022-2836(64)80115-7.
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Bicapa lipídica.
Wikimedia Commons alberga una categoría multimedia sobre Bicapa lipídica.- Avanti Lipids Uno de los más grandes proveedores comerciales de lípidos. Información técnica sobre las propiedades de los lípidos y las técnicas de preparación y manipulación de bicapa lipídica.
- LIPIDAT Una base de datos extensa de las propiedades físicas de los lípidos
- Structure of Fluid Lipid Bilayers Simulaciones y enlaces relacionados con la sección transversal de bicapas lipídicas.
- Lipid Bilayers and the Gramicidin Channel (requires Java plugin) Imágenes y películas que muestran los resultados de la dinámica molecular de las simulaciones de bicapas lipídicas.
- Structure of Fluid Lipid Bilayers, del laboratorio Stephen White en University of California, Irvine
- Animations of lipid bilayer dynamics Archivado el 12 de junio de 2007 en Wayback Machine. (requires Flash plugin)

