Transfección
En sentido amplio, la transfección consiste en la introducción de material genético externo en células eucariotas mediante plásmidos u otras herramientas para la transferencia. En un sentido más reducido, frecuentemente se usa solo para referirse a la introducción de material genético en células animales, prefiriéndose otros términos para otras células (ver Origen del término y relación con otros términos).
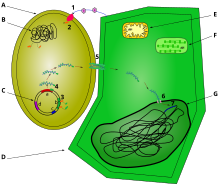
La transfección de células animales generalmente se lleva a cabo abriendo poros o "agujeros" transitorios en la membrana plasmática de las células mediante electroporación, para permitir el paso del material genético (como construcciones de DNA superenrollado o siRNA) aunque pueden ser transfectadas incluso proteínas (como anticuerpos, por ejemplo). Además de la electroporación, se pueden utilizar otras técnicas para efectuar la transfección, como por ejemplo liposomas producidos mediante la mezcla de lípidos catiónicos con el material genético, que se fusionarán con la membrana plasmática celular y depositarán su carga adentro.
Origen del término y relación con otros términos[editar]
El significado original de "transfección" era "infección por transformación", es decir, introducción de DNA o RNA desde un virus procariótico o bacteriófago en las células, resultando en una infección. Al tener el término transformación otro sentido en biología celular animal (un cambio genético que permite la propagación durante largos periodos de células en cultivo, o la adquisición de propiedades típicas de las células cancerígenas), el término transfección adquirió, para células animales, su actual significado de cambio en las propiedades celulares por la introducción de material genética.[1]
Actualmente, se recomienda emplear la siguiente terminología:
- 'Transfección': como término genérico para la transferencia génica, y el más común cuando esta se realiza sobre células animales.
- Transducción: transfección realizada por medio de virus, o que estos realizan de forma natural sobre distintas células.
- Transformación: transfección realizada sobre células no animales (como bacterias y eucariotas como hongos, algas o plantas[2]).
- Conjugación: proceso natural de transfección entre bacterias.
Métodos empleados[editar]
Métodos químicos[editar]
Basados en la formación de complejos que las células sean capaces de adquirir e incorporar, ya sea directo mediante la ruta endocítica o a las membranas. Algunos de los métodos químicos empleados son:[3]
- Método del fosfato cálcico: Basado en la formación de un precipitado, entre el cloruro de calcio y el DNA en una solución salina de fosfatos; estos forman unos agregados que son endocitados/fagocitados por las células. Aparentemente el agregado con calcio protege al DNA de la degradación por las nucleasas celulares.
- Método del DEAE dextrano: Basado en la obtención de complejos entre la resina y DEAE y el DNA, los polímeros del DEAE dextrano tienen una carga que les permite unirse a las cargas muy negativas de las moléculas del DNA. El DNA acomplejado se introduce en las células mediante choque osmótico mediante DMSO o glicerina.
- Método de lipofección: Se basa en la formación de complejos entre lípidos catónicos y DNA, este complejo tiene afinidad por la membrana y permite la entrada del DNA en el cito-sol; una de las vías es la incorporación de liposomas a la membrana y la entrada flip-flap.
- Método del FuGENE: el FuGENE HD es un reactivo comerciado por la casa Promega capaz de transfectar directamente una amplia variedad de células con alta eficacia y baja toxicidad. Se mantiene a temperatura ambiente, y se aplica directamente sobre cultivos celulares en torno al 80% de confluencia.[4] A continuación se vierte directamente el ADN sobre el cultivo, y se incuba entre 24 y 48 horas.
Métodos físicos[editar]
Basados en la introducción mecánica de las moléculas en el interior de la célula.
- Micro-inyección directa: Se emplea en la introducción del DNA recombinante en las células embrionarias en el proceso de obtención de animales transgénicos, esta técnica es muy efectiva pero laboriosa.
- Electroporación: se provoca un aumento significativo de la permeabilidad de la membrana plasmática celular mediante un campo eléctrico aplicado externamente, que genera poros que el ADN puede atravesar. Una variante es la nucleofección, una electroporación optimizada para dirigir ácidos nucleicos no solo al citoplasma, sino al núcleo celular.
- Biobalística: introducción del DNA adherido a micro-partículas que se disparan sobre la célula.
Bioquímicos y físicos[editar]
- Magnetofección es un método de transfección que utiliza la química de las nanopartículas magnéticas y campos magnéticos para concentrar partículas que contienen ácido nucleico y muestras en el útero para apuntar a las células del cuerpo.[5] Este método intenta unir las ventajas de los métodos de transfección bioquímicos (lípidos s catiónicos o poliméricos) y físicos (electroporación, biolísticos) en un solo sistema, excluyendo sus inconvenientes (baja eficacia, toxicidad).
Métodos biológicos[editar]
Basados en procesos naturales, aunque a menudo con eficiencia mejorada mediante técnicas de laboratorio:[6]
- Transformación bacteriana: aunque en sentido amplio se habla de transformación para la mayoría de transfecciones no animales o hechas por métodos no víricos, en sentido estricto se refiere a la propiedad natural de algunas procariotas para captar ADN de su entorno. Se las conoce como "competentes naturales". Sin embargo, hay otras que no presentan de forma natural esta tendencia o no de forma muy eficaz por la especial barrera natural que suponen la pared y membrana bacteriana a la penetración de las macro-moléculas de ácido nucleico eléctricamente cargadas. En estos casos, se requiere una previa preparación de las células receptoras bacterias para inducir su competencia por procedimientos en el laboratorio, donde las células son convertidas en permeables de forma pasiva a través de diversas condiciones que normalmente no ocurren en la naturaleza, como el choque térmico (cambios rápidos de temperatura que permeabilizan la membrana).
- Transformación por Agrobacterium: es un método de transformación utilizado en ingeniería genética de plantas que permite la introducción de ADN exógeno a una célula y la regeneración de esta célula transformada para obtener una planta genéticamente modificada empleando la bacteria Agrobacterium rhizogenes como vector.

- Transducción o transfección viral: el ADN puede ser introducido en células utilizando un virus auxiliar como vector de transfección. Suelen emplearse adenovirus, ya que pueden transferir genes en una amplia variedad de células humanas con alto índice de éxito. Los lentivirus son también muy útiles por su habilidad de transducir células que no se encuentran en mitosis. Existe también la transfección medida por un virus auxiliar: en este sistema la entrada de DNA vírico requiere una infección adicional con un fago intacto, este fago está constantemente mutando en alguna función biológica esencial, lo que trae como consecuencia que su replicación esté total o casi totalmente bloqueada. Este sistema fue descrito por Kaiser y Hogness para el fago Lambda; para la transfección se requiere la asociación entre el DNA transfectante y el DNA del virus auxiliar, su eficiencia depende de la multiplicidad de infección (MOI) del virus auxiliar.
- Conjugación: ciertos fragmentos de ADN pueden ser copiados de una bacteria a otra. La célula donadora provee un elemento génico móvil o conjugativo, generalmente un plásmido o un transposón. Estos fragmentos de ADN contienen (o se les añaden por técnicas de ingeniería genética) los genes responsables de su transferencia a otras bacterias, aunque la mayoría de los plásmidos conjugativos tienen sistemas que aseguran que la célula receptora no tenga ya un elemento similar.
- Hibridación somática: proceso por el cual se obtienen plantas híbridas a partir de la fusión de células o de protoplastos derivados de células somáticas.
Transfección estable y transitoria[editar]
Transfección estable[editar]
Para la generación de líneas celulares estables el transgen de interés debe ser co-transfectado con un marcador de selección que produzca resistencia a una droga. Para cada ensayo de transfección estable se debe monitorear de manera cuidadosa la integración del transgen en el genoma de la célula blanco. El método más utilizado en la investigación clínica para lograr una transfección estable es el de la transfección mediada por virus, también conocida como transducción. Este método es altamente eficiente debido a la naturaleza viral de la integración en el genoma del huésped. Por ejemplo, se ha utilizado el virus de la leucemia murine (MLV) como vector viral para establecer la expresión sostenible de genes de interés en humanos. El MLV integra su DNA en el genoma del hospedero, el cual es posteriormente expresado. El DNA del MLV integrado se replica con el genoma del hospedero, lo que permite la expresión sostenible del gen de interés.[7]
En un experimento de transfección típico se debe permitir a las células recuperarse de la transfección por un periodo de 24 a 72 horas en la ausencia de selección. Esto permite a la célula expresar la cantidad necesaria de la enzima de resistencia para proteger a las células transfectadas establemente contra la droga. Después de 48 o 72 horas de la transfección el medio de cultivo debe ser cambiado y reemplazado con medio nuevo complementado con la droga. La selección se produce dentro de la primera a las tercera semana posterior a la transfección con cambios frecuentes del medio de cultivo selectivo. Finalmente la integridad y número de copias del gen debe ser determinado por Southern Blot.[8]
Transfección transitoria[editar]
La transfección transitoria de genes está sujeta a varios parámetros. El método de transfección, la fisiología celular, el método enzimático o colorimétrico utilizado para cuantificar la actividad del gen reportero, la cantidad de DNA y la normalización de la data. El período de expresión del gen en una transfección génica que varía entre 24 a 72 horas y para el éxito del procedimiento son críticas las condiciones celulares, con las células saludables y las que se encuentren en división las más susceptibles a aceptar plásmidos recombinantes. Para determinar la eficiencia y reproducibilidad de la transfección se puede utilizar un segundo gen reportero que exprese un producto génico que pueda ser detectado y medido de manera sencilla. Tal gen reportero no debe estar presente en el genoma del tipo celular o, en el peor de los casos, puede estar presente pero debe ser expresado en bajos niveles. Es importante recalcar que la eficiencia en la expresión del gen reportero disminuye drásticamente con la integridad del plásmido y su habilidad por llegar al núcleo. Los métodos de transfección transitoria generalmente dirigen el DNA plasmático al citoplasma y no está claro qué porcentaje de estas moléculas son lineales o circulares los alcanzan el núcleo celular. Además, los parámetros experimentales deben ser definidos con cuidado para lograr cierto grado de reproducibilidad. Se ha sugerido que entre los diferentes mecanismos, la difusión pasiva de los plásmidos a través del citoplasma y los poros nucleares representa la forma más probable por la cual los genes reporteros pueden migrar al núcleo celular y ser activados transcripcionalmente. Sin embargo, existe evidencia que sugiere otro mecanismo para explicar la transferencia del DNA plasmático al núcleo celular, basándose en señales de importación del DNA. Se piensa que existe una interacción proteína-DNA plasmático en el citoplasma y que tales interacciones, con factores de transcripción producen señales de localización nuclear, permitiendo la importación de DNA exógeno al núcleo.[9]
Interés biológico de la transfección[editar]
La aplicación más común es su uso en transgénesis. También es muy empleado en investigación básica para estudiar la genética de los organismos y su respuesta ante ciertos cambios.[7] Otro uso es el rescate de marcadores empleado para estudiar la genética de los bacteriófagos; esta técnica consiste en adicionar a un cultivo bacteriano competente un bacteriófago con una mutación en su genoma, y después de su adsorción del DNA fágico añadir al cultivo DNA transfectante procedente de un bacteriófago silvestre. De este modo los genomas de los fagos silvestres de la descendencia provendrán de la recombinación de los dos DNA víricos.
Se ha demostrado que el empleo de combinado de la transfección con el rescate de marcadores es un método útil para la titulación de genes, lo cual permite determinar la proporción relativa de varios marcadores genéticos durante la síntesis de DNA fágico.[10]
Véase también[editar]
Referencias[editar]
- ↑ Iglesias, Juan; Villamonte, Gianfranco; Gonzales, Mauricio (2015). «Transfección de ADN de células de animales». ISSN version en linea 1994-9073. Consultado el 3 de marzo de 2017.
- ↑ Nota Técnica (15 de julio de 2006). «Transfección». Cultek. Archivado desde el original el 21 de febrero de 2016. Consultado el 3 de marzo de 2017.
- ↑ Pietrasanta, Lia (2001). «Tópicos en biofisica moleular». Consultado el 3 de marzo de 2017.
- ↑ Promega Corporation (22 de mayo de 2013), FuGENE® HD Transfection Reagent Video, consultado el 30 de marzo de 2017.
- ↑ Plank C, Zelphati O, Mykhaylyk O (2011). «Magnetically enhanced nucleic acid delivery. Ten years of magnetofection-progress and prospects». Adv. Drug Deliv. Rev. 63 (14–15). pp. 1300-31. PMC 7103316. PMID 21893135. doi:10.1016/j.addr.2011.08.002.
- ↑ Iglesias Artola, Juan M. et al. «DNA TRANSFECTION OF ANIMAL CELLS AS A TOOL USED IN ANIMAL BIOTECHNOLOGY». The Biologist.
- ↑ a b Cortázar, Tania; Walker, John. (2004). «Manipulación genética y el estudio del parásito protozoario Leishmania». Consultado el 4 de marzo de 2017.
- ↑ Lodish, Harvey (2005). «Biologia celular y moleular». Editorial Médica panamericana. Consultado el 4 de marzo de 2017.
- ↑ Castro, Fidel; Portelles, Yangtse. (1997). «Transfección de ADN a células de mamíferos». Consultado el 4 de marzo de 2017.
- ↑ Armenta, Valera, Martínez (2006). «Transfección de células por medio de ondas de choque». Consultado el 5 de marzo de 2017.
