Diferencia entre revisiones de «Trasplante de riñón»
Sin resumen de edición |
m Revertidos los cambios de 189.175.12.246 a la última edición de SieBot |
||
| Línea 37: | Línea 37: | ||
Los donantes a los que no les late el corazón son pacientes que no entran dentro del criterio de [[muerte cerebral]], pero no tienen ninguna oportunidad de recuperación. Normalmente, algunos minutos después de que la muerte se haya producido, rápidamente, el paciente es llevado al quirófano, donde los órganos son extraídos, después de lo cual la solución de almacenamiento es irrigada a través de los órganos directamente. Dado que la sangre ya no está circulando, la [[coagulación]] debe prevenirse con grandes cantidades de agentes [[anticoagulante]]s, como la [[heparina]]. |
Los donantes a los que no les late el corazón son pacientes que no entran dentro del criterio de [[muerte cerebral]], pero no tienen ninguna oportunidad de recuperación. Normalmente, algunos minutos después de que la muerte se haya producido, rápidamente, el paciente es llevado al quirófano, donde los órganos son extraídos, después de lo cual la solución de almacenamiento es irrigada a través de los órganos directamente. Dado que la sangre ya no está circulando, la [[coagulación]] debe prevenirse con grandes cantidades de agentes [[anticoagulante]]s, como la [[heparina]]. |
||
== Compatibilidad |
== Compatibilidad == |
||
El donante y el receptor tienen que ser de [[grupo sanguíneo|grupo sanguíneo ABO]] compatible, e idealmente deben compartir tantos [[HLA]] y "[[antígeno]]s de menor importancia" como sea posible. Esto disminuye el riesgo de [[rechazo de trasplante|rechazo]], la necesidad de [[diálisis renal|diálisis]], y de un futuro trasplante. El riesgo de rechazo después del trasplante puede ser reducido si el donante y el receptor comparten tantos antígenos HLA como sea posible, si el receptor no estuviera ya sensibilizado a antígenos HLA de donantes potenciales, y si los niveles de inmunosupresores son mantenidos en el rango apropiado. En los Estados Unidos, hasta un 17% de todos los trasplantes riñón de donantes fallecidos tienen HLA que concuerdan. |
|||
La evaluación inmunológica pretrasplante renal comprende los siguientes exámenes: (a) determinación del grupo sanguíneo ABO, (b) crossmatch, (c) evaluación de la reactividad contra el panel y (d) tipificación HLA del receptor y de sus posibles donantes. |
La evaluación inmunológica pretrasplante renal comprende los siguientes exámenes: (a) determinación del grupo sanguíneo ABO, (b) crossmatch, (c) evaluación de la reactividad contra el panel y (d) tipificación HLA del receptor y de sus posibles donantes. |
||
Revisión del 00:17 30 sep 2009
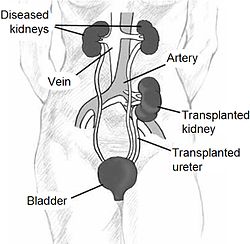
El trasplante de riñón o trasplante renal es el trasplante de un riñón en un paciente con enfermedad renal terminal. Dependiendo de la fuente del órgano receptor, el trasplante de riñón es típicamente clasificado como de donante fallecido (anteriormente conocido como cadavérico), o como trasplante de donante vivo. Los trasplantes renales de donantes vivos se caracterizan más a fondo como trasplante emparentado genéticamente (pariente-vivo) o trasplante no emparentado (no emparentado-vivo), dependiendo de si hay o no una relación biológica entre el donante y el receptor.
Historia
Los primeros trasplantes de riñón exitosos fueron hechos en Boston y París en 1954. El trasplante fue hecho entre los gemelos idénticos, para eliminar cualquier problema de una reacción inmune. La popularización del trasplante renal fue lenta. Por ejemplo, el primer trasplante de riñón en el Reino Unido no ocurrió hasta 1960 cuando Michael Woodruff realizó uno en Edimburgo entre gemelos idénticos. El trasplante de donante difunto se introdujo en 1964, cuando comenzó el uso rutinario de medicamentos para prevenir y tratar el rechazo agudo. El riñón era el órgano más fácil a trasplantar, pues la prueba de compatibilidad de tejidos era simple, el órgano era relativamente fácil de extirpar e implantar, los donantes vivos podían ser usados sin dificultad, y en caso de fallo, la diálisis renal estaba disponible desde los años 1940. La prueba de compatibilidad de tejidos es esencial para el éxito, las primeras tentativas en los años 1950 en personas que padecían la enfermedad de Bright habían sido muy poco exitosas. El trasplante fue hecho por el Dr. Joseph Edward Murray, quien recibió el premio Nobel de medicina en 1990. El donante está vivo todavía en fecha de 2005; el receptor murió ocho años después del trasplante.
Indicaciones
La indicación para el trasplante de riñón es la enfermedad renal en etapa terminal (ESRD), sin importar la causa primaria. Las enfermedades comunes que conducen a la ESRD incluyen la hipertensión, infecciones, diabetes mellitus y glomerulonefritis; las causas genéticas incluyen enfermedad poliquística renal. La mayoría de los receptores de trasplante renales está en hemodiálisis en el momento del trasplante. Sin embargo, individuos con insuficiencia renal crónica que tienen disponible a un donante vivo eligen a menudo ser sometidos al trasplante antes de que la diálisis sea necesaria.
Contraindicaciones
Hay pocos datos de trasplantes en personas de más de 80 años, y muchos centros no trasplantarán dichos pacientes. Sin embargo, esto probablemente cambiará pronto.
Recientemente el cáncer, el abuso de sustancias activas, o la falta en adherirse a los regímenes médicos prescritos pueden hacer a alguien inelegible para un trasplante.
Fuentes de riñones
Alrededor de la mitad de los trasplantes del riñón son de donantes vivos. La otra mitad son de donantes fallecidos. Puesto que los medicamentos para prevenir el rechazo son tan efectivos, los donantes no necesitan ser genéticamente similares al receptor.
Donantes vivos
Los donantes vivos potenciales son cuidadosamente evaluados en su cimientos médicos y psicológicos. Esto asegura que el donante está en buena forma para la cirugía y no tiene ninguna enfermedad del riñón, mientras que se confirma que el donante es puramente altruista. Tradicionalmente, el procedimiento para el donante ha sido a través de una incisión pero la donación viva cada vez más ha procedido por cirugía laparoscópica. Esto reduce el dolor y acelera vuelta al trabajo para el donante con efecto mínimo sobre el resultado del riñón. En forma total, los receptores de riñones de donantes vivos van extremadamente bien en comparación con los donantes fallecidos.
Donantes fallecidos
Los donantes difuntos pueden ser divididos en dos grupos:
- Donantes en muerte cerebral (BD)
- Donantes en corazón parado (NHB)
Aunque los donantes de muerte cerebral (o con 'corazón latiendo') son considerados que están muertos, el corazón del donante continúa bombeando y manteniendo la circulación. Esto permite que los cirujanos comiencen a operar mientras los órganos todavía están siendo perfundidos. Durante la operación, la aorta será canulada, y después la sangre de los pacientes será sustituida por una solución helada de almacenamiento, como UW (Viaspan), HTK o Perfadex (más de una solución puede ser usada simultáneamente dependiendo de cuáles son los órganos a trasplantar). Debido a la temperatura de la solución, una vez que se vierten grandes cantidades de solución de cloruro de sodio frío sobre los órganos (para un rápido enfriamiento éstos) el corazón deja de bombear.
Los donantes a los que no les late el corazón son pacientes que no entran dentro del criterio de muerte cerebral, pero no tienen ninguna oportunidad de recuperación. Normalmente, algunos minutos después de que la muerte se haya producido, rápidamente, el paciente es llevado al quirófano, donde los órganos son extraídos, después de lo cual la solución de almacenamiento es irrigada a través de los órganos directamente. Dado que la sangre ya no está circulando, la coagulación debe prevenirse con grandes cantidades de agentes anticoagulantes, como la heparina.
Compatibilidad
El donante y el receptor tienen que ser de grupo sanguíneo ABO compatible, e idealmente deben compartir tantos HLA y "antígenos de menor importancia" como sea posible. Esto disminuye el riesgo de rechazo, la necesidad de diálisis, y de un futuro trasplante. El riesgo de rechazo después del trasplante puede ser reducido si el donante y el receptor comparten tantos antígenos HLA como sea posible, si el receptor no estuviera ya sensibilizado a antígenos HLA de donantes potenciales, y si los niveles de inmunosupresores son mantenidos en el rango apropiado. En los Estados Unidos, hasta un 17% de todos los trasplantes riñón de donantes fallecidos tienen HLA que concuerdan.
La evaluación inmunológica pretrasplante renal comprende los siguientes exámenes: (a) determinación del grupo sanguíneo ABO, (b) crossmatch, (c) evaluación de la reactividad contra el panel y (d) tipificación HLA del receptor y de sus posibles donantes.
Procedimiento
Puesto que en la mayoría de los casos los riñones existentes, que apenas están funcionamiento, no son extirpados, el nuevo riñón normalmente es colocado en un lugar diferente del riñón original (a menudo en la fosa ilíaca), y como resultado a menudo es necesario usar una fuente diferente de sangre:
- La arteria renal, previamente ramificada de la aorta abdominal en el donante, a menudo es conectada con la arteria ilíaca externa en el receptor.
- La vena renal, que previamente drenaba a la vena cava inferior en el donante, a menudo es conectada con la vena ilíaca externa en el receptor.
Trasplante de riñón y páncreas
- Véase también: trasplante de páncreas.
Ocasionalmente, el riñón es trasplantado junto con el páncreas. Esto es un hecho en pacientes con diabetes mellitus tipo I, en la cual la diabetes se debe a la destrucción de las células beta del páncreas y en la que ha causado la insuficiencia renal (nefropatía diabética). Casi siempre, se trasplantan órganos de donantes difuntos en estos casos. Solamente se han hecho algunos trasplantes (parciales) de donantes vivos. Para los individuos con diabetes e insuficiencia renal, las ventajas de un trasplante temprano de un donante vivo son aproximadamente iguales a los riesgos de la diálisis continua hasta que un riñón y un páncreas combinados estén disponibles de un donante difunto.
Estos procedimientos son comúnmente abreviados como sigue:
- "trasplante SKP", para "trasplante riñón-páncreas simultáneo"
- "trasplante PAK", para "trasplante de páncreas después del de riñón"
(Por contraste, "PTA" se refiere al "trasplante de páncreas solamente").
El páncreas puede venir de un donante fallecido así como de uno vivo. Un paciente puede conseguir un riñón vivo seguido por un donante de páncreas en una fecha posterior (PAK, o páncreas después de riñón) o un páncreas-riñón combinado de un donante (SKP, riñón-páncreas simultáneo).
El trasplante sólo de las células islote del páncreas todavía está en la etapa experimental, pero se muestra prometedor. Esto implica tomar un páncreas de donante fallecido, romperlo, y extraer las células de islote que producen la insulina. Entonces, las células son inyectadas a través de un catéter en el receptor y ellas generalmente se alojan en el hígado. El receptor todavía necesita tomar inmunosupresores para evitar el rechazo, pero no se requiere ninguna cirugía. La mayoría de la gente necesita 2 ó 3 de tales inyecciones, y muchas no quedan totalmente libres de insulina.
Post operación
La cirugía del trasplante dura cerca de 3 horas. El riñón del donante será colocado en el bajo abdomen. Los vasos sanguíneos del riñón del donante serán conectados con las arterias y venas en el cuerpo receptor. Una vez hecho esto, la sangre vuelve a fluir a través del riñón, minimizándose el tiempo de isquemia. En la mayoría de los casos, el riñón pronto comenzará a producir la orina. Puesto que la orina es estéril, ésta no tiene ningún efecto en la operación. El último paso es conectar el uréter del riñón del donante con la vejiga del receptor.
El riñón nuevo normalmente comienza a funcionar inmediatamente después de la cirugía, pero dependiendo de la calidad del órgano éste puede tardar algunos días (riñón vago). La estancia habitual del receptor en el hospital está entre 4 y 7 días. Si se presentan complicaciones, se pueden administrar medicinas adicionales para ayudar al riñón a producir orina.
Las medicinas son usadas para suprimir el sistema inmune y evitar el rechazo del riñón del donante. Estas medicinas deben ser tomadas de por vida por el paciente. Hoy, el tratamiento más común de medicamentos es: tacrolimus, micofenolato, y prednisona. Algunos pacientes pueden tomar ciclosporina, rapamicina, o azathioprine, en lugar de los primeros.
El rechazo agudo puede ocurrir en el 10% al 25% de las personas durante los primeros 60 días después del trasplante. El rechazo no significa la pérdida del órgano, sino que puede requerir un tratamiento adicional[1].
Complicaciones
Los problemas después de un trasplante pueden incluir:
- Rechazo del trasplante (hiperagudo, agudo, o crónico)
- Infecciones y sepsis debido a las drogas inmunosupresoras que son requeridas para disminuir el riesgo de rechazo
- Desorden linfoproliferativo post trasplante (una forma de linfoma debido a los inmunosupresores)
- Desequilibrios en los electrolitos, incluyendo el calcio y el fosfato, que pueden conducir, entre otras cosas, a problemas en los huesos.
- Otros efectos secundarios de los medicamentos incluyendo la inflamación y la ulceración gastrointestinales del estómago y del esófago, hirsutismo (excesivo crecimiento del pelo en un patrón masculino), pérdida del pelo, obesidad, acné, diabetes mellitus (tipo 2), hipercolesterolemia y otros.
- El tiempo medio de vida de un riñón trasplantado es de entre 10 a 15 años. Cuando un trasplante falla un paciente puede optar por un segundo trasplante, y puede tener que volver a la diálisis por algún tiempo.
- Infeccion por cytomegalovirus o/y pargovirus debido a la inmunosupresion
Prognosis
Estudios recientes han indicado que el trasplante de riñón es un procedimiento para alargar la vida. El paciente tipo vivirá entre 10 a 15 años más con un trasplante de riñón que permaneciendo en diálisis. Los años de vida ganados son más para pacientes más jóvenes, pero incluso los pacientes de 75 años, el el grupo de edad más avanzada para el que hay datos, ganan un promedio de 4 años de vida con un trasplante de riñón. La calidad de vida aumenta, desapareciendo problemas relacionados con la diálisis como la restricción de líquidos, la dieta estricta, el cansancio, los calambres, la afonía...
Algunos estudios parecen sugerir que cuanto más tiempo haya permanecido un paciente en diálisis antes del trasplante, menos tiempo durará el riñón. No está claro por qué ocurre esto, pero subraya la necesidad de remitir rápidamente a un programa de trasplante a un paciente una vez detectada la insuficiencia renal crónica. Idealmente, el trasplante renal debe producirse antes de que el paciente comience en diálisis.
Por lo menos tres atletas profesionales han regresado a sus deportes después de recibir un trasplante – Los jugadores del NBA Sean Elliott y Alonzo Mourning, Jonah Lomu, una leyenda del rugby neozelandés e Ivan Klasnic, un futbolista internacional croata.
Requisitos del trasplante de riñón
Los requisitos del trasplante de riñón varían de un programa a otro y de un país a otro. Muchos programas ponen límites en la edad (por ejemplo, la persona debe tener menos de 69 años de edad cuando se ingresa en la lista de espera) y requiere que la persona deba estar en buen estado de salud (aparte de la enfermedad del riñón).
Una enfermedad cardiovascular significativa, las enfermedades infecciosas terminales incurables (por ejemplo, SIDA) y el cáncer a menudo son criterios de exclusión del trasplante. Además, se comprueba que los candidatos serán muy cuidadosos con los tratamientos médicos postrasplante, ya que deberán tomar esa medicación de por vida porque es esencial para la supervivencia del trasplante. Pueden ser excluidas las personas con enfermedades mentales y/o con significativos problemas de abuso de sustancias.
Estadísticas del trasplante de riñón
| País | Año | Donante fallecido |
Donante vivo |
Total de trasplantes |
|---|---|---|---|---|
| Canadá[1] | 2000 | 724 | 388 | 1,112 |
| Francia[2] | 2003 | 1.991 | 136 | 2,127 |
| Italia[2] | 2003 | 1.489 | 135 | 1.624 |
| España[2] | 2003 | 1.991 | 60 | 2.051 |
| Reino Unido[2] | 2003 | 1.297 | 439 | 1.736 |
| Estados Unidos[3] | 2003 | 8.667 | 6.479 | 15.137 |
| Pakistán - SIUT[cita requerida] | ? | ? | ? | 1.600 |
- El activista aborigen australiano Charles Perkins, es el receptor superviviente con más tiempo de un trasplante de riñón, dado que vivió 28 años con su órgano donado.
- El instituto de Sind de Urología y de Trasplante (SIUT - www.siut.org) es el único hospital en el mundo que realiza tratamiento gratuitamente para trasplante.
Referencias
- Brook NR, Nicholson ML (2003). «Kidney transplantation from non heart-beating donors». Surgeon 1 (6): 311-322. PMID 15570790.
Notas
- ↑ «Facts and FAQs». Canada's National Organ and Tissue Information Site. Health Canada. 16 July 2002. Archivado desde el original el 4 de abril de 2005. Consultado el 6 de enero de 2007.
- ↑ a b c d «European Activity Comparison 2003» (gif). UK Transplant. March de 2004. Consultado el 6 de enero de 2007.
- ↑ «National Data Reports». The Organ Procurement and Transplant Network (OPTN). dynamic. Consultado el 6 de enero de 2007. the link is to a query interface; Choose Category = Transplant, Organ = Kidney, and select the 'Transplant by donor type' report link
Enlaces externos
- Plantilla:MedlinePlusOverview
- [2] en eMedicine
- Patient-oriented summary at emedicinehealth.com
- Overview at mvm.ed.ac.uk - undergraduate created but high quality
- Kidney transplantation and renal disease
- International Kidney Transplantation Association
- The Kidney Patient Guide
- Sindh Institute of Urology and Transplantation
- Immune Tolerance Network
- What to Expect If Your Child Needs a Kidney Transplant from Seattle Children's Hospital
- Información sobre trasplante renal para médicos
