Ácido metacrílico
| Ácido metacrílico | ||
|---|---|---|
 | ||
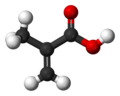 | ||
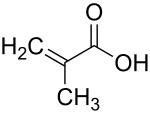
| Nombre IUPAC | ||
| Ácido 2-metilpropenoico | ||
| General | ||
| Otros nombres | Ácido α-metilacrílico | |
| Fórmula molecular | C4H6O2 | |
| Identificadores | ||
| Número CAS | 79-41-4[1] | |
| Número RTECS | OZ2975000 | |
| ChEBI | 25219 | |
| ChEMBL | CHEMBL1213531 | |
| ChemSpider | 3951 | |
| PubChem | 4093 | |
| UNII | 1CS02G8656 | |
| Propiedades físicas | ||
| Apariencia | blanco | |
| Densidad | 1015 kg/m³; 1015 g/cm³ | |
| Masa molar | 8606 g/mol | |
| Punto de fusión | 15 °C (288 K) | |
| Punto de ebullición | 161 °C (434 K) | |
| Peligrosidad | ||
| NFPA 704 |
2
3
2
| |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El ácido metacrílico es compuesto orgánico perteneciente al grupo de los ácidos carboxílicos, líquido y viscoso de olor desagradable. Polimeriza fácilmente por calentamiento intenso o presencia de luz, oxígeno, agentes oxidantes (tales como peróxidos), o la presencia de trazas de ácido clorhídrico. Normalmente contiene inhibidores para prevenir su propia polimerización.
Es soluble en agua caliente y miscible con la mayoría de disolventes orgánicos. El ácido metacrílico es producido industrialmente a gran escala como un precursor para sus ésteres, especialmente metacrilato de metilo (MMA) y polimetacrilato de metilo (PMMA). Los metacrilatos tienen numerosos usos, sobre todo en la fabricación de polímeros. Otro producto de polimerización de este ácido es el ácido polimetacrílico (PMAA).
Debido a la pequeña presión de vapor de este líquido, se evapora fácilmente, y por encima de 77 °C pueden formarse mezclas explosivas vapor/aire, por lo que al calentarlo se corre peligro de incendio o explosión. La sustancia se descompone al calentarla intensamente produciendo humos acres.
Propiedades químicas
[editar]El ácido metacrílico es altamente reactivo con grupos carboxilo, ésteres y vinilo.[2]
Las principales reacciones que da el ácido metacrílico son:[2]
- Adiciones al doble enlace carbono-carbono: La adición de grupos cianuro, halogenuros, alcoholes, sulfuros o aminas a este doble enlace del ácido metacrílico conduce a los derivados del ácido 2-metilpropanoico.
- Reacción de Diels-Alder: la reacción de dienos con el doble enlace del ácido metacrílico (que actúa como dienófilo) produce la cicloadición [4+2] que lleva el nombre de reacción de Diels-Alder.
- Esterificación: al reaccionar con distintos alcoholes se producen los correspondientes ésteres llamados metacrilatos.
- Polimerización: este ácido polimeriza fácilmente en presencia de iniciadores de radicales libres (como peróxidos o UV) formando el ácido polimetacrílico (PMAA). Los monómeros pueden ser recuperados después de la polimerización por calentamiento a temperaturas superiores a 300 °C.
Referencias
[editar]- ↑ Número CAS
- ↑ a b Bauer, William Jr. (2000). Ullmann's Encyclopedia of Industrial Chemistry, ed. Methacrylic Acid and Derivatives. Wiley-VCH Verlag GmbH & Co.

