Vestigialidad humana

En el contexto de la evolución humana, la vestigialidad humana involucra aquellos rasgos (como órganos o comportamientos) que ocurren en los humanos que han perdido la totalidad o la mayor parte de su función original a través de la evolución. Aunque las estructuras llamadas vestigiales a menudo parecen carecer de función, una estructura vestigiales puede retener funciones menores o desarrollar otras menores. En algunos casos, las estructuras una vez identificadas como vestigiales simplemente tenían una función no reconocida.
Los ejemplos de vestigios humanos son numerosos, incluidos el anatómico (como el coxis humano, las muelas del juicio y la esquina interna del ojo), el comportamiento (la piel de gallina y el reflejo de prensión) y molecular (pseudogenes). Muchas características humanas también son vestigiales en otros primates y animales relacionados.
Historia[editar]
Charles Darwin enumeró una serie de supuestos rasgos vestigiales humanos, que denominó rudimentarios, en El origen del hombre (1890). Estos incluyen los músculos de la oreja, las muelas del juicio, el apéndice, el hueso de la cola (Coxis), el vello corporal y el pliegue semilunar en la esquina del ojo. Darwin también comentó sobre la naturaleza esporádica de muchas características vestigiales, especialmente la musculatura. Haciendo referencia al trabajo del anatomista William Turner, Darwin destacó una serie de músculos esporádicos que identificó como vestigios remanentes del panículo carnoso, particularmente el músculo esternal.[1][2]
En 1893, Robert Wiedersheim publicó The Structure of Man, un libro sobre la anatomía humana y su relevancia para la historia evolutiva del hombre. Este libro contenía una lista de 86 órganos humanos que consideraba vestigiales, o como explicó el mismo Wiedersheim: "Los órganos se han vuelto completamente o en parte sin función, algunos aparecen en el embrión solo, otros presentes durante la vida de manera constante o inconstante. que se puede llamar justamente Vestigial ".[3] Su lista de órganos supuestamente vestigiales incluía muchos de los ejemplos en esta página, así como otros que erróneamente se creía que eran puramente vestigiales, como la glándula pineal, el timo y la glándula pituitaria. Algunos de estos órganos que habían perdido sus funciones obvias y originales más tarde resultaron haber conservado funciones que no habían sido reconocidas antes del descubrimiento de hormonas o de muchas de las funciones y tejidos del sistema inmune.[4][5] Ejemplos incluidos:
- el papel de la pineal en la regulación del ritmo circadiano (aún no se conocía la función ni la existencia de la melatonina);
- el descubrimiento del papel del timo en el sistema inmune yace muchas décadas en el futuro; permaneció como un órgano misterioso hasta después de mediados del siglo XX;
- la hipófisis y el hipotálamo con sus muchas y variadas hormonas estaban lejos de ser entendidos, y mucho menos la complejidad de sus interrelaciones.
Históricamente, hubo una tendencia no solo a descartar el apéndice vermiforme por ser inútilmente vestigial, sino también por un peligro anatómico, una responsabilidad ante una inflamación peligrosa. Todavía a mediados del siglo XX, muchas autoridades acreditadas no concedieron ninguna función beneficiosa.[6] Esta fue una opinión apoyada, o quizás inspirada, por el propio Darwin en la edición de 1874 de su libro El origen del hombre y la selección en relación al sexo. La patente responsabilidad del órgano ante la apendicitis y su papel poco conocido dejó al apéndice como culpable de una serie de condiciones posiblemente no relacionadas. Por ejemplo, en 1916, un cirujano afirmó que la extirpación del apéndice había curado varios casos de neuralgia del trigémino y otros dolores nerviosos en la cabeza y la cara, aunque afirmó que la evidencia de apendicitis en esos pacientes no era concluyente.[7] El descubrimiento de hormonas y principios hormonales, especialmente por Bayliss y Starling, argumentó en contra de estos puntos de vista, pero a principios del siglo XX, todavía quedaba una gran cantidad de investigación fundamental sobre las funciones de grandes partes del tracto digestivo. En 1916, un autor consideró necesario argumentar en contra de la idea de que el colon no tenía una función importante y que "... la desaparición definitiva del apéndice es una acción coordinada y no necesariamente asociada con inflamaciones frecuentes como las que estamos presenciando en el humano..."[8]
Hubo una larga historia de dudas sobre tales puntos de vista despectivos. Alrededor de 1920, el prominente cirujano Kenelm Hutchinson Digby documentó observaciones previas, que se remontaban a más de treinta años, que sugerían que los tejidos linfáticos, como las amígdalas y el apéndice, pueden tener funciones inmunológicas sustanciales.
Anatómico[editar]
Apéndice[editar]

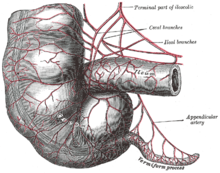
En los humanos modernos, el apéndice vermiforme es un vestigio de un órgano redundante que en las especies ancestrales tenía funciones digestivas, al igual que lo hace en pobo
ares.[9] Algunos animales herbívoros, como los conejos, tienen un apéndice vermiforme terminal y ciego que aparentemente tienen parches de tejido con funciones inmunitarias y también pueden ser importantes para mantener la composición de la flora intestinal. Sin embargo, no parece tener mucha función digestiva, y no está presente en todos los herbívoros, incluso en aquellos con grandes ciegos.[10] Sin embargo, como se muestra en las imágenes adjuntas, el apéndice humano es casi comparable al tamaño del conejo, aunque el ciego se reduce a un único bulto donde el íleon desemboca en el colon.[6] Algunos animales carnívoros también pueden tener apéndices, pero rara vez tienen más que ciegos vestigiales.[11] En línea con la posibilidad de que los órganos vestigiales desarrollen nuevas funciones, algunas investigaciones sugieren que el apéndice puede proteger contra la pérdida de bacterias simbióticas que ayudan a la digestión, aunque es poco probable que sea una función nueva, dada la presencia de apéndices vermiformes en muchos herbívoros.[12][13] Las poblaciones de bacterias intestinales atrincheradas en el apéndice pueden apoyar el restablecimiento rápido de la flora del intestino grueso después de una enfermedad, envenenamiento o después de que un tratamiento con antibióticos agota o causa cambios nocivos en la población bacteriana del colon.[14] Un estudio de 2013, sin embargo, refuta la idea de una relación inversa entre el tamaño del ciego y el tamaño y la presencia del apéndice. Está ampliamente presente en euarchontoglires (un superorden de mamíferos que incluye roedores y primates) y también ha evolucionado convergentemente en los marsupiales diprotodontes, monotremas, y es muy diverso en tamaño y forma, lo que podría sugerir que no es vestigial. Los investigadores deducen que el apéndice tiene la capacidad de proteger bacterias buenas en el intestino. De esta forma, cuando el intestino se ve afectado por una diarrea u otra enfermedad que limpia los intestinos, las bacterias buenas en el apéndice pueden repoblar el sistema digestivo y mantener a la persona sana.[15]
Coxis[editar]
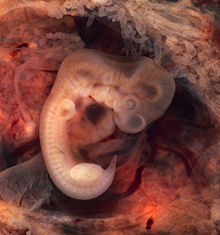
El coxis o cóccix es el remanente de una cola perdida. Todos los mamíferos tienen cola en algún momento de su desarrollo; en humanos, está presente por un período de 4 semanas, durante las etapas 14 a 22 de la embriogénesis humana.[16] Esta cola es más prominente en embriones humanos de 31-35 días de edad.[17] Sin embargo, en las próximas semanas de desarrollo, la cola desaparece, y con el tiempo las vértebras se fusionan para formar el coxis. El coxis, ubicado al final de la columna vertebral, ha perdido su función original para ayudar al equilibrio y la movilidad, aunque todavía cumple algunas funciones secundarias, como ser un punto de unión para los músculos, lo que explica por qué no se ha degradado aún más. El coxis sirve como sitio de unión para tendones, ligamentos y músculos. También funciona como un punto de inserción de algunos de los músculos del piso pélvico. Los humanos y sus parientes simios se distinguen de otros grupos de primates en parte por su ausencia de cola, aunque no está claro por qué los monos perdieron sus colas. En casos raros, el defecto congénito produce una estructura de cola corta que está presente en el momento del nacimiento. Veintitrés casos de bebés humanos nacidos con tal estructura se han reportado en la literatura médica desde 1884.[18][19] En casos raros como estos, se determinó que la columna vertebral y el cráneo eran completamente normales. La única anormalidad era la de una cola de aproximadamente doce centímetros de largo. Estas colas pudieron ser eliminadas quirúrgicamente, y las personas han reanudado sus vidas normales.[20]
Muelas del juicio[editar]
Las muelas del juicio son terceros molares vestigiales que los antepasados humanos utilizaron para ayudar a moler el tejido de la planta. La postulación común es que los cráneos de los ancestros humanos tenían mandíbulas más grandes con más dientes, que posiblemente se utilizaron para ayudar a masticar el follaje para compensar la falta de capacidad para digerir de manera eficiente la celulosa que forma la pared celular de una planta. A medida que las dietas humanas cambiaron, las mandíbulas más pequeñas se seleccionaron naturalmente, sin embargo, los terceros molares, o "muelas del juicio", todavía se desarrollan comúnmente en las bocas humanas.[21] Actualmente, las muelas del juicio se han vuelto inútiles e incluso dañinas en la medida en que a menudo se realizan procedimientos quirúrgicos para extirparlas.
La agenesia (falla en el desarrollo) de las muelas del juicio en las poblaciones humanas varía desde cero en los aborígenes de Tasmania hasta casi el 100% en los indígenas mexicanos.[22] La diferencia está relacionada con el gen PAX9 (y quizás otros genes).[23]
Órgano de Jacobson[editar]
En algunos animales, el órgano de Jacobson, conocido también como órgano vomeronasal (VNO) es parte de un segundo sentido del olfato completamente separado, conocido como el sistema olfativo accesorio. Se han realizado muchos estudios para determinar si hay presencia real de un VNO en seres humanos adultos. Trotier et al.[24] estimó que alrededor del 92% de los sujetos que no habían tenido cirugía septal tenían al menos un VNO intacto. Kjaer y Fisher Hansen, por otro lado,[25] declararon que la estructura del VNO desapareció durante el desarrollo fetal, como ocurre con algunos primates.[26] Sin embargo, Smith y Bhatnagar (2000)[27] afirmaron que Kjaer y Fisher Hansen simplemente omitieron la estructura en fetos viejos. Won (2000) encontró evidencia de un VNO en 13 de sus 22 cadáveres (59.1%) y en 22 de sus 78 pacientes vivos (28.2%).[28] Dados estos hallazgos, algunos científicos han argumentado que hay un VNO en seres humanos adultos.[29][30] Sin embargo, la mayoría de los investigadores han tratado de identificar la apertura del órgano vomeronasal en humanos, en lugar de identificar la estructura epitelial tubular en sí.[31] Por lo tanto, se ha argumentado que tales estudios, que emplean métodos de observación macroscópicos, a veces han omitido o incluso han identificado erróneamente el órgano vomeronasal.[32]
Entre los estudios que usan métodos microanatómicos, no hay evidencia de que los seres humanos tengan neuronas sensoriales activas, como las que funcionan en los sistemas vomeronasales de otros animales.[32][33] Además, hasta la fecha no hay evidencia que sugiera que haya conexiones de nervios y axones entre las células receptoras sensoriales existentes que puedan estar en el VNO humano adulto y en el cerebro.[34] Del mismo modo, no hay evidencia de ningún bulbo olfatorio accesorio en seres humanos adultos,[32] y los genes clave implicados en la función de VNO en otros mamíferos se han convertido en pseudogenes en seres humanos. Por lo tanto, mientras se debate la presencia de una estructura en seres humanos adultos, una revisión de la literatura científica realizada por Tristram Wyatt concluyó que "la mayoría en el campo ... son escépticos sobre la probabilidad de un VNO funcional en seres humanos adultos con la evidencia actual".[35]
Oreja[editar]
Las orejas de un mono macaco y la mayoría de los otros monos tienen músculos mucho más desarrollados que los de los humanos, y por lo tanto tienen la capacidad de mover sus oídos para escuchar mejor las posibles amenazas.[36] Los seres humanos y otros primates como el orangután y el chimpancé, sin embargo, tienen músculos de los oídos que están mínimamente desarrollados y no son funcionales, pero aún lo suficientemente grandes como para ser identificables.[9] Un músculo unido a la oreja que no puede mover la oreja, por la razón que sea, ya no puede decirse que tenga ninguna función biológica. En los humanos existe una variabilidad en estos músculos, tal que algunas personas pueden mover sus orejas en varias direcciones, y es posible que otros obtengan dicho movimiento mediante ensayos repetidos.[9][37] En tales primates, la incapacidad de mover la oreja se compensa principalmente por la capacidad de girar la cabeza en un plano horizontal, una habilidad que no es común para la mayoría de los monos: una función que una vez proporcionaba una estructura ahora es reemplazada por otra.[38]
La estructura externa de la oreja también muestra algunas características vestigiales, como el nodo o punto en la hélice de la oreja conocido como el tubérculo de Darwin que se encuentra en alrededor del 10% de la población.
Ojo[editar]
La plica semilunar es un pequeño pliegue de tejido en la esquina interna del ojo. Es el vestigio remanente de la membrana nictitante, un órgano que es completamente funcional en algunas otras especies de mamíferos.[39] Sus músculos asociados también son vestigiales.[9] Se sabe que solo una especie de primate, el Calabar angwantibo, tiene una membrana nictitante en funcionamiento.[40]
El músculo orbital es un músculo vestigial o rudimentario no estriado (músculo liso) del ojo que cruza desde el surco infraorbitario y la fisura esfenomaxilar y está íntimamente unido con el periostio de la órbita. Fue descrito por Johannes Peter Müller y a menudo se llama músculo de Müller. El músculo forma una parte importante de la pared orbitaria lateral en algunos animales, pero en los humanos no se sabe que tenga ninguna función significativa. [41][42]
Sistema reproductivo[editar]
Genitales[editar]
En los genitales internos de cada sexo humano, hay algunos órganos residuales de los conductos mesonéfrico y paramesonéfrico durante el desarrollo embrionario:
Las estructuras vestigiales humanas también incluyen remanentes embriológicos sobrantes que una vez cumplieron una función durante el desarrollo, como el ombligo, y estructuras análogas entre sexos biológicos. Por ejemplo, los hombres también nacen con dos pezones, que no cumplen una función en comparación con las mujeres.[43] Con respecto al desarrollo genitourinario, los genitales internos y externos de los fetos masculinos y femeninos tienen la capacidad de formar total o parcialmente su fenotipo análogo del sexo biológico opuesto si se exponen a una falta/sobreabundancia de andrógenos o al gen SRY durante el desarrollo fetal.[44][45] Ejemplos de vestigios remanentes de desarrollo genitourinario incluyen el himen, que es una membrana que rodea o cubre parcialmente la abertura vaginal externa que se deriva del tubérculo sinusal durante el desarrollo fetal y es homóloga al colículo seminal masculino.[46] Algunos investigadores han planteado la hipótesis de que la persistencia del himen puede proporcionar protección temporal contra la infección, ya que separa el lumen vaginal de la cavidad del seno urogenital durante el desarrollo.[47] Otros ejemplos incluyen el glande y el clítoris, los labios menores y el pene ventral, y los folículos ováricos y los túbulos seminíferos.[46]
Musculatura[editar]
Se cree que algunos músculos del cuerpo humano son vestigiales, ya sea por su tamaño reducido en comparación con los músculos homólogos de otras especies, por haberse vuelto principalmente tendinosos o por ser muy variables en su frecuencia dentro o entre las poblaciones.
Cabeza[editar]
El Occipitalis Menor es un músculo en la parte posterior de la cabeza que normalmente se une a los músculos auriculares de la oreja. Este músculo tiene una frecuencia muy esporádica, siempre presente en malayos, en el 56% de los africanos, en el 50% de los japoneses, en el 36% de los europeos, y no existe en el pueblo Khoikhoi del sudoeste de África y en los melanesios.[48] Otros músculos pequeños en la cabeza asociados con la región occipital y el complejo muscular post-auricular a menudo son variables en su frecuencia.[49]
El platisma, un músculo cuadrangular (cuatro lados) en forma de lámina, es un vestigio remanente del carnoso panniculo de los animales. En los caballos, es el músculo que le permite sacudir una mosca de su espalda.
Cara[editar]
En muchos mamíferos no humanos, el labio superior y el área sinusal están asociados con bigotes o vibrisas que cumplen una función sensorial. En los humanos, estos bigotes no existen, pero todavía hay casos esporádicos en los que se pueden encontrar elementos de los músculos capsulares vibrisales asociados o los músculos del pelo sinusal. Con base en estudios histológicos de los labios superiores de 20 cadáveres, Tamatsu et al. encontró que las estructuras que se asemejan a tales músculos estaban presentes en el 35% (7/20) de sus especímenes.[50]
Brazo[editar]
El músculo palmar largo se ve como un pequeño tendón entre el flexor radial del carpo y el flexor cubital del carpo, aunque no siempre está presente. El músculo está ausente en aproximadamente el 14% de la población, sin embargo, esto varía mucho con la etnia. Se cree que este músculo participó activamente en la locomoción arbórea de los primates, pero actualmente no tiene ninguna función, ya que no proporciona más fuerza de agarre.[51] Un estudio ha demostrado que la prevalencia de la agenesia de palmaris longus en 500 pacientes indios es del 17,2% (8% bilateral y 9,2% unilateral).[52] El palmar es una fuente popular de material tendinoso para injertos y esto ha llevado a estudios que han demostrado que la ausencia del palmar no tiene ningún efecto apreciable en la fuerza del agarre.[53]
El músculo elevador de la clavícula en el triángulo cervical posterior es un músculo supernumerario presente solo en el 2-3% de todas las personas,[54] pero casi siempre está presente en la mayoría de las especies de mamíferos, incluidos los gibones y los orangutanes.[55]
Torso[editar]
El músculo piramidal del abdomen es un músculo pequeño y triangular, anterior al músculo recto abdominal y está contenido en la vaina de los músculos rectos abdominales. Está ausente en el 20% de los humanos y cuando está ausente, el extremo inferior del recto se incrementa proporcionalmente en tamaño. Los estudios anatómicos sugieren que las fuerzas generadas por los músculos piramidales son relativamente pequeñas.[56]
El músculo dorsal ancho de la espalda tiene varias variaciones esporádicas. Una variante particular es la existencia del músculo dorsoepitrochlearis o latissimocondyloideus, que es un músculo que pasa del tendón del dorsal ancho a la cabeza larga del músculo tríceps braquial. Es notable debido a su carácter bien desarrollado en otros simios y monos, donde es un importante músculo de escalada, es decir, el dorsoepitrochlearis brachii.[57][58] Este músculo se encuentra en ≈5% de los humanos.[59]
Pierna[editar]
El músculo plantar se compone de un vientre muscular delgado y un tendón largo y delgado. El vientre muscular mide aproximadamente 5-10 centímetros (2-4 pulgadas) de largo, y está ausente en el 7-10% de la población humana. Tiene una funcionalidad débil para mover la rodilla y el tobillo, pero generalmente se considera redundante y se usa a menudo como fuente de tendones para injertos. El tendón largo y delgado de la plantar se llama humorísticamente "el nervio del estudiante de primer año", ya que los estudiantes de medicina de primer año a menudo lo confunden con un nervio.
Lengua[editar]
Otro ejemplo intrigante de la vestigialidad humana ocurre en la lengua, específicamente en el músculo condrogloso. En un estudio morfológico de 100 cadáveres japoneses, se encontró que el 86% de las fibras identificadas eran sólidas y se agrupaban de la manera adecuada para facilitar el habla y la masticación. El otro 14% de las fibras eran cortas, delgadas y poco densas, casi inútiles, por lo que se concluyó que eran de origen vestigial.[60]
Senos[editar]
Pezones o pechos adicionales a veces aparecen a lo largo de las líneas mamarias de los humanos, apareciendo como un remanente de antepasados de mamíferos que poseían más de dos pezones o senos.[61][62]
Comportamiento[editar]

Los humanos también tienen algunos comportamientos y reflejos vestigiales.[63] Por ejemplo, la formación de piel de gallina en humanos bajo estrés es un reflejo vestigial; una posible función de los ancestros evolutivos humanos era elevar el pelo del cuerpo, hacer que el antepasado pareciera más grande y ahuyentar a los depredadores.[64][63] Levantar el cabello también se usa para atrapar una capa extra de aire, manteniendo a un animal caliente.[63] Debido a la disminución de la cantidad de cabello en los humanos, la formación refleja de la piel de gallina cuando está fría también es vestigial.[63]
El Reflejo de prensión es compatible con un comportamiento vestigial en los bebés humanos. Cuando coloque un dedo u objeto en la palma de un bebé, lo agarrará firmemente. Este agarre es bastante fuerte.[65] Algunos bebés, 37% según un estudio de 1932, son capaces de soportar su propio peso con una varilla,[66] aunque no hay forma de que puedan aferrarse a su madre. El agarre también es evidente en los pies también. Cuando un bebé está sentado, sus pies prensiles adoptan una postura encorvada, similar a la observada en un chimpancé adulto.[67][68] Un primate ancestral habría tenido suficiente vello corporal al que un bebé podría aferrarse a diferencia de los humanos modernos, permitiendo así que su madre escape del peligro, como trepar a un árbol en presencia de un depredador sin tener que ocupar sus manos sosteniendo a su bebé.
Se ha propuesto que el hipo es un remanente evolutivo de la respiración anfibia anterior.[69] Los anfibios como los renacuajos tragan aire y agua a través de sus branquias a través de un reflejo motor bastante simple similar al hipo de los mamíferos. Las vías motoras que permiten el hipo se forman temprano durante el desarrollo fetal, antes de que se formen las vías motoras que permiten la ventilación pulmonar normal. Por lo tanto, de acuerdo con la teoría de la recapitulación, el hipo es evolutivamente anterior a la respiración pulmonar moderna. Además, señalan que el hipo y la inhalación de anfibios se ven inhibidos por el aumento de CO2 y pueden ser detenidos por los agonistas del receptor GABAB, lo que ilustra una posible fisiología compartida y herencia evolutiva. Estas propuestas pueden explicar por qué los bebés prematuros pasan el 2.5% de su tiempo con hipo, posiblemente tragándose como anfibios, ya que sus pulmones aún no están completamente formados. El hipo intrauterino fetal es de dos tipos. El tipo fisiológico ocurre antes de las 28 semanas después de la concepción y tiende a durar de cinco a diez minutos. Estos hipo son parte del desarrollo fetal y están asociados con la mielinización del nervio frénico, que controla principalmente el diafragma torácico. La hipótesis de la filogenia explica cómo pudo haber evolucionado el reflejo del hipo, y si no hay una explicación, puede explicar el hipo como un remanente evolutivo, retenido por los ancestros anfibios de los humanos. Esta hipótesis ha sido cuestionada debido a la existencia del asa aferente del reflejo, el hecho de que no explica la razón del cierre glótico, y debido a que la muy corta contracción del hipo es poco probable que tenga un efecto de fortalecimiento significativo en la contracción lenta los músculos de la respiración.
Molecular[editar]
También existen estructuras moleculares vestigiales en humanos, que ya no se usan, pero que pueden indicar ancestros comunes con otras especies. Un ejemplo de esto es la L-gulonolactone oxidasa, un gen que es funcional en la mayoría de los otros mamíferos y produce una enzima que sintetiza la vitamina C.[70] En humanos y otros miembros del suborden Haplorrhini, una mutación inhabilitó el gen y lo incapacitó para producir la enzima. Sin embargo, los restos del gen todavía están presentes en el genoma humano como una secuencia genética vestigial llamada pseudogén. [71]
Referencias[editar]
- ↑ Darwin C, The Descent of Man, and Selection in Relation to Sex, London: John Murray, 1890, p.13.[1]
- ↑ Turner W, On the musculus sternalis, Proc. Royal Soc. Edinburgh session 1866–1867, p.65.[2]
- ↑ Wiedersheim, R. (1893) The Structure of Man: An Index to His Past History. Second Edition. Translated by H. and M. Bernard. London: Macmillan and Co. 1895. [3]
- ↑ Muller, G. B. (2002) "Vestigial Organs and Structures." in Encyclopedia of Evolution. Mark Pagel, editor in chief, New York: Oxford University Press. pp. 1131–1133.
- ↑ Koerth-Baker, Maggie (30 de julio de 2009). «Vestigial Organs Not So Useless After All». National Geographic. Consultado el 27 de julio de 2013.
- ↑ a b Wells, H.g. Huxley, J. Wells, G. P. The Science of Life. Pub. Cassell 1931
- ↑ Rosenthal, M. I.: Journal of the American Medical Association, Volume 67, Issues 15-26, 1916. Page 1326
- ↑ W. Colin MacKenzie. A Contribution to the Biology of the Vermiform Appendix. Medical record, Volume 89 Page 342 1916
- ↑ a b c d Darwin, Charles (1871). The Descent of Man, and Selection in Relation to Sex. John Murray: London.
- ↑ Stevens, C. Edward; Hume, Ian (2004). Comparative Physiology of the Vertebrate Digestive System. Cambridge: Cambridge University Press. ISBN 978-0-521-61714-7.
- ↑ Peter Robert Cheeke, Ellen S. Dierenfeld, Comparative Animal Nutrition and Metabolism. Publisher: CABI; 2010 ISBN 978-1-84593-631-0
- ↑ «Appendix may be useful after all – Health – Health care – More health news – NBC News». MSNBC.
- ↑ Randal Bollinger, R.; Barbas, Andrew S.; Bush, Errol L.; Lin, Shu S.; Parker, William (2007). «Biofilms in the large bowel suggest an apparent function of the human vermiform appendix». Journal of Theoretical Biology 249 (4): 826-31. PMID 17936308. doi:10.1016/j.jtbi.2007.08.032.
- ↑ Charles Q. Choi, "The Appendix: Useful and in Fact Promising", Live Science, 2009, Appendix has useful function
- ↑ Smith, H. F.; Fisher, R. E.; Everett, M. L.; Thomas, A. D.; Randal Bollinger, R.; Parker, W. (2009). «Comparative anatomy and phylogenetic distribution of the mammalian cecal appendix». Journal of Evolutionary Biology 22 (10): 1984-99. PMID 19678866. doi:10.1111/j.1420-9101.2009.01809.x.
- ↑ Saraga-Babić, Mirna; Lehtonen, Eero; Švajger, Anton; Wartiovaara, Jorma (1994). «Morphological and immunohistochemical characteristics of axial structures in the transitory human tail». Annals of Anatomy - Anatomischer Anzeiger 176 (3): 277-86. PMID 8059973. doi:10.1016/S0940-9602(11)80496-6.
- ↑ Fallon, John F.; Simandl, B. Kay (1978). «Evidence of a role for cell death in the disappearance of the embryonic human tail». American Journal of Anatomy 152 (1): 111-29. PMID 677043. doi:10.1002/aja.1001520108.
- ↑ Dao, Anh H.; Netsky, Martin G. (1984). «Human tails and pseudotails». Human Pathology 15 (5): 449-53. PMID 6373560. doi:10.1016/S0046-8177(84)80079-9.
- ↑ Dubrow, Terry J.; Wackym, Phillip Ashley; Lesavoy, Malcolm A. (1988). «Detailing the Human Tail». Annals of Plastic Surgery 20 (4): 340-4. PMID 3284435. doi:10.1097/00000637-198804000-00009.
- ↑ Spiegelmann, Roberto; Schinder, Edgardo; Mintz, Mordejai; Blakstein, Alexander (1985). «The human tail: A benign stigma». Journal of Neurosurgery 63 (3): 461-2. PMID 3894599. doi:10.3171/jns.1985.63.3.0461.
- ↑ Johnson, Dr. George B. "Evidence for Evolution" Archivado el 10 de marzo de 2008 en Wayback Machine.. (Page 12) Txtwriter Inc. 8 Jun 2006.
- ↑ Rozkovcová, E; Marková, M; Dolejsí, J (1999). «Studies on agenesis of third molars amongst populations of different origin». Sbornik lekarsky 100 (2): 71-84. PMID 11220165.
- ↑ Pereira, T. V.; Salzano, F. M.; Mostowska, A.; Trzeciak, W. H.; Ruiz-Linares, A.; Chies, J. A. B.; Saavedra, C.; Nagamachi, C.; Hurtado, A. M.; Hill, K.; Castro-De-Guerra, D.; Silva-Junior, W. A.; Bortolini, M.-C. (2006). «Natural selection and molecular evolution in primate PAX9 gene, a major determinant of tooth development». Proceedings of the National Academy of Sciences 103 (15): 5676-81. Bibcode:2006PNAS..103.5676P. PMC 1458632. PMID 16585527. doi:10.1073/pnas.0509562103.
- ↑ Trotier, D.; Eloit, C; Wassef, M; Talmain, G; Bensimon, J. L.; Døving, K. B.; Ferrand, J (2000). «The Vomeronasal Cavity in Adult Humans». Chemical Senses 25 (4): 369-80. PMID 10944499. doi:10.1093/chemse/25.4.369.
- ↑ Kjær, Inger; Hansen, Birgit Fischer (1996). «The human vomeronasal organ: Prenatal developmental stages and distribution of luteinizing hormone-releasing hormone». European Journal of Oral Sciences 104 (1): 34-40. PMID 8653495. doi:10.1111/j.1600-0722.1996.tb00043.x.
- ↑ Smith, Timothy D.; Siegel, Michael I.; Bhatnagar, Kunwar P. (2001). «Reappraisal of the vomeronasal system of catarrhine primates: Ontogeny, morphology, functionality, and persisting questions». The Anatomical Record 265 (4): 176-92. PMID 11519019. doi:10.1002/ar.1152.
- ↑ Smith, Timothy D.; Bhatnagar, Kunwar P. (2000). «The human vomeronasal organ. Part II: Prenatal development». Journal of Anatomy 197 (3): 421-36. PMC 1468143. PMID 11117628. doi:10.1046/j.1469-7580.2000.19730421.x.
- ↑ Won, J; Mair, EA; Bolger, WE; Conran, RM (2000). «The vomeronasal organ: an objective anatomic analysis of its prevalence». Ear, nose, & throat journal 79 (8): 600-5. PMID 10969469.
- ↑ Johnson, A; Josephson, R; Hawke, M (1985). «Clinical and histological evidence for the presence of the vomeronasal (Jacobson's) organ in adult humans». The Journal of otolaryngology 14 (2): 71-9. PMID 4068105.
- ↑ Foltán, René; Šedý, Jiří (2009). «Behavioral changes of patients after orthognathic surgery develop on the basis of the loss of vomeronasal organ: a hypothesis». Head & Face Medicine 5: 5. PMC 2653472. PMID 19161592. doi:10.1186/1746-160X-5-5.
- ↑ Bhatnagar, Kunwar P.; Smith, Timothy D. (2001). «The human vomeronasal organ. III. Postnatal development from infancy to the ninth decade». Journal of Anatomy 199 (Pt 3): 289-302. PMC 1468331. PMID 11554506. doi:10.1046/j.1469-7580.2001.19930289.x.
- ↑ a b c Bhatnagar, Kunwar P.; Kennedy, Ray C.; Baron, Georg; Greenberg, Richard A. (1987). «Number of mitral cells and the bulb volume in the aging human olfactory bulb: A quantitative morphological study». The Anatomical Record 218 (1): 73-87. PMID 3605663. doi:10.1002/ar.1092180112.
- ↑ Witt, M; Hummel, T (2006). «Vomeronasal Versus Olfactory Epithelium: Is There a Cellular Basis for Human Vomeronasal Perception?». International Review of Cytology. International Review of Cytology 248: 209-59. ISBN 978-0-12-364652-1. PMID 16487792. doi:10.1016/S0074-7696(06)48004-9.
- ↑ Wysocki CJ, Preti G (November 2004). «Facts, fallacies, fears, and frustrations with human pheromones». The Anatomical Record Part A: Discoveries in Molecular, Cellular, and Evolutionary Biology 281 (1): 1201-11. PMID 15470677. doi:10.1002/ar.a.20125.
- ↑ Wyatt, Tristram D. (2003). Pheromones and Animal Behaviour: Communication by Smell and Taste. Cambridge: Cambridge University Press. p. 295. ISBN 0-521-48526-6.
- ↑ Prof. A. Macalister, Annals and Magazine of Natural History, vol. vii., 1871, p. 342.
- ↑ Bair, J. H. (1901). «Development of voluntary control.». Psychological Review 8 (5): 474-510. doi:10.1037/h0074157.
- ↑ Mr. St. George Mivart, Elementary Anatomy, 1873, p. 396.
- ↑ Owen, R. 1866–1868. Comparative Anatomy and Physiology of Vertebrates. London.
- ↑ Montagna, W.; Machida, H.; Perkins, E. M. (1966). «The skin of primates. XXXIII. The skin of the angwantibo (Arctocebus calabarensis)». American Journal of Physical Anthropology 25 (3): 277-90. PMID 5971502. doi:10.1002/ajpa.1330250307.
- ↑ Toerien, M. J.; Gous, A. E. (1978). «The orbital muscle of Müller». South African Medical Journal 53 (4): 139-41. PMID 653491.
- ↑ Dutton, J.J., Atlas of Clinical and Surgical Orbital Anatomy, 2nd Edition, Elsevier, 2011. p.116-117.
- ↑ "Breast Anatomy and Embryology." Essentials of Plastic Surgery (2015): 355-61
- ↑ Hadjiathanasiou, C.G.; Brauner, R.; Lortat-Jacob, S.; Nivot, S.; Jaubert, F.; Fellous, M.; Nihoul-Fékété, C.; Rappaport, R. (1994). «True hermaphroditism: Genetic variants and clinical management». The Journal of Pediatrics 125 (5): 738-44. PMID 7965425. doi:10.1016/S0022-3476(06)80172-1.
- ↑ Eren, Erdal; Edgünlü, Tuba; Asut, Emre; Karakaş Çelik, Sevim (2016). «Homozygous Ala65Pro Mutation with V89L Polymorphism in SRD5A2 Deficiency». Journal of Clinical Research in Pediatric Endocrinology 8 (2): 218-23. PMC 5096479. PMID 26761946. doi:10.4274/jcrpe.2495.
- ↑ a b Healey, Andrew (2010). «Embryology of the Female Reproductive Tract». Imaging of Gynecological Disorders in Infants and Children. Medical Radiology. pp. 21-30. ISBN 978-3-540-85601-6. doi:10.1007/174_2010_128.
- ↑ Basaran, Mustafa; Usal, Deniz; Aydemir, Cumhur (2009). «Hymen Sparing Surgery for Imperforate Hymen: Case Reports and Review of Literature». Journal of Pediatric and Adolescent Gynecology 22 (4): e61-4. PMID 19646660. doi:10.1016/j.jpag.2008.03.009.
- ↑ Macalister, Alexander (1875). «Additional Observations on Muscular Anomalies in Human Anatomy. (Third Series) With a Catalogue of the Principal Muscular Variations Hitherto Published». The Transactions of the Royal Irish Academy 25: 1-134. JSTOR 30079154.
- ↑ Guerra, Aldo Benjamin; Metzinger, Stephen Eric; Metzinger, Rebecca Crawford; Xie, Chen; Xie, Yue; Rigby, Peter Lister; Naugle, Thomas (2004). «Variability of the Postauricular Muscle Complex». Archives of Facial Plastic Surgery 6 (5): 342-7. PMID 15381582. doi:10.1001/archfaci.6.5.342.
- ↑ Tamatsu, Yuichi; Tsukahara, Kazue; Hotta, Mitsuyuki; Shimada, Kazuyuki (2007). «Vestiges of vibrissal capsular muscles exist in the human upper lip». Clinical Anatomy 20 (6): 628-31. PMID 17458869. doi:10.1002/ca.20497.
- ↑ Aversi-Ferreira, Roqueline A. G. M. F.; Bretas, Rafael Vieira; Maior, Rafael Souto; Davaasuren, Munkhzul; Paraguassú-Chaves, Carlos Alberto; Nishijo, Hisao; Aversi-Ferreira, Tales Alexandre (2014). «Morphometric and Statistical Analysis of the Palmaris Longus Muscle in Human and Non-Human Primates». BioMed Research International 2014: 178906. PMC 4016873. PMID 24860810. doi:10.1155/2014/178906.
- ↑ Kapoor, Sudhir K.; Tiwari, Akshay; Kumar, Abhishek; Bhatia, Rajesh; Tantuway, Vinay; Kapoor, Saurabh (2008). «Clinical relevance of palmaris longus agenesis: Common anatomical aberration». Anatomical Science International 83 (1): 45-8. PMID 18402087. doi:10.1111/j.1447-073X.2007.00199.x.
- ↑ Sebastin, S; Lim, A; Bee, W; Wong, T; Methil, B (2005). «Does the absence of the palmaris longus affect grip and pinch strength?». The Journal of Hand Surgery: Journal of the British Society for Surgery of the Hand 30 (4): 406-8. PMID 15935531. doi:10.1016/j.jhsb.2005.03.011.
- ↑ Rubinstein, David; Escott, Edward J.; Hendrick, Laura L. (April 1999). «The prevalence and CT appearance of the levator claviculae muscle: a normal variant not to be mistaken for an abnormality». AJNR Am J Neuroradiol (American Society of Neuroradiology) 20 (4): 583-6. PMID 10319965.
- ↑ Loukas, M.; Sullivan, A.; Tubbs, R.S.; Shoja, M.M. (2008). «Levator claviculae: a case report and review of the literature». Folia Morphol. 67 (4): 307-310.
- ↑ Lovering, Richard M.; Anderson, Larry D. (2008). «Architecture and fiber type of the pyramidalis muscle». Anatomical Science International 83 (4): 294-7. PMC 3531545. PMID 19159363. doi:10.1111/j.1447-073X.2007.00226.x.
- ↑ P., Haninec; R., Tomáš; R., Kaiser; R., Čihák (2009). «Development and clinical significance of the musculus dorsoepitrochlearis in men». Clinical Anatomy 22 (4): 481-8. PMID 19373904. doi:10.1002/ca.20799.
- ↑ Edwards, William E., The Musculoskeletal Anatomy of the Thorax and Brachium of an Adult Female Chimpanzee,6571st Aeromedical Research Laboratory, New Mexico, 1965. http://www.dtic.mil/dtic/tr/fulltext/u2/462433.pdf Archivado el 11 de febrero de 2017 en Wayback Machine.
- ↑ http://www.anatomyatlases.org/AnatomicVariants/MuscularSystem/Text/L/06Latissimus.shtml
- ↑ Ogata, Shigemitsu; Mine, Kazuharu; Tamatsu, Yuichi; Shimada, Kazuyuki (2002). «Morphological study of the human chondroglossus muscle in Japanese». Annals of Anatomy - Anatomischer Anzeiger 184 (5): 493-9. PMID 12392330. doi:10.1016/S0940-9602(02)80087-5.
- ↑ Kajava, Y (1915). «The proportions of supernumerary nipples in the Finnish population». Duodecim 1: 143-70.
- ↑ Goyal, Tarang; Bakshi, SK; Varshney, Anupam (2012). «Seven nipples in a male: World′s second case report». Indian Journal of Human Genetics 18 (3): 373-5. PMC 3656534. PMID 23716953. doi:10.4103/0971-6866.108051.
- ↑ a b c d Laura Spinney (2008), «Remnants of evolution», New Scientist 198 (2656): 42-45, doi:10.1016/S0262-4079(08)61231-2.
- ↑ Darwin, Charles. (1872) The Expression of the Emotions in Man and Animals John Murray, London.[página requerida]
- ↑ Peter Gray (2007). Psychology (fifth edición). Worth Publishers. p. 66. ISBN 0-7167-0617-2.
- ↑ Behavior Development in Infants (via Google Books) by Evelyn Dewey, citing a study "Reflexes and other motor activities in newborn infants: a report of 125 cases as a preliminary study of infant behavior" published in the Bull. Neurol. Inst. New York, 1932, Vol. 2, pp. 1–56.
- ↑ Jerry Coyne (2009). Why Evolution is True. Penguin Group. pp. 85–86. ISBN 978-0-670-02053-9.
- ↑ Anthony Stevens (1982). Archetype: A Natural History of the Self. Routledge & Kegan Paul. p. 87. ISBN 0-7100-0980-1.
- ↑ Straus, C.; Vasilakos, K.; Wilson, R. J. A.; Oshima, T.; Zelter, M.; Derenne, J-Ph.; Similowski, T.; Whitelaw, W. A. (2003). «A phylogenetic hypothesis for the origin of hiccough». BioEssays 25 (2): 182-8. PMID 12539245. doi:10.1002/bies.10224.
- ↑ Ohta, Yuriko; Nishikimi, Morimitsu (1999). «Random nucleotide substitutions in primate nonfunctional gene for l-gulono-γ-lactone oxidase, the missing enzyme in l-ascorbic acid biosynthesis». Biochimica et Biophysica Acta (BBA) - General Subjects 1472 (1–2): 408-11. PMID 10572964. doi:10.1016/S0304-4165(99)00123-3.
- ↑ Nishikimi M, Fukuyama R, Minoshima S, Shimizu N, Yagi K (6 de mayo de 1994). «Cloning and chromosomal mapping of the human nonfunctional gene for L-gulono-gamma-lactone oxidase, the enzyme for L-ascorbic acid biosynthesis missing in man». J. Biol. Chem. 269 (18): 13685-8. PMID 8175804. Archivado desde el original el 2 de febrero de 2009. Consultado el 7 de mayo de 2018.


