Umpolung
En química orgánica, umpolung o inversión de la polaridad es la modificación química de un grupo funcional con el objetivo de revertir la polaridad del grupo.[1][2] Esta modificación permite reacciones secundarias del grupo funcional, que de otra forma no serían posibles.[3] El concepto fue introducido por D. Seebach (de ahí la palabra alemana umpolung para indicar la polaridad invertida) y por E.J. Corey. Puede encontrarse algunas aplicaciones clásicas de la inversión de la polaridad en los reactivos Grignard y en la condensación benzoínica.
Inversión de la polaridad carbonílica[editar]
Se observa un ejemplo clásico de la polaridad de inversión en la química de los ditianos.
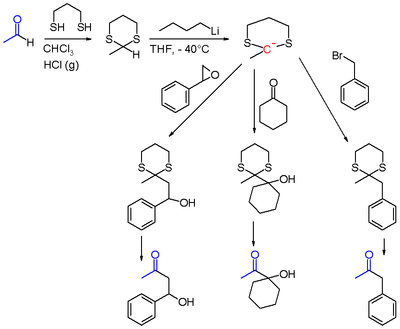
Ordinariamente, el átomo de oxígeno en el grupo carbonilo es más electronegativo que el átomo de carbono y, en consecuencia, el grupo carbonilo reacciona como un electrófilo en el carbono. Esta polaridad puede ser invertida cuando el grupo carbonilo es convertido a un ditiano o un tioacetal. En terminología sintón, el grupo carbonilo ordinario es un catión acilo, y el ditiano es un anión acilo enmascarado.
Cuando el ditiano deriva de un aldehído como el acetaldehído, el protón acílico puede ser abstraído por n-butil-litio en THF a temperaturas bajas. El 2-litio-1,3-ditiano generado reacciona como un nucleófilo en un desplazamiento nucleofílico con halogenuros de alquilo tales como el bromuro de bencilo, con otros compuestos carbonílicos como la ciclohexanona u oxiranos tales como el fenilepoxietano, mostrado a continuación. Después de la hidrólisis del grupo ditiano, los productos finales de la reacción son α-alquilcetonas o α-hidroxicetonas. Un reactivo común para la hidrólisis del ditiano es el (bis(trifluoroacetoxi)yodo)benceno.
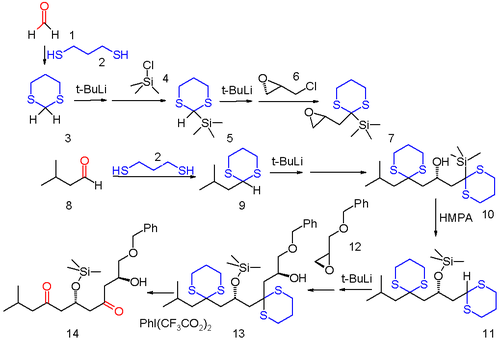
La química del ditiano abre camino a muchas transformaciones químicas nuevas. Un ejemplo se encuentra en la denominada química de aniones relé, en la que un grupo funcional aniónico que resulta de una reacción orgánica es transferido a una ubicación diferente dentro del mismo esqueleto de carbono, y está disponible para reacciones secundarias.[4] En este ejemplo de una reacción multicomponente, tanto el formaldehído (1) y el isopropilaldehído (8) son convertidos en los ditianos 3 y 9 con 1,3-propanoditiol. Primero, el sulfuro 3 es sililado por reacción con tert-butillitio y luego cloruro de trimetilsililo 4, siendo eliminado posteriormente el segundo protón de acilo, y luego se hace reaccionar con In this example of a multi-component reaction both formaldehyde (1) and (-)-epiclorhidrina 6 ópticamente activa, reemplazando al cloro. Este compuesto sirve como sustrato para la reacción con el otro ditiano 9, para conducir al producto de apertura del anillo oxirano 10. Bajo influencia de la fuerte base HMPA, 10 sufre una transposición de Brook para formar el éter de sililo 1, reactivando el grupo ditiano formaldehído como un anión (de ahí el concepto de relé de aniones). Este grupo ditiano reacciona con el oxirano 12 para producir el alcohol 13, y en la etapa final, los grupos sulfuro son eliminados con (bis(trifluoroacetoxi)yodo)benceno
Inversión de polaridad en enonas[editar]
En la adición nucleofílica conjugada ordinaria, el átomo de carbono β actúa como un electrófilo. En casos especiales, esta posición puede ser modificada para que reaccione como un nucleófilo.[5] La reacción representada en el esquema 3 es un equivalente de la reacción de Heck. El catalizador activo no es un compuesto de paladio, sino un carbeno persistente derivado de triazol.

Este carbeno reacciona con un éster α,β-unsaturado 1 en la posición β, formando el enolato intermediario 2. Por medio de una tautomerización, 2b puede desplazar al átomo de bromo terminal para formar 3. Una reacción de eliminación regenera al carbeno y libera el producto 4.
Para contraste: en la reacción de Baylis-Hillman, el mismo átomo de carbono β electrofílico es atacado por un reactivo, pero resulta en la activación de la posición α de la enona del nucleófilo.
Inversión de polaridad de aminas[editar]
Ordinariamente, el átomo de nitrógeno en el grupo amina reacciona como un nucleófilo por medio de su par solitario. Esta polaridad puede ser invertida cuando una amina primaria o secundaria es sustituida con un buen grupo saliente (como un átomo de halógeno o un grupo alcoxi). El compuesto resultante N-sustituido puede comportarse como un electrófilo en el átomo de carbono, y reacciona con un nucleófilo, como por ejemplo en la aminación electrofílica de carbaniones.[6]
Referencias[editar]
- ↑ Seebach D. (1979). «Methods of Reactivity Umpolung». Angewandte Chemie International Edition in English 18 (4): 239-258. doi:10.1002/anie.197902393.
- ↑ Gröbel B. T., Seebach D. (1977). «Reactivity of Carbonyl-Compounds Through Sulfur-Containing Reagents». Synthesis-Stuttgart 6: 357-402. doi:10.1055/s-1977-24412.
- ↑ Seebach D., Corey E. J. (1975). «Generation and synthetic applications of 2-lithio-1,3-dithianes». Journal of Organic Chemistry 40 (2): 231-237. doi:10.1021/jo00890a018.
- ↑ Smith A. B. , III, Xian M. (2006). «Anion Relay Chemistry: An Effective Tactic for Diversity Oriented Synthesis». Journal of the American Chemical Society 128 (1): 66-67. doi:10.1021/ja057059w.
- ↑ Fischer C., Smith S. W., Powell D. A., Fu G. C. (2006). «Umpolung of Michael Acceptors Catalyzed by N-Heterocyclic Carbenes». Journal of the American Chemical Society 128 (5): 1472-1473. doi:10.1021/ja058222q.
Enlaces externos[editar]
- Unión Internacional de Química Pura y Aplicada. «umpolung». Compendium of Chemical Terminology. Versión en línea (en inglés).