Fosgeno
| Fosgeno | ||
|---|---|---|
 | ||
| Archivo:Phosgene-3D-balls.png y Phosgene-3D-vdW.png | ||
| Nombre IUPAC | ||
| Dicloruro de carbonilo | ||
| General | ||
| Otros nombres | CG, oxicloruro de carbono, cloruro de cloroformilo, dicloroformaldehído, diclorometanona | |
| Fórmula estructural |
 | |
| Fórmula molecular | CCl2O | |
| Identificadores | ||
| Número CAS | 75-44-5[1] | |
| Número RTECS | SY5600000 | |
| ChEBI | 29365 | |
| ChemSpider | 6131 | |
| PubChem | 6371 | |
| UNII | 117K140075 | |
|
ClC(Cl)=O
| ||
| Propiedades físicas | ||
| Apariencia | Gas incoloro | |
| Densidad | 1432 kg/m³; 1,432 g/cm³ | |
| Masa molar | 98,92 g/mol | |
| Punto de fusión | 155 K (−118 °C) | |
| Punto de ebullición | 281 K (8 °C) | |
| Propiedades químicas | ||
| Solubilidad en agua | Hidrólisis | |
| Momento dipolar | 1,17 D | |
| Peligrosidad | ||
| NFPA 704 |
0
4
1
| |
| Riesgos | ||
| Más información | ICSC 0007 | |
| Compuestos relacionados | ||
| Compuestos relacionados |
Tiofosgeno Formaldehído Ácido carbónico Urea Monóxido de carbono Ácido clorofórmico | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El fosgeno (CCl2O), del griego: φωσ (phos): "luz" y γένος-ου (genos): "generador", es un componente químico industrial utilizado para hacer plásticos y pesticidas. A temperatura ambiente (21 °C), el fosgeno es un gas venenoso. Si es enfriado y presurizado, el gas de fosgeno puede ser convertido en líquido, de forma que pueda ser transportado y almacenado. Cuando se libera fosgeno líquido, este se transforma rápidamente en gas que permanece cerca del suelo y se propaga con rapidez (es más denso que el aire y por esa razón se expande hacia áreas más bajas). Al fosgeno también se le conoce por su denominación militar “CG”.
El gas de fosgeno puede ser incoloro o puede verse como una nube que varía de blanca a amarilla pálida. En bajas concentraciones, tiene un olor agradable como a heno recién cortado o maíz verde, pero es posible que no todas las personas expuestas se den cuenta del olor. En altas concentraciones, el olor puede ser fuerte y desagradable.[cita requerida]Este componente fue utilizado ampliamente durante la Primera Guerra Mundial como un agente asfixiante (que afecta el sistema pulmonar). Entre los agentes químicos utilizados en la guerra, el fosgeno fue el responsable del mayor número de muertes. No se encuentra en forma natural en el ambiente.
El fosgeno, por sí mismo, no es inflamable (no se enciende ni se quema con facilidad) pero es un comburente (puede causar que prendan las sustancias inflamables que hay a su alrededor).
El gas es utilizado en la industria para producir muchas otras sustancias químicas como los pesticidas. Puede formarse cuando ciertos compuestos están expuestos al calor, como en el caso de varios tipos de plásticos.
Historia[editar]
El fosgeno fue sintetizado en 1812 por vez primera por el químico amateur inglés John Davy (1790-1868) mediante la exposición de una mezcla de monóxido de carbono y cloro a la luz solar. Lo llamó phosgene en referencia a la utilización de la luz para promover la reacción; del griego, phos (luz) y gene (nacido).[2] Se convirtió poco a poco en un elemento importante en la industria química a medida que avanzaba el siglo XIX, sobre todo en la fabricación de colorantes.
Características[editar]
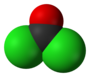

El fosgeno u oxicloruro de carbono, cuya fórmula química es CCl2O, es un gas generalmente incoloro y no inflamable, con un olor agradable, similar al del heno recién cortado. Es una sustancia química artificial, aunque pequeñas cantidades son formadas en la naturaleza a partir de la degradación de compuestos del cloro.
Se usa en la creación de tinturas, isocianatos, policarbonatos, cloruros ácidos, plaguicidas y, en otro orden de cosas, algunos medicamentos. Además es usado en la separación de algunos minerales. También fue usado como arma química en la Primera Guerra Mundial.
El fosgeno es un gas a temperatura ambiente, pero (en menor medida) también puede ser almacenado en estado líquido, bajo presión o refrigeración.
Reacciones en la naturaleza[editar]
Cuando el fosgeno se libera al aire existe solamente como gas. Este gas se degrada en la atmósfera cuando reacciona con otras sustancias que se encuentran en el aire, mediante procesos generalmente lentos. En el aire, también reacciona con la humedad de la lluvia y de las nubes dando lugar a otras sustancias.
En el agua, reacciona y se degrada a otros productos. El fosgeno mezclado con agua que no se degrada, se evapora con el aire y forma la reacción del punto anterior.
Con respecto al medio terrestre, no suele adherirse al suelo. Una pequeña parte se evapora al aire, la otra parte baja al agua subterránea y la contamina. La mayor parte se degradará con la humedad.
El fosgeno es un producto no acumulativo en la cadena alimentaria.
Toxicidad[editar]
Exposición[editar]
El fosgeno existe en el aire en bajas concentraciones a las que estamos expuestos.[cita requerida]
Este tóxico es liberado en la soldadura de metales que han sido limpiados con solventes clorados, los profesionales que se dedican a esta actividad son los que más riesgo de exposición tienen. Cuando se produce una temperatura aproximada de 120 °C en uno de esos disolventes se forma fosgeno y si el metal tiene alguna grasa, aproximadamente un 60% del disolvente, la temperatura de formación del fosgeno baja incluso a 70 °C).[cita requerida]
TLV: (Valor umbral límite de exposición) = 0,1 ppm.[3]
Sintomatología[editar]
Afecta poco a la mucosa, por lo que sus efectos no se perciben hasta varias horas después de su inhalación. En presencia de agua, el fosgeno se descompone en ácido clorhídrico, lo que ocurre con facilidad en el interior del alvéolo pulmonar, lesionando el endotelio, provocando edema, sofocación, cianosis y expectoración serosa abundante. Lo puede llevar a la muerte por asfixia o shock.[4]
Al contacto con la piel y los ojos produce quemadura química y congelación, aunque es altamente improbable el contacto con fosgeno líquido.[5]
Tratamiento[editar]
En el caso en el que ya haya habido contacto con el fosgeno, se recomienda quitarse la ropa contaminada y aclararse la piel con abundante agua, enjuagarse los ojos y quitarse inmediatamente las lentes de contacto, siempre que sea posible.[6] Si el tóxico se encuentra en suspensión y hay riesgo de ser inhalado, hay que abandonar el lugar y guardar reposo, para reducir al mínimo el consumo de oxígeno. Al afectado hay que suministrarle oxígeno, aunque en presencia de edema, este no puede exceder una concentración del 30 al 40%. Para prevenir o aliviar el edema hay que suministrar una solución glucosada hipertónica intravenosa. Ayuda administrar gluconato de calcio al 10% por vía intravenosa. Si no hay shock, se puede practicar una sangría de entre 400 y 700 ml. Para la insuficiencia cardíaca hay que inyectar 0,125 mg de estrofantina por vía intravenosa. Para prevenir las infecciones pulmonares es altamente recomendable suministrar antibióticos. Para disminuir el riesgo de secuelas pulmonares hay que utilizar corticoides.[4]
Véase también[editar]
Referencias[editar]
- ↑ Número CAS
- ↑ John Davy (1812). «On a Gaseous Compound of Carbonic Oxide and Chlorine». Philosophical Transactions of the Royal Society of London 102: 144-151. JSTOR 107310. doi:10.1098/rstl.1812.0008.
- ↑ https://labor.ny.gov/workerprotection/safetyhealth/PDFs/table.pdf
- ↑ a b Calabrese, Alberto I.; Astolfi, Emilio A. (enero de 1969). Toxicología. Buenos Aires, Argentina: Kapelusz. p. 72. OCLC 14501248.
- ↑ Agencia para Sustancias Tóxicas y el Registro de Enfermedades (6 de mayo de 2016). «Fichas internacionales de Seguridad Química». Consultado el 10 de noviembre de 2016.
- ↑ Instituto Nacional de Seguridad e Higiene en el Trabajo (octubre de 2002). «Resúmenes de Salud Púbica - Fosgeno (Fosgene)». Archivado desde el original el 17 de mayo de 2017. Consultado el 10 de noviembre de 2016.

