Embryophyta
| Plantas terrestres | ||
|---|---|---|
| Rango temporal: Ordovícico-reciente | ||
 | ||
| Taxonomía | ||
| Reino: | Plantae | |
| Subreino: | Viridiplantae | |
| (sin rango) |
Streptophyta Streptophytina | |
| (sin rango): |
Embryophyta Engler, 1892[1][2] | |
| Divisiones | ||
| ||
Las plantas terrestres o embriofitas (Embryophyta) son el clado (grupo monofilético) que está formado por los descendientes de ciertas algas verdes, que se caracterizan por poseer una serie de adaptaciones para la vida fuera del agua, y que son por lo tanto los responsables de la colonización de la tierra por parte de las plantas. El clado comprende a todas las plantas terrestres: los briófitos (hepáticas, antoceros y musgos), los licopodios, los helechos, y las plantas con semilla, entre las que están las gimnospermas y las angiospermas.
La monofilia de las embriofitas está ampliamente consensuada tanto por los estudios morfológicos como por los moleculares (Kenrick y Crane 1997a,[3] 1997b,[4] Karol et al. 2001).[5] El nombre embryophyta proviene de su característica etapa de embrión por la que pasa el esporófito diploide, lo que las diferencia de sus ancestros que no tenían esporófito multicelular ni embrión (por lo tanto eran haploides). Técnicamente, es preferible llamarlas «embriofitas» en lugar de «plantas terrestres», ya que muchas líneas de algas no emparentadas con los ancestros de las embriofitas han hecho su transición a la vida sobre la superficie de la tierra (por ejemplo Trebouxiophyceae), si bien lo han hecho de forma menos conspicua que las embriofitas. Además de poseer esporófito multicelular con etapa de embrión, las embriofitas se caracterizan por poseer estructuras reproductivas multicelulares tanto en el esporófito (los «esporangios») como en el gametófito (los «anteridios» y «arquegonios»), como también cutícula, y esporas de pared gruesa con característica marca trilete.
Tradicionalmente, las embriofitas fueron divididas en dos grandes grupos, las Briofitas en sentido amplio (antoceros, musgos y hepáticas), y las plantas vasculares (helechos y afines, gimnospermas y angiospermas).
Sinonimia
[editar]Las plantas terrestres conforman un taxón que ha sido denominado Cormophyta (Endlicher 1836, Wettstein 1924, Chadefaud & Emberger 1960, Cavalier-Smith 1998), Embryophyta (Engler 1892, Ruggiero et al 2015), Phyta (Barkley 1939), Cormobionta (Rothmaler 1948), Euplanta (Barkley 1949), Telomobionta (Takhtajan 1964), Embryobionta (Cronquist et al 1966), Metaphyta (Whittaker 1969), Plantae (Margulis 1971, Benton 1993), Embryophyceae (Lewis & McCourt 2004), Equisetopsida (Chase & Reveal 2009) y Embryopsida (Pirani & Prado 2012).
Ciclo de vida y morfología de las embriofitas
[editar]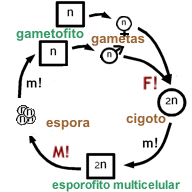 Referencias: n : generación haploide, 2n : generación diploide, m! : mitosis, M! : meiosis, F! : fecundación |
A diferencia de su ancestro haploide, las embryophytas se caracterizan por poseer un ciclo de vida haplo-diplonte, con gametófito (individuo de la generación haploide) y esporófito (individuo de la generación diploide) multicelulares. El esporófito multicelular pasa primero por una etapa de embrión, que se caracteriza por estar protegido por el gametófito donde se produjo la ovocélula, y también por ser nutrido a expensas del gametófito, a través de un tejido de transferencia llamado placenta. El huevo, y después de la fecundación, el embrión, están protegidos por una estructura multicelular del gametófito llamada arquegonio. También el esperma es producido y protegido por una estructura multicelular del gametófito: el anteridio. En principio, el esperma es una célula que posee dos o más flagelos que le permiten nadar hasta el huevo (pero en muchas espermatofitas se ve una reducción del esperma a solo unos núcleos espermáticos, y lo que se transporta hasta el huevo es todo el gametófito masculino dentro del grano de polen). Inicialmente, la fase gametofítica era dominante, como todavía hoy se puede apreciar en las hepáticas, los antoceros y los musgos. En las plantas vasculares (lycofitas, helechos y plantas con semilla) el esporófito se volvió dominante y nutricionalmente independiente, y se encuentra una reducción progresiva de la generación gametofítica.
Ecología y Evolución
[editar]Este clado parece haber recibido una gran presión de selección para fijar los caracteres morfológicos que lo adaptaran a la vida terrestre, algunos de los cuales ya están presentes en algunos clados de algas verdes.
Adaptaciones para la vida terrestre
[editar]- La aparición de la cutícula protegiendo al esporófito, y de la esporopolenina formando una gruesa pared en la espora, parecen ser respuestas a la desecación.
- El intercambio de gases con el ambiente se logra a través de pequeños poros en la epidermis o, en los grupos más avanzados, a través de estomas genuinos.
- Los flavonoides ayudan a absorber la luz ultravioleta.
- Este clado también sufrió adaptaciones para sobrellevar la alta concentración de oxígeno en la atmósfera (mucho más alta que en el agua), ya que una alta concentración de oxígeno inhibe la fijación de dióxido de carbono. El metabolismo de este clado incluye un «sistema de oxidación del glicolato» (glycolate oxidation system).
- La interacción entre plantas terrestres y hongos fue documentada en muchos briofitos y también en plantas vasculares. En esta interacción, las plantas proveen a los hongos de los productos de la fotosíntesis, y a cambio los hongos exploran el suelo y las plantas obtienen los nutrientes del suelo a través de los hongos.
Orígenes de las embriofitas
[editar]
Probablemente las primeras plantas terrestres dependían de su asociación con hongos para sobrevivir en tierra, de los que obtenían nutrientes que éstos tomaban del suelo. Aparentemente estas asociaciones fueron al principio solo con el gametófito de las embriofitas, y fueron establecidas muy temprano, en el Silúrico/Devónico (Selosse y Tacon 1998;[6] Redecker et al. 2000;[7] Nebel et al. 2004;[8] Köttke y Nebel 2005).[9] Los glomales parecen haber sido los hongos que participaron inicialmente en la asociación. Es interesante que esta asociación no ocurre en musgos (Read et al. 2000).[10]
Los precursores de muchas de las adaptaciones a la tierra antes citadas, y también de muchos aspectos del ciclo de vida, pueden ser encontrados en los clados de algas verdes Chlorokybales y también Charales, que están altamente emparentados. El ciclo de vida de las plantas terrestres probablemente derivó de un ciclo de vida del tipo charofita, que son algas de ciclo de vida haplonte que retienen al cigoto diploide unicelular en el gametófito, y lo nutren a través de una placenta. Aparentemente el ancestro de las plantas terrestres retardó la meiosis que daría las gametas, y mediante una serie de divisiones mitóticas del cigoto diploide generó una generación multicelular diploide.
Las plantas verdes pueden tener mil millones de años de vida en la Tierra, o aún más, y es posible que algunos linajes de algas verdes ya hayan existido en el Precámbrico. Una variedad de fósiles de algas verdes datan ya del Cámbrico (hace unos 550 millones de años), incluyendo Ulvophyceae. Las charofitas no aparecen en el registro fósil hasta mediados del Silúrico. La ocupación de la tierra por las algas verdes probablemente sucedió recién a mediados del Ordovícico, hace unos 450 millones de años. Hay esporas fósiles que datan de esa época, y probablemente de antes también, parecidas a las que hoy vemos en las hepáticas. Del Ordovícico parecen datar unos trozos de cutícula y estructuras tulares provenientes de plantas. Del Silúrico parecen datar unas esporas con la característica marca trilete de las plantas terrestres.
Es probable que los briófitos y las plantas terrestres como las conocemos hoy, hayan aparecido recién en el Ordovícico tardío. Un poco más tarde, empezando a mediados del Silúrico, se encontraron macrofósiles bien preservados del clado de las plantas vasculares. La ocupación de la superficie terrestre parece haber tomado poco después de eso.
La especialización de los órganos sexuales del gametófito («gametangios»), los tallos con mecanismos de transporte de fluidos («tejidos vasculares»), los tejidos estructurales (como el leño), las estructuras en la epidermis para el intercambio gaseoso (como los «estomas»), las hojas y raíces de varios tipos, los diversos órganos portadores de esporas («esporangios»), las semillas y el hábito arborescente, son caracteres que evolucionaron hacia el final del período Devónico.
Dominancia del gametófito frente a dominancia del esporófito
[editar]En años recientes, estudios paleobotánicos cuidadosos han revelado que algunos fósiles de embriofitas tempranas son en realidad los gametófito haploides, portando anteridios y arquegonios (Remy 1982,[11] Remy et al. 1993).[12] Estos fósiles son remarcables, porque son bastante grandes, erguidos, y ramificados, y en general tienen el aspecto de la fase esporofítica del ciclo de vida. Este descubrimiento ha llevado a la hipótesis de que los primeros miembros del linaje de las plantas vasculares exhibían alternancia de generaciones más o menos similares. Entonces, teniendo cuenta los grupos briofitos, parece que tanto el gametófito como el esporófito eran fases elaboradas.
Este conocimiento nos permite unir la secuencia de eventos que llevó al ciclo de vida que vemos en las plantas vasculares actuales. Este ciclo de vida incluye una dramática reducción en la fase gametofítica y una igualmente impresionante elaboración de la fase esporofítica. En las primeras plantas vasculares, el gametófito era nutricionalmente independiente del esporófito, y esta condición es retenida hoy en los linajes de «esporas libres» como los helechos y las lycophytas. Con la evolución de las plantas con semilla, sin embargo, el gametófito se ha reducido muchísimo y finalmente se ha vuelto completamente dependiente del esporófito.
Vistos en este contexto, los grupos briófitos sensu lato (en especial los musgos) y las plantas vasculares parecen haber explorado dos diferentes mecanismos para incrementar el número de esporas producidas por evento de fertilización (Mishler y Churchill 1985).[13] En los musgos este incremento en la producción de esporas era logrado al intercalar un estado protonemal filamentoso que podía producir numerosos gametófitos foliosos no ramificados, cada uno portando un único esporófito no ramificado terminado en un único esporangio. En contraste, en el linaje de las plantas vasculares el número de esporangios fue incrementado al ramificar el esporófito de forma que cada punta de cada rama pudiera portar un esporangio.
¿Qué ventaja adaptativa encontraron los clados más modernos de embriofitas, que los volvieron dominantes de la superficie terrestre? Los investigadores no pueden dejar de notar la evidente reducción de la fase gametofítica y la dominancia progresiva de la fase esporofítica. Esto los lleva a pensar que este cambio de dominancia puede ser un responsable del éxito ecológico de los clados modernos. Puestos a pensar en el mecanismo a través del cual estaría obrando esta ventaja adaptativa, hay dos hipótesis que dominan el pensamiento científico:
- La más difundida es la hipótesis de que el esporófito, al tener dos juegos de cromosomas en lugar de uno, es menos vulnerable ante las mutaciones genéticas, lo cual como consecuencia aumenta la diversidad de genes y por lo tanto las probabilidades de estar adaptado cuando cambia el ambiente.
- Una segunda hipótesis, que no necesariamente se contradice con la primera, que es remarcada por Judd et al. (2002), es que el esporófito no tiene limitantes ecológicos para crecer en altura, ya que no necesita ningún tipo de interacción para producir las esporas y liberarlas. En cambio el gametófito, productor de gametas masculinas y femeninas, debe tener una constitución que le asegure que las gametas masculinas puedan nadar hasta las femeninas, para que se produzca la fecundación y se reinicie el ciclo. Esto limitaría en gran medida la exploración de diferentes morfologías en el gametófito, que debe estar ligado al suelo para asegurar la fecundación y por lo tanto la supervivencia de la especie.
Filogenia
[editar]
Los grupos monofiléticos de las embriofitas vivientes están representados en el siguiente cladograma:[14][15][16][17]
| Embryophyta |
| ||||||||||||||||||||||||||||||||||||||||||
Los correspondientes grupos parafiléticos son:
- Pteridophyta, que comprende a los licopodios, equisetos y helechos.
- Se ha sugerido que las briofitas Bryophyta sensu lato son un grupo parafilético, sin embargo esta hipótesis no ha sido aceptada por muchos análisis moleculares.
Grupos extintos
[editar]Si tomamos en cuenta los principales grupos extintos, la filogenia aproximada (Kenrick & Crane 1997)[18] es la siguiente:
| Embryophyta |
| ||||||||||||||||||||||||||||||||||||||||||||||||
Otras consideraciones
[editar]Siguiendo clasificaciones tradicionales, en el siguiente cladograma se compara la filogenia de Judd et al (2002)[19] con el sistema de Engler (1924):
 Árbol filogenético de los diferentes grupos de embriofitos. |
Las relaciones filogenéticas entre las briofitas sensu lato y con el resto de las embriofitas aún no están del todo consensuadas (ver por ejemplo Quandt y Stech 2003). Todos los análisis de filogenia hechos hasta ahora concluyeron que «Bryophyta sensu lato» es parafilético. Sin embargo, las relaciones exactas se mantienen controversiales. Inicialmente los análisis morfológicos apoyaron una división basal entre el linaje de Marchantiophyta y todo lo demás, y ubicaba a los musgos como clado hermano de las plantas vasculares. Así «Bryophyta sensu lato» hubiera sido una serie de grados sucesivos, en que el primer linaje que se desprendía del resto era Marchantiophyta, luego en el otro clado aparecían los estomas por única vez, luego se desprendían los antoceros, luego en el resto aparecía un meristema apical en el esporófito, y finalmente se desprendían los musgos o Bryophyta sensu stricto del clado que derivaría en las plantas vasculares (Mishler y Churchill 1984).[20] 1985).[13] Bajo este punto de vista, ciertas células de los musgos especializadas en el transporte de fluidos, llamadas hydroides y leptoides (y presentes tanto en el esporófito como en el gametófito en algunas especies) fueron interpretadas como los precursores del sistema vascular de las plantas vasculares.
Los musgos y las plantas vasculares tienen esporófito que crecen en altura debido a la división celular de un meristema apical, y las primeras plantas vasculares también tenían gametófitos erguidos, como los musgos. Estas interpretaciones han sido sostenidas por algunos análisis moleculares, incluyendo un análisis que muestra que en todas las plantas terrestres excepto Marchantiophyta, aparecen 3 intrones mitocondriales (Qiu et al. 1998).[21]
Sin embargo, muchos estudios recientes de datos moleculares (individualmente o combinados con una variedad de caracteres morfológicos y ultraestructurales, especialmente la ultraestructura del esperma), sostienen una hipótesis alternativa. En estos árboles filogenéticos, los antoceros son los que ocupan el lugar de clado basal, hermano de todo el resto, y un clado que contiene a Marchantiophyta y a los musgos es el hermano de las plantas vasculares (Nickrent et al. 2002,[22] Renzaglia et al. 2002).[23]
Esta hipótesis es consistente con estudios detallados que indican que los hydroides y los leptoides de los musgos probablemente no sean homólogos con las traqueidas y las células cribosas, que conforman respectivamente el xilema primitivo y el floema primitivo de las plantas vasculares. (Ligrone et al. 2000).[24] El problema de este árbol filogenético es que supone que tanto los estomas como el meristema apical del tallo, o bien se perdieron en una línea, o bien aparecieron dos veces en dos eventos independientes. Este improbable escenario aún está en discusión. Lo único que es seguro hasta ahora, es que las briofitas como las conocíamos, son parafiléticas con respecto a las plantas vasculares.
Las embriofitas son descendientes de un alga verde y por lo tanto son un clado dentro de Viridiplantae.
Para algunos autores, las plantas terrestres son el reino Plantae. Otros incluyen a las algas verdes en el reino, por lo que consideran como el reino de las plantas a lo que hoy se conoce como Viridiplantae. Algunos consideran como parte del reino Plantae también a las algas rojas y los glaucófitos, clado Archaeplastida. Finalmente otros consideran que también deberían pertenecer al reino Plantae todos los organismos autótrofos que tengan clorofila, y que fijen el dióxido de carbono atmosférico utilizando la energía del Sol.
Diversidad
[editar] Hábito de gametófito de Sphagnum. . |
Musgos o Bryophyta sensu stricto. Son probablemente las plantas briofitas que resultan más familiares, y con unas 15.000 especies, son también el grupo más diverso de briofitos. La fase dominante de su ciclo de vida es la gametofítica, siendo el gametófito de vida libre, erguido y folioso. El esporófito forma un tallo único no ramificado terminado en un único esporangio (también llamado «cápsula»), donde por meiosis se producen las esporas haploides. Típicamente la dehiscencia del esporangio ocurre por el desprendimiento de una tapita llamada «opérculo». Cuando una espora germina, pasa por un estadio de «protonema», que tiene el aspecto de filamento de alga. El protonema produce uno o más gametófitos erguidos, que en última instancia produce esperma y huevos en los respectivos anteridios y arquegonios. Cuando se fusionan las gametas se forma el cigoto, que se desarrolla mediante una serie de divisiones mitóticas en un embrión, y después en un esporófito maduro. Los análisis filogenéticos dentro de los musgos han sostenido en general la hipótesis de que Sphagnum está situado cerca de la base del árbol filogenético, y que Andraea y unos pocos parientes cercanos también forman una ramificación temprana de la rama principal (ver Kenrick y Crane 1997a).[3] El enigmático Takakia, que era considerado un marchantiofito hasta el reciente descubrimiento de su fase esporofítica, también está probablemente situado cerca de la base del árbol filogenético de los musgos. El esporangio en Andreaea se abre a través de 4 hendiduras verticales, y en Takakia por una única hendidura helical, en cambio en la mayor parte de las especies el esporangio se abre a través de un opérculo. El opérculo de la mayoría de los musgos también se caracteriza por una distintiva fila de estructuras parecidas a dientes, que en conjunto forman lo que se conoce como «peristoma».
 Hábito de gametófito de Marchantia. . |
Hepáticas. Hay alrededor de 9.000 especies de marchantiofitas (hepáticas), cuyo gametófito posee una morfología taloide o, más comúnmente, foliosa. A diferencia de los musgos y los antoceros, las marchantiofitas son plantas sin estomas, aunque algunas de ellas poseen poros en la epidermis sin células acompañantes. También les falta la característica masa columnar de tejido estéril (llamada «columella») en el esporangio, que sí está presente en los musgos, los antoceros, y las plantas vasculares tempranas. Estas características de las marchantiofitas a veces han sido interpretadas como ancestrales dentro de las embriofitas, pero hoy en día ya no está claro si es así. La reproducción sexual en marchantiofitas ocurre mediante esperma y huevos producidos por anteridios y arquegonios respectivamente. La fase esporofítica, con su esporangio terminal, es más bien pequeña e inconspicua. La cápsula típicamente se abre gracias a 4 valvas, y puede ser que unas células higroscópicas estériles («eláteres») entre las esporas ayuden a la dispersión.
 Hábito de gametófito de Anthoceros. . |
Antoceros. Hay solo unas 100 especies de antoceros, que son mucho más difíciles de encontrar que los musgos y las hepáticas. Su gametófito es completamente taloide. Una característica que probablemente sea única de este grupo, es la presencia de un meristema intercalar en el esporófito, ubicado en la base de la cápsula. La actividad de este meristema es responsable del continuo crecimiento hacia arriba de la cápsula, que es bastante larga en algunos grupos (por ejemplo Anthoceros).
 Hábito de esporófito de una planta vascular con crecimiento secundario del tallo. . |
Plantas vasculares. Un clado bien definido de las embriofitas son las plantas vasculares, que comprenden a las lycophytas, monilophytas, gimnospermas y angiospermas. Todo indica que las primeras plantas vasculares eran pequeñas y muy simples en su estructura. Mucho de lo que sabemos acerca de las primeras plantas vasculares y su transición a la vida terrestre se encuentra en el registro fósil, ya que esos valiosos linajes están todos extintos (para más detalles ver Evolución de traqueofitas).
Véase también
[editar]Enlaces externos
[editar]- Stevens, P. F. (2001 en adelante). Angiosperm Phylogeny Website . Versión 7, mayo de 2006.
Referencias
[editar]- Kenrick P, Crane PR. 1997. The Origin and Early Evolution of Land Plants. Smithsonian Institution Press, Washington, DC
- Judd, W. S. Campbell, C. S. Kellogg, E. A. Stevens, P.F. Donoghue, M. J. 2002. Plant systematics: a phylogenetic approach, Second Edition. Sinauer Axxoc, USA.
Referencias citadas
[editar]- ↑ Engler, A. 1892. Syllabus der Vorlesungen über specielle und medicinisch-pharmaceutische Botanik: Eine Uebersicht über das ganze Pflanzensystem mit Berücksichtigung der Medicinal- und Nutzpflanzen. Berlin: Gebr. Borntraeger.
- ↑ Pirani, J. R.; Prado, J. (2012). «Embryopsida, a new name for the class of land plants» (PDF). Taxon 61 (5): 1096-1098.
- ↑ a b Kenrick, P y PR Crane. 1997a. The origin and early diversification of land plants: A cladistic study. Smithsonian Institution Press, Washington, DC.
- ↑ Kenrick, P y PR Crane. 1997b. The origin and early evolution of plants on land. Nature 389: 33-39.
- ↑ Karol, KG, RM McCourt, MT Cimino y CF Delwiche. 2001. The closest living relatives of land plants. Science 294: 2351-2353. (resumen aquí)
- ↑ Selosse, M.-A., y Le Tacon, F. 1998. The land flora: A phototroph-fungal partnership? Trends Ecol. Evol. 13: 15-20.
- ↑ Redecker, D., Kodner, R., y Graham, L. E. 2000. Glomalean fungi from the Ordovician. Science 289: 1920-1921.
- ↑ Nebel, M., Kreier, H.-P., Pressing, M., Weiß, M., y Köttke, I. 2004. Symbiotic fungal associations of liverworts are the possible ancestors of mycorrhizae. En: Agerer, R., Piepenbring, M., y Blanz, P. (editores), Frontiers in Basidiomycota Mycology. IHW-Verlag, Eching. pp. 339-360.
- ↑ Köttke, I, y Nebel, M. 2005. The evolution of mycorrhiza-like associations in liverworts: An update. New Phytol. 167: 330-334.
- ↑ Read, D. J., Duckett, J. G., Francis, R., Ligrone, R., y Russell, A. 2000. Symbiotic fungal associations in 'lower' land plants. Phil. Trans. Roy. Soc. London B. 355: 815-831.
- ↑ Remy, W. 1982. Lower Devonian gametophytes: Relation to the phylogeny of land plants. Science 215: 1625-1627.
- ↑ Remy, W, PG Gensel, y H Hass. 1993. The gametophyte generation of some early Devonian land plants. Int. J. Plant Sci. 154: 35-58.
- ↑ a b Mishler BD y SP Churchill. 1985. Transition to a land flora: Phylogenetic relarionships of the green algae and bryophytes. Cladistics 1: 305-328.
- ↑ Cox, Cymon J. (2014). «Conflicting Phylogenies for Early Land Plants are Caused by Composition Biases among Synonymous Substitutions». Systematic Biology 63 (2): 272-279. PMC 3926305. PMID 24399481. doi:10.1093/sysbio/syt109.
- ↑ Leebens-Mack, James H. (2019). «One thousand plant transcriptomes and the phylogenomics of green plants». Nature 574 (7780): 679-685. PMC 6872490. PMID 31645766. doi:10.1038/s41586-019-1693-2.
- ↑ Sousa, Filipe (2020). «The Chloroplast Land Plant Phylogeny: Analyses Employing Better-Fitting Tree- and Site-Heterogeneous Composition Models». Frontiers in Plant Science 11: 1062. PMC 7373204. PMID 32760416. doi:10.3389/fpls.2020.01062.
- ↑ Harris, Brogan J. (2020). «Phylogenomic Evidence for the Monophyly of Bryophytes and the Reductive Evolution of Stomata». Current Biology 30 (11): P2201-2012.E2. PMID 32302587. S2CID 215798377. doi:10.1016/j.cub.2020.03.048. hdl:1983/fbf3f371-8085-4e76-9342-e3b326e69edd.
- ↑ Kenrick, Paul & Crane, Peter R. (1997), The Origin and Early Diversification of Land Plants: a Cladistic Study, Washington, D.C.: Smithsonian Institution Press, ISBN 978-1-56098-730-7
- ↑ Judd, W. S. Campbell, C. S. Kellogg, E. A. Stevens, P.F. Donoghue, M. J. 2002. Plant systematics: a phylogenetic approach, Second Edition. Sinauer Axxoc, USA.
- ↑ Mishler, BD y SP Churchill. 1984. A cladistic approach to the phylogeny of the "bryophytes". Brittonia 36: 406-424.
- ↑ Qiu, Y-L, Y. Cho, JC. Cox y JD Palmer. 1998. The gain of three mitochondrial introns identifies liverworts as the earliest land plants. Nature 402: 404-407.
- ↑ Nickrent D, CL Parkinson, JD Palmer, y RJ Duff. 2000. Multigene phylogeny of land plants with special reference to bryophytes and the earliest land plants. Mol. Biol. Evol. 17: 19: 1885-1895.
- ↑ Renzaglia KS, RJ Duff, DL Nickrent y DJ Garbary. 2000. Vegetative and reproductive innovations of early land plants: Implications for a unified phylogeny. Philos. Trans. R. Soc. London [Biol.] 355: 769-793.
- ↑ Ligrone, R, JG Duckett y JS Renzaglia. 2000. Conducting tissues and phyletic relationships of bryophytes. Philos. Trans. R. Soc. London [Biol.] 355: 795-813.
