Amphiprion ocellaris
| Pez payaso | ||
|---|---|---|
 Pez payaso (Amphiprion ocellaris) | ||
| Estado de conservación | ||
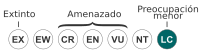 Preocupación menor (UICN 3.1) | ||
| Taxonomía | ||
| Reino: | Animalia | |
| Filo: | Chordata | |
| Clase: | Actinopterygii | |
| Orden: | Perciformes | |
| Suborden: | Labroidei | |
| Familia: | Pomacentridae | |
| Subfamilia: | Amphiprioninae | |
| Género: | Amphiprion | |
| Especie: |
A. ocellaris Cuvier, 1830 | |
| Sinonimia | ||
[1]
| ||






El pez payaso común o falso pez percula (Amphiprion ocellaris) es una especie de pez perciforme de la familia Pomacentridae.
El pez payaso es un pequeño pez marino, que forma parte del paisaje de los arrecifes de coral del océano Indo-Pacífico. Se caracteriza por sus intensos colores naranja y blanco bordeados por una delgada franja negra. Vive conjuntamente con las anémonas.
El término "pez payaso" es un nombre común, que engloba todas las especies de los géneros Amphiprion y Premnas, de la subfamilia Amphiprioninae.
Fácil de obtener en el mercado de acuariofilia marina, es un pez de mantenimiento sencillo. Por ello, constituyen una buena opción para acuarios marinos de principiantes. Se trata de una especie depredadora omnívora, que necesita un ligero aporte vegetal en su dieta.
La reproducción del pez payaso es muy compleja. Varios individuos hermafroditas facultativos, viven juntos en la misma anémona. El individuo más grande es siempre una hembra y el segundo en jerarquía, por orden de tamaño, es siempre el macho reproductor. Todos los demás peces son machos en estados diferentes de madurez (fenómeno conocido como protandria). Si muere la hembra, el macho más agresivo y grande del grupo cambia su sexo a hembra, y el segundo pez payaso más grande y agresivo, se convierte en el macho alfa o reproductor.[2]
Descripción[editar]
La coloración del cuerpo es de naranja brillante a marrón-rojizo, con tres franjas blancas, que cruzan longitudinalmente el cuerpo, dividiéndolo en tres porciones. Estas bandas están delimitadas con estrechos márgenes negros. La franja del medio, en su parte central, tiene un crecimiento mayor en dirección a la cabeza.
Los ejemplares juveniles tienen el color base del cuerpo más vivo y rojizo, mientras que los adultos van atenuando esa viveza de coloración, tornándose más naranja-marrón claro.
A. ocellaris tiene una aleta caudal redondeada y puede crecer hasta 110 mm de longitud.[3][4] Posee once espinas en la aleta dorsal, lo que le distingue del estrechamente relacionado Amphiprion percula, que posee 10. Cuenta con 13-17 radios dorsales suaves, 2 espinas anales y de 11-13 radios anales suaves.
Las hembras son más grandes que los machos de esta especie.[5][3] Normalmente doblan su tamaño.
Morfología[editar]
La especie A. Percula es casi idéntica, pero se puede diferenciar por sus respectivos colores y patrones. En A. ocellaris son por lo general menos vivos, además de que tienen 11 espinas de la aleta dorsal, mientras que A. percula tiene 10 (a veces 9). Además, la parte espinosa anterior de la aleta dorsal en A. ocellaris es más alta (la altura se ajusta alrededor de 2,1 -2,9 cm en la longitud de la cabeza, en comparación con 3,1-3,3 cm en A. percula). La mayoría de los A. percula tienen un margen negro más grueso, bordeando las franjas blancas de los peces. Las distribuciones de estas dos especies no se superponen.[6] También existen diferencias en la disposición de la coloración en los ojos, los A. percula tienen iris de color naranja brillante, haciendo que sus ojos parecen más pequeños, mientras que A. ocellaris posee una coloración gris o naranja grisácea, que hace que los ojos parezcan más grandes.[7]
Existe una rara variedad negra o mélanica, en la que se presenta el fondo en negro, en vez de la tonalidad naranja, con las rayas blancas normales. Se encuentra fuera del territorio norte de Australia,[8] en los arrecifes alrededor de Darwin. Aunque no es común en la naturaleza, se está volviendo más y más popular en la acuariofilia.
Mucosa superficial[editar]
Todos los peces tienen una membrana mucosa que cubre sus escamas. El moco suele contener altas cantidades de lípidos y glicoproteínas, sin embargo la familia Pomacentridae (pez de anémona) tienen una adaptación especial en la capa mucosa, siendo mucho más gruesa y espesa. A diferencia de otras especies de peces, la capa de protección de las especies del género Amphiprion, carece de una sustancia específica que desencadena el ataque de los nematocistos (las picaduras de una anémona), lo que permite la inmunidad contra las picaduras de peces tóxicos. Poco se sabe sobre el moco, excepto que su secreción se debe a factores genéticos, y la naturaleza de su composición pasa a través de las generaciones en cada especie. En otras familias de peces, el moco se utiliza como protección contra las bacterias dañinas, un regulador osmótico y también ayuda a los peces en la fabricación del nido. La diferencia en el moco ha llevado a la trayectoria divergente de los peces de anémonas y otras especies.[9]
Filogenia[editar]

La especie Amphiprion ocellaris se relaciona con la clase de los osteíctios (Osteichthyes), la misma que contiene a los peces óseos y los peces de aletas radiales. A. ocellaris es la especie más basal en el género Amphiprion, que está estrechamente relacionado con el género Premnas. La especie más estrechamente relacionada con un ancestro común, es el pez payaso naranja Amphiprion percula. Se cree que A. ocellaris especió rápidamente, divergiendo poco después de separarse el género Premnas.
La evidencia científica confirma que todos los peces payaso pertenecientes al género Amphiprion, en un comienzo debieron de soportar las picaduras de un solo tipo de anémona. A partir de este ancestro en común, divergieron las 28 diferentes especies de pez payaso, incluyendo a A. ocellaris. Estas especies fueron paulatinamente evolucionando para ser capaces de resistir las picaduras venenosas de muchas especies diferentes de anémonas.[10]
Ecología[editar]
Hábitat y distribución[editar]



Amphiprion ocellaris habita en los arrecifes de coral[5] y lagunas marinas protegidas por arrecifes de coral, hasta una profundidad de 15 metros.[11] Más concretamente, se encuentra principalmente en, o cerca, de las anémonas,[11] como parte de una relación simbiótica.[5][12]
Se encuentra en arrecifes de coral no muy lejanos de la costa, a no mucha profundidad, entre 1 y 15 metros (usualmente de 3 a 15 metros). Suelen habitar en grietas de los arrecifes de sustrato rocoso o calizo. Comensal de anémonas. Se alimenta de plantas (34%), invertebrados bentónicos (44%), y zooplancton.[13] Se suele encontrar con anémonas, en asociación de mutualismo, se asocia principalmente a las anémonas Heteractis magnifica, Stichodactyla gigantea y Stichodactyla mertensii.[5][12]
Su distribución comprende los mares de Asia y Australia, en el Indo-Pacífico occidental,[14] al éste del océano Índico, como islas de Andaman y Nicobar, Tailandia, Malasia, y del noroeste de Australia al sudeste asiático, Singapur, Indonesia y las Filipinas; limitando su rango al norte a Taiwán y las islas Ryukyu.[15][16]
Comportamiento[editar]
A. ocellaris mantiene una relación simbiótica no estricta, mutualista, con las anémonas de mar.[17] Estos peces dependen de la anémona de refugio. En aguas abiertas estos peces son más susceptibles a los depredadores, además de ser malos nadadores.
También las anémonas proveen protección a los nidos. Por su parte, en las anémonas se observa que, por lo general, están mejor con una especie hospedadora, también pueden beneficiarse por el consumo de parásitos por parte del pez y el aumento en la circulación del agua producto del aleteo.[18] Los peces anémona están protegidos contra la picadura de la anémona por su moco.[18] Ambos, el pez payaso y las anémonas de mar, pueden sobrevivir (con las dificultades antes mencionadas), cuando se separan el uno del otro. Sin embargo, curiosamente, si la separación dura más de unos pocos días o semanas (dependiendo de las especies de peces y de anémonas), cuando los compañeros se reúnen, y el pez nada entre los tentáculos de la hospedera, parece que ya no es inmune a la picadura de su vieja anémona. Por lo tanto, se ha inferido que la inmunidad a los nematocistos de las diferentes especies de anémonas es adquirida.
Hay evidencias de un período de aclimatación, que debe ocurrir antes de que el pez sea inmune a la picadura de la anémona. Esto implica un proceso en el que el pez nada en torno a la anémona, frotando su vientre y las aletas ventrales en los extremos de los tentáculos.[19] Un pez picado por su anémona retorna a su hospedera en varias ocasiones, pasando por una complicada y estereotipada danza de natación, cuidando de tocar los tentáculos en primer lugar sólo con sus aletas ventrales, y luego a todo su vientre. Finalmente, después de algunos minutos a varias horas de tal comportamiento de "aclimatación", es capaz de zambullirse en ella completamente. Adicionalmente, un pez que había estado viviendo lejos de las anemonas, podría ser sensible a los nematocistos de una anémona que no ha recibido peces payaso. A medida que los alevines comienzan la búsqueda de una anémona, su supervivencia depende de encontrar una anémona en la que residir, pero este proceso es complicado por la dinámica jerárquica dentro de las anémonas ya ocupadas por otros peces payaso, el pez juvenil recién llegado entra en el sistema social desde la parte inferior y se expone a la peor agresión y puede ser expulsado.[20] Las bases del sistema jerárquico se comunican a través de la agresión por los cohabitantes mayores hacia los individuos más pequeños.
A. ocellaris son capaces de encontrar las especies de anémonas de mar hospedadoras y regresar (si se alejan demasiado) a su propia anemona hospedera por pistas olfativas, debido a la impresión olfativa, o impronta, que tiene lugar cuando todavía estaba en su nido.[15][21][22][11][23]
Una curiosidad sobre el comportamiento de los A. ocellaris en cautividad, es la "adopción", a falta de una anémona, del coral blando Sarcophyton o del coral duro Catalaphyllia jardinei. Dada la similitud de los tentáculos de estos corales con los de algunas anémonas hospedantes, estos peces payaso se comportan con ellos como si fueran anémonas, manteniendo una relación mutualista: apenas se separan del coral, lo defienden de otras especies o géneros, y lo limpian de residuos. Se ha observado que, incluso han fijado la puesta de huevos en el esqueleto de un Catalaphyllia jardinei, quedando protegidos de posibles predadores por los tentáculos de éste, ya que los nematocistos de esta especie de coral son de los más potentes.
Mutualismo[editar]
A. ocellaris generalmente tiene una relación simbiótica con las anémonas de mar. El término más correcto sería mutualismo, dado que la supervivencia de ninguno de los dos involucrados depende completamente del otro, en pocas palabras, tanto la anémona como el pez pueden vivir separados sin mayores problemas, mientras que en una simbiosis estricta no es posible. Una anémona posee nematocistos sobre la superficie de sus tentáculos, estos nematocistos son capaces de inyectar una toxina paralizante, que utiliza para atrapar y matar sus presas, incluidos los peces. El pez payaso no nace inmune a la toxina de las anémonas, sino que se inmuniza lentamente con la ayuda de una capa de moco que segrega sobre su piel, impidiendo que los nematocistos de la anémona se adhieran en gran cantidad, lo que permite que su cuerpo absorba pequeñas dosis con las que paulatinamente se va acostumbrando el pez, llegando a ser completamente inmune a la toxina cuando es adulto.
Un pez payaso inmunizado puede moverse libremente entre los tentáculos de la anémona, lo que le permite utilizarlas como un microhábitat, donde encuentra alimento, refugio y protección contra peces de mayor tamaño. Al mismo tiempo el pez se alimenta de las partículas sobrantes de la alimentación de la anémona, así como de parásitos y otros organismos que pudieran afectarla. Ocasionalmente, A. ocellaris se encuentra compartiendo anémonas en armonía con el camarón anémona Periclimenes holthuisi.[24]
A. ocellaris acogerá más frecuentemente como hospedador a una o varias de las siguientes especies de anémonas:
- Heteractis magnifica
- Condylactis gigantea
- Stichodactyla gigantea
- Stichodactyla mertensii
- Entacmaea quadricolor
Alimentación[editar]

Alimentos planctónicos tales como el zooplancton, los copépodos, y las algas son la fuente primaria de alimento para A. ocellaris.[12] Se clasifican como omnívoros generalistas, ya que se alimentan de la misma cantidad de algas y animales.[25] También se reporta que llegan a consumir los parásitos de sus anémonas hospederas.[23] La alimentación, es también dominada por la dinámica en la estructura jerárquica del grupo en la anémona.
Debido a que los peces más pequeños reciben la mayor agresión de los demás, se ven obligados a reducir la energía invertida para alimentarse a grandes distancias de la anémona y tienden a estar cerca, donde la competencia interespecifica es mayor. Además, no es seguro para los peces más pequeños alejarse de la seguridad de la anémona.[26] El pez dominante busca alimento a mayores distancias, pero en general no más lejos que a varios metros de la anémona[26][12][25][27]
Depredadores[editar]
La depredación sobre los peces anémona, se reduce considerablemente debido a la relación con la anémona hospedera, cuya picadura disuade a los posibles depredadores. Los huevos son más susceptibles a la depredación, principalmente por otros peces damisela, de la familia Pomacentridae, sin incluir otros peces anémona, y lábridos.[28] La susceptibilidad a la depredación en los huevos aumenta en la noche, cuando el macho no los está vigilando y pueden ser víctimas de estrellas de mar u ofiuros.[28]
Funciones en el ecosistema[editar]


Como se mencionó anteriormente, A.ocellaris es parte de una relación simbiótica.[17] En esta relación, el pez recibe protección de la anémona en forma de un refugio diario para su nido. La anémona recibe protección también, como se ha documentado, ya que en ausencia de un pez huésped, las anémonas pueden ser atacadas por los peces mariposa o incluso tortugas.[29] Además, en presencia de los peces, las anemonas de la especie Entacmaea quadricolor desarrollan bulbos que se encuentran en el extremo de los tentáculos, se sospecha que dichas estructuras aumentan la superficie disponible para recibir energía solar, incrementando su metabolismo con ventajas considerables para la anémona.[21] Los bulbos no están presentes en la ausencia de los peces.[30][31][32]
Reproducción[editar]

Protandria[editar]
Las especies de peces pertenecientes al género Amphiprion nacen con órganos sexuales masculinos y femeninos en un mismo individuo, a esta condición se le denomina hermafroditismo, conviene aclarar en este punto, que existen especies de organismos hermafroditas con reproducción sexual y asexual, estos peces poseen reproducción sexual, por lo que requieren dos individuos de diferente sexo para aparearse exitosamente.
En los peces payaso, al dejar su estado larvario y comenzar a madurar sexualmente, los órganos masculinos son los que maduran primero (a esta condición ontogénica se le denomina protandria), por lo que, en cierta etapa, todos los individuos de una generación son machos. Posteriormente, al crecer y llegar la época de reproducción, en los grupos que conviven juntos, el macho de mayor tamaño y agresividad del grupo desarrolla sus órganos femeninos (al mismo tiempo que se atrofian los masculinos), convirtiéndose en la hembra dominante. Los demás peces se quedan como machos, y, la nueva hembra, se acoplará con el macho más grande de su grupo. Una vez un macho se convierta en hembra, el cambio es irreversible.[33][34]
Las hembras controlan a los machos mediante una agresiva dominación, así evitan la generación de otras hembras.[35] El macho más grande, a su vez domina a los juveniles y evita que otros machos consigan la fecundación durante el desove.[35]
La información específica sobre los hábitos de apareamiento de A. ocellaris es escasa, pero el comportamiento general que se cree típico de todos los peces anémona está documentado. Son territoriales a la anémona específica en la que habitan y son monógamos.[36] Antes del desove, la preparación del nido se hace por el macho, en un lugar seguro cerca de la anémona donde habite, por lo general una cavidad del arrecife o entre piedras con una superficie lisa. A su alrededor, el macho despejará el sustrato. La roca desnuda que elija, deberá estar lo suficientemente cerca de la anémona para que el nido tenga la protección de los tentáculos colgantes.[36]
Los machos atraen a la hembra mediante la extensión de las aletas, mordiéndola, y persiguiéndola.[26] Durante el desove, los machos son cada vez más agresivos.[26][36]
A. ocellaris es capaz de reproducirse durante casi todo el año, ya que vive en aguas tropicales,[36] aunque puede ser algo limitado en el extremo norte de su área de distribución durante los meses de invierno. El desove se concentra alrededor de la luna llena y ocurre generalmente en la mañana. Las posibles razones para esto son: fuertes corrientes de agua para la distribución de larvas, mayor abastecimiento de alimentos debido a desove sincronizado de invertebrados al mismo tiempo, y la visibilidad total aumentada.[36]
Cuando el desove está por ocurrir, el macho perseguirá a la hembra hasta el nido, pero la hembra comienza realmente el proceso. La hembra hace varias pasadas sobre el nido y, finalmente, pone huevos de color naranja durante el período de 1-2 horas antes de abandonar el nido.[36] Durante el desarrollo de la puesta, el macho mantendrá el flujo constante de oxígeno en el agua circundante, abanicando con sus aletas. Los huevos son de aproximadamente 3-4 mm de longitud y varían en número de 100 a 1000, dependiendo de la edad y el tamaño de los peces.[26] El macho entonces, continúa el proceso, fecundándolos conforme van saliendo, dando giros alrededor de la hembra al mismo tiempo que expulsa su esperma al pasar sobre los huevos.

Los huevos se pegan al sustrato con un hilo fino. La incubación se ve afectada por la temperatura del agua. Cuanto más fría sea el agua, el período de incubación será más largo. Pero, en general, requiere de 6 a 8 días antes de que la eclosión se produzca.[36] La etapa larval planctónica dura de 8 a 12 días y termina cuando los peces juveniles deciden volver al fondo, para tratar de encontrar una anémona que habitar.[26][35][12][36]
Los machos aportan la mayor parte del cuidado a la puesta, pero las hembras participan de forma esporádica. Las funciones principales del macho durante este periodo incluyen el abanicado de agua oxigenada a los huevos, proteger la puesta de otros peces y el comer los huevos que son infértiles o están dañados por hongos.[36]

Desarrollo[editar]
Después de la incubación, Amphiprion ocellaris entra en un estadio larval corto, en el que reside cerca de la superficie en una fase planctónica. A medida que cambian de larvas a alevines, por lo general dentro de un día, los peces se mudan moviéndose desde la superficie hasta el fondo, en busca de una anémona hospedera.[26] Una vez que los huevos eclosionan, pasan a la etapa larval, y son independientes de los padres, lo que implica que, los peces jóvenes que integran un grupo dentro de una misma anémona, no necesariamente están emparentados entre sí.[36]

Longevidad[editar]
A la fecha, la expectativa de vida no se ha estudiado plenamente en la naturaleza, pero se cree que A. ocellaris puede vivir de 2 hasta los 15 años.[26] Las larvas de peces son muy susceptibles a la depredación, ya que no tienen manera de defenderse a sí mismas, y porque tienen altas tasas de mortalidad. Experimentos de transferencia de cautividad se han realizado para abordar la posibilidad de repoblar los peces en las zonas donde se han agotado, en los cuales se ha encontrado que la supervivencia de los peces transferidos es mayor en comparación con los A. ocellaris más pequeños[26] .[3][3]
Relación con los humanos[editar]
Importancia económica[editar]
A. ocellaris es una especie importante en el comercio de peces de acuario tropicales, y ciertas coloraciones raras entre sus especies son especialmente buscadas.[37] Son fáciles de reproducir en cautiverio y pueden ser utilizados en la investigación.[36][37]
Conservación y amenazas[editar]
La alta demanda de A.ocellaris en el comercio de acuarios, ha reducido el tamaño de las poblaciones en algunos lugares, haciéndolas más susceptibles a la sobreexplotación y otras amenazas.[3] La especie no está clasificada como amenazada o en peligro de extinción (IUCN 2003), sin embargo, se incrementan las amenazas para los arrecifes de coral donde las poblaciones de A. ocellaris y de otras especies de peces payaso habitan, tales como: la sedimentación, la eutrofización, la contaminación del agua, la sobrepesca y la degradación de su hábitat producto del blanqueo de coral, debido al aumento de la temperatura del mar como consecuencia del calentamiento global.[38][3]
CITES reconoce como un riesgo para la conservación de cualquier especie, el que su comercio se popularice en el mercado de animales de ornato y/o de compañía. Afortunadamente A. ocellaris se reproduce exitosamente en cautiverio, lo que ha reducido la presión existente sobre las poblaciones silvestres para esta especie en particular.






Mantenimiento en cautividad[editar]
Requiere de una temperatura tropical en el agua, entre 24 y 27°.
En cautiverio, los ejemplares de A. ocellaris responden bien a una amplia variedad de alimentos procesados secos o extruidos para peces marinos tropicales, aun así, es recomendable el enriquecer su dieta con complementos y alimentos frescos para mantener los ejemplares sanos. La alimentación se basa en alimentos balanceados para peces tropicales, algas, zooplancton, gusanos y pequeños crustáceos. También son comúnmente utilizadas como alimento, especialmente durante las primeras etapas de desarrollo de las crías recién eclosionadas, al estadio de alevines, las larvas de crustáceos de los géneros: Mysis y Artemia.
Requiere de un acuario profusamente decorado con roca viva, corales y anémonas, que brinden resguardo a los peces y les den la sensación de protección. Estos peces tienen poca agresividad y gustan de formar grupos pequeños de 2 a 8 individuos. Generalmente viven de 2 a 6 años, habiendo casos excepcionales de una edad de 12 años en cautiverio.[39]
Compra en acuarios[editar]
El pez payaso es un pez tropical de agua de mar. Se recomienda comprar peces de criadero, ya que, aunque son un poco más caros, esta acción permitirá evitar la extinción de la especie en su medio natural.
Cría en cautividad[editar]
A. ocellaris ha sido exitosamente criado en cautividad, intensivamente en Florida para el comercio de acuarios. Los ejemplares criados en cautiverio destacan por tener una mayor tasa de supervivencia, están disponibles en varios sitios, incluso por Internet, y los distribuyen proveedores certificados.[40]
Cultura popular[editar]
La exitosa película de los estudios Pixar "Buscando a Nemo", popularizó este pez como mascota de acuario. Al comienzo de la película, el dentista que secuestra a Nemo erróneamente, se jacta de haberlo "salvado" de vivir en el arrecife. Desafortunadamente, al parecer, el mensaje ecológico de la película no tuvo el impacto esperado, dado que la venta de peces payasos se incrementó muchísimo después de la película, llegándose a vender más de 150.000 ejemplares por año de este pez.
Referencias[editar]
- ↑ [FishBase, Amphiprion ocellaris" (On-line)]
- ↑ [Newcomb, D. and W. Fink. 2004. "Amphiprion ocellaris" (On-line), Animal Diversity Web. Accessed January 02, 2012 http://animaldiversity.ummz.umich.edu/site/accounts/information/Amphiprion_ocellaris.html. ]
- ↑ a b c d e f [Nelson, J., P. Phang, L. Chou. 1996. Survival and growth rates of the anemonefish Amphiprion ocellaris: a transfer experiment. Journal of Fish Biology, 48: 1130-1138.]
- ↑ [Ref.1: «Copia archivada». Archivado desde el original el 3 de enero de 2012. Consultado el 2 de enero de 2012.]
- ↑ a b c d [Allen, G. 1997. Marine Fishes of Tropical Australia and South-East Asia. Perth: Western Australian Museum.]
- ↑ [Froese, Rainer, and Daniel Pauly, eds. (200). "Amphiprion ocellaris" in FishBase. April 2010 version.]
- ↑ [Amphiprion ocellaris (TSN 615174). Integrated Taxonomic Information System. Retrieved on 27 April 2010.]
- ↑ [Allen GR (1972) The Anemonefishes: Their Classification and Biology,2nd edn. TFH Publications, Neptune, NJ.]
- ↑ [Fricke, H.W. and S. Fricke. 1977. Monogamy and sex change by aggressive dominance in coral reef fish. Nature, 266:830-832.]
- ↑ [Ollerton J, McCollin D, Fautin DG, Allen GR. 2007. Finding NEMO: nestedness engendereg by mutualistic organization in anemonefish and their hosts. Proceedings of the Royal Society of London, Series B, 274, 591–598.]
- ↑ a b c [Myers, R. 1999. Miconesian Reef Fish: A Field Guide for Divers and Aquarists. Barrigada: Territory of Guam: Coral Graphics]
- ↑ a b c d e [Myers, R. 1999. Miconesian Reef Fish: A Field Guide for Divers and Aquarists. Barrigada: Territory of Guam: Coral Graphics.]
- ↑ [Sano, M., M. Shimizu and Y. Nose 1984 Food habits of teleostean reef fishes in Okinawa Island, southern Japan. University of Tokyo Press, Tokyo, Japan. 128 p.]
- ↑ [Fuente: http://www.aquamaps.org/preMap.php?cache=1&SpecID=Fis-31857&expert_id=7 Archivado el 9 de octubre de 2017 en Wayback Machine.]
- ↑ a b [Allen, G. 1997. Marine Fishes of Tropical Australia and South-East Asia. Perth: Western Australian Museum]
- ↑ [1]
- ↑ a b [ Myers, R. 1999. Miconesian Reef Fish: A Field Guide for Divers and Aquarists. Barrigada: Territory of Guam: Coral Graphics.]
- ↑ a b [ Fautin, D., G. Allen. 1992. Field Guide to Anemonefishes and their Host Sea Anemones. Perth: Western Australian Museum. ]
- ↑ [ MarineBio, 1998. "False Clownfish" (On-line). Accessed October 21, 2004 at http://www.marinebio.com/species.asp?id=29 Archivado el 23 de octubre de 2007 en Wayback Machine..]
- ↑ [ Thresher, R. 1984. Reproduction in Reef Fishes. New Jersey: T.F.H. Publications, Inc.. 2010/05/09 01:36:55.921 GMT-4.]
- ↑ a b [Fautin, D., G. Allen. 1992. Field Guide to Anemonefishes and their Host Sea Anemones. Perth: Western Australian Museum]
- ↑ [MarineBio, 1998. "False Clownfish" (On-line). Accessed October 21, 2004 at http://www.marinebio.com/species.asp?id=29 Archivado el 23 de octubre de 2007 en Wayback Machine.]
- ↑ a b [Thresher, R. 1984. Reproduction in Reef Fishes. New Jersey: T.F.H. Publications, Inc.. 2010/05/09 01:36:55.921 GMT-4]
- ↑ [Jake Pehrson: «Copia archivada». Archivado desde el original el 3 de marzo de 2012. Consultado el 3 de marzo de 2012.]
- ↑ a b [Sano, M., M. Shimizu, Y. Nose. 1984. Food habits of teleostean reef fishes in Okinawa Island, Southern Japan. Japan: University of Tokyo Press.]
- ↑ a b c d e f g h i [Fautin, D., G. Allen. 1992. Field Guide to Anemonefishes and their Host Sea Anemones. Perth: Western Australian Museum.]
- ↑ [Thresher, R. 1984. Reproduction in Reef Fishes. New Jersey: T.F.H. Publications, Inc.. 2010/05/09 01:36:55.921 GMT-4.]
- ↑ a b [ Arvedlund, M., I. Bundgaard, L. Nielsen. 2000. Host imprinting in anemonefishes (Pisces: Pomacentridae): does it dictate spawning site preferences?. Environmental Biology of Fishes, 58: 203-213.]
- ↑ [(MarineBio, 1998. "False Clownfish" (On-line). Accessed October 21, 2004 at http://www.marinebio.com/species.asp?id=29 Archivado el 23 de octubre de 2007 en Wayback Machine.) ]
- ↑ [Fautin, D., G. Allen. 1992. Field Guide to Anemonefishes and their Host Sea Anemones. Perth: Western Australian Museum. ]
- ↑ [MarineBio, 1998. "False Clownfish" (On-line). Accessed October 21, 2004 at http://www.marinebio.com/species.asp?id=29 Archivado el 23 de octubre de 2007 en Wayback Machine.. ]
- ↑ [Myers, R. 1999. Miconesian Reef Fish: A Field Guide for Divers and Aquarists. Barrigada: Territory of Guam: Coral Graphics. ]
- ↑ [Fricke H, Fricke S (1977) Monogamy and sex change by aggressive dominance in coral reef fish. Nature, 266, 830–832. ]
- ↑ [Buston PM (2003c) Morality is associated with social rank in the clown anemonefish (Amphiprion Percula). Marine Biology, 143,811–815. ]
- ↑ a b c [Fricke, H., S. Fricke. 1977. Monogamy and sex change by aggressive dominance in coral reef fish. Nature, 266: 830-832.]
- ↑ a b c d e f g h i j k [Thresher, R. 1984. Reproduction in Reef Fishes. New Jersey: T.F.H. Publications, Inc.. 2010/05/09 01:36:55.921 GMT-4.
- ↑ a b [Sadovy, Y., A. Vincent. 2002. Ecological Issue and the Trade in Live Reef Fishes. Pp. 395 in P. Sale, ed. Coral Reef Fishes. San Diego, California: Academic Press.]
- ↑ [Bhat, A. 2004. Coral reefs and their fauna: An underwater fantasyland. Resonance, September: 62-73.]
- ↑ [Florida Museum of Natural History 2005 Biological profiles: clown anemonefish. Retrieved on 26 August 2005, from: www.flmnh.ufl.edu/fish/Gallery/Descript/FalseClownAnemone/FalseClown Anemone.html. Ichthyology at the Florida Museum of Natural History: Education-Biological Profiles. FLMNH, University of Florida.]
- ↑ [Reproduction of Amphiprion ocellaris Document source:http://www.fishbase.org/Reproduction/FishReproSummary.php?ID=6509&GenusName=Amphiprion&SpeciesName=ocellaris&fc=350&StockCode=6830
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Amphiprion ocellaris.
Wikimedia Commons alberga una categoría multimedia sobre Amphiprion ocellaris. Wikispecies tiene un artículo sobre Amphiprion ocellaris.
Wikispecies tiene un artículo sobre Amphiprion ocellaris.
