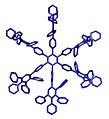
Molécula

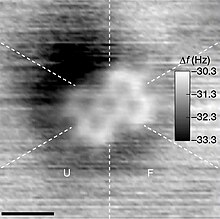


En química, una molécula (del nuevo latín molecula, que es un diminutivo de la palabra moles, 'masa') es un grupo eléctricamente neutro y suficientemente estable de al menos dos átomos en una configuración definida, unidos por enlaces químicos fuertes covalentes.[4][5][6][7][8][9]
En este estricto sentido, las moléculas se diferencian de los iones poliatómicos. En la química orgánica y la bioquímica, el término "molécula" se utiliza de manera menos estricta y se aplica también a los compuestos orgánicos (moléculas orgánicas) y en las biomoléculas.
Antes, se definía la molécula de forma menos general y precisa, como la más pequeña parte de una sustancia que podía tener existencia independiente y estable conservando aún sus propiedades fisicoquímicas. De acuerdo con esta definición, podían existir moléculas monoatómicas. En la teoría cinética de los gases, el término molécula se aplica a cualquier partícula gaseosa con independencia de su composición. De acuerdo con esta definición, los átomos de un gas noble se considerarían moléculas aunque se componen de átomos no enlazados.[10]
Una molécula puede consistir en varios átomos de un único elemento químico, como en el caso del oxígeno diatómico (O2),[11] o de diferentes elementos, como en el caso del agua (H2O).[12] Los átomos y complejos unidos por enlaces no covalentes como los enlaces de hidrógeno o los enlaces iónicos no se suelen considerar como moléculas individuales.
Las moléculas como componentes de la materia son comunes en las sustancias orgánicas (y por tanto en la bioquímica). También conforman la mayor parte de los océanos y de la atmósfera. Sin embargo, un gran número de sustancias sólidas familiares, que incluyen la mayor parte de los minerales que componen la corteza, el manto y el núcleo de la Tierra, contienen muchos enlaces químicos, pero no están formados por moléculas. Además, ninguna molécula típica puede ser definida en los cristales iónicos (sales) o en cristales covalentes, aunque estén compuestos por celdas unitarias que se repiten, ya sea en un plano (como en el grafito) o en tres dimensiones (como en el diamante o el cloruro de sodio). Este sistema de repetir una estructura unitaria varias veces también es válida para la mayoría de las fases condensadas de la materia con enlaces metálicos, lo que significa que los metales sólidos tampoco están compuestos por moléculas. En el vidrio (sólidos que presentan un estado vítreo desordenado), los átomos también pueden estar unidos por enlaces químicos sin que se pueda identificar ningún tipo de molécula, pero tampoco existe la regularidad de la repetición de unidades que caracteriza a los cristales.
Casi toda la química orgánica y buena parte de la química inorgánica se ocupan de la síntesis y reactividad de moléculas y compuestos moleculares. La química física y, especialmente, la química cuántica también estudian, cuantitativamente, en su caso, las propiedades y reactividad de las moléculas. La bioquímica está íntimamente relacionada con la biología molecular, ya que ambas estudian a los seres vivos a nivel molecular. El estudio de las interacciones específicas entre moléculas, incluyendo el reconocimiento molecular es el campo de estudio de la química supramolecular. Estas fuerzas explican las propiedades físicas como la solubilidad o el punto de ebullición de un compuesto molecular.[13]
Las moléculas rara vez se encuentran sin interacción entre ellas, salvo en gases enrarecidos y en los gases nobles. Así, pueden encontrarse en redes cristalinas, como el caso de las moléculas de H2O en el hielo o con interacciones intensas, pero que cambian rápidamente de direccionalidad, como en el agua líquida. En orden creciente de intensidad, las fuerzas intermoleculares más relevantes son: las fuerzas de Van der Waals y los puentes de hidrógeno.
La dinámica molecular es un método de simulación por computadora que utiliza estas fuerzas para tratar de explicar las propiedades de las moléculas.
No se puede definir una molécula típica para sales ni para cristales covalentes, aunque estos a menudo se componen de células unitarias repetidas que se extienden en un plano, por ejemplo, el grafeno ; o tridimensionalmente, por ejemplo, el diamante, el cuarzo, o el cloruro de sodio. El tema de la estructura celular unitaria repetida también se aplica a la mayoría de los metales que son fases condensadas con enlaces metálicos. Por tanto, los metales sólidos no están hechos de moléculas.
En los vidrios, que son sólidos que existen en un estado vítreo desordenado, los átomos se mantienen unidos por enlaces químicos sin presencia de ninguna molécula definible, ni ninguna de la regularidad de la estructura celular unitaria repetida que caracteriza a las sales, cristales covalentes y rieles.
Ciencia molecular[editar]
La ciencia de las moléculas se denomina química molecular o física molecular, dependiendo de si se centra en la química o en la física. La química molecular se ocupa de las leyes que rigen la interacción entre las moléculas que da lugar a la formación y ruptura de enlaces químicos, mientras que la física molecular se ocupa de las leyes que rigen su estructura y propiedades. En la práctica, sin embargo, esta distinción es imprecisa. En las ciencias moleculares, una molécula consiste en un sistema estable (estado ligado) compuesto por dos o más átomos. Los iones poliatómicos pueden considerarse a veces como moléculas cargadas eléctricamente. El término molécula inestable se utiliza para especies muy reactivas, es decir, conjuntos de corta duración (resonancias) de electrones y núcleos, como radicales, iones moleculares, moléculas de Rydberg, estados de transición, complejos de van der Waals, o sistemas de átomos en colisión como en el condensado de Bose-Einstein.
Historia y etimología[editar]
Según la Real Academia Española el vocablo «molécula» deriva del latín moles 'mole' o 'masa' y el sufijo diminutivo -ula 'masa pequeña'.[14]
- Molécula (1794) - «partícula extremadamente diminuta», del francés molécule (1678), del Nuevo Latín molecula, diminutivo del latín moles masa, barrera. Un significado vago al principio; la moda de la palabra (utilizada hasta finales del siglo XVIII solo en forma latina) se remonta a la filosofía de Descartes.[15][16]
La definición de molécula ha ido evolucionando a medida que ha aumentado el conocimiento de la estructura de las moléculas. Las definiciones anteriores eran menos precisas, y definían las moléculas como las partículas más pequeñas de sustancia químicas puras que aún conservan su composición y sus propiedades químicas.[17] Esta definición a menudo se rompe ya que muchas sustancias en la experiencia ordinaria, como rocas, sales, y metales, se componen de grandes redes cristalinas de átomos de enlace químico o iones, pero no están hechas de moléculas discretas.
Definición y sus límites[editar]
De manera menos general y precisa, se ha definido molécula como la parte más pequeña de una sustancia química que conserva sus propiedades químicas, y a partir de la cual se puede reconstituir la sustancia sin reacciones químicas. De acuerdo con esta definición, que resulta razonablemente útil para aquellas sustancias puras constituidas por moléculas, podrían existir las "moléculas monoatómicas" de gases nobles, mientras que las redes cristalinas, sales, metales y la mayoría de vidrios quedarían en una situación confusa.
Las moléculas lábiles pueden perder su consistencia en tiempos relativamente cortos, pero si el tiempo de vida medio es del orden de unas pocas vibraciones moleculares, estamos ante un estado de transición que no se puede considerar molécula. Actualmente, es posible el uso de láser pulsado para el estudio de la química de estos sistemas.
Las entidades que comparten la definición de las moléculas, pero tienen carga eléctrica se denominan iones poliatómicos, iones moleculares o moléculas ion. Las sales compuestas por iones poliatómicos se clasifican habitualmente dentro de los materiales de base molecular o materiales moleculares.

Las moléculas están formadas por partículas. Una molécula viene a ser la porción de materia más pequeña que aún conserva las propiedades de la materia original. Las moléculas se encuentran fuertemente enlazadas con la finalidad de formar materia. Las moléculas están formadas por átomos unidos por medio de enlaces químicos.
Una molécula es una unidad de sustancia que puede ser monoatómica o poliatómica. La unidad de todas las sustancias gaseosas es la molécula.[18]
Tipos de moléculas[editar]
Las moléculas se pueden clasificar en:
- Moléculas discretas: constituidas por un número bien definido de átomos, sean estos del mismo elemento (moléculas homonucleares, como el dinitrógeno o el fullereno) o de elementos distintos (moléculas heteronucleares, como el agua).
-
Molécula de agua, «disolvente universal», de importancia fundamental en innumerables procesos bioquímicos e industriales
-
Representación poliédrica del anión de Keggin, un polianión molecular
- Macromoléculas o polímeros: constituidas por la repetición de una unidad comparativamente simple —o un conjunto limitado de dichas unidades— y que alcanzan pesos moleculares relativamente altos.
-
Representación de un fragmento lineal de polietileno, el plástico más usado
-
Primera generación de un dendrímero, un tipo especial de polímero que crece de forma fractal
Enlaces[editar]
Los átomos que forman las moléculas se mantienen juntos mediante enlaces covalentes o enlaces iónicos. Varios tipos de elementos no metálicos existen solo como moléculas en el medio ambiente. Por ejemplo, el hidrógeno solo existe como molécula de hidrógeno. Una molécula de un compuesto está formada por dos o más elementos.[19] Una molécula homonuclear está formada por dos o más átomos de un solo elemento.
Mientras que algunas personas dicen que un cristal metálico puede considerarse una sola molécula gigante unida por enlaces metálicos,[20] otros señalan que los metales actúan de manera muy diferente a las moléculas.[21]
Covalente[editar]

Un enlace covalente es un enlace químico que implica el intercambio de pares de electrones entre átomos. Estos pares de electrones se denominan pares compartidos o pares de enlace, y el equilibrio estable de fuerzas atractivas y repulsivas entre átomos, cuando comparten electrones, se denomina enlace covalente.[22]
Iónico[editar]

El enlace iónico es un tipo de enlace químico que implica la atracción electrostática entre iones con carga eléctrica opuesta y es la interacción principal que se produce en los compuestos iónicos. Los iones son átomos que han perdido uno o más electrones (denominados cationes) y átomos que han ganado uno o más electrones (denominados aniones).[23] Esta transferencia de electrones se denomina electrovalencia en contraste con la covalencia. En el caso más simple, el catión es un átomo de metal y el anión es un átomo no metálico, pero estos iones pueden ser de naturaleza más complicada, por ejemplo, iones moleculares como NH4+ o SO4 2−.
A temperaturas y presiones normales, la unión iónica crea principalmente sólidos (u ocasionalmente líquidos) sin moléculas identificables separadas, pero la vaporización/sublimación de tales materiales produce pequeñas moléculas separadas donde los electrones aún se transfieren lo suficiente como para que los enlaces se consideren iónicos en lugar de covalentes.
Descripción[editar]
La estructura molecular puede ser descrita de diferentes formas. La fórmula molecular es útil para moléculas sencillas, como H2O para el agua o NH3 para el amoniaco. Contiene los símbolos de los elementos presentes en la molécula, así como su proporción indicada por los subíndices.
Para moléculas más complejas, como las que se encuentran comúnmente en química orgánica, la fórmula química no es suficiente, y vale la pena usar una fórmula estructural o una fórmula esqueletal, las que indican gráficamente la disposición espacial de los distintos grupos funcionales.
Cuando se quieren mostrar variadas propiedades moleculares, o se trata de sistemas muy complejos como proteínas, ADN o polímeros, se utilizan representaciones especiales, como los modelos tridimensionales (físicos o representados por ordenador). En proteínas, por ejemplo, cabe distinguir entre estructura primaria (orden de los aminoácidos), secundaria (primer plegamiento en hélices, hojas, giros…), terciaria (plegamiento de las estructuras tipo hélice/hoja/giro para dar glóbulos) y cuaternaria (organización espacial entre los diferentes glóbulos).

Moléculas en la teoría cuántica[editar]
La mecánica clásica y el electromagnetismo clásico no podían explicar la existencia y estabilidad de las moléculas, ya que de acuerdo con sus ecuaciones una carga eléctrica acelerada emitiría radiación por lo que los electrones necesariamente perderían energía cinética por radiación hasta caer sobre el núcleo atómico. La mecánica cuántica proveyó el primer modelo cualitativamente correcto que además predecía la existencia de átomos estables y proporcionaba explicación cuantitativa muy aproximada para fenómenos empíricos como los espectros de emisión característicos de cada elemento químico.
En mecánica cuántica una molécula o un ion poliatómico se describe como un sistema formado por electrones de masa y núcleos de masas . En mecánica cuántica las interacciones físicas de estos elementos se presentan por un hamiltoniano cuántico, cuyos autovalores serán las energías permitidas del sistema y cuyas autofunciones describirán los orbitales moleculares de la molécula, y de esos objetos se podrán deducir las propiedades químicas de la molécula. En lo que sigue se designará mediante e, la carga de cada electrón, mientras que la de cada núcleo, con protones, será . Para estudiar este sistema es necesario analizar el siguiente hamiltoniano cuántico:
(1)
definido sobre el espacio de funciones antisimetrizadas de cuadrado integrable , las coordenadas asociadas a las posiciones de los electrones vienen dadas por y la de los núcleos atómicos vienen dadas por . Y las interacciones electrostáticas entre electrones y núcleos vienen dadas por el potencial que se puede escribir como:
(2)
donde el primer término representa la interacción de los electrones entre sí, el segundo la interacción de los electrones con los núcleos atómicos, y el tercero las interacciones de los núcleos entre sí. En una molécula neutra se tendrá obviamente que:
Si se tendrá un átomo polielectrónico si , y un átomo hidrogenoide si .
Aproximación de Born-Oppenheimer[editar]
Resolver el problema de autovalores y autofunciones para el hamiltoniano cuántico dado por () es un problema matemático difícil, por lo que es común simplificarlo de alguna manera. Así dado que los núcleos atómicos son mucho más pesados que los electrones (entre 103 y 105 veces más) puede suponerse que los núcleos atómicos apenas se mueven comparados con los electrones, por lo que se considera que están congelados en posiciones fijas, con lo cual se puede aproximar el hamiltoniano () por la aproximación de Born-Oppenheimer dada por:
(3)
definido sobre el espacio de funciones y donde es la posición de los núcleos que para el análisis se considera fija. El resultado básico de este análisis viene dado por el siguiente resultado matemático:
|
La propiedad de ser autoadjunto implicará que las energías son cantidades reales, y el que sean acotados inferiormente implicará que existe un estado fundamental de mínima energía por debajo del cual los electrones no pueden decaer, y por tanto, las moléculas serán estables, ya que los electrones no pueden perder y perder energía como parecían predecir las ecuaciones del electromagnetismo clásico. Dos resultados matemáticos adicionales nos dicen como son las energías permitidas de los electrones dentro de una molécula:[24]
|
Además dentro de la mecánica cuántica puede demostrarse que pueden existir iones positivos (cationes, con carga positiva comparable al núcleo atómico), mientras que no es igual de fácil tener iones negativos (aniones), el siguiente resultado matemático implica tiene que ver con la posibilidad de cationes y aniones:[24]
|
Véase también[editar]
Referencias[editar]
- ↑ Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo; Hapala, Prokop; Ondráček, Martin; Jelínek, Pavel; Sugimoto, Yoshiaki (2015). «Chemical structure imaging of a single molecule by atomic force microscopy at room temperature». Nature Communications 6: 7766. Bibcode:2015NatCo...6.7766I. PMC 4518281. PMID 26178193. doi:10.1038/ncomms8766.
- ↑ Dinca, L.E.; De Marchi, F.; MacLeod, J.M.; Lipton-Duffin, J.; Gatti, R.; Ma, D.; Perepichka, D.F.; Rosei, F. (2015). «Pentacene on Ni(111): Room-temperature molecular packing and temperature-activated conversion to graphene». Nanoscale 7 (7): 3263-9. Bibcode:2015Nanos...7.3263D. PMID 25619890. doi:10.1039/C4NR07057G.
- ↑ Hapala, Prokop; Švec, Martin; Stetsovych, Oleksandr; Van Der Heijden, Nadine J.; Ondráček, Martin; Van Der Lit, Joost; Mutombo, Pingo; Swart, Ingmar et al. (2016). «Mapping the electrostatic force field of single molecules from high-resolution scanning probe images». Nature Communications 7: 11560. Bibcode:2016NatCo...711560H. PMC 4894979. PMID 27230940. doi:10.1038/ncomms11560.
- ↑ Unión Internacional de Química Pura y Aplicada: (1994) /M04002.html molecule, Compendium of Chemical Terminology, conocido como Gold Book.
- ↑ Pauling, Linus (1970). General Chemistry. Nueva York: Dover Publications, Inc. ISBN 0-486-65622-5.
- ↑ Ebbin, Darrell, D. (1990). General Chemistry, 3th Ed. Boston: Houghton Mifflin Co. ISBN 0-395-43302-9.
- ↑ Brown, T. L. (2003). Chemistry - the Central Science, 9th Ed.. Nueva Jersey: Prentice Hall. ISBN 0-13-066997-0.
- ↑ Chang, Raymond (1998). Chemistry, 6th Ed.. Nueva York: McGraw Hill. ISBN 0-07-115221-0.
- ↑ Zumdahl, Steven S. (1997). Chemistry, 4th ed. Boston: Houghton Mifflin. ISBN 0-669-41794-7.
- ↑ Chandra, Sulekh. Comprehensive Inorganic Chemistry. Nueva Era Publishers. ISBN 8122415121.
- ↑ Thibodeau, Gary A.; Patton, Kevin T. (2008-06). Estructura y función del cuerpo humano. Elsevier España. ISBN 9788480863551. Consultado el 5 de febrero de 2018.
- ↑ Vaquerizo, Dulce María Andrés (2016). Ciencias aplicadas a la actividad profesional 4º ESO. Editex. ISBN 9788490788097. Consultado el 5 de febrero de 2018.
- ↑ «Molecule». Encyclopædia Britannica. 22 de enero de 2016. Consultado el 23 de febrero de 2016.
- ↑ «molécula». RAE.
- ↑ Harper, Douglas. «molécula». Online Etymology Dictionary.
- ↑ «molecule». Merriam-Webster. Consultado el 22 de febrero de 2016.
- ↑ Molecule Definition Archivado el 13 de octubre de 2014 en Wayback Machine. (Frostburg State University)
- ↑ Ocampo, Dapueto, Piovano (2009). «1». En Universidad Nacional del Litoral, ed. Química General. Santa Fé, Argentina: Ediciones UNL. p. 9. ISBN 978-987-508-965-5.
- ↑ The Hutchinson unabridged encyclopedia with atlas and weather guide. Oxford, England. OCLC 696918830.
- ↑ Harry B. Gray. Chemical Bonds: An Introduction to Atomic and Molecular Structure. 1994. "Chapter 6: Bonding in Solids". p. 210-211.
- ↑ "How many gold atoms make gold metal?".
- ↑ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston: Pearson Prentice Hall. ISBN 978-0-13-250882-7. Consultado el 5 de febrero de 2012.
- ↑ Campbell, Flake C. (2008). Elements of Metallurgy and Engineering Alloys (en inglés). ASM International. ISBN 978-1-61503-058-3.
- ↑ a b Gustafson, S. J. & I. M. Sigal, 2011, p. 101.
Bibliografía[editar]
- Gustafson, S. J. & I. M. Sigal (2011): Mathematical Concepts of Quantum Mechanics, Springer-Verlag, ISBN 978-3-642-21866-8.
Enlaces externos[editar]
- Esta obra contiene una traducción automática y parcial derivada de «Molècula» de Wikipedia en catalán, concretamente de esta versión, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
 Wikimedia Commons alberga una categoría multimedia sobre Molécula.
Wikimedia Commons alberga una categoría multimedia sobre Molécula. Wikcionario tiene definiciones y otra información sobre molécula.
Wikcionario tiene definiciones y otra información sobre molécula.