Espectro de emisión


El espectro de emisión de un elemento químico o compuesto químico es el espectro de frecuencias de radiación electromagnética emitida debido a un átomo o molécula que realiza una transición de un estado de alta energía a un estado de menor energía. La energía fotónica emitida es igual a la diferencia de energía entre los dos estados. Hay muchas transiciones de electrones posibles para cada átomo, y cada transición tiene una diferencia de energía específica. Esta colección de diferentes transiciones, que conducen a diferentes longitudes de onda radiadas, conforman un espectro de emisión. El espectro de emisión de cada elemento es único. Por lo tanto, la espectroscopía se puede utilizar para identificar los elementos en materia de composición desconocida. De manera similar, los espectros de emisión de moléculas pueden usarse en el análisis químico de sustancias.
Emisión[editar]
En física, la emisión es el proceso por el cual un estado mecánico cuántico de mayor energía de una partícula se convierte en uno más bajo a través de la emisión de un fotón, lo que resulta en la producción de luz. La frecuencia de la luz emitida es una función de la energía de la transición. Dado que la energía debe conservarse, la diferencia de energía entre los dos estados es igual a la energía que se lleva el fotón. Los estados energéticos de las transiciones pueden conducir a emisiones en un amplio rango de frecuencias. Por ejemplo, la luz visible es emitida por el acoplamiento de estados electrónicos en átomos y moléculas (entonces el fenómeno se llama fluorescencia o fosforescencia). Por otro lado, las transiciones de cáscara nuclear pueden emitir rayos gamma de alta energía, mientras que las transiciones de giro nuclear emiten ondas de radio de baja energía.
La emisión de un objeto cuantifica la cantidad de luz que emite. Esto puede estar relacionado con otras propiedades del objeto a través de la ley de Stefan-Boltzmann. Para la mayoría de las sustancias, la cantidad de emisión varía con la temperatura y la composición espectroscópica del objeto, lo que lleva a la aparición de la temperatura de color y las líneas de emisión. Las mediciones precisas en muchas longitudes de onda permiten la identificación de una sustancia mediante espectroscopia de emisión.
La emisión de radiación se describe típicamente usando mecánica cuántica semiclásica: los niveles de energía de las partículas y los espaciamientos se determinan a partir de la mecánica cuántica, y la luz se trata como un campo eléctrico oscilante que puede conducir una transición si está en resonancia con la frecuencia natural del sistema. El problema de la mecánica cuántica se trata utilizando la teoría de la perturbación dependiente del tiempo y conduce al resultado general conocido como la regla de oro de Fermi. La descripción ha sido sustituida por la electrodinámica cuántica, aunque la versión semi-clásica sigue siendo más útil en los cálculos más prácticos.
Orígenes[editar]
Cuando los electrones en el átomo se excitan, por ejemplo, al calentarse, la energía adicional empuja los electrones a orbitales de mayor energía. Cuando los electrones vuelven a caer y dejan el estado excitado, la energía se vuelve a emitir en forma de fotón. La longitud de onda (o la frecuencia equivalente) del fotón está determinada por la diferencia de energía entre los dos estados. Estos fotones emitidos forman el espectro del elemento.
El hecho de que solo aparezcan ciertos colores en el espectro de emisión atómica de un elemento significa que solo se emiten ciertas frecuencias de luz. Cada una de estas frecuencias está relacionada con la energía por la fórmula:
- ,
donde es la energía del fotón, es su frecuencia, y es la constante de Planck. Esto concluye que solo los fotones con energías específicas son emitidos por el átomo. El principio del espectro de emisión atómica explica la variedad de colores en letreros de neón, así como los resultados de las pruebas de llama química.
Las frecuencias de luz que un átomo puede emitir dependen de los estados en los que se encuentran los electrones. Cuando está excitado, un electrón se mueve a un nivel de energía más alto u orbital. Cuando el electrón vuelve a su nivel del suelo, la luz se emite.

La imagen de arriba muestra el espectro de emisión de luz visible para el hidrógeno. Si solo estuviera presente un solo átomo de hidrógeno, entonces solo se observaría una longitud de onda en un instante dado. Se observan varias de las posibles emisiones porque la muestra contiene muchos átomos de hidrógeno que se encuentran en diferentes estados de energía iniciales y alcanzan diferentes estados de energía final. Estas diferentes combinaciones conducen a emisiones simultáneas en diferentes longitudes de onda.
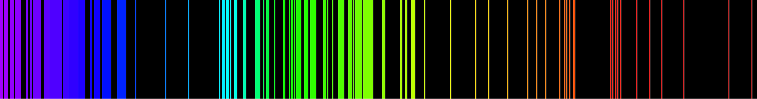
Radiación de las moléculas[editar]
Además de las transiciones electrónicas discutidas anteriormente, la energía de una molécula también puede cambiar a través de transiciones rotacionales, vibracionales y vibrónicas (combinadas vibratorias y electrónicas). Estas transiciones de energía a menudo conducen a grupos muy espaciados de muchas líneas espectrales diferentes, conocidas como bandas espectrales. Los espectros de banda sin resolver pueden aparecer como un continuo espectral.
Espectroscopia de emisión[editar]
La luz consiste en radiación electromagnética de diferentes longitudes de onda. Por lo tanto, cuando los elementos o sus compuestos se calientan en una llama o por un arco eléctrico, emiten energía en forma de luz. El análisis de esta luz, con la ayuda de un espectroscopio, nos da un espectro discontinuo. Un espectroscopio o un espectrómetro es un instrumento que se utiliza para separar los componentes de la luz, que tienen diferentes longitudes de onda. El espectro aparece en una serie de líneas llamadas el espectro de líneas. Este espectro lineal se denomina espectro atómico cuando se origina a partir de un átomo en forma elemental. Cada elemento tiene un espectro atómico diferente. La producción de espectros de línea por los átomos de un elemento indica que un átomo puede irradiar solo una cierta cantidad de energía. Esto lleva a la conclusión de que los electrones unidos no pueden tener cualquier cantidad de energía, sino solo una cierta cantidad de energía.
El espectro de emisión se puede utilizar para determinar la composición de un material, ya que es diferente para cada elemento de la tabla periódica. Un ejemplo es la espectroscopia astronómica: identificar la composición de las estrellas mediante el análisis de la luz recibida. Las características del espectro de emisión de algunos elementos son claramente visibles a simple vista cuando estos elementos se calientan. Por ejemplo, cuando el alambre de platino se sumerge en una solución de nitrato de estroncio y luego se inserta en una llama, los átomos de estroncio emiten un color rojo. De manera similar, cuando el cobre se inserta en una llama, la llama se vuelve verde. Estas características definidas permiten identificar los elementos por su espectro de emisión atómica. No todas las luces emitidas son perceptibles a simple vista, ya que el espectro también incluye los rayos ultravioleta y la iluminación infrarroja. Una emisión se forma cuando un gas excitado se ve directamente a través de un espectroscopio.

La espectroscopia de emisión es una técnica espectroscópica que examina las longitudes de onda de los fotones emitidos por los átomos o moléculas durante su transición de un estado excitado a un estado de menor energía. Cada elemento emite un conjunto característico de longitudes de onda discretas de acuerdo con su estructura electrónica, y al observar estas longitudes de onda se puede determinar la composición elemental de la muestra. La espectroscopia de emisión se desarrolló a fines del siglo XIX y los esfuerzos en la explicación teórica de los espectros de emisión atómica condujeron finalmente a la mecánica cuántica.
Hay muchas maneras en que los átomos pueden ser llevados a un estado excitado. La interacción con la radiación electromagnética se utiliza en espectroscopia de fluorescencia, protones u otras partículas más pesadas en la emisión de rayos X inducida por partículas y electrones o fotones de rayos X en espectroscopia de rayos X de dispersión de energía o fluorescencia de rayos X. El método más simple es calentar la muestra a una temperatura alta, después de lo cual las excitaciones se producen por colisiones entre los átomos de la muestra. Este método se utiliza en la espectroscopia de emisión de llama, y también fue el método utilizado por Anders Jonas Ångström cuando descubrió el fenómeno de las líneas de emisión discretas en la década de 1850.[1]
Aunque las líneas de emisión son causadas por una transición entre estados de energía cuantificados y pueden parecer muy nítidas al principio, tienen un ancho finito, es decir, están compuestas por más de una longitud de onda de luz. Esta ampliación de líneas espectrales tiene muchas causas diferentes.
La espectroscopia de emisión a menudo se denomina espectroscopia de emisión óptica debido a la naturaleza luminosa de lo que se está emitiendo.
Historia[editar]
Líneas de emisión de gases calientes fueron descubiertas por primera vez por Ångström, y la técnica fue desarrollada por David Alter, Gustav Kirchhoff y Robert Bunsen.
Técnica experimental en espectroscopia de emisión de llama[editar]
La solución que contiene la sustancia relevante a analizar se introduce en el quemador y se dispersa en la llama como un rocío fino. El disolvente se evapora primero, dejando partículas sólidas finamente divididas que se mueven a la región más caliente de la llama donde se producen los átomos y los iones gaseosos. Aquí los electrones se excitan como se describe anteriormente. Es común que se use un monocromador para permitir una fácil detección.
En un nivel simple, la espectroscopia de emisión de llama se puede observar utilizando solo una llama y muestras de sales metálicas. Este método de análisis cualitativo se llama prueba de llama. Por ejemplo, las sales de sodio colocadas en la llama brillarán de color amarillo de los iones de sodio, mientras que los iones de estroncio (que se usan en los destellos de la carretera) los colorearán de rojo. El alambre de cobre creará una llama de color azul, sin embargo, en presencia de cloruro da verde (contribución molecular por CuCl).
Coeficiente de emisión[editar]
El coeficiente de emisión es un coeficiente en la potencia de salida por unidad de tiempo de una fuente electromagnética, un valor calculado en física. El coeficiente de emisión de un gas varía con la longitud de onda de la luz. Tiene unidades de ms−3 sr−1.[2] También se usa como una medida de las emisiones ambientales (en masa) por MWh de electricidad generada.
Dispersión de la luz[editar]
En la dispersión de Thomson una partícula cargada emite radiación bajo la luz incidente. La partícula puede ser un electrón atómico ordinario, por lo que los coeficientes de emisión tienen aplicaciones prácticas.
Si X dV dΩ dλ es la energía dispersada por un elemento de volumen dV en un ángulo sólido dΩ entre las longitudes de onda λ y λ + dλ por unidad de tiempo, entonces el coeficiente de emisión es X.
Los valores de X en la dispersión de Thomson se pueden predecir a partir del flujo incidente, la densidad de las partículas cargadas y su sección transversal diferencial de Thomson (área/ángulo sólido).
Emisión espontánea[editar]
Un cuerpo cálido que emite fotones tiene un coeficiente de emisión monocromático relacionado con su temperatura y la radiación de potencia total. Esto a veces se denomina segundo coeficiente de Einstein y puede deducirse de la teoría de la mecánica cuántica.
Véase también[editar]
- Espectroscopia de absorción
- Línea espectral atómica
- Espectroscopia electromagnética
- Líneas de Fraunhofer
- Lámpara de descarga
- Cambio isomérico
- Cambio isotópico
- Coeficiente luminoso
- Fórmula de Rydberg
- Línea espectral
- Teoría espectral
- La ecuación de diodo incluye el coeficiente de emisión.
- Emisión termoiónica
Referencias[editar]
- ↑ Incorporated, SynLube. «Spectroscopy Oil Analysis». www.synlube.com (en inglés). Consultado el 24 de febrero de 2017.
- ↑ Carroll, Bradley W. (2007). An introduction to modern astrophysics (2nd ed edición). Pearson Addison-Wesley. p. 256. ISBN 0-8053-0402-9. OCLC 69020924.




