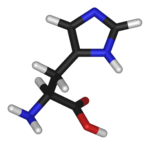
Histidina
| Histidina | ||
|---|---|---|
  | ||
| Nombre IUPAC | ||
| Ácido 2-amino-3-(1H-imidazol-5-il) propanoico | ||
| General | ||
| Símbolo químico | His, H | |
| Fórmula estructural |
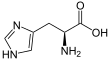 | |
| Fórmula molecular | C6H9N3O2 | |
| Identificadores | ||
| Número CAS | 71-00-1[1] | |
| ChEBI | 57595 15971, 57595 | |
| ChEMBL | CHEMBL17962 | |
| ChemSpider | 6038 | |
| DrugBank | DB00117 | |
| PubChem | 6274 | |
| UNII | 4QD397987E | |
| KEGG | C00135 | |
|
C1=C(NC=N1)CC(C(=O)O)N
| ||
| Propiedades físicas | ||
| Masa molar | 155,16 g/mol | |
| Punto de fusión | 560 K (287 °C) | |
| Propiedades químicas | ||
| Acidez | 1,70; 6,04; 9,09 pKa | |
| Familia | Aminoácido | |
| Esencial | Sí | |
| Codón | CAU, CAC | |
| Punto isoeléctrico (pH) | 7,59 | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La histidina (abreviado como His o H) es un aminoácido esencial en animales (no puede ser fabricado por su propio organismo y debe ser ingerido en la dieta), mientras que bacterias, hongos y plantas pueden sintetizarlo internamente.[2] Es uno de los 20 aminoácidos que forman parte de las proteínas codificadas genéticamente. Las abreviaturas oficiales son His y H. Su grupo funcional es un imidazol, que puede estar cargado positivamente dependiendo del pH del medio. La histidina fue purificada por primera vez por Albrecht Kossel en 1896, en Alemania.
Los productos lácteos, la carne, el pollo y el pescado contienen histidina en cantidades significativas. La histidina es un precursor de la histamina, en la que se transforma mediante una descarboxilación. La histamina es una sustancia liberada por las células del sistema inmune durante una reacción alérgica. Participa también en el desarrollo y manutención de los tejidos sanos, particularmente en la mielina que cubre las neuronas.
Propiedades químicas
[editar]El grupo imidazol de la histidina tiene un pKa de 6,0.[3] Esto significa que pequeñas variaciones del pH fisiológico cambiarán su carga total. Por debajo de un pH de 6, el anillo imidazol está mayoritariamente protonado, con carga positiva.
Durante la catálisis el nitrógeno básico de la histidina es capaz de captar un protón de la serina, tirosina y cisteína, por eso forma parte del centro catalítico de determinados enzimas.
Su cadena lateral está cargada positivamente (aminoácido básico) a valores de pH fisiológico. De los veinte alfa-aminoácidos, únicamente la cadena lateral de la histidina (con un pKa=6) cambia su estado de ionización dentro de la escala de pH fisiológicos. Este hecho tiene como consecuencia que las cadenas laterales de la histidina participen en las reacciones catalíticas de las enzimas.
En lo que respecta a su papel en la molécula de hemoglobina, el quinto ligando del hemo Fe(II) es HisF8, la histidina proximal (cercana). En la oxihemoglobina el Fe(II) está posicionado 0,22 Å fuera del plano del hemo del lado de la histidina proximal y, además, está coordinado por oxígeno. La histidina distal (distante) se une mediante un puente de hidrógeno al oxígeno. En la hemoglobina la sexta posición del ligando Fe (II) se movió hasta un punto de 0,55 Å fuera del plano del hemo.
La histidina puede degradarse dando lugar a alfa-cetoglutarato, aunque la conversión de la histidina en glutamato es más complicada respecto a la del resto de aminoácidos que se degradan mediante esta reacción. Se desamina de forma no oxidativa, luego se hidrata y su anillo imidazol se fragmenta para formar N-formiminoglutamato. Luego el grupo formimino transfiere el tetrahidrofolato para formar ácido glutámico y N5-formimino-tetrahidrofolato.
Biosíntesis de la histidina
[editar]Cinco de los seis átomos de la histidina derivan del 5-fosforribosil-alfa-pirofosfato (PRPP), un intermediario también involucrado en la biosíntesis del triptófano, los nucleótidos de purina y los de pirimidina. El sexto carbono de la histidina se origina a partir del ATP. Los átomos de ATP que no se incorporan en la histidina se eliminan como 5-aminoimidazol-4-carboxamida, ribonucleótido que también es un intermediario en la síntesis de purinas. La biosíntesis inusual de la histidina a partir de una purina se citó como evidencia que apoya la hipótesis de que la vida en su origen se basó en el ARN. Los residuos de histidina son con frecuencia componentes de los centros activos de las enzimas, donde actúan como nucleófilos o catalizadores generales ácido-base, o ambos. Por consiguiente, el descubrimiento de que el ARN tiene propiedades catalíticas sugiere que la mitad imidazol de las purinas cumple un papel similar en estos enzimas ARN (ribozimas). Esto sugiere que la vía de la síntesis de la histidina es un fósil de la transición hacia una forma de vida más eficiente basada en proteínas.
Características y beneficios
[editar]Al eliminar el grupo ácido carboxílico de la histidina, gracias a la enzima histidina descarboxilasa, se convierte en histamina, una importante sustancia fisiológica que se encuentra libremente presente en el intestino y en los gránulos basófilos de las células del sistema fagocítico mononuclear.
La histamina es un poderoso vasodilatador, y está involucrado en reacciones alérgicas, como la urticaria o la inflamación. La histamina también estimula la secreción de pepsina y ácido clorhídrico por el estómago.
La histidina se encuentra elevada en plasma y cerebro durante deficiencias de proteínas y también en algunas condiciones patológicas, lo que dirige la posibilidad de provocar efectos directos en funciones del sistema nervioso central.
Usos terapéuticos de la histidina
[editar]Este aminoácido es vital para nuestro organismo ya que su descarboxilación permite su transformación en histamina, por lo que es utilizada en el tratamiento de la artritis reumatoide (inflamación y falta de movilidad), enfermedades alérgicas, úlceras y anemia. En combinación con la hormona de crecimiento y otros aminoácidos, contribuye a la reparación de los tejidos, especialmente en el sistema cardiovascular. En el sistema nervioso central es sintetizada y liberada por las neuronas y utilizada como neuromodulador.
Fuera del sistema nervioso es un mediador de medios fisiológicos. La deficiencia de histidina puede causar problemas en la audición. También se sabe que la histidina ayuda en la desintoxicación de metales pesados, ayuda en el tratamiento de la impotencia y la frigidez, mejora la respuesta inmunitaria, ayuda a evitar los vómitos en el embarazo. Es importante también en el mantenimiento de las vainas de mielina que rodean los axones neuronales. Es necesaria también tanto para la producción de glóbulos rojos como blancos en la sangre, protege al organismo de los daños por radiación y reduce la presión arterial.
Enfermedades asociadas
[editar]Escombroidosis
[editar]La actividad bacteriana presente en algunos alimentos, principalmente en la carne de los pescados (producto de la descomposición bacteriana que se produce después de ser capturado el pez), provoca la degradación del aminoácido histidina presente en la carne, la cual conlleva a que se produzca concentraciones elevadas de histamina en este tipo de alimentos; provocando una intoxicación alimentaria denominada Escombroidosis al aportar histamina al organismo.[4]
Referencias
[editar]- ↑ Número CAS
- ↑ Robert A. Ingle: Histidine Biosynthesis. Sin embargo, el ser humano adulto lo produce de manera normal (los niños no). The Arabidopsis Book. American Society of Plant Biologists, 9, e0141. doi:10.1199/tab.0141.
- ↑ PubChem: Histidine (compound summary)
- ↑ A Hijano Baola, P Carreño Freire, JC Estévez Muñoz, C García de la Rasilla Cooper: Sospecha de escombroidosis. Archivado el 21 de febrero de 2014 en Wayback Machine. SEMERGEN - Medicina de familia. Vol. 31. Núm. 07, julio 2005, doi: 10.1016/S1138-3593(05)72941-5. Consultado el 7 de febrero de 2014.
- BIOQUÍMICA: Fundamentos para medicina y ciencias de la vida / Müller-Sterl, Werner; [Versión española por Josep Joan Centelles Serra].- Barcelona: Reverté, 2008
- BIOQUÍMICA / Donald Voet y Judith G. Voet - 3ª edición - Buenos Aires: Médica Panamericana, 2006. Traducido por: Silvia Rondinone, Diana Klajn y M.V. Preciado
- LEHNINGER: PRINCIPIOS DE BIOQUÍMICA / David L. Nelson y Michael M. Cox - 5.ª edición - Barcelona: Ediciones Omega 2009. Traducido por: Claudi M. Cuchillo
