Eje hipotalámico-hipofisario-gonadal

El eje hipotálamo-hipofisario-gonadal o eje hipotálamo-pituitario-gonadal (eje HPG, del inglés Hypothalamic–pituitary–gonadal axis) se refiere al hipotálamo, la hipófisis y las glándulas gonadales como si estas glándulas endocrinas individuales fueran una sola entidad. Debido a que estas glándulas a menudo actúan en conjunto, los fisiólogos y endocrinólogos encuentran conveniente y descriptivo hablar de ellas como un solo sistema.
El eje HPG juega un papel fundamental en el desarrollo y la regulación de una serie de sistemas del cuerpo, como los sistemas reproductivo e inmunológico. Las fluctuaciones en este eje provocan cambios en las hormonas producidas por cada glándula y tienen diversos efectos locales y sistémicos en el cuerpo.
El eje controla el desarrollo, la reproducción y el envejecimiento en los animales. La hormona liberadora de gonadotropina (GnRH) es secretada por las neuronas de GnRH del hipotálamo. La porción anterior de la hipófisis produce hormona luteinizante (LH) y hormona estimulante del folículo (FSH), y las gónadas producen estrógeno y testosterona.
En organismos ovíparos, el eje HPG se denomina comúnmente eje hipotálamo-hipófisis-gonadal-hígado (eje HPGL) en las hembras. Muchas proteínas coriónicas y de yema de huevo se sintetizan heterólogamente en el hígado, que son necesarias para el crecimiento y desarrollo de los ovocitos. Ejemplos de tales proteínas hepáticas necesarias son la vitelogenina y la coriogenina.
Los ejes HPA, HPG y HPT son tres vías en las que el hipotálamo y la hipófisis dirigen la función neuroendocrina.
Ubicación y regulación
[editar]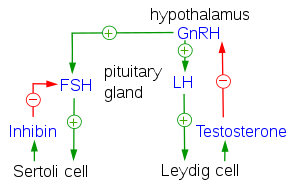
El hipotálamo se encuentra en el cerebro y secreta GnRH.[1] La GnRH desciende por la porción anterior de la hipófisis a través del sistema portal hipofisario y se une a los receptores de las células secretoras de la adenohipófisis.[2] En respuesta a la estimulación de GnRH, estas células producen LH y FSH, que viajan al torrente sanguíneo.[3]
Estas dos hormonas juegan un papel importante en la comunicación con las gónadas. En las mujeres, la FSH y la LH actúan principalmente para activar los ovarios para que produzcan estrógeno e inhibina y para regular el ciclo menstrual y el ciclo ovárico. El estrógeno forma un bucle de retroalimentación negativa al inhibir la producción de GnRH en el hipotálamo. La inhibina actúa para inhibir la activina, que es una hormona producida periféricamente que estimula positivamente a las células productoras de GnRH. La folistatina, que también se produce en todos los tejidos del cuerpo, inhibe la activina y le da al resto del cuerpo más control sobre el eje. En los hombres, la LH estimula las células intersticiales ubicadas en los testículos para producir testosterona, y la FSH juega un papel en la espermatogénesis. Los machos solo secretan pequeñas cantidades de estrógeno. Investigaciones recientes han demostrado que existe un eje de neuroesteroides, que ayuda a la corteza a regular la producción de GnRH en el hipotálamo.[4]
Además, la leptina y la insulina tienen efectos estimulantes y la grelina tiene efectos inhibitorios sobre la secreción de la hormona liberadora de gonadotropina (GnRH) del hipotálamo.[5] La kisspeptina también influye en la secreción de GnRH.[6]
Función
[editar]Reproducción
[editar]Una de las funciones más importantes del eje HPG es regular la reproducción controlando los ciclos uterino y ovárico.[7] En las mujeres, el ciclo de retroalimentación positiva entre el estrógeno y la hormona luteinizante ayuda a preparar el folículo en el ovario y el útero para la ovulación y la implantación. Cuando se libera el óvulo, el saco folicular vacío comienza a producir progesterona para inhibir el hipotálamo y la hipófisis anterior, deteniendo así el ciclo de retroalimentación positiva de estrógeno-LH. Si ocurre la concepción, la placenta se hará cargo de la secreción de progesterona; por lo tanto, la madre no puede volver a ovular. Si no se produce la concepción, la disminución de la excreción de progesterona permitirá que el hipotálamo reinicie la secreción de GnRH. Estos niveles de hormonas también controlan el ciclo uterino (menstrual) que provoca la fase de proliferación en preparación para la ovulación, la fase secretora después de la ovulación y la menstruación cuando no se produce la concepción. La activación del eje HPG tanto en hombres como en mujeres durante la pubertad también hace que los individuos adquieran características sexuales secundarias.
En los hombres, la producción de GnRH, LH y FSH es similar, pero los efectos de estas hormonas son diferentes.[8] La FSH estimula las células sustentaculares para que liberen proteína transportadora de andrógenos, que promueve la unión de testosterona. La LH se une a las células intersticiales y hace que secreten testosterona. La testosterona es necesaria para la espermatogénesis normal e inhibe el hipotálamo. La inhibina es producida por las células espermatogénicas, que, también mediante la inactivación de la activina, inhibe el hipotálamo. Después de la pubertad, los niveles de estas hormonas permanecen relativamente constantes.
Ciclo vital
[editar]La activación y desactivación del eje HPG también ayuda a regular los ciclos de vida.[7] Al nacer, los niveles de FSH y LH están elevados, y las hembras también tienen un suministro de por vida de ovocitos primarios. Estos niveles disminuyen y permanecen bajos durante la niñez. Durante la pubertad, el eje HPG es activado por las secreciones de estrógeno de los ovarios o de testosterona de los testículos. Esta activación de estrógenos y testosterona provoca cambios fisiológicos y psicológicos. Una vez activado, el eje HPG continúa funcionando en los hombres por el resto de su vida, pero se desregula en las mujeres, lo que lleva a la menopausia. Esta desregulación se debe principalmente a la falta de ovocitos que normalmente producen estrógeno para crear el ciclo de retroalimentación positiva. Durante varios años, la actividad del eje HPG disminuye y las mujeres ya no son fértiles.[9]
En la menopausia, el organismo detecta como si el ovario estuviera sufriendo un “fallo”, sin embargo, este proceso es totalmente fisiológico.[10] En la menopausia se producirá un aumento de la hormonas que se encuentran «aguas arriba» del ovario, para intentar compensar la disminución funcional que se está produciendo en este. En un análisis de sangre de una mujer menopáusica, encontraremos los niveles de FSH y LH elevados, respecto a los valores fisiológicos.
Aunque los machos siguen siendo fértiles hasta la muerte, la actividad del eje HPG disminuye. A medida que los hombres envejecen, los testículos comienzan a producir menos testosterona, lo que lleva a una condición conocida como hipogonadismo pospuberal.[8] La causa de la disminución de la testosterona no está clara y es un tema de investigación actual. El hipogonadismo pospuberal produce una disminución progresiva de la masa muscular, aumento de la masa grasa visceral, pérdida de la libido, impotencia, disminución de la atención, mayor riesgo de fracturas y producción anormal de espermatozoides.
Dimorfismo sexual y comportamiento
[editar]Los esteroides sexuales también afectan el comportamiento, porque los esteroides sexuales afectan la estructura y el funcionamiento del cerebro. Durante el desarrollo, las hormonas ayudan a determinar cómo las neuronas hacen sinapsis y migran para dar como resultado dimorfismos sexuales.[11] Estas diferencias físicas conducen a diferencias en el comportamiento. Si bien no se ha demostrado que la GnRH tenga una influencia directa en la regulación de la estructura y función del cerebro, se ha demostrado que las gonadotropinas, los esteroides sexuales y la activina tienen tales efectos. Se cree que la FSH puede tener un papel importante en el desarrollo y la diferenciación del cerebro.
Se ha demostrado que los niveles de testosterona se relacionan con el comportamiento prosocial.[12] Esto ayuda a crear sinaptogénesis al promover el desarrollo y la migración de neuritas. La activina promueve la plasticidad neuronal a lo largo de la vida y regula los neurotransmisores de las neuronas periféricas. El medio ambiente también puede afectar las hormonas y la interacción del comportamiento.[13]
Relevancia clínica
[editar]Trastornos
[editar]Los trastornos del eje hipotálamo-hipofisario-gonadal están clasificados por la Organización Mundial de la Salud (OMS) como:[14]
- Grupo I de la OMS de trastornos de la ovulación: insuficiencia hipotálamo-hipofisario
- Grupo II de la OMS de trastornos de la ovulación: Disfunción hipotálamo-hipofisario El grupo II de la OMS es la causa más común de trastornos de la ovulación, y el miembro causal más común es el síndrome de ovario poliquístico (SOP).[15]
Mutaciones genéticas
[editar]Las mutaciones genéticas y las anomalías cromosómicas son dos fuentes de alteración del eje HPG.[16] Las mutaciones únicas generalmente conducen a cambios en la capacidad de unión de la hormona y el receptor que conducen a la inactivación o sobreactivación. Estas mutaciones pueden ocurrir en los genes que codifican GnRH, LH y FSH o sus receptores. Dependiendo de qué hormona y receptor no puedan unirse, se producen diferentes efectos, pero todos alteran el eje HPG.
Por ejemplo, la mutación masculina del gen que codifica la GnRH podría provocar un hipogonadismo hipogonadotrófico. Una mutación que causa una ganancia de función para el receptor de LH puede resultar en una condición conocida como testotoxicosis, que causa que la pubertad ocurra entre los 2 y 3 años de edad. La pérdida de función de los receptores de LH puede causar pseudohermafroditismo masculino. En las hembras, las mutaciones tendrían efectos análogos. El reemplazo hormonal se puede usar para iniciar la pubertad y continuar si la mutación genética ocurre en el gen que codifica la hormona. Las mutaciones cromosómicas tienden a afectar la producción de andrógenos en lugar del eje HPG.
Supresión
[editar]El eje HPG puede suprimirse mediante la administración de anticonceptivos hormonales. Aunque a menudo se describe como prevención del embarazo al imitar el estado del embarazo, el control de la natalidad hormonal es efectivo porque funciona en el eje HPG para imitar la fase lútea del ciclo de una mujer. Los principales ingredientes activos son las progestinas sintéticas, que imitan la progesterona de origen biológico. La progestina sintética evita que el hipotálamo libere GnRH y que la pituitaria libere LH y FSH; por lo tanto, evita que el ciclo ovárico entre en la fase menstrual e impide el desarrollo de folículos y la ovulación. También como resultado, muchos de los efectos secundarios son similares a los síntomas del embarazo. Se ha demostrado que el Alzheimer tiene un componente hormonal, que posiblemente podría usarse como método para prevenir la enfermedad.[17] Los anticonceptivos masculinos que utilizan hormonas sexuales abordan el problema de manera similar.
El eje HPG también puede suprimirse mediante antagonistas de GnRH o la administración continua de agonistas de GnRH, como en las siguientes aplicaciones
- La supresión ovárica como tratamiento del cáncer de mama, para prevenir la formación de estrógeno en el cuerpo que puede estimular las células cancerosas de mama. Esto generalmente se hace mediante la administración continua del agonista de GnRH.
- Supresión de la ovulación como parte de la hiperestimulación ovárica controlada en la fertilización in vitro, para evitar la ovulación espontánea de los folículos ováricos antes de que puedan ser recolectados.
Estimulación
[editar]La inducción de la ovulación generalmente se realiza inicialmente administrando un antiestrógeno como el citrato de clomifeno o el letrozol para disminuir la retroalimentación negativa sobre la glándula pituitaria, lo que resulta en un aumento de la FSH con el objetivo de aumentar la foliculogénesis. Es el principal tratamiento médico inicial para la anovulación.
Factores ambientales
[editar]El medio ambiente puede tener un gran impacto en el eje HPG. Un ejemplo son las mujeres con trastornos alimentarios que sufren de oligomenorrea y amenorrea secundaria. La inanición por anorexia nerviosa o bulimia hace que el eje HPG se desactive y los ciclos ovárico y uterino de la mujer se detengan. El estrés, el ejercicio físico y la pérdida de peso se han correlacionado con la oligomenorrea y la amenorrea secundaria.[18] Del mismo modo, los factores ambientales también pueden afectar a los hombres, como el estrés que causa impotencia. La exposición prenatal al alcohol puede afectar las hormonas que regulan el desarrollo fetal, lo que resulta en un trastorno del espectro alcohólico fetal.[19]
Anatomía comparada
[editar]El eje HPG está muy conservado en el reino animal.[20] Si bien los patrones reproductivos pueden variar, los componentes físicos y los mecanismos de control siguen siendo los mismos. Se utilizan las mismas hormonas con algunas modificaciones evolutivas menores. Gran parte de la investigación se realiza en modelos animales, porque imitan muy bien el mecanismo de control de los humanos. Es importante recordar que los humanos son la única especie que oculta su período fértil, pero este efecto es una diferencia en el efecto de las hormonas más que una diferencia en el eje HPG.
Véase también
[editar]- Eje hipotalámico pituitario adrenal
- Eje hipotálamo-pituitario-tiroideo
- Sistema hipotalámico-neurohipofisario
- Neuroendocrinología
- Endocrinología reproductiva
Referencias
[editar]- ↑ Millar, Robert P.; Lu, Zhi-Liang; Pawson, Adam J.; Flanagan, Colleen A.; Morgan, Kevin; Maudsley, Stuart R. (2004-04). «Gonadotropin-releasing hormone receptors». Endocrine Reviews 25 (2): 235-275. ISSN 0163-769X. PMID 15082521. doi:10.1210/er.2003-0002.
- ↑ Charlton, H. (2008-06). «Hypothalamic control of anterior pituitary function: a history». Journal of Neuroendocrinology 20 (6): 641-646. ISSN 1365-2826. PMID 18601683. doi:10.1111/j.1365-2826.2008.01718.x.
- ↑ Vadakkadath Meethal, S.; Atwood, C. S. (2005-02). «The role of hypothalamic-pituitary-gonadal hormones in the normal structure and functioning of the brain». Cellular and molecular life sciences: CMLS 62 (3): 257-270. ISSN 1420-682X. PMID 15723162. doi:10.1007/s00018-004-4381-3.
- ↑ Meethal, Sivan Vadakkadath; Liu, Tianbing; Chan, Hsien W.; Ginsburg, Erika; Wilson, Andrea C.; Gray, Danielle N.; Bowen, Richard L.; Vonderhaar, Barbara K. et al. (2009-08). «Identification of a regulatory loop for the synthesis of neurosteroids: a steroidogenic acute regulatory protein-dependent mechanism involving hypothalamic-pituitary-gonadal axis receptors». Journal of Neurochemistry 110 (3): 1014-1027. ISSN 1471-4159. PMC 2789665. PMID 19493163. doi:10.1111/j.1471-4159.2009.06192.x.
- ↑ Comninos, A. N.; Jayasena, C. N.; Dhillo, W. S. (2013). «The relationship between gut and adipose hormones, and reproduction». Human Reproduction Update 20 (2): 153-74. PMID 24173881. doi:10.1093/humupd/dmt033.
- ↑ Skorupskaite, K.; George, J. T.; Anderson, R. A. (2014). «The kisspeptin-GnRH pathway in human reproductive health and disease». Human Reproduction Update 20 (4): 485-500. ISSN 1355-4786. PMC 4063702. PMID 24615662. doi:10.1093/humupd/dmu009.
- ↑ a b Katja Hoehn; Marieb, Elaine Nicpon (2007). Human anatomy & physiology. San Francisco: Pearson Benjamin Cummings. pp. 1090-1110. ISBN 978-0-8053-5909-1.
- ↑ a b Veldhuis, Johannes D.; Keenan, Daniel M.; Liu, Peter Y.; Iranmanesh, Ali; Takahashi, Paul Y.; Nehra, Ajay X. (5 de febrero de 2009). «The Aging Male Hypothalamic-Pituitary-Gonadal Axis: pulsatility and feedback». Molecular and cellular endocrinology 299 (1): 14-22. ISSN 0303-7207. PMC 2662347. PMID 18838102. doi:10.1016/j.mce.2008.09.005.
- ↑ Downs, Jodi L.; Wise, Phyllis M. (5 de febrero de 2009). «The role of the brain in female reproductive aging». Molecular and Cellular Endocrinology 299 (1): 32-38. ISSN 0303-7207. PMC 2692385. PMID 19063938. doi:10.1016/j.mce.2008.11.012.
- ↑ «60.FISIOLOGÍA Y PATOLOGÍA DEL CLIMATERIO Y LA SENECTUD». sintesis.med.uchile.cl. Consultado el 16 de diciembre de 2023.
- ↑ Hines M (July 1982). «Prenatal gonadal hormones and sex differences in human behavior». Psychol Bull 92 (1): 56-80. PMID 7134329. doi:10.1037/0033-2909.92.1.56.
- ↑ Wibral, Matthias; Dohmen, Thomas; Klingmüller, Dietrich; Weber, Bernd; Falk, Armin (2012). «Testosterone administration reduces lying in men». PloS One 7 (10): e46774. ISSN 1932-6203. PMC 3468628. PMID 23071635. doi:10.1371/journal.pone.0046774.
- ↑ Shepard, Kathryn N.; Michopoulos, Vasiliki; Toufexis, Donna J.; Wilson, Mark E. (25 de mayo de 2009). «Genetic, epigenetic and environmental impact on sex differences in social behavior». Physiology & Behavior 97 (2): 157-170. ISSN 1873-507X. PMC 2670935. PMID 19250945. doi:10.1016/j.physbeh.2009.02.016.
- ↑ Page 54 in: Guillebaud, John; Enda McVeigh; Roy Homburg (2008). Oxford handbook of reproductive medicine and family planning. Oxford [Oxfordshire]: Oxford University Press. ISBN 978-0-19-920380-2.
- ↑ Baird, D. T.; Balen, A.; Escobar-Morreale, H. F.; Evers, J. L. H.; Fauser, B. C. J. M.; Franks, S.; Glasier, A.; Homburg, R. et al. (2012). «Health and fertility in World Health Organization group 2 anovulatory women». Human Reproduction Update 18 (5): 586-599. PMID 22611175. doi:10.1093/humupd/dms019.
- ↑ Isidori, Andrea M.; Giannetta, Elisa; Lenzi, Andrea (2008). «Male hypogonadism». Pituitary 11 (2): 171-180. ISSN 1386-341X. PMID 18404386. doi:10.1007/s11102-008-0111-9.
- ↑ Haasl, Ryan J.; Ahmadi, M. Reza; Meethal, Sivan Vadakkadath; Gleason, Carey E.; Johnson, Sterling C.; Asthana, Sanjay; Bowen, Richard L.; Atwood, Craig S. (25 de abril de 2008). «A luteinizing hormone receptor intronic variant is significantly associated with decreased risk of Alzheimer's disease in males carrying an apolipoprotein E epsilon4 allele». BMC medical genetics 9: 37. ISSN 1471-2350. PMC 2396156. PMID 18439297. doi:10.1186/1471-2350-9-37.
- ↑ Wiksten-Almströmer, Marianne; Hirschberg, Angelica Lindén; Hagenfeldt, Kerstin (2007). «Menstrual disorders and associated factors among adolescent girls visiting a youth clinic». Acta Obstetricia Et Gynecologica Scandinavica 86 (1): 65-72. ISSN 0001-6349. PMID 17230292. doi:10.1080/00016340601034970.
- ↑ Weinberg, J.; Sliwowska, J. H.; Lan, N.; Hellemans, K. G. C. (2008-04). «Prenatal alcohol exposure: foetal programming, the hypothalamic-pituitary-adrenal axis and sex differences in outcome». Journal of Neuroendocrinology 20 (4): 470-488. ISSN 1365-2826. PMID 18266938. doi:10.1111/j.1365-2826.2008.01669.x.
- ↑ Sower, Stacia A.; Freamat, Mihael; Kavanaugh, Scott I. (2009-03). «The origins of the vertebrate hypothalamic-pituitary-gonadal (HPG) and hypothalamic-pituitary-thyroid (HPT) endocrine systems: new insights from lampreys». General and Comparative Endocrinology 161 (1): 20-29. ISSN 1095-6840. PMID 19084529. doi:10.1016/j.ygcen.2008.11.023.
