Cloruro de fenacilo
| Cloruro de fenacilo | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 2-cloro-1-Fenilacetona | ||
| General | ||
| Fórmula estructural |
 | |
| Fórmula molecular | ? | |
| Identificadores | ||
| Número CAS | 532-27-4[1] | |
| ChEMBL | CHEMBL105712 | |
| Propiedades físicas | ||
| Apariencia | Polvo blanco | |
| Punto de fusión | 54 °C (327 K) | |
| Punto de ebullición | 244,5 °C (518 K) | |
| Propiedades químicas | ||
| Solubilidad en agua | Insoluble | |
| Riesgos | ||
| Riesgos principales | Combustible[2] | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El cloruro de fenacilo, también conocido como cloroacetofenona, es una acetofenona sustituida. Se trata de una sustancia orgánica ampliamente utilizada como agente de control de disturbios, conociéndose como gas CN.[3] No debe confundirse con el cianuro, otra sustancia química con fórmula CN-
Preparación[editar]
El compuesto se puede encontrar con facilidad a nivel comercial y se sintetiza mediante la acilación de Friedel-Crafts de benceno con cloruro de cloroacetilo, añadiendo un catalizador de cloruro de aluminio:[4]
Catalizador:[5]
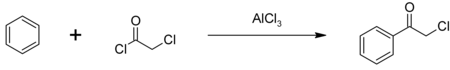
Usos[editar]
Si bien fue investigado, no llegó a emplearse durante la Primera Guerra Mundial y Segunda Guerra Mundial.
Debido a su toxicidad significativamente mayor,[6] ha sido sustituido en gran medida por el gas CS. Aunque todavía se suministra CN a las fuerzas paramilitares y policiales en un pequeño aerosol presurizado conocido como "Mace" o gas lacrimógeno, su uso está disminuyendo, ya que el spray de pimienta funciona y se dispersa más rápidamente que el CN y es menos tóxico que éste.
El término "Mace" surgió porque fue la marca inventada por uno de los primeros fabricantes estadounidenses de aerosoles de CN. Posteriormente, en Estados Unidos, Mace se convirtió en sinónimo de aerosol lacrimógeno del mismo modo que Kleenex se ha asociado fuertemente a los pañuelos faciales (un fenómeno conocido como marca generizada).
Al igual que el gas CS, este compuesto irrita las mucosas (oral, nasal, conjuntival y traqueobronquial). A veces puede dar lugar a reacciones más generalizadas como síncope, pérdida temporal del equilibrio y de la orientación.[6] Más raramente, se han observado brotes irritativos cutáneos y dermatitis alérgica permanente de contacto.[3]
En concentraciones elevadas, el CN puede provocar daños en el epitelio corneal y quemaduras. También ha causado al menos cinco muertes, que han sido consecuencia de lesiones pulmonares y/o asfixia.[7]
El canal iónico TRPA1 (Transient Receptor Potential-Ankyrin 1) expresado en los nociceptores (especialmente en el trigémino) ha sido implicado como el lugar de acción del CN, in vivo e in vitro.[8][9]
Véase también[editar]
Referencias[editar]
- ↑ Número CAS
- ↑ CDC - NIOSH Pocket Guide to Chemical Hazards
- ↑ a b Treudler, R.; Tebbe, B.; Blume-Peytavi, U.; Krasagakis, K.; Orfanos, C. E. (1999). «Occupational contact dermatitis due to 2-chloracetophenone tear gas». British Journal of Dermatology 140 (3): 531-534. PMID 10233281. S2CID 45123933. doi:10.1046/j.1365-2133.1999.02724.x.
- ↑ «Ketones of the aromatic group». Journal of the Chemical Society, Abstracts 34: 419. 1878. doi:10.1039/CA8783400392.
- ↑ Levin, N. (1955). "ω-Chloroisonitrosoacetophenone". Org. Synth.; Coll. Vol. 3: 191.
- ↑ a b Ballantyne, B.; Swanston, D. W. (1978). «The comparative acute mammalian toxicity of 1-chloroacetophenone (CN) and 2-chlorobenzylidene malononitrile (CS)». Archives of Toxicology 40 (2): 75-95. PMID 350195. doi:10.1007/BF01891962.
- ↑ Blain, P. G. (2003). «Tear Gases and Irritant Incapacitants: 1-Chloroacetophenone, 2-Chlorobenzylidene Malononitrile and Dibenz[b,f]-1,4-Oxazepine». Toxicological Reviews 22 (2): 103-110. PMID 15071820. S2CID 21164652. doi:10.2165/00139709-200322020-00005.
- ↑ Bessac, Bret F.; Sivula, Michael; Hehn, Christian A.; Caceres, Ana I.; Escalera, Jasmine; Jordt, Sven-Eric (2009-04). «Transient receptor potential ankyrin 1 antagonists block the noxious effects of toxic industrial isocyanates and tear gases». The FASEB Journal (en inglés) 23 (4): 1102-1114. ISSN 0892-6638. PMID 19036859. doi:10.1096/fj.08-117812. Consultado el 10 de enero de 2023.
- ↑ Brône, Bert; Peeters, Pieter J.; Marrannes, Roger; Mercken, Marc; Nuydens, Ronny; Meert, Theo; Gijsen, Harrie J. M. (1 de septiembre de 2008). «Tear gasses CN, CR, and CS are potent activators of the human TRPA1 receptor». Toxicology and Applied Pharmacology (en inglés) 231 (2): 150-156. ISSN 0041-008X. doi:10.1016/j.taap.2008.04.005. Consultado el 10 de enero de 2023.
Enlaces externos[editar]
- Esta obra contiene una traducción parcial derivada de «Phenacyl chloride» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.
- http://www.alcayata.com/cromagnon/tear_gas/gas.htm
- https://web.archive.org/web/20050210042449/http://www.zarc.com/espanol/tear_gases/agentCN_sp.html
