Calor
Se denomina calor a la energía en tránsito que se reconoce solo cuando se cruza la frontera de un sistema termodinámico.[1] Una vez dentro del sistema, o en los alrededores (si la transferencia es de adentro hacia afuera) el calor transferido se vuelve parte de la energía interna del sistema (o de los alrededores). El término calor, por tanto, se debe entender como transferencia de calor y ocurre cuando hay diferencia de temperatura entre el sistema y su entorno, o entre dos zonas del sistema. Si bien las leyes o principios de la Termodinámica no establecen una dirección para el proceso, empíricamente se observa siempre que el calor fluye de la región a mayor temperatura hacia la región a menor temperatura. El flujo neto de calor entre dos sistemas a la misma temperatura es nulo, lo que se interpreta en que ambas regiones intercambian calor mutuamente con idéntica rapidez.
Naturaleza del calor[editar]

A menudo en el habla coloquial se usan expresiones como Cantidad de calor de un cuerpo o ganancia de calor y se hace porque no producen ningún malentendido y quizás porque no hay ninguna alternativa técnica que sea tan intuitiva, pero en un sentido técnico son incorrectas. El calor, visto desde la física, no se tiene, el calor es una transferencia.[2] Lo que tiene un cuerpo es energía térmica; mejor aún, si se considera el cuerpo como un sistema termodinámico, la energía total del sistema tiene dos formas: macroscópica y microscópica. La energía macroscópica es la que tiene el sistema con referencia a un origen exterior, como la energía cinética y la potencial. La microscópica es su grado de actividad molecular, que es independiente del sistema de referencia externo y es lo que se conoce como energía interna del sistema y se representa por .
Las moléculas de un sistema se agitan con cierta velocidad; además giran y vibran de manera irregular y todo este movimiento les confiere una energía cinética que es la parte de la energía interna que es energía sensible, porque la velocidad promedio de las moléculas es proporcional a la temperatura, que es lo que podemos percibir. Pero también las moléculas están unidas por fuerzas de atracción que son más fuertes en los sólidos, disminuyen en los líquidos y aún más en los gases, de forma que un sistema en estado gaseoso implica una energía que ha sido necesaria para vencer las fuerzas intermoleculares. Esta energía que tiene que ver con la fase en que está el sistema se llama energía latente. Los átomos están unidos por enlaces que se forman y se destruyen en las reacciones químicas. La energía interna asociada con los enlaces atómicos es la energía química. Y por fin, las fuerzas de atracción en el núcleo de los átomos constituyen la energía nuclear, que se libera en las reacciones nucleares. Todas estas formas de energía se almacenan en el interior del sistema y conforman su energía interna.
Pero hay formas de energía que no se pueden almacenar, que solo aparecen cuando hay interacción y constituyen lo que llamamos la energía ganada o perdida por el sistema. Estas formas de energía son la transferencia de calor y el trabajo. Cuando el origen o la fuerza motriz de la interacción es una diferencia de temperatura, se dice que es calor; en caso contrario es trabajo.
Resumiendo, es muy común referirse a la energía sensible y latente como calor, y está bien coloquialmente, pero en realidad es energía térmica, que es muy distinta de la transferencia de calor.
Historia de la teoría del calor[editar]
La primera referencia formal sobre la importancia del fuego se encuentra en Heráclito (540 a. C.-475 a. C.), quien sostenía que el fuego era el origen primordial de la materia.
Para Anaxímenes lo caliente y lo frío son estados comunes de la materia. Consideraba que lo comprimido y condensado era frío, y que lo raro y “laxo” era caliente, por tanto, según él, la ‘‘rarefacción’’ daba cuenta del proceso mediante el cual se calentaban las cosas, hasta quedar convertidas en vapor.
Aristóteles (384 a. C.-322 a. C.), agregó dos pares de cualidades fundamentales: caliente y frío, seco y húmedo. La razón por la cual un cuerpo tenía cierta temperatura, venía dada por las cantidades que en él se encontraban estas dos cualidades fundamentales.
Galeno (129-199) propuso una escala cualitativa que constaba de cuatro estados de calor y cuatro de frío, el punto neutro se obtenía agregando cuatro partes de agua hirviendo y cuatro partes de hielo.[3]
Estas ideas se mantuvieron durante más de 23 siglos. Es curioso observar, que en este período ya se apreciaba que algunos de los fenómenos físicos, como la dilatación de sólidos y líquidos, y la expansión térmica del aire y el vapor, dependían del calor, pero no se prestaba atención a las temperaturas porque no eran parte de las cualidades referidas en la física aristotélica.
Las ideas de Aristóteles comienzan a ser cuestionadas a mediados del siglo XVI, cuando se propone la existencia de una quintaesencia de la materia, la existencia de un agente universal responsable de todas las reacciones químicas. Robert Boyle (1627-1691), negó al fuego todo carácter corpóreo y consideró que debía existir cierta unidad de la materia, lo que implicaba que debería estar compuesta por corpúsculos.
Mientras, en el siglo XVII y los primeros años del XVIII, se originaron discusiones sobre la estructura de la materia y ocurrió otro acontecimiento importante en la historia del calor, Georg Stahl (1660-1734) enuncia la teoría del flogisto. Este no debe ser confundido con el fuego material, el que se manifiesta en la llama y en el calor cuando se producen combustiones, sino que es un elemento inaccesible que poseen todos los cuerpos combustibles.
En el transcurso del siglo XVII se oponen dos teorías sobre el calor, la del flogisto, y la que defendían los seguidores de los atomistas griegos, quienes admitían la corporeidad del fuego, considerando que este se constituía por partículas pequeñas, ligeras y sutiles, que tenían a su vez una enorme movilidad para penetrar en la materia en sus diferentes estados, capaces de operar simplemente con su presencia en forma de fluido imponderable, el calórico. Entre 1775 y 1787 Lavoisier elaboró una teoría de los gases, en las que introducía el principio del calórico. En este periodo surgía el concepto de temperatura y empezaron a construirse termómetros, para medir la frialdad de las cosas. Joseph Black (1728-1799) utilizó estos termómetros para estudiar el calor, observando cómo las diferentes sustancias que se encontraban a desiguales temperaturas tendían a llegar a un equilibrio cuando se les ponía en contacto.[4]
En 1798 Benjamin Thompson, conde de Rumford, observó en Baviera, que al perforar cañones, la cantidad de calor que se obtenía dependía del estado del taladro y llegó a la conclusión de que el calor no era un fluido, sino una forma de movimiento. Dedujo la posibilidad de generar por rozamiento una cantidad ilimitada de calor, ya que el calor generado era aproximadamente proporcional al trabajo realizado, hecho que no era fácilmente argumentable con la teoría del calórico. En 1812 Humphry Davy confirmó la presunción anterior. Esta idea culmina con los trabajos del médico y físico Julio R. von Mayer en 1842 y posterior y definitivamente en 1850 con James Prescott Joule, que establecen que el calor y el trabajo no son más que manifestaciones de la energía térmica, la cual puede ser convertida en un porcentaje en trabajo, mientras que el trabajo puede ser totalmente convertido en calor.[5]
Finalmente se comprobó que el calor no podía ser entendido como una sustancia material, sino que es una forma de energía. Las medidas del equivalente mecánico del calor señalaron el fin de la teoría del calórico. De todo esto surge la termodinámica y de ella la máquina térmica. En la misma época en que se inició la termodinámica, estaba desarrollándose la teoría molecular de la materia, que permite formarse una idea coherente del calor y de los fenómenos que intervienen. La teoría cinética de los gases explicaba muchos de los fenómenos que por medio de la teoría del calórico no podían ser explicados.
Calor específico[editar]
El calor específico es un parámetro que depende del material y relaciona el calor que se proporciona a una masa determinada de una sustancia con el incremento de temperatura:
donde:
- es el calor aportado al sistema.
- es la masa del sistema.
- es el calor específico del sistema.
- y son las temperaturas inicial y final del sistema respectivamente.
- es el diferencial de temperatura.
Las unidades de calor específico son El calor específico de un material depende de su temperatura; no obstante, en muchos procesos termodinámicos su variación es tan pequeña que puede considerarse que el calor específico es constante.

Si se representa en un gráfico el calentamiento de un líquido llevando las cantidades de calor por unidad de masa como ordenadas y las temperaturas como abcisas. Entre dos temperaturas cualesquiera, el calor específico medio se expresa:[6]
En la que es la cantidad de calor que la sustancia recibe o cede entre las temperaturas y . Sin embargo, el calor específico verdadero para será
El calor específico verdadero está dado por la variación de la cantidad de calor intercambiado por unidad de masa con respecto a la temperatura, o gráficamente, por la pendiente de la tangente geométrica en el punto de la curva de estado. Se puede ver en la figura, la diferencia entre los calores específicos verdaderos, representados por las pendientes de las tangentes a la curva y los calores específicos medios entre dos temperaturas, representados por la pendiente de la cuerda que une ambos puntos.
Para la mayoría de los cuerpos, el calor específico aumenta con la temperatura y la diferencia entre valores medios y verdaderos es pequeña, siempre que la variación de temperatura sea también pequeña. Para el agua, la curva q-t es prácticamente una recta, lo cual indica que su calor específico se mantiene, dentro de ciertos límites, prácticamente constante, normalmente se toma como 4186 kJ/kg.
Calor específico molar[editar]
Con frecuencia es muy útil hablar de calor específico molar denotado por cmol, y definido como la cantidad de energía necesaria para elevar la temperatura de un mol de una sustancia en 1 grado es decir, está definida por:
donde n indica la cantidad de moles en la sustancia presente.
Capacidad calorífica[editar]
La capacidad calorífica de una sustancia es una magnitud que indica la mayor o menor dificultad que presenta dicha sustancia para experimentar cambios de temperatura bajo el suministro de calor. Se denota por , se mide en , y se define como:
Dado que:
De igual forma se puede definir la capacidad calorífica molar como:
Cambios de fase[editar]
En la naturaleza existen tres estados usuales de la materia: sólido, líquido y gaseoso. Al aplicarle calor a una sustancia, ésta puede cambiar de un estado a otro. A estos procesos se les conoce como cambios de fase. Los posibles cambios de fase son:
- de estado sólido a líquido, llamado fusión,
- de estado líquido a sólido, llamado solidificación,
- de estado líquido a gaseoso, llamado evaporación o vaporización,
- de estado gaseoso a líquido, llamado condensación,
- de estado sólido a gaseoso, llamado sublimación progresiva,
- de estado gaseoso a sólido, llamado sublimación regresiva o deposición,
- de estado gaseoso a plasma, llamado ionización.
- de estado plasma a gaseoso, llamado Desionización

Calor latente[editar]
Que un cuerpo sólido puede estar en equilibrio térmico con un líquido o un gas, o que un líquido y un gas pueden estar en equilibrio térmico entre sí, en una amplia gama de temperaturas, es algo normal y frecuente. Pero lo que no es tan normal es que dos fases o estados de agregación distintos de una misma sustancia, puedan estar en equilibrio térmico entre sí, naturalmente en circunstancias apropiadas.
Un sistema que consiste en formas sólida y líquida de determinada sustancia, a una presión constante dada, puede estar en equilibrio térmico, pero únicamente a una temperatura llamada punto de fusión simbolizado a veces como . A esta temperatura, todo el calor agregado se invierte en fundir el material mientras quede una partícula sólida, sin que haya un cambio significativo de su temperatura. La cantidad de energía agregada, se llama calor de fusión, calor latente de fusión o entalpía de fusión, y es diferente para cada sustancia. Se denota por .
Para pasar de líquido a sólido se necesita la misma cantidad de energía, por ello el calor de fusión representa la energía necesaria para cambiar del estado sólido al líquido, y viceversa.
De manera similar, un líquido y un vapor de una misma sustancia pueden estar en equilibrio térmico a una temperatura llamada punto de ebullición simbolizado por . El calor necesario para evaporar una sustancia en estado líquido ( o condensar una sustancia en estado de vapor ) se llama calor de ebullición o calor latente de ebullición o entalpía de ebullición, y se mide en las mismas unidades que el calor latente de fusión. Se denota por .
En la siguiente tabla[7] se muestran algunos valores de los puntos de fusión y ebullición, y los calores latentes de fusión y evaporación de algunas sustancias:
| sustancias | [°C] | [kJ/kg] | [°C] | [kJ/kg] |
| Agua - Hielo | 0, 00 | 334 | 100, 00 | 2260 |
| Alcohol etílico | -114, 00 | 105 | 78, 3 | 846 |
| Acetona | -94, 3 | 96 | 56, 2 | 524 |
| Benceno | 5, 5 | 127 | 80, 2 | 396 |
| Aluminio | 658, 7 | 322-394 | 2300 | 9220 |
| Estaño | 231, 9 | 59 | 2270 | 3020 |
| Hierro | 1530 | 293 | 3050 | 6300 |
| Cobre | 1083 | 214 | 2360 | 5410 |
| Mercurio | -38, 9 | 11, 73 | 356, 7 | 285 |
| Plomo | 327, 3 | 22, 5 | 1750 | 880 |
| Potasio | 64 | 60, 8 | 760 | 2080 |
| Sodio | 98 | 113 | 883 | 4220 |
Transmisión de calor[editar]
En general, se admiten tres formas distintas de transmitir el calor: por conducción, por convección y por radiación. En rigor, solo la conducción y la radiación son formas de transmisión del calor, que para producirse dependen exclusivamente de la existencia de un desequilibrio térmico. El caso de la convección depende además del transporte mecánico de masa, sin embargo como sigue habiendo una transferencia de calor desde una zona de mayor temperatura a otra de temperatura inferior, se adopta la expresión transmisión de calor por convección.
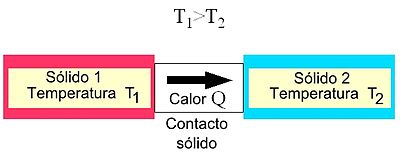
- Conducción térmica: Siempre que existe un gradiente de temperatura en un medio sólido, el calor fluye desde la región o cuerpo con mayor temperatura a la región o cuerpo con menor temperatura.
- Convección térmica: se compone de dos mecanismos que operan al mismo tiempo; transferencia de energía generada por el movimiento molecular, es decir, conducción, y transferencia de energía mediante el movimiento de partes de fluido impulsadas por una fuerza externa, que puede ser natural en el caso de un gradiente de densidad, o forzada en el caso de un ventilador o una bomba.
- Radiación térmica: Todos los cuerpos emiten radiación electromagnética con una intensidad que depende de su temperatura y de la longitud de onda considerada.
La transmisión simple, es decir, debida exclusivamente a una de las tres formas es en la práctica inexistente y se produce siempre en forma simultánea, al menos por la combinación de dos de las formas de transmisión y muy a menudo por las tres.
Medida del calor[editar]
Si se tiene un cuerpo en equilibrio termodinámico y se le deja en un medio que tiene una temperatura diferente, se produce una transferencia de energía entre el cuerpo y los alrededores hasta que se alcanza el equilibrio térmico, es decir, hasta que ambos están a la misma temperatura, en cuyo momento cesa la transferencia. Se dice que la energía se ha transferido en forma de calor.
La termodinámica estudia los estados de equilibrio y nos permite por la primera ley, determinar la diferencia de calor entre el estado 1 y el estado 2, tanto del cuerpo, como del medio en que se le sumergió. Si se admite que no ha habido más interacción que la debida a la diferencia de temperatura, la variación de energía interna del cuerpo y del medio son iguales y tanto una como la otra, informan sobre la cantidad de calor necesaria para pasar del estado 1 al 2, pero no nos dicen nada de cómo ha sido el flujo de calor entre ambos estados, ni cuál ha sido el tiempo necesario para la transferencia.
Como forma de energía, el calor tiene unidades de energía, por lo que si nos atenemos al Sistema Internacional de Unidades, se medirá en Julios .[8] Teniendo en cuenta que esta unidad es muy pequeña y que la unidad de masa es el kg, se toma normalmente el kilojulio , que definido como calor sería:
Un kiloJulio es el calor que hay que transferir a 1 kg de agua para aumentar su temperatura 0,24 K aproximadamente.[9]
Cuando es necesario conocer el flujo de calor o cantidad de calor transferido por unidad de tiempo, lo que se busca es y se medirá en kJ/s, es decir, en kW. El cálculo del flujo de calor y de sus modos de transmisión no corresponden a la termodinámica, sino a otra parte de la física que es la Transferencia de calor.
El calor es una magnitud con dirección, por tanto es necesario darle un signo para completar la información. No hay un acuerdo total sobre el signo convencional, pero el más aceptado es:
La transferencia de calor hacia un sistema es positiva y la transferencia de calor desde el sistema es negativa.[10]
Calorimetría[editar]
Para determinar de manera directa el calor que se pone de manifiesto en un proceso de laboratorio, se suele emplear un calorímetro. En esencia se trata de un recipiente que contendrá el líquido en el que se va a estudiar la variación de energía por transferencia de calor, cuya envolvente debe estar perfectamente aislada para garantizar que el proceso se acerque lo más posible al adiabático.
Termodinámica y transferencia de calor[editar]
La termodinámica informa de transferencia de calor de un proceso, sin considerar el mecanismo de flujo de calor ni el tiempo necesario para efectuar la transferencia. Un estudio termodinámico determina cuánto calor debe transferirse para que se realice el paso de un estado a otro, apoyándose en el primer principio o principio de conservación de la energía. Desde un punto de vista de la ingeniería, el problema clave es calcular la velocidad de transferencia de calor para una diferencia de temperatura determinada. La termodinámica trata de los estados de equilibrio y de los cambios que ocurren entre un estado de equilibrio y otro. La transferencia de calor sin embargo se ocupa de los fenómenos que se producen a partir de que existe un desequilibrio térmico y por tanto, exige una condición de no equilibrio. En consecuencia, el estudio de la transferencia de calor no puede basarse solo en los principios de la termodinámica, sin embargo estos y cualquier ley física que tenga que ser satisfecha por un proceso, proporcionan ecuaciones que pueden utilizarse en el análisis.
La forma de aplicar la primera ley de la termodinámica es establecer un volumen de control que es una región fija del espacio limitada por una superficie de control y a través de la cual puede pasar calor, trabajo y masa. A partir de ahí se puede realizar un balance de energía:[11]
La velocidad a la cual las energías térmica y mecánica entran en un volumen de control, más la velocidad a la que se genera energía en el interior del mismo, menos la velocidad a la cual las energía térmica y mecánica salen de él, deben ser iguales a la velocidad a la que se acumula energía en el interior de este volumen.
Anteriormente mencionamos que el análisis termodinámico no se ocupa de la velocidad de la transferencia de calor en una dirección pero se puede decir que este parámetro depende de la magnitud del gradiente de temperatura, o diferencia de temperatura por unidad de longitud, o la razón o relación de cambio de la temperatura en esa dirección. A mayor gradiente de temperatura, mayor es la velocidad de transferencia de calor.
Transferencia de calor en la ingeniería[editar]
Los problemas de capacidad nominal se ocupan de la determinación de la velocidad de transferencia de calor en un sistema existente con una diferencia dada de temperatura. Los problemas de dimensionamiento, se ocupan de la determinación del tamaño de un sistema, con el fin de transferir calor a una velocidad determinada con una diferencia dada de la temperatura. Un proceso o un equipo de transferencia de calor puede ser analizado de forma experimental o de forma analítica. El procedimiento experimental tiene la ventaja de tratar con el sistema físico real y, gracias a ello, la cantidad deseada se determina mediante medición, dentro de los límites del error experimental. El procedimiento analítico tiene la ventaja de que es rápido y barato, pero los resultados obtenidos dependen de la exactitud de las hipótesis e idealizaciones establecidas en el análisis. En los estudios de transferencia de calor a menudo se logra una buena aproximación reduciendo, mediante el análisis, las opciones a solo unas cuantas y, a continuación, verificando los hallazgos experimentalmente.
Sensación de calor en el ser humano[editar]
Intentar cuantificar calor en el sentido en que lo usamos coloquial y cotidianamente, es más complicado de lo que parece, ya que ello depende de muchas más variables y sobre todo más impredecibles de las que se han apuntado hasta ahora. Empezando por el país, zona, clima, pasando por la luminosidad o el color predominante y hasta el sexo y la situación anímica del individuo pueden influir en la sensación térmica.
Generalmente en la mayoría de los países, se habla ya de calor cuando la temperatura supera los 26 °C en cualquier hora del día, aunque varía mucho según la estación del año. Por ejemplo, 20 °C en verano es considerado una temperatura fresca, mientras que en invierno, esta temperatura es considerada templada o cálida.
El fenómeno "ola de calor" se anuncia cuando las temperaturas diurnas superan los 32 °C y las nocturnas (o al amanecer) no bajan de los 23 °C durante tres días. Es común en casi todo tipo de climas en época veraniega, a excepción de los países cerca de los polos, donde es muy infrecuente o casi nulo, y se hace más frecuente a medida que los países están más cerca de los trópicos. Esta denominación de ola de calor, no quiere decir necesariamente calor excesivo ni temperaturas inusuales para la estación, sino que pretende alertar sobre consecuencias perjudiciales en personas o colectivos vulnerables.
Se tiene una sensación de más calor cuando hay más humedad en el ambiente. Por ejemplo, una temperatura de 30 °C, con humedad ambiental del 10 %, se sentirá como si el ambiente fuese de solo 28 °C. Pero con humedad ambiental del 90 %, se sentirá como si el ambiente fuese de 40 °C.
Véase también[editar]
- Sensación térmica
- Calorimetría
- Temperatura
- Termodinámica
- Bolsa de agua caliente
- Teoría calórica
- Teoría cinética de los gases ideales
- Introducción a la mecánica de fluidos
Referencias[editar]
- ↑ Bernal, José Alfredo Jiménez; Torres, Claudia del Carmen Gutiérrez; Saldaña, Juan Gabriel Barbosa (21 de octubre de 2014). Termodinámica. Grupo Editorial Patria. ISBN 9786074389388. Consultado el 8 de febrero de 2018.
- ↑ Gómez, Pedro & Esteban Glez. Termodinámica.
- ↑ Taton, René. Historia General de las ciencias. Las ciencias en el mundo grecorromano. isbn 84-4020-16-13.
- ↑ Asimov, Isaac. Introducción a la ciencia, página 335.
- ↑ Facorro, J. A. Curso de Termodinámica, página 30.
- ↑ Facorro Ruiz, L. A. Curso de Termodinámica, página 12. Ediciones Melior (1989).
- ↑ Koshkin, N. I. & M. G. Shirkévich. Manual de física elemental, pp. 74-75. Edit. Mir. (1975).
- ↑ Sigue utilizándose en algunos textos, en las especificaciones de algunos aparatos de calefacción y sobre todo en el poder energético de los alimentos, la caloría y la kilocaloría, pero se recomienda el abandono de estas unidades y el uso exclusivo del Sistema Internacional de Unidades. Lo mismo ocurre con la BTU
- ↑ Es aproximada porque habría que definir las condiciones del agua en todos los aspectos, no solo en su temperatura inicial, ya que su calor específico puede variar mucho.
- ↑ El aporte de calor es positivo y la extracción de calor es negativa. Por ejemplo: las pérdidas de calor de un local en invierno son negativas y el calor aportado por el sistema de calefacción para compensarlas, es positivo.
- ↑ Kreith, Frank & Mark S. Bohn. Principios de Transferencia de calor, página 47. Thomson Editores. (2001)
Bibliografía[editar]
- Çengel, Yunus A. & Michael A. Boles. (1995). Termodinámica. Mc Graw-Hill. isbn970-10-0909-6
- Kreith, Frank & Mark S. Bohn. (2001)Principios de Transferencia de calor. Thomson Editores.isbn 84-9732-061-1
- Cengel, Yunus A. (2004), Transferencia de calor (2ª edición), México: McGraw-Hill.
- Abbott, M. M.; Vanness, H. C. (1991), Termodinámica (2ª edición), México: McGraw-Hill.
- Callen, H. B. (1985), Thermodynamics, New York: Wiley & Sons.
- Valderrama, J. O. (2009), Apuntes de Termodinámica Básica.
- Wark, K. (1991), Termodinámica (5ª edición), México: McGraw-Hill.
- Faires, V. M. (1973), Termodinámica, México: Uteha.
Enlaces externos[editar]
 Wikcionario tiene definiciones y otra información sobre calor.
Wikcionario tiene definiciones y otra información sobre calor.






























