Diferencia entre revisiones de «Iridio»
Sin resumen de edición |
m Revertidos los cambios de 190.22.34.75 a la última edición de 189.209.105.221 |
||
| Línea 130: | Línea 130: | ||
Es de color blanco, parecido al platino, pero presenta una ligera coloración amarilla. Es difícil trabajar este [[metal]], pues es muy duro y quebradizo. Es el metal más resistente a la [[corrosión]]. No es atacado por los ácidos, ni siquiera por el [[agua regia]]. Para disolverlo se emplea [[ácido clorhídrico]], HCl, concentrado con clorato de sodio, NaClO<sub>3</sub> a temperaturas altas. |
Es de color blanco, parecido al platino, pero presenta una ligera coloración amarilla. Es difícil trabajar este [[metal]], pues es muy duro y quebradizo. Es el metal más resistente a la [[corrosión]]. No es atacado por los ácidos, ni siquiera por el [[agua regia]]. Para disolverlo se emplea [[ácido clorhídrico]], HCl, concentrado con clorato de sodio, NaClO<sub>3</sub> a temperaturas altas. |
||
El iridio es un metal [[extraterrestre]], abundante en los [[meteoritos]], y que en la [[corteza terrestre]] sólo tiene una concentración de 0,001 [[ppm]]. |
|||
| ⚫ | |||
| ⚫ | |||
El núcleo de la Tierra está formado por este metal junto al hierro y níquel. |
El núcleo de la Tierra está formado por este metal junto al hierro y níquel. |
||
Revisión del 21:01 8 dic 2009
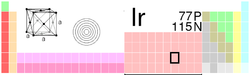
El iridio es un elemento químico de número atómico 77 que se sitúa en el grupo 9 de la tabla periódica. Su símbolo es Ir. Fue descubierto en 1803 por el químico inglés Smithson Tennant. Se trata de un metal de transición, del grupo del platino, duro, frágil, pesado, de color blanco plateado. Se emplea en aleaciones de alta resistencia que pueden soportar altas temperaturas. Es un elemento poco abundante y se encuentra en la naturaleza en aleaciones con platino y osmio. Es el elemento más resistente a la corrosión. Se emplea en contactos eléctricos, aparatos que trabajan a altas temperaturas, y como agente endurecedor del platino.
Características principales
Es de color blanco, parecido al platino, pero presenta una ligera coloración amarilla. Es difícil trabajar este metal, pues es muy duro y quebradizo. Es el metal más resistente a la corrosión. No es atacado por los ácidos, ni siquiera por el agua regia. Para disolverlo se emplea ácido clorhídrico, HCl, concentrado con clorato de sodio, NaClO3 a temperaturas altas.
El iridio es un metal extraterrestre, abundante en los meteoritos, y que en la corteza terrestre sólo tiene una concentración de 0,001 ppm.
El iridio NO es un metal extraterrestre falso. Que si bien es cierto es muy raro encontrarlo en la superficie de la Tierra este se encuentra en las profundidades del planeta. El núcleo de la Tierra está formado por este metal junto al hierro y níquel.
Aplicaciones
Se emplea aleado con el platino para catalizadores de célula combustible de amoníaco; para material de laboratorio; en electrodos comerciales y alambres de resistencias; como catalizador; en colorantes de extrusión para fibras de vidrio y en joyería fina. Se esta usando para hacer los electrodos de la bujias, en motores de combustion interna, haciendo eficiente de la combustion de gasolina.
Véase también
Enlaces externos
- Características mecánicas del iridio puro (en inglés) Matweb