Diferencia entre revisiones de «Dibenzodioxinas policloradas»
Etiquetas: Edición desde móvil Edición vía web móvil Edición móvil avanzada |
Etiquetas: Edición desde móvil Edición vía web móvil Edición móvil avanzada |
||
| Línea 85: | Línea 85: | ||
== Efectos sobre la salud en humanos == |
== Efectos sobre la salud en humanos == |
||
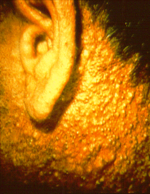
[[Archivo:Chloracne-in-herbicide-worker.png|thumb|150px|[[Cloracné]] en la oreja y el cuello de un trabajador de producción de [[Herbicida|herbicidas]]]] |
[[Archivo:Chloracne-in-herbicide-worker.png|thumb|150px|[[Cloracné]] en la oreja y el cuello de un trabajador de producción de [[Herbicida|herbicidas]]]] |
||
Las dioxinas se acumulan principalmente en los tejidos grasos con el tiempo ([[bioacumulación]]), por lo que incluso exposiciones pequeñas pueden llegar a alcanzar niveles peligrosos. En 1994, la EPA de los Estados Unidos informó que las dioxinas son un [[carcinógeno]] probable, pero señaló que los efectos no cancerosos (reproducción y desarrollo sexual, sistema inmunológico) pueden representar una mayor amenaza para la salud humana. La [[2,3,7,8-tetraclorodibenzo-p-dioxina|TCDD]], la más tóxica de las dibenzodioxinas, está clasificada como carcinógeno del Grupo 1 por el [[Centro Internacional de Investigaciones sobre el Cáncer]] (CIIC). La TCDD tiene una vida media de aproximadamente 8 años en humanos, aunque a altas concentraciones, el metabolismo mejora la tasa de eliminación.<ref name="pmid12107649">{{cite journal |author=Geusau A, Schmaldienst S, Derfler K, Päpke O, Abraham K |title=Severe 2,3,7,8-tetrachlorodibenzo- p-dioxin (TCDD) intoxication: kinetics and trials to enhance elimination in two patients |journal=Arch. Toxicol. |volume=76 |issue=5–6 |pages=316–25 |year=2002 |pmid=12107649 |doi=10.1007/s00204-002-0345-7|last2=Schmaldienst |last3=Derfler |last4=Päpke |last5=Abraham }}</ref> Los efectos sobre la salud de las dioxinas están mediados por su acción sobre un receptor celular, el receptor de hidrocarburos arilo (AhR).<ref name="pmid16545780">{{cite journal |author=Bock KW, Köhle C |title=Ah receptor: dioxin-mediated toxic responses as hints to deregulated physiologic functions |journal=Biochem. Pharmacol. |volume=72 |issue=4 |pages=393–404 |year=2006 |pmid=16545780 |doi=10.1016/j.bcp.2006.01.017|last2=Köhle }}</ref> |
|||
La exposición a altos niveles de dioxinas en humanos causa una forma severa de [[acné]] persistente, conocido como [[cloracné]].<ref name="pmid11564625">{{cite journal |author=Geusau A, Abraham K, Geissler K, Sator MO, Stingl G, Tschachler E |title=Severe 2,3,7,8-tetrachlorodibenzodioxin (TCDD) intoxication: clinical and laboratory effects |journal=Environ. Health Perspect. |volume=109 |issue=8 |pages=865–9 |year=2001 |pmid=11564625 | doi = 10.1289/ehp.01109865 |pmc=1240417 |jstor=3454832|last2=Abraham |last3=Geissler |last4=Sator |last5=Stingl |last6=Tschachler }}</ref> Estudios epidemiológicos han demostrado que los altos niveles ocupacionales o accidentales de exposición a las dioxinas conducen a un mayor riesgo de tumores en todos los sitios.<ref>[http://monographs.iarc.fr/ENG/Monographs/vol69/index.php IARC monograph: "Polychlorinated Dibenzo-''para''-dioxins"]</ref> Otros efectos en humanos (a dosis altas) pueden incluir: |
|||
*Developmental abnormalities in the [[tooth enamel|enamel]] of children's [[teeth]].<ref name="pmid15345345">{{cite journal |vauthors=Alaluusua S, Calderara P, Gerthoux PM |title=Developmental dental aberrations after the dioxin accident in Seveso |journal=Environ. Health Perspect. |volume=112 |issue=13 |pages=1313–8 |year=2004 |pmid=15345345 |doi= 10.1289/ehp.6920|pmc=1247522 |display-authors=etal }}</ref><ref name="pmid8260069">{{cite journal |author=Peterson RE, Theobald HM, Kimmel GL |title=Developmental and reproductive toxicity of dioxins and related compounds: cross-species comparisons |journal=Crit. Rev. Toxicol. |volume=23 |issue=3 |pages=283–335 |year=1993 |pmid=8260069| doi = 10.3109/10408449309105013|last2=Theobald |last3=Kimmel }}</ref> |
|||
*[[Central nervous system|Central]] and [[peripheral nervous system]] pathology<ref name="pmid16898675">{{cite journal |vauthors=Pelclová D, Urban P, Preiss J |title=Adverse health effects in humans exposed to 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) |journal=Reviews on Environmental Health |volume=21 |issue=2 |pages=119–38 |year=2006 |pmid=16898675 |doi=10.1515/reveh.2006.21.2.119 |display-authors=etal }}</ref> |
|||
*[[Thyroid]] disorders<ref name="pmid12821272">{{cite journal |author=Pavuk M, Schecter AJ, Akhtar FZ, Michalek JE |title=Serum 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) levels and thyroid function in Air Force veterans of the Vietnam War |journal=Annals of Epidemiology |volume=13 |issue=5 |pages=335–43 |year=2003 |pmid=12821272| doi = 10.1016/S1047-2797(02)00422-2|last2=Schecter |last3=Akhtar |last4=Michalek }}</ref> |
|||
*Damage to the [[immune system]]s<ref name="pmid12460794">{{cite journal |vauthors=Baccarelli A, Mocarelli P, Patterson DG |title=Immunologic effects of dioxin: new results from Seveso and comparison with other studies |journal=Environ. Health Perspect. |volume=110 |issue=12 |pages=1169–73 |year=2002 |pmid=12460794 |pmc=1241102 |doi=10.1289/ehp.021101169 |display-authors=etal }}</ref> |
|||
*[[Endometriosis]]<ref name="pmid12117638">{{cite journal |vauthors=Eskenazi B, Mocarelli P, Warner M |title=Serum dioxin concentrations and endometriosis: a cohort study in Seveso, Italy |journal=Environ. Health Perspect. |volume=110 |issue=7 |pages=629–34 |year=2002 |pmid=12117638 |doi= 10.1289/ehp.02110629|pmc=1240907 |display-authors=etal }}</ref> |
|||
*[[Diabetes]]<ref name="pmid15751269">{{cite journal |author=Arisawa K, Takeda H, Mikasa H |title=Background exposure to PCDDs/PCDFs/PCBs and its potential health effects: a review of epidemiologic studies |journal=J. Med. Invest. |volume=52 |issue=1–2 |pages=10–21 |year=2005 |pmid=15751269| doi = 10.2152/jmi.52.10|last2=Takeda |last3=Mikasa |doi-access=free }}</ref> |
|||
Recent studies have shown that high exposure to dioxins changes the ratio of male to female births among a population such that more females are born than males.<ref>{{cite news |url=https://www.reuters.com/article/healthNews/idUSN1836384520071018?feedType=RSS&feedName=healthNews |title=Dioxin pollution leads to more baby girls -study |work= Reuters |access-date=2007-10-22 | date=2007-10-18}}</ref> |
|||
Dioxins accumulate in food chains in a fashion similar to other chlorinated compounds ([[bioaccumulation]]). This means that even small concentrations in contaminated water can be concentrated up a food chain to dangerous levels because of the long biological half life and low water solubility of dioxins. |
|||
== Véase también == |
== Véase también == |
||
Revisión del 16:53 28 mar 2021
Las dibenzodioxinas policloradas (PCDD), o simplemente dioxinas, son un grupo de compuestos orgánicos polihalogenados que son contaminantes ambientales importantes.

Por simplicidad, se las denomina comúnmente, pero de manera inexacta, dioxinas, porque cada molécula de PCDD contiene una estructura esquelética de dibenzo-1,4-dioxina, con 1,4-dioxina como anillo central. Los miembros de la familia PCDD se bioacumulan en humanos y en la vida silvestre debido a sus propiedades lipofílicas y pueden causar alteraciones del desarrollo y cáncer.
Las dioxinas se producen como subproductos en la fabricación de algunos organocloruros, en la incineración de sustancias que contienen cloro, como el policloruro de vinilo (PVC), en el blanqueo con cloro del papel y en fuentes naturales como volcanes e incendios forestales.[1] Ha habido muchos incidentes de contaminación por dioxinas como resultado de emisiones industriales y accidentes; los primeros incidentes de este tipo se produjeron a mediados del siglo XIX durante la Revolución Industrial.[2]
La palabra "dioxinas" también puede referirse a otros compuestos clorados de acción similar (ver Dioxinas y compuestos similares a las dioxinas).
Estructura química de las dibenzo-1,4-dioxinas

La estructura de la dibenzo-1,4-dioxina consta de dos anillos de benceno unidos por dos puentes de oxígeno. Esto hace que el compuesto sea un diéter aromático. El nombre dioxina se refiere formalmente al anillo central dioxigenado, que está estabilizado por los dos anillos de benceno flanqueantes.
En los PCDD, los átomos de cloro están unidos a esta estructura en cualquiera de los 8 lugares diferentes de la molécula, en las posiciones 1-4 y 6-9. Hay 75 diferentes congéneres de PCDD (es decir, compuestos de dioxina relacionados).[3]
La toxicidad de los PCDD depende del número y la posición de los átomos de cloro. Se ha descubierto que los congéneres que tienen cloro en las posiciones 2, 3, 7 y 8 son significativamente tóxicos. De hecho, 7 congéneres tienen átomos de cloro en las posiciones relevantes que fueron considerados tóxicos por el esquema de equivalentes tóxicos de la Organización Mundial de la Salud (WHO-TEQ).[4]
Perspectiva histórica

Las bajas concentraciones de dioxinas existían en la naturaleza antes de la industrialización como resultado de la combustión natural y los procesos geológicos.[5][6] Las dioxinas se produjeron por primera vez involuntariamente como subproductos a partir de 1848 cuando las plantas de proceso Leblanc comenzaron a funcionar en Alemania.[2] La primera síntesis intencional de dibenzodioxina clorada fue en 1872. Hoy en día, las concentraciones de dioxinas se encuentran en todos los seres humanos, con niveles más altos que se encuentran comúnmente en personas que viven en países más industrializados. La dioxina más tóxica, 2,3,7,8-tetraclorodibenzo-p-dioxina (TCDD), se hizo conocida como contaminante del Agente Naranja, un herbicida utilizado en la Emergencia Malaya y la Guerra de Vietnam.[7] Más tarde, se encontraron dioxinas en Times Beach, Misuri[8] y Love Canal, Nueva York[9] y Seveso, Italia.[10] Más recientemente, las dioxinas han aparecido en las noticias con el envenenamiento del presidente Víktor Yúshchenko de Ucrania en 2004,[11] la crisis de la mozzarella de Nápoles[12] la crisis del cerdo irlandés de 2008 y el incidente de la alimentación en Alemania de 2010.[13]
Fuentes de dioxinas
El inventario de fuentes de compuestos similares a las dioxinas de la Agencia de Protección Ambiental de Estados Unidos es posiblemente la revisión más completa de las fuentes y liberaciones de dioxinas,[14] pero otros países ahora también tienen investigaciones sustanciales.

La exposición ocupacional es un problema para algunos en las industrias químicas, históricamente para aquellos que fabrican herbicidas de clorofenoles o clorofenoxiácidos o en la aplicación de productos químicos, en particular herbicidas. En muchas naciones desarrolladas existen ahora regulaciones sobre emisiones que han disminuido drásticamente las emisiones[14] y, por lo tanto, han aliviado algunas preocupaciones, aunque la falta de muestreo continuo de las emisiones de dioxinas causa preocupación por la subestimación de las emisiones. En Bélgica, mediante la introducción de un proceso llamado AMESA, el muestreo continuo mostró que el muestreo periódico subestimaba las emisiones en un factor de 30 a 50 veces. Pocas instalaciones cuentan con muestreo continuo.
Las dioxinas se producen en pequeñas concentraciones cuando se quema material orgánico en presencia de cloro, ya sea que el cloro esté presente como iones cloruro o como compuestos organoclorados, por lo que se producen ampliamente en muchos contextos. Según los datos más recientes de la EPA de Estados Unidos, las principales fuentes de dioxinas se encuentran en general en los siguientes tipos:[14]
- Fuentes de combustión, por ejemplo, incineradores de desechos municipales o desechos médicos y quema de barriles de patio trasero
- Fundición de metales
- Fuentes de refino y proceso
- Fuentes de fabricación de productos químicos
- Fuentes naturales
- Reservorios ambientales
Cuando se llevó a cabo por primera vez en 1987, el inventario original de fuentes de dioxinas de la EPA de EE. UU. Reveló que la incineración representaba más del 80% de las fuentes de dioxinas conocidas. Como resultado, la EPA de EE. UU. Implementó nuevos requisitos de emisiones. Estas regulaciones lograron reducir las emisiones de dioxinas de los incineradores. La incineración de desechos sólidos urbanos, desechos médicos, lodos de aguas residuales y desechos peligrosos juntos produce ahora menos del 3% de todas las emisiones de dioxinas. Sin embargo, desde 1987, la quema de barriles en el patio trasero casi no ha disminuido y ahora es la mayor fuente de emisiones de dioxinas, produciendo alrededor de un tercio de la producción total.[14]
En la incineración, las dioxinas también pueden reformarse o formarse de novoen la atmósfera sobre la chimenea a medida que los gases de escape se enfrían a través de una ventana de temperatura de 600 a 200 °C. El método más común para reducir la cantidad de dioxinas que se reforman o se forman de novo es mediante el enfriamiento rápido (30 milisegundos) de los gases de escape a través de esa ventana de 400 °C.[15] Las emisiones de dioxinas del incinerador se han reducido en más del 90% como resultado de los nuevos requisitos de control de emisiones. La incineración en los países desarrollados es ahora un contribuyente muy pequeño a las emisiones de dioxinas.
Las dioxinas también se generan en reacciones que no implican quemaduras, como fibras blanqueadoras con cloro para papel o textiles, y en la fabricación de fenoles clorados, particularmente cuando la temperatura de reacción no está bien controlada.[16] Los compuestos implicados incluyen el conservante de la madera pentaclorofenol y también herbicidas como el ácido 2,4-diclorofenoxiacético (o 2,4-D) y el ácido 2,4,5-triclorofenoxiacético (2,4,5-T). Los niveles más altos de cloración requieren temperaturas de reacción más altas y una mayor producción de dioxinas. También se pueden formar dioxinas durante la descomposición fotoquímica del compuesto antimicrobiano común triclosán.[17]
Fuentes de ingesta humana
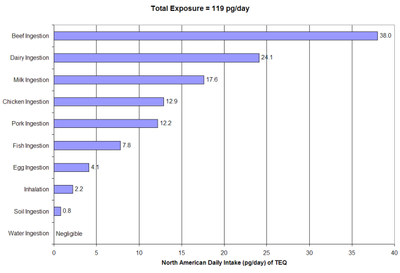
La Organización Mundial de la Salud y varios gobiernos han establecido ingestas tolerables diarias, mensuales o anuales. Las dioxinas ingresan a la población general casi exclusivamente por la ingestión de alimentos, específicamente a través del consumo de pescado, carne y productos lácteos, ya que las dioxinas son solubles en grasa y escalan fácilmente en la cadena alimentaria.[18][19]
Las madres transmiten a los niños cargas corporales sustanciales y la lactancia materna aumenta la carga corporal del niño.[20] La exposición a dioxinas también puede ocurrir por contacto con madera tratada con pentaclorofenol (Penta) ya que el pentaclorofenol a menudo contiene dioxinas como contaminante. La ingesta diaria de los niños durante la lactancia a menudo supera con creces la ingesta de los adultos en función del peso corporal. Es por eso que el grupo de consulta de la OMS evaluó la ingesta tolerable para evitar que una mujer acumule cargas corporales nocivas antes de su primer embarazo.[21] Los niños amamantados por lo general todavía tienen cargas corporales de dioxinas más altas que los niños no amamantados. La OMS todavía recomienda la lactancia materna por sus otros beneficios.[22] En muchos países, las dioxinas en la leche materna han disminuido incluso en un 90% durante las dos últimas décadas.[23]
Las dioxinas están presentes en el humo del cigarrillo.[24] Las dioxinas en el humo del cigarrillo fueron consideradas "subestimadas" por la EPA de los Estados Unidos en su "Reevaluación de las dioxinas" (1995). En ese mismo documento, la EPA de los Estados Unidos reconoció que la dioxina en los cigarrillos es "antropogénica" (artificial, "poco probable en la naturaleza").
Metabolismo
Las dioxinas se absorben principalmente a través de la ingesta dietética de grasas, ya que aquí es donde se acumulan en animales y humanos. En los seres humanos, las dioxinas altamente cloradas se almacenan en los tejidos grasos y no se metabolizan ni excretan fácilmente. La vida media de eliminación estimada de las dioxinas altamente cloradas (4 a 8 átomos de cloro) en los seres humanos varía de 4.9 a 13.1 años.[25]
Se cree que la persistencia de un congénere de dioxinas en particular en un animal es una consecuencia de su estructura. Las dioxinas sin cloro laterales (2, 3, 7 y 8), que por tanto contienen átomos de hidrógeno en pares de carbonos adyacentes, pueden oxidarse más fácilmente por los citocromos P450. Las dioxinas oxidadas pueden entonces excretarse más fácilmente en lugar de almacenarse durante un tiempo prolongado.
Toxicidad

La 2,3,7,8-tetraclorodibenzodioxina (TCDD) se considera el más tóxico de los congéneres. Otros congéneres de dioxinas, incluidos los PCDF y los PCB con toxicidad similar a las dioxinas, reciben una clasificación de toxicidad de 0 a 1, donde TCDD = 1. Esta clasificación de toxicidad se denomina concepto de factor de equivalencia tóxica o TEF. Los TEF son valores de consenso y, debido a la fuerte dependencia de las especies para la toxicidad, se enumeran por separado para mamíferos, peces y aves. Los TEF para especies de mamíferos son generalmente aplicables a los cálculos de riesgo humano. Los TEF se han desarrollado a partir de una evaluación detallada de los datos de la literatura para facilitar tanto la evaluación de riesgos como el control reglamentario.[4] Muchos otros compuestos también pueden tener propiedades similares a las de las dioxinas, en particular los PCB no ortográficos, uno de los cuales tiene un TEF tan alto como 0,1.
El valor de equivalencia tóxica total de dioxinas (EQT) expresa la toxicidad como si la mezcla fuera TCDD pura. El enfoque TEQ y los TEF actuales se han adoptado internacionalmente como la forma más apropiada de estimar los riesgos potenciales para la salud de la mezcla de dioxinas. Los datos recientes sugieren que este tipo de factor de escala simple puede no ser el tratamiento más apropiado para mezclas complejas de dioxinas; tanto la transferencia desde la fuente como la absorción y eliminación varían entre diferentes congéneres, y el valor de TEF no puede reflejar esto con precisión.[26]
Las dioxinas y otros contaminantes orgánicos persistentes (COP) están sujetos a la Convención de Estocolmo. El tratado obliga a los signatarios a tomar medidas para eliminar, cuando sea posible, y minimizar cuando no sea posible eliminar, todas las fuentes de dioxinas.
Efectos sobre la salud en humanos
Las dioxinas se acumulan principalmente en los tejidos grasos con el tiempo (bioacumulación), por lo que incluso exposiciones pequeñas pueden llegar a alcanzar niveles peligrosos. En 1994, la EPA de los Estados Unidos informó que las dioxinas son un carcinógeno probable, pero señaló que los efectos no cancerosos (reproducción y desarrollo sexual, sistema inmunológico) pueden representar una mayor amenaza para la salud humana. La TCDD, la más tóxica de las dibenzodioxinas, está clasificada como carcinógeno del Grupo 1 por el Centro Internacional de Investigaciones sobre el Cáncer (CIIC). La TCDD tiene una vida media de aproximadamente 8 años en humanos, aunque a altas concentraciones, el metabolismo mejora la tasa de eliminación.[27] Los efectos sobre la salud de las dioxinas están mediados por su acción sobre un receptor celular, el receptor de hidrocarburos arilo (AhR).[28]
La exposición a altos niveles de dioxinas en humanos causa una forma severa de acné persistente, conocido como cloracné.[29] Estudios epidemiológicos han demostrado que los altos niveles ocupacionales o accidentales de exposición a las dioxinas conducen a un mayor riesgo de tumores en todos los sitios.[30] Otros efectos en humanos (a dosis altas) pueden incluir:
- Developmental abnormalities in the enamel of children's teeth.[31][32]
- Central and peripheral nervous system pathology[33]
- Thyroid disorders[34]
- Damage to the immune systems[35]
- Endometriosis[36]
- Diabetes[37]
Recent studies have shown that high exposure to dioxins changes the ratio of male to female births among a population such that more females are born than males.[38]
Dioxins accumulate in food chains in a fashion similar to other chlorinated compounds (bioaccumulation). This means that even small concentrations in contaminated water can be concentrated up a food chain to dangerous levels because of the long biological half life and low water solubility of dioxins.
Véase también
- Dioxinas y compuestos similares a las dioxinas
- Dibenzofuranos policlorados (PCDF): Un grupo de compuestos, producido por las mismas condiciones que las dioxinas y comúnmente co-presente con dioxinas en incidentes de contaminación. Tienen el mismo modo de acción tóxica y se incluyen en el esquema de equivalentes tóxicos para evaluar los niveles de dioxinas.
- Bifenilos policlorados: Grupo de compuestos que se han utilizado históricamente en la fabricación de transformadores eléctricos, algunos de cuyos miembros también pueden contribuir a la toxicidad similar a las dioxinas. Estos compuestos similares a las dioxinas también se incluyen en el esquema de equivalentes tóxicos cuando se miden los niveles de dioxinas.
Referencias
- ↑ Beychok, Milton R. (January 1987). «A data base for dioxin and furan emissions from refuse incinerators». Atmospheric Environment 21 (1): 29-36. Bibcode:1987AtmEn..21...29B. doi:10.1016/0004-6981(87)90267-8.
- ↑ a b Weber R, Tysklind M, Gaus C (2008). «Dioxin - contemporary and future challenges of historical legacies». Environmental Science and Pollution Research 15 (2): 96-100 (p.97). PMID 18380226. doi:10.1065/espr2008.01.473.
- ↑ Nomenclature and physico-chemical properties of PCDDs and PCDFs. In: Dioxins in the Environment: What are the health risks? INSERM Collective Expert Evaluation Reports (2000). Ncbi.nlm.nih.gov (2011-03-18). Retrieved on 2011-06-09.
- ↑ a b Van den Berg M, Birnbaum LS, Denison M (2006). «The 2005 World Health Organization reevaluation of human and Mammalian toxic equivalency factors for dioxins and dioxin-like compounds». Toxicol. Sci. 93 (2): 223-41. PMC 2290740. PMID 16829543. doi:10.1093/toxsci/kfl055.
- ↑ «Compilation of EU Dioxin Exposure and Health Data». Archivado desde el original el 16 de junio de 2007. Consultado el 4 de junio de 2007.
- ↑ «FDA/CFSAN — Questions and Answers about Dioxins». Archivado desde el original el 1 de junio de 2007. Consultado el 4 de junio de 2007.
- ↑ Schecter A, Birnbaum L, Ryan JJ, Constable JD; Birnbaum; Ryan; Constable (2006). «Dioxins: an overview». Environ. Res. 101 (3): 419-28. Bibcode:2006ER....101..419S. PMID 16445906. doi:10.1016/j.envres.2005.12.003.
- ↑ «Times Beach Record of Decision Signed». United States Environmental Protection Agency. Consultado el 4 de junio de 2007.
- ↑ «Love Canal Record of Decision Signed». United States Environmental Protection Agency. Consultado el 4 de junio de 2007.
- ↑ «4 Seveso: A paradoxical classic disaster». Consultado el 4 de junio de 2007.
- ↑ «Yushchenko's acne points to dioxin poisoning». Consultado el 14 de enero de 2009.
- ↑ McCarthy, Michael; Phillips, John (22 de marzo de 2008). «Italy's toxic waste crisis, the Mafia – and the scandal of Europe's mozzarella». The Independent (London). Consultado el 28 de marzo de 2008.
- ↑ http://ec.europa.eu/food/committees/regulatory/scfcah/animal_health/presentations/1112012011_dioxin_germany.pdf
- ↑ a b c d «An Inventory of Sources and Environmental Releases of Dioxin-Like Compounds in the U.S. for the Years 1987, 1995, and 2000» (PDF). 1 de noviembre de 2006. EPA/600/P-03/002f, Final Report
- ↑ Cheung WH, Lee VK, McKay G; Lee; McKay (2007). «Minimizing dioxin emissions from integrated MSW thermal treatment». Environ. Sci. Technol. 41 (6): 2001-7. Bibcode:2007EnST...41.2001C. PMID 17410797. doi:10.1021/es061989d.
- ↑ Kulkami P.S.; Crespo J.G.; Afonso C.A.M. (2008). «Dioxins sources and current remediation technologies - a review». Environment International 34 (1): 139-153. PMID 17826831. doi:10.1016/j.envint.2007.07.009.
- ↑ Latch DE, Packer JL, Stender BL, VanOverbeke J, Arnold WA, McNeill K; Packer; Stender; Vanoverbeke; Arnold; McNeill (2005). «Aqueous photochemistry of triclosan: formation of 2,4-dichlorophenol, 2,8-dichlorodibenzodioxin, and oligomerization products». Environ. Toxicol. Chem. 24 (3): 517-25. PMID 15779749. doi:10.1897/04-243R.1.
- ↑ a b Schecter A, Cramer P, Boggess K (2001). «Intake of dioxins and related compounds from food in the U.S. population». J. Toxicol. Environ. Health Part A 63 (1): 1-18. PMID 11346131. doi:10.1080/152873901750128326.
- ↑ Liem A.K.; Furst P.; Rappe C. (2000). «Exposure of populations to dioxins and related compounds». Food Additives and Contaminants 17 (4): 241-259. PMID 10912239. doi:10.1080/026520300283324.
- ↑ Przyrembel H, Heinrich-Hirsch B, Vieth B; Heinrich-Hirsch; Vieth (2000). Exposition to and Heal Theffects of Residues in Human Milk. «Exposition to and health effects of residues in human milk». Adv. Exp. Med. Biol. Advances in Experimental Medicine and Biology 478. pp. 307-25. ISBN 978-0-306-46405-8. PMID 11065082. doi:10.1007/0-306-46830-1_27.
- ↑ «Consultation on assessment of the health risks of dioxins; re-evaluation of the tolerable daily intake (TDI): Executive summary». Food Additives and Contaminants 17 (4): 223-240. 2000. PMID 10912238. doi:10.1080/713810655.
- ↑ Healthy Milk, Healthy Baby – Chemical Pollution and Mother's Milk – Chemicals: Dioxins and Furans. Nrdc.org. Retrieved on 2011-06-09.
- ↑ «WHO Fact Sheet – "Persistent organic pollutants in human milk». Diciembre de 2009. Consultado el 29 de abril de 2017.
- ↑ Ball M, Paepke O, Lis A (1990). «Polychlordibenzodioxine und Polychlordibenzofurane in Cigarettenrauch». Beitr. Tabakforsch. Int. 14 (6): 393-402. Archivado desde el original el 18 de diciembre de 2008.
- ↑ Milbrath MO, Wenger Y, Chang C, Emond C, Garabrant D, Gillespie BW, Jolliet O; Wenger; Chang; Emond; Garabrant; Gillespie; Jolliet (2009). «Apparent half-lives of dioxins, furans, and polychlorinated biphenyls as a function of age, body fat, smoking status, and breast-feeding». Environmental Health Perspectives 117 (3): 417-425. PMC 2661912. PMID 19337517. doi:10.1289/ehp.11781.
- ↑ Tuomisto, J. The toxic equivalency principle and its application in dioxin risk assessment. In: R. Pohjanvirta (editor): The AH Receptor in Biology and Toxicology. Wiley, 2011. ISBN 978-0-470-60182-2.
- ↑ Geusau A, Schmaldienst S, Derfler K, Päpke O, Abraham K; Schmaldienst; Derfler; Päpke; Abraham (2002). «Severe 2,3,7,8-tetrachlorodibenzo- p-dioxin (TCDD) intoxication: kinetics and trials to enhance elimination in two patients». Arch. Toxicol. 76 (5–6): 316-25. PMID 12107649. doi:10.1007/s00204-002-0345-7.
- ↑ Bock KW, Köhle C; Köhle (2006). «Ah receptor: dioxin-mediated toxic responses as hints to deregulated physiologic functions». Biochem. Pharmacol. 72 (4): 393-404. PMID 16545780. doi:10.1016/j.bcp.2006.01.017.
- ↑ Geusau A, Abraham K, Geissler K, Sator MO, Stingl G, Tschachler E; Abraham; Geissler; Sator; Stingl; Tschachler (2001). «Severe 2,3,7,8-tetrachlorodibenzodioxin (TCDD) intoxication: clinical and laboratory effects». Environ. Health Perspect. 109 (8): 865-9. JSTOR 3454832. PMC 1240417. PMID 11564625. doi:10.1289/ehp.01109865.
- ↑ IARC monograph: "Polychlorinated Dibenzo-para-dioxins"
- ↑ «Developmental dental aberrations after the dioxin accident in Seveso». Environ. Health Perspect. 112 (13): 1313-8. 2004. PMC 1247522. PMID 15345345. doi:10.1289/ehp.6920. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ Peterson RE, Theobald HM, Kimmel GL; Theobald; Kimmel (1993). «Developmental and reproductive toxicity of dioxins and related compounds: cross-species comparisons». Crit. Rev. Toxicol. 23 (3): 283-335. PMID 8260069. doi:10.3109/10408449309105013.
- ↑ «Adverse health effects in humans exposed to 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD)». Reviews on Environmental Health 21 (2): 119-38. 2006. PMID 16898675. doi:10.1515/reveh.2006.21.2.119. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ Pavuk M, Schecter AJ, Akhtar FZ, Michalek JE; Schecter; Akhtar; Michalek (2003). «Serum 2,3,7,8-tetrachlorodibenzo-p-dioxin (TCDD) levels and thyroid function in Air Force veterans of the Vietnam War». Annals of Epidemiology 13 (5): 335-43. PMID 12821272. doi:10.1016/S1047-2797(02)00422-2.
- ↑ «Immunologic effects of dioxin: new results from Seveso and comparison with other studies». Environ. Health Perspect. 110 (12): 1169-73. 2002. PMC 1241102. PMID 12460794. doi:10.1289/ehp.021101169. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ «Serum dioxin concentrations and endometriosis: a cohort study in Seveso, Italy». Environ. Health Perspect. 110 (7): 629-34. 2002. PMC 1240907. PMID 12117638. doi:10.1289/ehp.02110629. Parámetro desconocido
|vauthors=ignorado (ayuda) - ↑ Arisawa K, Takeda H, Mikasa H; Takeda; Mikasa (2005). «Background exposure to PCDDs/PCDFs/PCBs and its potential health effects: a review of epidemiologic studies». J. Med. Invest. 52 (1–2): 10-21. PMID 15751269. doi:10.2152/jmi.52.10. Parámetro desconocido
|doi-access=ignorado (ayuda) - ↑ «Dioxin pollution leads to more baby girls -study». Reuters. 18 de octubre de 2007. Consultado el 22 de octubre de 2007.
Enlaces externos
- Hoja de datos de NIEHS sobre dioxinas
- "Dioxinas y Compuestos Similares a las Dioxinas en el Suministro de Alimentos: Estrategias para Disminuir la Exposición", un informe de 2003 de la Academia Nacional de Ciencias
- "Evaluación de los Riesgos para la Salud de las Diooxinas", un informe de 1998 de la Organización Mundial de la Salud.
