Vibrio cholerae
| Vibrio cholerae | ||
|---|---|---|
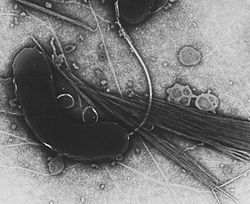 Imagen TEM | ||
| Taxonomía | ||
| Dominio: | Bacteria | |
| Filo: | Pseudomonadota | |
| Clase: | Gammaproteobacteria | |
| Orden: | Vibrionales | |
| Familia: | Vibrionaceae | |
| Género: | Vibrio | |
| Especie: |
V. cholerae Pacini 1854 | |
Vibrio cholerae es una bacteria gram negativa con forma de bastón curvo (género vibrio) que provoca el cólera en humanos.[1][2] Junto con otra especie de género Vibrio pertenece a la subdivisión gamma de las proteobacterias. Hay dos cepas principales de V. cholerae, clásica y El Tor, y numerosos serogrupos.
Historia[editar]
Durante siglos, la enfermedad siguió siendo desconocida en Europa, extendiéndose principalmente en Asia y África. La primera mención de esta enfermedad en Europa la hizo en 1503 un oficial portugués al regresar de la India, contando que una enfermedad había ocasionado 20 000 muertes. Apareció más tarde en Europa y fue objeto de una multitud de interpretaciones y teorías por parte de los médicos. Fue durante la epidemia de 1854 en Londres cuando la comprensión de la enfermedad experimentó un gran avance, al apreciarse que la enfermedad se producía cerca de algunos pozos, lo que sugería la contaminación del agua. Pero esta hipótesis no fue aceptada de inmediato en el momento daña al ser humano .
Vibrio cholerae fue hallado como responsable del cólera por el anatomista italiano Filippo Pacini en 1854.[3] Pero su descubrimiento será ignorado por el predominio de la teoría de los miasmas, atribuyendo la responsabilidad del cólera (y de otras enfermedades que eran origen desconocido) a la mala calidad del aire. En el mismo año, Joaquim Balcells i Pascual[4][5] describió Vibrio cholerae. Treinta años más tarde, en 1884, Robert Koch, que no sabía los resultados de Pacini, publicó los resultados de su trabajo[3] y los medios para luchar contra la Vibrio cholerae.
En 1965, la bacteria fue renombrada como Vibrio cholerae (Pacini, 1854) en homenaje a Filippo Pacini.
Epidemiología[editar]
El cólera es endémico en las regiones del mundo con infraestructuras de agua, saneamiento e higiene deficientes, como el África subsahariana y las regiones de Oriente Medio. En países desarrollados, se ve esporádicamente. Actualmente, es endémica en 69 países, incluidos Asia, África y las Américas, con 1300 millones de personas en riesgo, siendo África subsahariana la peor. V. cholerae se originó en el subcontinente indio y causó seis pandemias entre 1827 y 1923. La séptima pandemia ha estado en curso desde 1961 y llegó a América del Sur y la mayor parte del hemisferio occidental en 1991. Aunque ampliamente subestimado, la Organización Mundial de la Salud estima un total de 2,8 millones de casos con 91.000 muertes al año. Recientemente, el cólera ha seguido afectando a comunidades vulnerables como Haití después del terremoto (2010), Irak y Yemen, donde los desastres naturales, el movimiento de refugiados, la guerra y los conflictos aumentan el riesgo de infección y brotes. Aunque el agua potable segura y los sistemas de saneamiento avanzados han hecho del cólera una enfermedad tratable y limitada en Europa y América del Norte, las nuevas cepas de V. cholerae, la facilidad para viajar y la migración constante de personas posiblemente infectadas han planteado graves problemas de salud pública.[6]
Características[editar]

Vibrio es un género de bacterias gram negativas, perteneciente al orden de los Vibrionales, de las gamma-proteobacterias, con forma de bacilos curvados. Bioquímicamente se caracterizan por dar positivo en las pruebas de la catalasa y de la oxidasa, también dan negativo en la adenina dihidrolasa, y positivo en la ornitina descarboxilasa. Vibrio cholerae concretamente es sacarosa y manitol positivo y nitrato reductasa positivo. Es una bacteria anaerobia facultativa, y su metabolismo es fermentativo; pueden fermentar, entre otros sustratos, la glucosa.[7] Poseen flagelación polar, que les otorga una movilidad máxima.
Pese a que nutricionalmente son poco exigentes, se emplean medios específicos para aislarlos de muestras clínicas. El sodio estimula su crecimiento y además tolera pH alcalinas, por eso se utiliza para su cultivo agua de peptona alcalina.[7] En presencia de V. cholereae se observa ausencia de polimorfonucleares.
En el caso de la cepa bacteriana inocua de Vibrio cholerae, producto de una conversión lisogénica por acción de un bacteriófago, esta igualmente se transforma en una cepa tremendamente virulenta que puede causar cólera.
Aislamiento[editar]
A partir de vómitos o heces diarreicas, se extrae una alícuota que es introducido en un medio de transporte. De este, se puede efectuar la observación en fresco, al microscopio de contraste de fase, o mediante una tinción de Gram. Existen kits de anticuerpos para efectuar su determinación e identificación por inmunofluorescencia.
Una vez dirigida la sospecha al grupo, se siembra un alícuota en un medio de enriquecimiento que sea selectivo, como el TCBS (que contiene tiosulfato, citrato, sales biliares y sacarosa).
Una vez obtenido en cultivo puro, se procesa la muestra mediante diversos tests bioquímicos: oxidasa, LDC, ODC, entre otros.
Existen procedimientos de aglutinación para determinar el biotipo; por ejemplo, el O1 (llamado El Tor) y el O139 son los más relevantes clínicamente.
Crecen con rapidez en agar peptona, agar sangre con pH cercano a 9,0; o sobre agar TCBS, y en 18 horas se pueden observar colonias típicas. Pueden incubarse unas pocas gotas de heces, para enriquecimiento, durante 6 a 8 horas en caldo taurocolato-peptona (pH 8 a 9).
Factores de virulencia[editar]
- Como adhesinas poseen pili TCP, corregulados con la toxina.
- Antígeno somático O, un pirógeno del lipopolisacárido.
- Antígeno H, del flagelo; antígeno proteico que permite el establecimiento de la bacteria en la mucosa del intestino delgado.
- Hemolisinas, en el biotipo El Tor.
- Neuraminidasa.
- Exotoxina, la toxina colérica, principal factor de virulencia.
- Toxina Zot: Incrementa la permeabilidad de la mucosa intestinal afectando a la estructura de las uniones intercelulares de tipo zonula ocludens[8].
- Toxina Ace: Incrementa la diferencia de potencial a ambos lados de la membrana[8].
La transcripción de los TCP y la toxina colérica está regulada por la proteína reguladora ToxT, que activa la cascada de virulencia[9].
Toxina colérica[editar]
Es del tipo AB[2] . Sus genes están agrupados en el operón Ctx AB, corregulado con los pili TCP antes mencionados.
- CtxA codifica para la subunidad A, activa biológicamente.
- CtxB codifica para la subunidad B, de unión al gangliósido GM1 de las células epiteliales.
Existe una regulación traduccional que favorece la mayor expresión de la subunidad B; consiste en la posesión por parte de su mRNA de una secuencia de unión a ribosomas de más fuerza que la de A.
Un hexámero AB5 interacciona con el gangliósido facilitando la penetración de la subunidad A (en realidad del fragmento A1) de la toxina en el citoplasma del enterocito. Este hecho permite la activación de la adenilato ciclasa celular por ADP-ribosilación de la proteína G estimuladora que regula dicha actividad adenilil ciclasa. Esto provoca un incremento en los niveles intracelulares de AMPc, abriendo los canales de Cl- de la membrana apical y manteniendo los abiertos. La secreción de Cl- se acompaña de secreción de Na+ y como estas son moléculas osmóticamente activas van a favorecer la secreción de agua hacia el lumen intestinal. El volumen de líquido secretado hacia el lumen intestinal supera los mecanismos de absorción de intestino delgado y colon generando la diarrea masiva.[10]
Los pacientes de cólera, en la fase activa de secreción de la enfermedad, tienen concentraciones elevadas de prostaglandina E2, que además se ha demostrado que estimulan a la adenilato ciclasa y la secreción de ácido araquidónico de los fosfolípidos de membrana[8].
Tratamiento[editar]
El tratamiento principal se basa en una rehidratación adecuada hasta que la enfermedad termina su curso. La rehidratación se puede acompañar de la infusión de intravenosa de líquido. La terapia antimicrobiana juega un papel secundario disminuyendo la severidad de la enfermedad y la duración del tiempo de excreción del microorganismo.
- Rehidratación intravenosa: Para adultos, la solución de reemplazo intravenosa debe infundirse lo más rápido posible para que se administren aproximadamente 2 litros en los primeros 30 minutos. Si en este punto la condición clínica del paciente mejora, la perfusión puede reducirse para administrar aproximadamente 100 ml/kg de peso corporal dentro de las primeras 4 h de terapia. Los niños en shock deben recibir 30 ml de líquido intravenoso por kg de peso corporal en el primera hora y 40 ml/kg adicionales en las siguientes 2 h. Tanto en adultos como en niños, las SRO (con su glucosa y potasio) deben administrarse lo antes posible en el curso de la enfermedad. Las tasas precisas de administración de líquidos deben ajustarse de acuerdo con el control del estado de hidratación del paciente y las pérdidas continuas de heces.
- Rehidratación oral: Los pacientes con deshidratación leve o moderada pueden recibir reposición inicial de líquidos para reparar los déficits de agua y electrolitos exclusivamente por vía oral. Para la deshidratación leve, la OMS recomienda administrar SRO en un volumen de 50 ml/kg dentro de las primeras 4 h. Para deshidratación moderada, se debe administrar el doble de este volumen (100 ml/kg) en el mismo período de tiempo. Los vómitos rara vez impiden el uso exitoso de SRO y no son una contraindicación para su uso.
- Terapia antimicrobiana: El tratamiento debe iniciarse al desaparecer los vómitos. La tetraciclina es el antibiótico de elección.
Dosis en adultos: Doxiciclina 300mg vía oral dosis única alternativa Tetraciclina 500 mg cada 6 horas por 3 días o trimetropin-sulfametasona 80/400 mg cada 12 horas por 5 días.
Dosis en niños: 10 a 14 años 200 mg doxiciclina dosis única . 5 a 9 años 100 mg doxiciclina dosis única. menor a 5 años eritromicina 30mg/kg por 3 días.
Diagnóstico[editar]
Las muestras para el cultivo consisten en tomar algo de moco de la heces y se cultivan en agar TCBS que produce colonias color amarillas que son fácilmente visibles contra el fondo verde-oscuro del agar. Si la prueba de la oxidasa para detectar la bacteria Vibrio cholerae es positiva, el mismo ha detectado un organismo gram negativo.
Véase también[editar]
- Cepa El Tor (bacteria)
Referencias[editar]
- ↑ Ryan KJ; Ray CG (editors) (2004). Sherris Medical Microbiology (4ª ed. edición). McGraw Hill. ISBN 0838585299.
- ↑ a b Faruque SM; Nair GB (eds). (2008). Vibrio cholerae: Genomics and Molecular Biology. Caister Academic Press. ISBN 978-1-904455-33-2 .
- ↑ a b Howard-Jones, Norman (4 de febrero de 1984). «Robert Koch and the cholera vibrio: a centenary». British Medical Journal (Clinical Research) (en inglés) 288 (6414): 379-381. doi:10.1136/bmj.288.6414.379. Archivado desde el original el 1 de agosto de 2020. Consultado el 1 de agosto de 2020.
- ↑ Real Academia de la Historia, ed. (2018). «Joaquín Balcells y Pasqual». Archivado desde el original el 8 de julio de 2019. Consultado el 1 de agosto de 2020.
- ↑ Colegio Oficial de Médicos de Barcelona, ed. (2015). «Joaquim Balcells i Pascual» (en catalán). Archivado desde el original el 1 de agosto de 2020. Consultado el 1 de agosto de 2020.
- ↑ Ojeda Rodriguez, Jafet A.; Kahwaji, Chadi I. (2022). Vibrio Cholerae. StatPearls Publishing. Consultado el 16 de diciembre de 2022.
- ↑ a b Merrell, D. S., Butler, S. M., Qadri, F., Dolganov, N. A., Alam, A., Cohen, M. B., Calderwood, S. B., Schoolnik, G. K., Camilli, A. Host-induced epidemic spread of the cholera bacterium. Nature. 6 de junio de 2002; 417(6889):642-5
- ↑ a b c Kaper, J B; Morris, J G; Levine, M M (1995-01). «Cholera». Clinical Microbiology Reviews (en inglés) 8 (1): 48-86. ISSN 0893-8512. PMC 172849. PMID 7704895. doi:10.1128/CMR.8.1.48. Consultado el 16 de diciembre de 2022.
- ↑ Liu, Yutao; Xu, Tingting; Wang, Qian; Huang, Junxi; Zhu, Yangfei; Liu, Xingmei; Liu, Ruiying; Yang, Bin et al. (8 de junio de 2022). «Vibrio cholerae senses human enteric α-defensin 5 through a CarSR two-component system to promote bacterial pathogenicity». Communications Biology (en inglés) 5 (1): 559. ISSN 2399-3642. doi:10.1038/s42003-022-03525-3. Consultado el 16 de diciembre de 2022.
- ↑ Costanzo, Linda (2000). Fisiologia.
