Proteína G
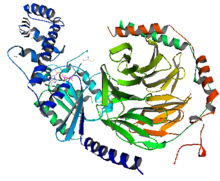
Las proteínas G (Proteína fijadora de nucleótido de Guanina) son una familia de proteínas transductoras de señales desde el receptor al que están acopladas hasta una o más proteínas efectoras y dependen del nucleótido guanosin trifosfato (GTP) para su activación.[2] Los receptores acoplados a la proteína G (GPCR, del inglés: G protein-coupled receptors) comprenden las dianas de varias aminas biógenas, eicosanoides y otras moléculas que envían señales a células diana como lípidos, péptidos hormonales, opiáceos, aminoácidos (GABA) y muchos otros péptidos y ligandos proteínicos. Los efectores que son regulados por la proteína G comprenden enzimas como la adenilil ciclasa, fosfolipasa C, fosfodiesterasas y canales de iones de la membrana plasmática selectivos para Ca²+ y K+. Gracias a su número e importancia fisiológica, los GPCR constituyen objetivos muy utilizados para los fármacos; quizás la mitad de los fármacos que no son antibióticos están dirigidos hacia estos receptores, que constituyen la tercera familia más grande de genes en el ser humano.[3]
Caracterizadas por su interacción con guanosín trifosfato (GTP) conducente a la hidrólisis del nucleótido a guanosín difosfato (GDP). Su nombre deriva de la inicial de guanosina. En la fisiología celular actúan como interruptores biológicos mediante la transducción de señales. De esta manera, un estímulo del exterior celular, un ligando por ejemplo, accede al receptor celular asociado a proteína G o GPCR desencadenando una cascada de actividades enzimáticas o segundos mensajeros como respuesta.[4]
Debido a su estructura molecular, las proteínas G se clasifican en dos tipos, heterotriméricas y monoméricas. Las primeras, grandes o heterotriméricas, están constituidas por tres subunidades distintas, denominadas αβγ; se trata de proteínas ancladas a membrana, aunque no integrales de membrana. Las segundas, pequeñas o monoméricas, con una única subunidad, se encuentran libres en el citosol y nucleoplasma.[5]


Estas proteínas se encuentran activadas cuando poseen GTP en su estructura, e inactivadas cuando se trata de GDP. Por tanto, la actividad GTPasa es crucial para su funcionamiento como interruptores biológicos. Dicha actividad hidrolítica se modula también mediante proteínas accesorias, como son las pertenecientes a los siguientes grupos:[6]
- GEF, de las siglas en inglés de factor intercambiador de nucleótido de guanina. Se trata de un factor proteico que facilita el intercambio de GDP de la estructura de la proteína G por GTP, por lo cual la activa.
- GAP, de las siglas en inglés de proteína aceleradora de la actividad GTPasa, que favorece la ruptura del enlace fosfodiéster del GTP a GDP, por lo cual inactiva a la proteína G.
Estos reguladores, denominados a veces en la literatura como RGS (siglas en inglés de regulator of G protein signaling), modifican la actividad hidrolítica de las proteínas G mediante mecanismos moleculares que han sido descritos en algunos casos, puesto que hay decenas de reguladores identificados. De hecho, se cree que proteínas reguladoras concretas, expresadas en células específicas en momentos definidos, tienen un papel importante en la modulación de la transducción de señales.[6]
Es de resaltar que GAP solo aumenta la velocidad de la actividad GTPasa; el punto clave de la regulación mediada por proteínas G consiste en su tenencia de una actividad GTPasa que proporcione un lapso de actividad corto y definido. La activación permanente de la proteína G es muy perniciosa y, de hecho, es causa de enfermedades (por ejemplo, algunos cánceres,[7] o bien la deshidratación por la toxina del vibrio del cólera).[8]
Proteínas G heterotriméricas[editar]
Las proteínas G heterotriméricas, se sitúan en la membrana plasmática, a la cual están ligadas por sus subunidades α y γ mediante estructuras hidrofóbicas, de tipo ácido graso o isoprenoide. Queda una tercera subunidad, la β, que se asocia a la subunidad γ. En conjunto, y en reposo, es decir, con GDP unido a la subunidad α, las tres subunidades se sitúan en algún lugar de la membrana biológica, poseyendo movimiento dada su fluidez. Cuando un GPCR recibe un estímulo y se activa a la proteína G, con la consiguiente adquisición de GTP, hidrolizado tras un lapso después, ésta se disgrega en dos partes: una, βγ, que puede ejercer funciones biológicas como la apertura de canales; y otra, α, que activa cascadas de señalización celular, como por ejemplo mediante adenilato ciclasa y la generación de AMP cíclico.

El proceso de activación de proteínas efectoras inducidas por ligando puede explicarse según un modelo en tres fases:[4][5]
- El receptor (azul claro) se encuentra en estado de reposo, así como el efector (rojo pálido). La proteína G se encuentra con todas sus subunidades asociadas y unido a GDP; por lo tanto, inactiva.
- La unión del ligando induce un cambio conformacional en el receptor (azul oscuro).
- El cambio conformacional en el receptor tiene resonancia en la estructura de , la cual sufre cambios conformacionales en sus terminales amino y carboxilo..
- A consecuencia de dichos cambios conformacionales, pierde afinidad por GDP, y a su vez el amino terminal se gira permitiendo la salida de GDP y se entra GTP, por lo que la proteína entra en su estado activo. Dicha unión de con GTP provoca la disociación del dimero respecto al , por lo que tanto como el dimero activan a sus respectivos efectores.
- El ligando se disocia del receptor, por lo cual se inactiva (azul claro). tiene actividad catalítica intrínseca por lo que se favorece su recambio nuevamente a GDP.
- La hidrólisis de GTP a GDP causa la disociación de del efector y se reasocia con . Todo el sistema queda en reposo, inactivo.
La activación catalítica de las proteínas G heterotriméricas mediada por la interacción con los receptores (GPCRs) puede interpretarse como una actividad de factor intercambiador de nucleótidos de guanina de estos últimos. La comunicación estructural entre la subunidad βγ de la proteína G y el receptor es motivo de interés en la comunidad científica puesto que algunos de estos receptores son el objetivo de nuevas drogas para combatir enfermedades;[9] además, dichos receptores son abundantes en el genoma (representando más del 1 % del humano),[10] y están involucrados en funciones tanto cardiovasculares, como nerviosas, endocrinas y sensoriales.[11][12][13]
Proteínas G monoméricas[editar]
Las proteínas G monoméricas o pequeñas son GTPasas de masas moleculares entre 20 y 40 kDa.[14] Actúan como reguladoras de procesos claves, como la proliferación celular (p. ej. Ras), tráfico de vesículas (p. ej. Rab) o la estructura del citoesqueleto (p. ej. Rho). Actúan en el mismo polipéptido la actividad GTPasa y la capacidad reconocimiento de motivos estructurales en otras moléculas, siendo además muy móviles en el interior celular, sin poseer la restricción de su ligación a las membranas celulares. Para regular su actividad GTPasa, existen también proteínas GEF y GAP, antes mencionadas. En muchos casos, se encuentran solubles en el citosol, puesto que, aunque albergan en su estructura una cadena hidrofóbica que les permite anclarse a las membranas, la mantienen escondida hasta que un estímulo les sugiere un cambio conformacional para exponerla. Así, existe una dicotomía entre posesión de GDP o GTP pero también de exposición o salvaguardia de la cadena hidrofóbica.[4][5] Sus primeros representantes, Ha-Ras y Ki-Ras, fueron descubiertos como oncogones de virus de sarcoma (v-Ha-Ras y v-Ki-Ras) a finales de los años 70.[15][16] Durante los años siguientes, se describieron centenares de miembros de la superfamilia en todo tipo de eucariotas, desde levaduras a humanos.[14]
Estructuralmente, los análisis de cristalografía y resonancia magnética nuclear efectuados sobre distintos representantes de la superfamilia determinaron la existencia de dominios de unión a nucleótidos de guanina con una topología común. Mediante el estudio de moléculas tanto unidas a GDP como a GTP, y sus diferencias, se encontró que existen dos regiones flexibles en torno al carbono γ del GTP: una primera región «bisagra» entre los giros L2 y β2 (que determinan una región efectora) y una segunda entre los giros L4 y la hélice alfa 2. La región efectora giraría dando lugar a dos estados: el de interacción con GTP o GDP, mediante la interacción del fosfato situado en γ con la Tyr-32 de la proteína.[17]
Receptores y efectores[editar]

Los receptores asociados a proteína G se reconocen por su estructura en serpentín, esto es, con siete dominios transmembrana, por lo que a veces son denominados «receptores 7TM». Comprenden multitud de proteínas, puesto que el término corresponde a una familia de receptores transmembrana que detectan señales extracelulares y las transmiten a las cascadas de transducción de señales del interior celular, que desencadenan a su vez las respuestas pertinentes (por ejemplo, la modulación de la transcripción genética). Están presentes en eucariotas, tanto en levaduras, coanoflagelados, plantas y animales.[18] Reconocen gran variedad de ligandos, como son los neurotransmisores, feromonas, hormonas, odorivectores, y gran variedad de péptidos y proteínas. Su disfunción ocasiona enfermedades, y se emplean como diana en quimioterapia.[19]
En cuanto a su estructura, los siete dominios transmembrana poseen dos características clave:[5]
- Orientación con el extremo amino terminal hacia el exterior y el carboxilo terminal hacia el interior.
- Estructura de siete alfa-hélices transmembrana (H1 a H7), cuatro segmentos extracelulares (E1 a E4) y cuatro segmentos citosólicos (C1 a C4). El segmento carboxiterminal, el tercer bucle citosólico (C3) y, a veces, también el segundo (C4) están implicados en la interacción con la proteína G.
De acuerdo a la homología de secuencia y similitud funcional, se clasifican en seis grandes grupos:[20][21][22][23]
- Clase A (o 1) (receptores semejantes a rodopsina)
- Clase B (o 2) (receptores de la familia secretina)
- Clase C (o 3) (receptor metabotrópico de glutamato)
- Clase D (o 4) (receptores fúngicos involucrados en la determinación sexual)
- Clase E (o 5) (receptores de AMPc)
- Clase F (o 6) (Frizzled/Smoothened, de las vías Wnt y hedgehog, respectivamente)
En cuanto a los efectores de las proteínas G, los de mamíferos pueden clasificarse de acuerdo a los siguientes grupos:[5]
| Clase | Efector asociado | Segundo mensajero | Ejemplos de receptores |
|---|---|---|---|
| Adenilil ciclasa | Aumento de AMPc | β-adrenérgico, glucagón, serotonina, vasopresina | |
| Adenililciclasa, canal de K+ | Disminución AMPc, cambio en el potencial de membrana | α2-adrenérgico, muscarínico de acetilcolina | |
| Adenilil ciclasa | Aumento AMPc | Olfatorios | |
| Fosfolipasa C | Aumento , DAG | α1-adrenérgico, muscarínico (M1, M3, M5) | |
| Fosfolipasa C | Aumento , DAG | Acetilcolina de células endoteliales | |
| cGMP fosfodiesterasa | Disminución cGMP | Rodopsina de las células bastón |
Participación en patologías[editar]
Enfermedades cardiovasculares: ateroesclerosis[editar]
Un estudio publicado en 2021 en la revista Nature Communications demostró la implicación de la regulación de la proteína G en la cascada de señalización para la activación de las plaquetas. Los autores demostraron que las proteínas RGS10 y RGS18 estaban sobre expresadas en muestras de pacientes afectados por ateroesclerosis, lo que influía de forma directa en elementos reguladores de la proteína G. Estos elementos se identificaron posteriormente como GATA1 y NFE2, factores de transcripción cuyo sitio de unión se veía alterado en aquellos pacientes que contenía el alelo responsable para el gen RGS18. En el estudio comprobaron estos resultados con bases de datos actuales y vieron que la presencia de estos alelos estaba asociados a un mayor riesgo de trombosis, embolia, accidentes cerebrovasculares y otros, reafirmando el papel de este gen en el funcionamiento de las plaquetas.
Véase también[editar]
Referencias[editar]
- ↑ Lambright, D.G. and Sondek, J. and Bohm, A. and Skiba, N.P. and Hamm, H.E. and Sigler, P.B. (1996). The 2.0 A crystal structure of a heterotrimeric G protein. Nature Publishing Group.
- ↑ Miriam Ruiz Ballester. Las proteínas G, receptores acoplados y el Nobel de química Journal of Feelsynapsis (JoF). ISSN 2254-3651. 2013.(8): 85-89
- ↑ Kawasawa, Yuka; McKenzie, Louise M.; Hill, David P.; Bono, Hidemasa; Yanagisawa, Masashi (2003-6). «G Protein-Coupled Receptor Genes in the FANTOM2 Database». Genome Research 13 (6b): 1466-1477. ISSN 1088-9051. PMID 12819145. doi:10.1101/gr.1087603. Consultado el 25 de agosto de 2018.
- ↑ a b c Alberts et al (2004). Biología molecular de la célula. Barcelona: Omega. ISBN 978-84-282-1351-6.
- ↑ a b c d e Lodish et al. (2005). Biología celular y molecular. Buenos Aires: Médica Panamericana. ISBN 950-06-1374-3.
- ↑ a b De Vries, L, «The regulator of G protein signaling family», Annual Review of Pharmacology and Toxicology 40 (1): 235--271, archivado desde el original el 15 de septiembre de 2012, consultado el 30 de julio de 2009.
- ↑ Dammann, R. and Li, C. and Yoon, J.H. and Chin, P.L. and Bates, S. and Pfeifer, G.P. (2000). «Epigenetic inactivation of a RAS association domain family protein from the lung tumour suppressor locus 3p21. 3». Nature genetics (Nature Publishing Group) 25 (3): 315--319.
- ↑ Herrington, DA and Hall, RH and Losonsky, G. and Mekalanos, JJ and Taylor, RK and Levine, MM (1988). «Toxin, toxin-coregulated pili, and the toxR regulon are essential for Vibrio cholerae pathogenesis in humans». Journal of Experimental Medicine 168 (4): 1487--1492.
- ↑ Spiegel AM and Weinstein LS (2004) Inherited diseases involving G proteins and G protein-coupled receptors. Annu Rev Med 55: 27-39
- ↑ Takeda S, Kadowaki S, Haga T, Takaesu H, and Mitaku S (2002) Identification of G protein-coupled receptor genes from the human genome sequence. FEBS Lett 520: 97-101
- ↑ Rohrer DK and Kobilka BK (1998) G protein-coupled receptors: functional and mechanistic insights through altered gene expression. Physiol Rev 78: 35-52
- ↑ Yang AH, Ishii I, and Chun J (2002) In vivo roles of lysophospholipid receptors revealed by gene targeting studies in mice Biochim Biophys Acta 1582: 197-203
- ↑ Karasinska JM, George SR, and O'Dowd BF (2003) Family 1 G protein-coupled receptor function in the CNS. Insights from gene knockout mice. Brain Res Brain Res Rev 41: 125-152.
- ↑ a b Takai, Y. and Sasaki, T. and Matozaki, T. (2001). «Small GTP-binding proteins». Physiological reviews (Am Physiological Soc) 81 (1): 153--208.
- ↑ Chien UH, Lai M, Shih TY, Verma IM, Scolnick EM, Roy-Burman P, and Davidson N. Heteroduplex analysis of the sequence relationships between the genomes of Kirsten and Harvey sarcoma viruses, their respective parental murine leukemia viruses, and the rat endogenous 30S RNA. J Virol 31: 752-760, 1979
- ↑ hih TY, Williams DR, Weeks MO, Maryak JM, Vass WC, and Scolnick EM. Comparison of the genomic organization of Kirsten and Harvey sarcoma viruses. J Virol 27: 45-55, 1978
- ↑ McCormick F, and Wittinghofer A. Interactions between Ras proteins and their effectors. Curr Opin Biotechnol 7: 449-456, 1996
- ↑ King N, Hittinger CT, Carroll SB (2003). «Evolution of key cell signaling and adhesion protein families predates animal origins». Science 301 (5631): 361-3. PMID 12869759. doi:10.1126/science.1083853.
- ↑ Filmore, David (2004). «It's a GPCR world». Modern Drug Discovery (American Chemical Society) 2004 (November): 24-28.
- ↑ Attwood TK, Findlay JB (1994). «Fingerprinting G-protein-coupled receptors». Protein Eng 7 (2): 195-203. PMID 8170923. doi:10.1093/protein/7.2.195.
- ↑ Kolakowski LF Jr (1994). «GCRDb: a G-protein-coupled receptor database». Receptors Channels 2 (1): 1-7. PMID 8081729.
- ↑ Foord SM, Bonner TI, Neubig RR, Rosser EM, Pin JP, Davenport AP, Spedding M, Harmar AJ (2005). «International Union of Pharmacology. XLVI. G protein-coupled receptor list». Pharmacol Rev 57 (2): 279-88. PMID 15914470. doi:10.1124/pr.57.2.5.
- ↑ InterPro
Enlaces externos[editar]
 Wikimedia Commons alberga una categoría multimedia sobre Proteína G.
Wikimedia Commons alberga una categoría multimedia sobre Proteína G.- Proteína G










