Umbeliferona
| Umbeliferona | ||
|---|---|---|
 | ||
| Nombre IUPAC | ||
| 7-Hidroxicromen-2-ona | ||
| General | ||
| Fórmula estructural |
| |
| Fórmula molecular | C9H6O3 | |
| Identificadores | ||
| Número CAS | 93-35-6[1] | |
| ChEBI | 27510 | |
| ChEMBL | 51628 | |
| ChemSpider | 4444774 | |
| PubChem | 5281426 | |
| UNII | 60Z60NTL4G | |
| KEGG | C09315 | |
| Propiedades físicas | ||
| Masa molar | 162,031694 g/mol | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
La umbeliferona, también llamada 7-hidroxicumarina, hidrangina, esquimetina, y beta-umbeliferona, es un producto natural generalizado de la familia de la cumarina.
Absorbe fuertemente la radiación ultravioleta en varias longitudes de onda. A pesar de varias indicaciones de que esta sustancia química es fotomutagénica, se utiliza en filtros solares.[2] Se ha reportado que la umbeliferona tiene propiedades antioxidantes.[3]
Es un sólido cristalino de color blanco amarillento que tiene una ligera solubilidad en agua caliente, pero de alta solubilidad en etanol.
Producción natural[editar]
La umbeliferona se encuentra en muchas plantas conocidas de la familia Apiaceae (umbelíferas), tales como la zanahoria, el cilantro y la angélica de jardín, así como en plantas de otras familias, tales como Hieracium pilosella, Asteraceae o la hoja ancha hortensia (Hydrangea macrophylla, Hydrangeaceae, bajo el nombre de hidrangina).
Es uno de los componentes de la asafétida, el látex seco del hinojo gigante (Ferula communis). También se encuentra en Justicia pectoralis (Acanthaceae).[4][5]
Biosíntesis[editar]
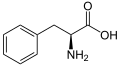
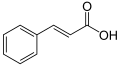
La umbeliferona es un fenilpropanoide y, como tal, se sintetiza a partir de L-fenilalanina, que es un intermedio de la vía del shikimato. La fenilalanina se transforma en ácido cinámico, seguido de una hidroxilación por la enzima cinamato 4-hidroxilasa para producir ácido 4-cumárico. El ácido 4-cumárico es de nuevo hidroxilado por cinamato / cumarato 2-hidroxilasa para producir ácido 2,4-dihidroxi-cinámico (ácido umbelico) seguido de una isomerización del doble enlace adyacente al ácido carboxílico. Por último se da un ataque intramolecular del grupo hidroxilo del C2 al ácido carboxílico y se cierra el anillo, formando la lactona correspondiente, la umbeliferona.
Síntesis química[editar]
La umbeliferona se sintetiza tradicionalmente por medio de la Condensación de Pechmann del resorcinol y el ácido formilacético (generado del ácido malico in situ).
Una síntesis más reciente utiliza propionato de metilo y un catalizador de paladio.
Fluorescencia ultravioleta[editar]
La umbeliferona absorbe intensamente a 300, 305 y 325 nm, con valores de absortividad de 3.9, 3.95 y 4.15, respectivamente, y emite fluorescencia azul bajo luz ultravioleta y luz visible. La potente absorción de tres longitudes de onda diferentes, junto con el hecho de que la energía se disipa de manera segura como luz visible, hace a la umbeliferona un agente de filtro solar útil. En solución alcalina cambia su absorción debido a la desprotonación del grupo hidroxilo del fenol (pKa = 7.7).
Usos[editar]
La actividad ultravioleta de umbeliferona la llevó a su uso como un agente protector solar y un abrillantador óptico para los textiles. También se ha utilizado como un medio activo para los láseres de colorante . Umbeliferona se puede utilizar como un indicador de fluorescencia de iones metálicos tales como cobre y calcio. Actúa como un indicador de pH en el rango de 6.5 a 8.9.
Derivados de umbelliferona[editar]
La umbeliferona es el compuesto de origen de un gran número de productos naturales. La Herniarina (7 - O -metilumbeliferona o 7-metoxicumarina) se produce en las hojas de cáñamo agua ( Eupatorium ayapana ) y Herniaria. También se han reportado derivados naturales glicosilados, tales como la eskimmina (7 - O -β- D -glucopiranosilumbeliferona) y se utilizan para la determinación fluorimétrica de enzimas de glucosidasas. Los derivados de isopreno también están muy extendidos, tales como la marmina (que se encuentra en la piel del pomelo y en la corteza de Aegle marmelos) y furanocumarinas y la marmesina, angelicina, y psoraleno.
Umbelliferone 7-apiosylglucoside puede ser aislado de la raíz de Gmelina arborea.[6]
Referencias[editar]
- ↑ Número CAS
- ↑ cancerweb
- ↑ «UMBELLIFERONE». www.chemicalland21.com. Consultado el 21 de noviembre de 2011.
- ↑ Leal, L. K. A. M.; A. A. G. Ferreira, G. A. Bezerra, F. J. A. Matos, G. S. B. Viana (2000-05). «Antinociceptive, anti-inflammatory and bronchodilator activities of Brazilian medicinal plants containing coumarin: a comparative study». Journal of Ethnopharmacology 70 (2): 151-159. ISSN 0378-8741. PMID 10771205. doi:10.1016/S0378-8741(99)00165-8. Consultado el 26 de junio de 2010.
- ↑ Lino, C. S.; M. L. Taveira, G. S. B. Viana, F. J. A. Matos (1997). «Analgesic and antiinflammatory activities of Justicia pectoralis Jacq and its main constituents: coumarin and umbelliferone». Phytotherapy Research 11 (3): 211-215. doi:10.1002/(SICI)1099-1573(199705)11:3<211::AID-PTR72>3.0.CO;2-W. Archivado desde el original el 5 de enero de 2013. Consultado el 26 de junio de 2010.
- ↑ P. Satyanarayana, P. Subrahmanyam, R. Kasai and O. Tanaka (1985). «An apiose-containing coumarin glycoside from gmelina arborea root». Phytochemistry 24 (8): 1862-1863. doi:10.1016/S0031-9422(00)82575-3.
Enlaces externos[editar]