Síndrome de Klinefelter
| Síndrome de Klinefelter | ||
|---|---|---|
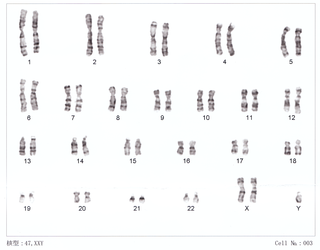 47,XXY | ||
| Especialidad | genética médica | |
El síndrome de Klinefelter (SK) o 47,XXY es la caracterización clínica de una mutación cromosómica que afecta a varones y que incluye, entre otras manifestaciones, hipogonadismo hipergonadotrópico, ginecomastia, dificultades en el aprendizaje e infertilidad. Es la enfermedad genética más común en varones, con una incidencia de 1 en cada 660 nacimientos. Algunos no presentan síntomas y no saben que padecen esta condición hasta la edad adulta al presentarse infertilidad.[1][2]
El sexo está determinado por los cromosomas X e Y. Los machos tienen los cromosomas sexuales XY (46,XY) y las hembras, los cromosomas sexuales XX (46,XX). En el síndrome de Klinefelter, el macho cuenta, como mínimo, con un cromosoma X extra, dando lugar en el 75 % de los casos a un cariotipo (47,XXY). No obstante, aproximadamente un 20 % de los casos son mosaicos cromosómicos, con variantes como (48,XXXY), y (49,XXXXY) en el 5 % de los casos. Este síndrome se da debido a la separación incorrecta de los cromosomas homólogos durante las meiosis que dan lugar a los gametos de uno de los progenitores, aunque también puede darse por errores en las primeras divisiones del cigoto dando lugar a un mosaico genético. Constituye la causa más frecuente de hipogonadismo masculino de carácter permanente.[2][3]
Se cree que el rey Carlos II de España sufrió este síndrome, debido fundamentalmente a los sucesivos matrimonios endogámicos de sus antepasados.[4]
Cuadro clínico[editar]

El cuadro clínico del síndrome de Klinefelter se presenta en diversas manifestaciones y complicaciones, varía en ocasiones de un paciente a otro. La principal característica es la infertilidad, así como escroto hipoplásico y en ocasiones criptorquidia o micropene. Los signos externos pueden no ser evidentes y por lo tanto la enfermedad puede tardar en identificarse.[5]
Prenatal[editar]
Cerca del 40 % de los embarazos con fetos portadores del síndrome de Klinefelter sobreviven llegan a término. Por lo general, la severidad de las malformaciones somáticas en el síndrome de Klinefelter es proporcional al número extra de cromosomas X presentes. Por ejemplo, pacientes con 49 cromosomas (XXXXY) presentan mayor severidad en retraso mental e hipogonadismo que aquellos pacientes con 48 cromosomas (XXXY).[6]
Manifestaciones físicas[editar]
Los bebés con síndrome de Klinefelter suelen gatear y comenzar a andar de forma más torpe y tardía que los demás infantes. En promedio, los bebés varones con KS no comienzan a caminar hasta los 18 meses.[7]
Durante la pubertad presentan escasez de vello en la cara y en todo el cuerpo, consecuencia directa de la baja concentración de testosterona, así como gonadotrofinas elevadas. Tienen vello pubiano disminuido, o siguiendo un claro patrón femenino. Presentan escroto hipoplásico (testículos pequeños y poco funcionales), y en ocasiones criptorquidia o micropene.[8][9]
En la edad adulta presentan una talla elevada y tendencia al sobrepeso; los individuos afectados tienen brazos y piernas largos.Pueden manifestar ginecomastia unilateral o bilateral, la cual se caracteriza por el desarrollo de pechos en el hombre (tejido mamario agrandado). Esto da a lugar una mayor propensión a padecer cáncer de pecho, alteraciones venarias y osteoporosis. La mayoría de los pacientes son infértiles o con esterilidad por azoospermia y no pueden concebir un hijo sin ayuda de un especialista en fertilidad.[7][8]
Características psicológicas[editar]
Desarrollo cognitivo[editar]
Aunque algunas fuentes describen que los pacientes con SK pueden tener un coeficiente intelectual normal,[7] la mayoría informa que el coeficiente intelectual de dichos pacientes es menor al promedio.[8][10] Las personas XXY por lo general aprenden a hablar más tarde que otros en la infancia, lo que demuestra un coeficiente intelectual verbal menor que el de desempeño. Algunos pacientes suelen tener algún grado de dificultad con el lenguaje de por vida. Se ha notificado también que les cuesta más tiempo procesar la información que escuchan, especialmente si se encuentran en ambientes ruidosos. Es particularmente difícil para estos pacientes interpretar los sentimientos de otras personas solamente al escuchar lo que les dicen.[10]
Presentan dificultades para leer y escribir. Esto se demuestra también con una poca comprensión lectora. Al llegar a la adultez, la mayoría aprende a conversar como la población promedio. Sin embargo, presentan mayor dificultad al realizar trabajos que impliquen mucha lectura y escritura.[7]
Conducta y personalidad[editar]
Un estudio realizado en 1995 que evaluó las adaptaciones psicosociales en 39 adolescentes con anormalidades cromosómicas demostró que estos sujetos tienden a ser tímidos, reservados, con dificultades para integrarse a un grupo de pares. En una autoevaluación, ellos se describen como sensibles, aprensivos e inseguros. Estos pacientes también presentan trastornos emocionales como ansiedad, depresión, y tendencia al abuso de sustancias.[8][11]
En la edad adulta presentan una disminución de la libido sexual así como baja autoestima, debida en la mayoría de los casos a los caracteres femeninos perceptibles por el varón (ginecomastia).[8]
Enfermedades concomitantes[editar]
Las personas con síndrome de Klinefelter tienen un mayor riesgo de osteoporosis, ginecomastia, la aparición de trombosis y cáncer de mama en comparación con la población general. Sin embargo, el riesgo de cáncer de seno está por debajo del riesgo normal para las mujeres. Esos pacientes son más propensos a enfermedades cardiovasculares dada la prevalencia en anormalidades metabólicas incluyendo dislipidemia y diabetes mellitus tipo 2. Se ha demostrado que la hipertensión no está relacionada con el SK.[1][12]
Etiología[editar]

El síndrome de Klinefelter no es una condición hereditaria. El exceso de cromosoma X proviene de la madre en aproximadamente la mitad de los casos y del padre en la otra mitad. La edad materna es el único factor de riesgo para el síndrome de Klinefelter: A partir de una edad materna de 40 años, el riesgo de tener un hijo con síndrome de Klinefelter es cuatro veces mayor que en las mujeres menores de 24 años.[10][13][14][15]
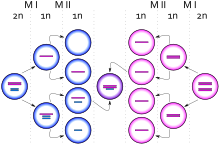
La anomalía cromosómica puede originarse también por un error durante las divisiones mitóticas del cigoto, produciendo así los casos de mosaicismo. El cromosoma X adicional en los pacientes con síndrome de Klinefelter a menudo es adquirido por la no disyunción durante la meiosis I maternal o paternal, o la meiosis maternal II (gametogénesis). El error en el proceso de separación de cromosomas durante la división celular se da cuando cromosomas homólogos; en este caso, los cromosomas sexuales X e Y, fallan al separarse, originando gametos (masculinos o femeninos) con 24 cromosomas, debido a dicho cromosoma adicional. Ya sea un espermatozoide con un cromosoma X e Y, o un óvulo con un dos cromosomas X. Fertilizar un óvulo X normal con un espermatozoide XY dará un descendiente XXY (Klinefelter).[8][13][14]
Otro mecanismo para retener un cromosoma extra es mediante la no disyunción en la meiosis II en el óvulo. La no disyunción ocurre cuando dos cromátidas hermanas en el cromosoma de sexo (en este caso X y X) no llegan a separarse. Esto produce un óvulo XX que posteriormente será fertilizado por un espermatozoide normal, dando un descendiente XXY (Klinefelter).[13][14]
En mamíferos con más de un cromosoma X (en el caso de humanos, mujeres), se da la inactivación de uno de los dos cromosomas, de modo que se equipare la carga génica con el hombre. A esto se le conoce como lionización. Esto también ocurre en los varones XXY, aunque hay cierta evidencia que sugiere que algunos genes localizados en las regiones pseudoautosomales de sus cromosomas X presentan correspondencia con su cromosoma Y, siendo capaces de expresarse.[16]
Variaciones[editar]
Existen variaciones del síndrome de Klinefelter, conocidas como poli-X, es decir, que tienes más de un cromosoma X extra. En estos casos la sintomatología puede ser más pronunciada que en los pacientes con síndrome de Klinefelter típico (47,XXY). Por lo general, se presentan convulsiones en la infancia, estrabismo, problemas intestinales como estreñimiento, e infecciones en los oídos.[7][17][18]
48,XXYY[editar]
Los varones con este cariotipo llegan a ser muy altos, con piernas muy largas; lo que puede resultar en úlceras y várices en las mismas. Tienen poco vello corporal, testículos y pene pequeño, hipogonadismo hipergonadotrópico y ginecomastia. Son propensos a enfermedades vasculares.
Su coeficiente intelectual se encuentra en el rango de los 60 a 80 puntos, por lo que presentan un retraso en el habla, y déficits en el ámbito académico, conductual, y social. Un estudio publicado en 2005 comparando las habilidades verbales de sujetos 47,XXY y 48,XXYY, demostró que los varones 48,XXYY tienen un coeficiente verbal significativamente más bajo.[19]
En el ámbito conductual, son extremadamente tímidos, aunque pueden llegar a ser agresivos e impulsivos. Tienen la tendencia a tener mayores problemas de hiperactividad, agresión y depresión en comparación con los varones 46,XY o incluso 47,XXY.[20]
48,XXXY[editar]
Quienes tienen este cariotipo presentan hipertelorismo ocular, un puente nasal plano, y son de baja estatura. Los huesos de sus brazos pueden estar conectados de manera inusual, a lo que se le conoce como sinostosis radioulnar, o presentar clinodactilia, es decir que el dedo meñique se encuentra curvado hacia adentro.[17]
Su coeficiente intelectual estará entre los 40 y 60 puntos, lo que se hará evidente al tener un severo retraso en el habla. Consistente con ello, son sujetos inmaduros, considerados incluso pasivos, cooperativos y no agresivos.[18]
49,XXXXY[editar]
Estos individuos presentan el fenotipo más severo. Además de los síntomas visibles en los otros cariotipos, una de las principales manifestaciones en este caso es microcefalia, muy baja estatura, hipertelorismo ocular, puente nasal plano, y arco plantar alto. Las cámaras cardiacas no se forman adecuadamente, lo que trae como consecuencia, defectos cardiacos.[17][21]
El coeficiente intelectual de estas personas será ente 20 y 60. Conductualmente son sujetos tímidos y amigables. Ocasionalmente pueden ser irritables, con cambios drásticos en el temperamento, poca tolerancia a la frustración y dificultades para cambiar de rutina.[20]
Patogenia[editar]
Los estudios en sujetos prepuberales 47,XXY no muestran deficiencias en las concentraciones de la hormona luteinizante, foliculoestimulante o testosterona, comparados con sujetos prepúberes 46,X. Sin embargo, la respuesta a la gonadoliberina (LHRH, hormona hipotalámica liberadora de gonadotropinas) es normal en ambos grupos. Se ha notado que entre los 12 y 14 años de edad en los sujetos 47,XXY las concentraciones de gonadotropinas se incrementan y la testosterona permanece en límites inferiores para la edad.[22]

En biopsias realizadas a niños con el síndrome de Klinefelter, se ha observado una disminución en el número de células germinales. No obstante, después de la pubertad se aprecia hialinización y fibrosis de los túbulos seminíferos. Estos cambios histológicos son muy característicos del síndrome, y los cuales originan disminución en el volumen testicular así como aumento de su consistencia. También se observa ausencia de células germinales, hiperplasia y agregación de las células de Leydig, como respuesta a la hiperestimulación por la hormona hormona luteinizante.[23]
Por otro lado, la pérdida de túbulos seminíferos y células de Sertoli produce una disminución en las cifras de inhibina B, el factor regulador de FSH, y de la hormona antimülleriana (AMH). Esto ocasiona una disminución en la retroalimentación negativa sobre la FSH, generando un aumento en la misma. La ausencia de espermatogénesis es secundaria a la presencia de cromosomas supernumerarios, que se mantienen activos durante la gametogénesis.[22][24]
Diagnóstico[editar]
El método estándar de diagnóstico es mediante un análisis cromosómico al detectar un cromosoma X adicional. Una pequeña muestra de sangre es suficiente como material de prueba. A inicios de los 2000 se realizaba también un diagnóstico mediante el análisis de los corpúsculos de Barr, dando resultados con una sensibilidad del 82 %. Por otra parte, para determinar si tiene forma de mosaico, también se puede realizar un análisis cromosómico en las células de la mucosa oral.[25]
Durante la pubertad y la edad adulta, los niveles bajos de testosterona con niveles elevados de las hormonas pituitarias FSH y LH en la sangre pueden indicar la presencia del síndrome de Klinefelter. Un espermiograma también puede ser parte de la investigación adicional. A menudo hay una azoospermia, rara vez una oligospermia.[2][26]
Otra forma de diagnosticar a pacientes con el síndrome de Klinefelter de forma prenatal es por amniocentesis o por la muestra del villus coriónico. Se ha demostrado que cerca del 10 % de los casos se pueden determinar en un diagnóstico prenatal.[8][27]
Tratamiento[editar]
La terapia causal no es posible porque el síndrome de Klinefelter es causado por una alteración cromosómica.
Desde el inicio de la pubertad, la deficiencia de testosterona existente puede ser compensada por la terapia de sustitución hormonal adecuada. Preparaciones de testosterona están disponibles en forma de jeringas, parches o gel.[3][23][28]
Los pacientes con síndrome de Klinefelter a menudo tienen una deficiencia de vitamina D. Por lo tanto, los niveles de vitamina D en adolescentes y adultos deben controlarse regularmente. Una sustitución de vitamina D conduce a una mejor densidad ósea.[29][30][31]
Si existe ginecomastia, existe la posibilidad de una mastectomía (extirpación quirúrgica del tejido mamario). Si niños con síndrome de Klinefelter tienen dislexia, dificultad para concentrarse o conducción débil, existe la posibilidad de medidas de apoyo como la terapia del hablar o la terapia ocupacional.[32][33]
Terapia conductual[editar]
La terapia de lenguaje es particularmente esencial en el desarrollo infantil de los pacientes con síndrome de Klinefelter. Esto les ayudará a desarrollar habilidades que les permitan entender y producir lenguaje complejo. De igual forma se recomienda hacer una evaluación profunda de las habilidades académicas y psicosociales para determinar sus fortalezas y debilidades en el aprendizaje.[23][28]
Para los niños que padecen hipotonia o retraso en el desarrollo de sus habilidades motoras, es necesaria terapia física que les ayude a mejorar su tono muscular, balance y coordinación.[8]
La terapia ocupacional es altamente recomendada para aquellos sujetos que presentan dispraxia. Esto también es beneficioso para el resto de los pacientes, ya que puede mejorar sus habilidades de comunicación verbal y no verbal, así como a socializar más.[28]
Oportunidades de tratamiento para la infertilidad[editar]

Métodos modernos de medicina reproductiva, tales como la inyección intracitoplasmática de espermatozoides (ICSI) con extracción previa de espermatozoides testiculares (TESE), han dado lugar a descendencia de varones con síndrome de Klinefelter. Para 2010, se habían reportado más de 100 embarazos exitosos en los que se utilizó fertilización in vitro obteniendo espermatozoides de pacientes 47,XXY. Otro estudio reportado en 2013 que los niños biológicos de los hombres con síndrome de Klinefelter (esperma obtenido por TESE) no tienen un cromosoma X adicional y por lo tanto, no tienen síndrome de Klinefelter.[34][35][36]
En el caso en que no se puedan obtener espermatozoides funcionales a partir del semen o TESE, no hay posibilidad de producir hijos biológicos; esto debido a que el tratamiento de testosterona suprimiría la espermatogénesis. La posibilidad de TESE con el paciente y sus padres debe ser discutido en consulta con los médicos asistentes antes del inicio de la terapia de testosterona. Si la terapia de testosterona ya se ha iniciado, pero el paciente se desea todavía una TESE, la terapia de testosterona debe pausarse durante al menos 6 meses para que la espermatogénesis puede recuperarse.[37][38]
Asesoramiento genético[editar]
Ya que el síndrome de Klinefelter no es hereditaria, sino consecuencia de un proceso de no disyunción cromosomal, el riesgo de recurrencia no es mayor al de la población en general. No existe evidencia que indique de dicho proceso se repita en una familia en particular. Sin embargo, tan pronto como se sospeche o se detecte un paciente 47,XXY es aconsejable buscar asesoramiento especializado con el fin de planificar el mejor proceso de maduración y el mayor nivel de bienestar a largo plazo.[28][39][40]
Historia[editar]
Fue descrito en 1942 por Harry Klinefelter, Edward C. Reifentein y Fuller Albright quienes en el Hospital General de Massachusets estudiaron a nueve pacientes con alta estatura, ginecomastia, deficiencia en los niveles de testosterona, testículos pequeños, azoospermia y elevada concentración de gonadotropinas. En sus inicios se sugirió que las manifestaciones clínicas eran resultado de un defecto primario estaba en las células de Sertoli. Se propuso entonces que en estos pacientes había una deficiencia en una hormona testicular que regulaba la concentración de gonadotropinas hipofisiarias, a la que llamaron hormona X o inhibina.[41]
No fue sino hasta 1956 que se demostró la presencia del corpúsculo de Barr en pacientes con síndrome de Klinefelter. Tres años más tarde, en 1959, investigadores del Western General Hospital en Edimburgo, Escocia identificaron que el cariotipo de un sujeto con la enfermedad era 47,XXY. De esta manera se estableció que la presencia de un cromosoma X extra era el factor etiológico fundamental para desarrollar las características de dicho síndrome.[42][43]
En septiembre de 2020, la European Academy of Andrology (Academia Europea de Andrología) publicó por primera vez directrices para el síndrome de Klinefelter.[44]
En 2021, una investigación de un individuo enterrado con una espada suontaka, reveló que quien por muchos años se pensó que era una mujer, se trataba más bien de un hombre con síndrome de Klinefelter. Al año siguiente, en 2022, se reportó la identificación de un esqueleto en el este de Portugal, el cual era en realidad un hombre fallecido cerca de 1000 a. c. con un cariotipo 47,XXY.[45][46]
Véase también[editar]
Referencias[editar]
- ↑ a b Salzano, Andrea; Arcopinto, Michele; Marra, Alberto M; Bobbio, Emanuele; Esposito, Daniela; Accardo, Giacomo; Giallauria, Francesco; Bossone, Eduardo et al. (julio de 2016). «Klinefelter syndrome, cardiovascular system, and thromboembolic disease: review of literature and clinical perspectives». European Journal of Endocrinology 175 (1): R27-R40. ISSN 0804-4643. doi:10.1530/eje-15-1025. Consultado el 28 de octubre de 2023.
- ↑ a b c Groth, Kristian A.; Skakkebæk, Anne; Høst, Christian; Gravholt, Claus Højbjerg; Bojesen, Anders (enero de 2013). «Klinefelter Syndrome—A Clinical Update». The Journal of Clinical Endocrinology & Metabolism (en inglés) 98 (1): 20-30. ISSN 0021-972X. doi:10.1210/jc.2012-2382. Consultado el 28 de octubre de 2023.
- ↑ a b Artigas López, Mercé. «8». Síndrome de Klinefelter. España: Asociación Española de Pediatría. pp. 49-51. Consultado el 28 de octubre de 2023.
- ↑ Cerda L, Jaime (2008-02). «Charles II of Spain, «the bewitched»». Revista médica de Chile 136 (2): 267-270. ISSN 0034-9887. doi:10.4067/S0034-98872008000200019. Consultado el 28 de octubre de 2023.
- ↑ Oficina de Comunicaciones (21 de julio de 2015). «Síndrome de Klinefelter (KS por sus siglas en inglés): Generalidades». Eunice Kennedy Shriver National Institute of Child Health and Human Development. p. Temas de Salud. Consultado el 28 de octubre de 2023.
- ↑ Germaine L Defendi (31 de enero de 2022). «Klinefelter Syndrome». En Luis O Rohena, ed. Medscape (en inglés). p. Pediatrics: Genetics and Metabolic Disease. Consultado el 28 de octubre de 2023.
- ↑ a b c d e Oficina de Comunicaciones (21 de julio de 2015). «¿Cuáles son los síntomas comunes del síndrome de Klinefelter (KS por sus siglas en inglés)?». Eunice Kennedy Shriver National Institute of Child Health and Human Development. pp. Síndrome de Klinefelter (KS por sus siglas en inglés): Información sobre la enfermedad. Consultado el 28 de octubre de 2023.
- ↑ a b c d e f g h Visootsak, Jeannie; Graham, John M (2006-12). «Klinefelter syndrome and other sex chromosomal aneuploidies». Orphanet Journal of Rare Diseases (en inglés) 1 (1). ISSN 1750-1172. PMC 1634840. PMID 17062147. doi:10.1186/1750-1172-1-42. Consultado el 28 de octubre de 2023.
- ↑ Smyth, Cynthia M.; Bremner, William J. (22 de junio de 1998). «Klinefelter Syndrome». Archives of Internal Medicine (en inglés) 158 (12): 1309. ISSN 0003-9926. doi:10.1001/archinte.158.12.1309. Consultado el 28 de octubre de 2023.
- ↑ a b c Kanakis, George A.; Nieschlag, Eberhard (4 de febrero de 2018). «Klinefelter syndrome: more than hypogonadism». Metabolism (en inglés) 86: 135-144. doi:10.1016/j.metabol.2017.09.017. Consultado el 12 de marzo de 2020.
- ↑ Bg, Bender; Rj, Harmon; Mg, Linden; A, Robinson (Agosto de 1995). «Psychosocial adaptation of 39 adolescents with sex chromosome abnormalities». Pediatrics (en inglés) 96 (2 Pt 1). ISSN 0031-4005. PMID 7630689. Consultado el 21 de noviembre de 2023.
- ↑ Nieschlag, Eberhard (17 de mayo de 2013). «Klinefelter Syndrome: The Commonest Form of Hypogonadism, but Often Overlooked or Untreated». Deutsches Aerzteblatt Online. ISSN 1866-0452. PMC 3674537. PMID 23825486. doi:10.3238/arztebl.2013.0347. Consultado el 12 de marzo de 2020.
- ↑ a b c Tuttelmann, F.; Gromoll, J. (1 de junio de 2010). «Novel genetic aspects of Klinefelter's syndrome». Molecular Human Reproduction (en inglés) 16 (6): 386-395. ISSN 1360-9947. doi:10.1093/molehr/gaq019. Consultado el 12 de marzo de 2020.
- ↑ a b c «Klinefelter syndrome». MedlinePlus (en inglés). pp. Genetics: Genetic Conditions. Consultado el 21 de noviembre de 2023.
- ↑ «Síndrome de Klinefelter». Mayo Clinic. 3 de marzo de 2020. Enfermedades y afecciones. Consultado el 26 de noviembre de 2023.
- ↑ Blaschke, Rüdiger Jörg; Rappold, Gudrun (1 de junio de 2006). «The pseudoautosomal regions, SHOX and disease». Current Opinion in Genetics & Development. Genetics of disease 16 (3): 233-239. ISSN 0959-437X. doi:10.1016/j.gde.2006.04.004. Consultado el 21 de noviembre de 2023.
- ↑ a b c Linden, M. G.; Bender, B. G.; Robinson, A. (1995-10). «Sex chromosome tetrasomy and pentasomy». Pediatrics 96 (4 Pt 1): 672-682. ISSN 0031-4005. PMID 7567329. Consultado el 26 de noviembre de 2023.
- ↑ a b Visootsak, Jeannie; Aylstock, Melissa; Graham, John M. (2001-12). «Kilnefelter Syndrome and Its Variants: An Update and Review for the Primary Pediatrician». Clinical Pediatrics (en inglés) 40 (12): 639-651. ISSN 0009-9228. doi:10.1177/000992280104001201. Consultado el 26 de noviembre de 2023.
- ↑ Visootsak, J. J.; Rosner, B.; Dykens, E.; Tartaglia, N.; Graham, J. M. (1 de enero de 2006). «Adaptative and maladaptive behavior of males with sex chromosome aneuploidy». Journal of Investigative Medicine (en inglés) 54 (1): S280.2-S280. ISSN 1081-5589. doi:10.2310/6650.2005.X0008.135. Consultado el 26 de noviembre de 2023.
- ↑ a b Tartaglia, N.; Reynolds, A.; Visootsak, J.; Gronli, S.; Hansen, R.; Hagerman, R. (2005-12). «Behavioral Phenotypes of Males with Sex Chromosome Aneuploidy». Journal of Developmental & Behavioral Pediatrics (en inglés estadounidense) 26 (6): 464. ISSN 0196-206X. Consultado el 26 de noviembre de 2023.
- ↑ Kassai, R.; Hamada, I.; Furuta, H.; Cho, K.; Abe, K.; Deng, H. X.; Niikawa, N. (1 de julio de 1991). «Penta X syndrome: a case report with review of the literature». American Journal of Medical Genetics 40 (1): 51-56. ISSN 0148-7299. PMID 1887850. doi:10.1002/ajmg.1320400110. Consultado el 26 de noviembre de 2023.
- ↑ a b Vales García, Manuel; Llerena Martínez, Vilma; Gil Díaz, Felipe (septiembre-octubre de 1984). «Hallazgos clínicos y de laboratorio en el síndrome de Klinefelter». Rev Cub Med: 1-10. Consultado el 25 de noviembre de 2024.
- ↑ a b c Riola, Arturo R. «Síndrome de Klinefelter XXY». Archivado desde el original el 17 de junio de 2012. Consultado el 25 de noviembre de 2023.
- ↑ Pacenza, N.; Pasqualini, T.; Gottlieb, S.; Knoblovits, P.; Costanzo, P.; Stewart Usher, J.; Rey, R.; Martínez, M. et al. (2010). «Síndrome de Klinefelter en las distintas edades: experiencia multicéntrica». Rev. argent. endocrinol. metab: 29-39. Consultado el 25 de noviembre de 2023.
- ↑ Kamischke, Axel; Baumgardt, Arthur; Horst, Jürgen; Nieschlag, Eberhard (2003). «Clinical and diagnostic features of patients with suspected Klinefelter syndrome». Journal of Andrology 24 (1): 41-48. ISSN 0196-3635. PMID 12514081. Consultado el 25 de noviembre de 2023.
- ↑ Nieschlag, Eberhard (17 de mayo de 2013). «Klinefelter Syndrome». Deutsches Ärzteblatt International 110 (20): 347-353. ISSN 1866-0452. PMC 3674537. PMID 23825486. doi:10.3238/arztebl.2013.0347. Consultado el 25 de noviembre de 2023.
- ↑ Abramsky, L.; Chapple, J. (1997-04). «47,XXY (Klinefelter Syndrome) and 47,XYY: Estimated rates of and indication for postnatal diagnosis with implications for prenatal counseling». Prenatal Diagnosis (en inglés) 17 (4): 363-368. doi:10.1002/(SICI)1097-0223(199704)17:4<363::AID-PD79>3.0.CO;2-O. Consultado el 25 de noviembre de 2023.
- ↑ a b c d Defendi, Gernaine L (31 de enero de 2022). «Klinefelter Syndrome Treatment & Management» [Síndrome de Klinefelter: Tratmiento y manejo]. En Luis O Rohena, ed. Medscape (en inglés). Drugs & Diseases: Pedriatrics: Genetics and Metabolic Disease. Consultado el 25 de noviembre de 2023.
- ↑ Ferlin, A.; Selice, R.; Di Mambro, A.; Ghezzi, M.; Di Nisio, A.; Caretta, N.; Foresta, C. (2015-08). «Role of vitamin D levels and vitamin D supplementation on bone mineral density in Klinefelter syndrome». Osteoporosis international: a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA 26 (8): 2193-2202. ISSN 1433-2965. PMID 25963234. doi:10.1007/s00198-015-3136-8. Consultado el 4 de marzo de 2020.
- ↑ Bojesen, A.; Birkebæk, N.; Kristensen, K.; Heickendorff, L.; Mosekilde, L.; Christiansen, J. S.; Gravholt, C. H. (2011-05). «Bone mineral density in Klinefelter syndrome is reduced and primarily determined by muscle strength and resorptive markers, but not directly by testosterone». Osteoporosis International (en inglés) 22 (5): 1441-1450. ISSN 0937-941X. doi:10.1007/s00198-010-1354-7. Consultado el 4 de marzo de 2020.
- ↑ Ferlin, A.; Selice, R.; Di Mambro, A.; Ghezzi, M.; Di Nisio, A.; Caretta, N.; Foresta, C. (2015-08). «Role of vitamin D levels and vitamin D supplementation on bone mineral density in Klinefelter syndrome». Osteoporosis International (en inglés) 26 (8): 2193-2202. ISSN 0937-941X. doi:10.1007/s00198-015-3136-8. Consultado el 4 de marzo de 2020.
- ↑ Gabriele, R.; Borghese, M.; Conte, M.; Egidi, F. (2002). «[Clinical-therapeutic features of gynecomastia]». Il Giornale Di Chirurgia 23 (6-7): 250-252. ISSN 0391-9005. PMID 12422780. Consultado el 26 de noviembre de 2023.
- ↑ «¿Qué es el síndrome?». SindromedeKlinefelter.es. España. Inicio: El Síndrome. Archivado desde el original el 3 de septiembre de 2011. Consultado el 25 de noviembre de 2023.
- ↑ Corona, Giovanni; Pizzocaro, Alessandro; Lanfranco, Fabio; Garolla, Andrea; Pelliccione, Fiore; Vignozzi, Linda; Ferlin, Alberto; Foresta, Carlo et al. (1 de mayo de 2017). «Sperm recovery and ICSI outcomes in Klinefelter syndrome: a systematic review and meta-analysis». Human Reproduction Update (en inglés) 23 (3): 265-275. ISSN 1355-4786. doi:10.1093/humupd/dmx008. Consultado el 4 de marzo de 2020.
- ↑ Fullerton, G.; Hamilton, M.; Maheshwari, A. (1 de marzo de 2010). «Should non-mosaic Klinefelter syndrome men be labelled as infertile in 2009?». Human Reproduction (en inglés) 25 (3): 588-597. ISSN 0268-1161. doi:10.1093/humrep/dep431. Consultado el 26 de noviembre de 2023.
- ↑ Greco, E.; Scarselli, F.; Minasi, M.G.; Casciani, V.; Zavaglia, D.; Dente, D.; Tesarik, J.; Franco, G. (2013-05). «Birth of 16 healthy children after ICSI in cases of nonmosaic Klinefelter syndrome». Human Reproduction (en inglés) 28 (5): 1155-1160. ISSN 1460-2350. doi:10.1093/humrep/det046. Consultado el 4 de marzo de 2020.
- ↑ Mehta, Akanksha; Bolyakov, Alexander; Roosma, Jordan; Schlegel, Peter N.; Paduch, Darius A. (2013-10). «Successful testicular sperm retrieval in adolescents with Klinefelter syndrome treated with at least 1 year of topical testosterone and aromatase inhibitor». Fertility and Sterility (en inglés) 100 (4): 970-974. doi:10.1016/j.fertnstert.2013.06.010. Consultado el 4 de marzo de 2020.
- ↑ Oates, Robert D. (1 de octubre de 2013). «Sperm retrieval in adolescents with Klinefelter syndrome». Fertility and Sterility 100 (4): 943-944. ISSN 0015-0282. doi:10.1016/j.fertnstert.2013.07.003. Consultado el 26 de noviembre de 2023.
- ↑ «Asesoramiento Genitico para Klinefelter Síndrome». FDNA Health. Consultado el 26 de noviembre de 2023.
- ↑ Linden, Mary G.; Bender, Bruce G.; Robinson, Arthur (1 de junio de 2002). «Genetic counseling for sex chromosome abnormalities». American Journal of Medical Genetics 110 (1): 3-10. ISSN 0148-7299. PMID 12116264. doi:10.1002/ajmg.10391. Consultado el 26 de noviembre de 2023.
- ↑ Klinefelter, Harry F.; Reifenstein, Edward C.; Albright, Fuller (1942-11). «Syndrome Characterized by Gynecomastia, Aspermatogenesis without A-Leydigism, and Increased Excretion of Follicle-Stimulating Hormone1». The Journal of Clinical Endocrinology & Metabolism (en inglés) 2 (11): 615-627. ISSN 0021-972X. doi:10.1210/jcem-2-11-615. Consultado el 26 de noviembre de 2023.
- ↑ Odom, Samuel L.; Horner, Robert H.; Snell, Martha E. (21 de enero de 2009). Handbook of Developmental Disabilities (en inglés). Guilford Press. ISBN 978-1-60623-248-4. Consultado el 26 de noviembre de 2023.
- ↑ Jacobs, Patricia A.; Strong, J. A. (1959-01). «A Case of Human Intersexuality Having a Possible XXY Sex-Determining Mechanism». Nature (en inglés) 183 (4657): 302-303. ISSN 0028-0836. doi:10.1038/183302a0. Consultado el 26 de noviembre de 2023.
- ↑ Zitzmann, Michael; Aksglaede, Lise; Corona, Giovanni; Isidori, Andrea M.; Juul, Anders; T'Sjoen, Guy; Kliesch, Sabine; D'Hauwers, Kathleen et al. (6 de octubre de 2020). «European academy of andrology guidelines on Klinefelter Syndrome: Endorsing Organization: European Society of Endocrinology». Andrology (en inglés): andr.12909. ISSN 2047-2919. doi:10.1111/andr.12909. Consultado el 24 de octubre de 2020.
- ↑ Moilanen, Ulla; Kirkinen, Tuija; Saari, Nelli-Johanna; Rohrlach, Adam B.; Krause, Johannes; Onkamo, Päivi; Salmela, Elina (2022-02). «A Woman with a Sword? – Weapon Grave at Suontaka Vesitorninmäki, Finland». European Journal of Archaeology (en inglés) 25 (1): 42-60. ISSN 1461-9571. doi:10.1017/eaa.2021.30. Consultado el 26 de noviembre de 2023.
- ↑ Roca-Rada, Xavier; Tereso, Sofia; Rohrlach, Adam B; Brito, André; Williams, Matthew P; Umbelino, Cláudia; Curate, Francisco; Deveson, Ira W et al. (27 de agosto de 2022). «A 1000-year-old case of Klinefelter's syndrome diagnosed by integrating morphology, osteology, and genetics». The Lancet 400 (10353): 691-692. ISSN 0140-6736. doi:10.1016/S0140-6736(22)01476-3. Consultado el 26 de noviembre de 2023.
