Fibra muscular

La fibra muscular o miocito esquelético[1] es una célula multinucleada o sincitio, cilíndrica y con capacidad contráctil y de la cual está compuesto el músculo esquelético. La principal propiedad de esta célula es la contractilidad, es decir: la capacidad de acortar su propia longitud desarrollando un trabajo al hacerlo.[2]
Embriología[editar]

El miocito se desarrolla a partir de la hoja germinativa llamada mesodermo. Las células precursoras son denominadas mioblastos y poseen un solo núcleo. Estos mioblastos individuales se fusionan y forman fibras alargadas multinucleadas.[3]

Cuando los mioblastos se fusionan, forman sincitios multinucleados, denominados miotubos. Estos miotubos presentan numerosos núcleos centrales, que luego se separan y se mueven hacia la periferia cuando maduran.[4]
En el humano dentro del citoplasma aparecen las miofibrillas y al tercer mes son visibles las estriaciones.
Estructura[editar]
El miocito esquelético (llamado también fibra muscular) es la unidad estructural del músculo estriado, muestra un diámetro de 40-100 micrómetros (μm) y su longitud por unidad llega a varios centímetros.[5]
Esta célula contiene orgánulos y varios núcleos celulares. Posee un citoplasma llamado sarcoplasma complejo, con un entramado de fibras de actina y miosina, cuya principal propiedad es la contractilidad.
Microarquitectura[editar]

Con microscopía óptica en el miocito se hace visible, su característica principal: la presencia de una sucesión de estrías claras y oscuras, en el sector central de su sarcoplasma. Las estrías se presentan de forma perpendicular al eje mayor del miocito. Están formadas por la alternancia de zonas claras y oscuras dentro de cada miofibrilla.[6]

La fibra muscular, está rodeada por una membrana celular que se denomina sarcolema. Esta membrana plasmática de los miocitos esqueléticos, presenta numerosas invaginaciones para formar los llamados túbulos T.[7]
El retículo endoplásmico del miocito recibe el nombre de retículo
sarcoplasmático.
Las mitocondrias son muy abundantes y se disponen en los espacios entre las miofibrillas.

Los núcleos celulares son múltiples, se disponen en la periferia de la célula esquelética, inmediatamente debajo del sarcolema. Son aplanados y ovalados de 10 μm de longitud y 4 μm de ancho.
Ultraestructura[editar]



Con el microscopio electrónico, la fibra muscular esquelética se caracteriza por: tener una organización intracelular muy compleja y por mostrar una disposición específica de los orgánulos con relación a la anatomía del sarcómero.[8]
En el miocito de mamífero los túbulos y cisternas del retículo forman una estructura llamada tríada.
Una tríada se compone de: un túbulo T centrado entre dos cisternas terminales del retículo sarcoplasmático (RS).
Las tríadas se ubican en la inmediata cercanía de la línea Z, en la unión de dos sarcómeros adyacentes de una miofibrilla. Estas estructuras tubulares están acompañadas por mitocondrias.[5]

Las mitocondrias se disponen en los espacios entre las miofibrillas, esto determina que estén estrechamente empacadas y en contacto entre ellas. Se encuentran en inmediata cercanía de las miofibrillas para facilitar la difusión de moléculas y son muy abundantes en esta célula, para aportar la energía que necesita la contracción.

Los núcleos celulares múltiples son alargados y estrechos con indentaciones. Tienen forma ovalada, una longitud media de 8-10 μm y su número puede superar los varios centenares a lo largo de una célula fibra muscular.
La cromatina es clara en el centro, con pocos centros de condensación periféricos sobre la membrana nuclear.[7][9]
El citoplasma del miocito llamado sarcoplasma, es complejo y característico, por mostrar una gran especialización celular.[6]

El citoesqueleto, está principalmente formado por actina filamentosa, que se asocia con una proteína contráctil: la miosina II. Ambas proteínas estructuran los sectores llamados sarcómeros y estos se unen de manera repetitiva para formar los haces intracelulares denominados miofibrillas.

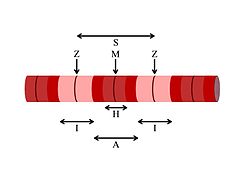
La miofibrilla observada al microscopio, exhibe bandas oscuras (la banda "A") y bandas claras (la banda "I"). A la banda clara I la interseca una línea llamada línea "Z". A su vez, a la banda oscura A la interseca la línea "M". Entre la banda oscura A y la línea M que la interseca hay un espacio claro llamado zona "H". Todas estas bandas y líneas no son más que la organización de la maquinaria contráctil de la fibra muscular llamada sarcómero, la cual se extiende desde una línea Z hasta la siguiente.
La banda I del sarcómero no es más que un grupo de fibras de actina una al lado de la otra. La banda A contiene las fibras de miosina, las cuales son ciertamente más gruesas que las de actina. Ambas fibras se superimponen en el espacio de la banda A.

Las distrofias musculares, que son las miopatías más frecuentes, provocan una degeneración progresiva del miocito (fibras musculares).
Recambio celular del miocito esquelético[editar]
En circunstancias normales, el músculo esquelético adulto de mamífero, es un tejido estable con muy poca recambio de núcleos. Se calcula que no se reemplaza más del 1–2% en un músculo normal cada semana.[10]
La diferenciación del miocito está definida por su salida del ciclo de la mitosis, quedando en la fase G0 de manera permanente.[11]
Las células del músculo esquelético están diferenciadas terminalmente, debido a su especialización en la función contráctil. Los miocitos y las "células periféricas" o "satélites" están en estrecho contacto anatómico y ambas constituyen una unidad en la integridad mecánica, estructural y funcional.[12]
Células satélites[editar]

Las "células satélite" son una población heterogénea, formada por células madre y células progenitoras residentes, localizadas entre la lámina externa y el sarcolema de cada fibra muscular. Representan entre el 1-4% de todos los núcleos asociados con las fibras musculares adultas.
Las "células satélite" son responsables de: el crecimiento, la reparación y la regeneración de la fibra muscular.[13]
Las células madre satélite habitualmente inactivas en la fase G0, se multiplican en respuesta a estímulos fisiológicos como: el ejercicio, las lesiones y el estrés.[14]
Después del daño de la miofibra, las células satélite, se activan para ingresar al ciclo celular y proliferar.[15]
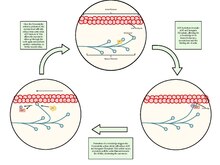
Rotura fibrilar y Reparación[editar]
En las lesiones musculares y las enfermedades musculares, la capacidad de regeneración es esencial para recuperar la función. En respuesta a la lesión muscular, las células satélite (SC) se activan para iniciar la diferenciación miogénica, acompañada de una expresión regulada al alza de miogenina (MYOG) y el factor4 regulador específico del músculo. El programa de diferenciación luego se completa con la activación de proteínas musculares específicas como miosina (MYHC) en los mioblastos que se fusionan para regenerar las miofibras.[16]
Función[editar]
Contracción muscular en músculo estriado[editar]
Contracción del músculo esquelético[editar]
Cuando se contraen, los filamentos delgados y gruesos se deslizan entre sí mediante el uso de trifosfato de adenosina. Esto acerca los discos Z en un proceso llamado mecanismo de filamento deslizante. La contracción de todos los sarcómeros da como resultado la contracción de toda la fibra muscular. Esta contracción del miocito es desencadenada por el potencial de acción sobre la membrana celular del miocito. El potencial de acción utiliza túbulos transversales para llegar desde la superficie al interior del miocito, que es continuo dentro de la membrana celular. Los retículos sarcoplásmicos son bolsas membranosas que los túbulos transversales tocan pero permanecen separados. Estos se envuelven alrededor de cada sarcómero y están llenos de Ca2+.[17]
La excitación de un miocito provoca la despolarización en sus sinapsis, las uniones neuromusculares, lo que desencadena un potencial de acción. Con una unión neuromuscular singular, cada fibra muscular recibe información de una sola neurona eferente somática. El potencial de acción en una neurona eferente somática provoca la liberación del neurotransmisor acetilcolina.[18]
Cuando se libera la acetilcolina, se difunde a través de la sinapsis y se une a un receptor en el sarcolema, un término exclusivo de las células musculares que se refiere a la membrana celular. Esto inicia un impulso que viaja a través del sarcolema.[19]
Cuando el potencial de acción alcanza el retículo sarcoplásmico desencadena la liberación de Ca2+ de los canales de Ca2+. El Ca2+ fluye desde el retículo sarcoplásmico hacia el sarcómero con sus dos filamentos. Esto hace que los filamentos comiencen a deslizarse y los sarcómeros se acorten. Esto requiere una gran cantidad de ATP, ya que se usa tanto en la unión como en la liberación de cada miosina cabeza. Muy rápidamente, el Ca2+ se transporta activamente de regreso al retículo sarcoplásmico, lo que bloquea la interacción entre el filamento delgado y el grueso. Esto, a su vez, hace que la célula muscular se relaje.[19]
Hay cuatro tipos principales de contracción muscular: contracción, treppe, tétanos e isométrica/isotónica. La contracción de contracción es el proceso en el que un solo estímulo señala una sola contracción. En la contracción de contracción, la duración de la contracción puede variar según el tamaño de la célula muscular. Durante la contracción treppe (o sumatoria), los músculos no comienzan con la máxima eficiencia; en cambio, logran una mayor fuerza de contracción debido a estímulos repetidos. El tétanos implica una contracción sostenida de los músculos debido a una serie de estímulos rápidos, que puede continuar hasta que los músculos se fatigan. Las contracciones isométricas son contracciones del músculo esquelético que no provocan el movimiento del músculo. Sin embargo, las contracciones isotónicas son contracciones del músculo esquelético que sí provocan movimiento.[19]
Contracción del músculo cardíaco[editar]
Los cardiomiocitos especializados del nodo sinoauricular generan impulsos eléctricos que controlan la frecuencia del corazón. Estos impulsos eléctricos coordinan la contracción en todo el resto del músculo cardíaco a través del sistema de conducción eléctrica del corazón. La actividad del nódulo sinoauricular es modulada, a su vez, por fibras nerviosas de los sistemas nerviosos simpático y parasimpático. Estos sistemas actúan para aumentar y disminuir, respectivamente, la tasa de producción de impulsos eléctricos por parte del nodo sinoauricular.
Véase también[editar]
Referencias[editar]
- ↑ OPS, OMS. Biblioteca virtual de salud: Descriptores en Ciencias de la Salud (ed.). «Fibras Musculares Esqueléticas/Fibras del Músculo/Miocitos Esqueléticos». Consultado el 16 de enero de 2020.
- ↑ Guyton, A.C.; Hall, J.E. (2011). Textbook of Medical Physiology [Tratado de fisiología médica] (12ª edición). Barcelona: Elsevier/GEA Consultoría Editorial. ISBN 9788480868198. Consultado el 22 de abril de 2013.
- ↑ Sadler T.W., Langman J. (2007). «Cap10: Sistema muscular». Embriología médica Con orientación clínica. Médica Panamericana. p. 149. Consultado el 31 de enero de 2020.
- ↑ Cadot B.; Gache V.; Gomes E.R. (2015). «Moving and positioning the nucleus in skeletal muscle –one step at a time». Nucleus 6 (5): 373-381. Consultado el 31 de enero de 2020.
- ↑ a b Welsch U.; Sobotta J. (2008). «cap3: Tejidos. Tejido muscular esquelético». Histología. Médica Panamericana. p. 157. Consultado el 16 de enero de 2020.
- ↑ a b Megías M., Molist P., Pombal M.A. . «Tipos celulares. Muscular esquelético. Miocito». Atlas de histología vegetal y animal. Consultado el 16 de enero de 2020.
- ↑ a b Kühnel W. (2005). «Imagen 230 y 231». Atlas color de citología e histología (11° edición). Médica Panamericana. pp. 167-169. Consultado el 17 de enero de 2020.
- ↑ Guarnieri S.; Morabito C.; Paolini C.; Boncompagni S.; Pilla R.; Fanò-Illic G, (2013). Growth Associated Protein 43 Is Expressed in Skeletal Muscle Fibers and Is Localized in Proximity of Mitochondria and Calcium Release Units. 8 (1). PLoS ONE. p. e53267. doi:10.1371/journal.pone.0053267. Consultado el 19 de enero de 2020.

- ↑ Roman W., Gomes E.R. (2018). «Nuclear positioning in skeletal muscle». Seminars in Cell & Developmental Biology 82: 51-56.
- ↑ Chargé S.B., Rudnicki M.A. (2004). «Cellular and molecular regulation of muscle regeneration.». Physiol Rev. (Revisión) 84 (1): 209-238. Consultado el 2 de febrero de 2020.
- ↑
Pajalunga D.; Puggioni E.M.R.; Mazzola A.; Leva V.; Montecucco A.; Crescenzi M. (2010). «DNA Replication Is Intrinsically Hindered in Terminally Differentiated Myotubes». PLoS ONE 5 (7): e11559. doi:10.1371/journal.pone.0011559. Consultado el 1 de febrero de 2020.

- ↑ Yablonka-Reuveni Z. (2011). The Skeletal Muscle Satellite Cell: Still Young and Fascinating at 50 59 (12). pp. 1041-1059. Consultado el 3 de febrero de 2020.
- ↑ Kaspar P., Ilencikova K., Zikova M., Horvath O., Cermak V., Bartunek P., Strand H. (2013). «c-Myb Inhibits Myoblast Fusion». PLoS ONE 8 (10): e76742. doi:10.1371/journal.pone.0076742. Consultado el 1 de febrero de 2020.

- ↑ Robson L.G., Di Foggia V., Radunovic A., Bird K., Zhang X., Marino S. (2011). «Bmi1 Is Expressed in Postnatal Myogenic Satellite Cells, Controls Their Maintenance and Plays an Essential Role in Repeated Muscle Regeneration». PLoS ONE 6 (11): e27116. doi:10.1371/journal.pone.0027116. Consultado el 3 de febrero de 2020.

- ↑ Karalaki M., Fili S., Philippou A., Koutsilieris M. (2009). «Muscle Regeneration: Cellular and Molecular Events». In Vivo 23 (5): 779-796. Consultado el 2 de febrero de 2020.
- ↑ Shi X.C.; Xia B.; Zhang J.F.; Zhang R.X.; Zhang D.Y.; Liu H.; Xie B.C.; Wang Y.L.; Wu J.W. (2022). «Optineurin promotes myogenesis during muscle regeneration in mice by autophagic degradation of GSK3β». PLoS Biology 20 (4): e3001614. doi:10.1371/journal.pbio.3001619. Consultado el 25 de setiembre de 2022.

- ↑ «Estructura y función de los músculos esqueléticos». courses.washington.edu. Archivado desde el original el 15 de febrero de 2015. Consultado el 13 de febrero de 2015.
- ↑ «Muscle Fiber Excitation». courses.washington.edu. University of Washington. Archivado desde el original el 27 de febrero de 2015. Consultado el 11 de febrero de 2015.
- ↑ a b c Ziser, Stephen. «Muscle Cell Anatomy & Function». www.austincc.edu. Archivado desde el original el 23 de septiembre de 2015. Consultado el 12 de febrero de 2015.
