Carcinoma adrenocortical
| Carcinoma adrenocortical | ||
|---|---|---|
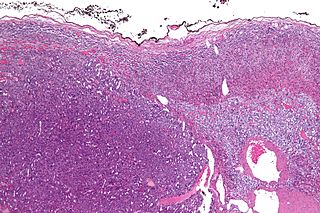 Micrografía de un carcinoma adrenocortical (a la izquierda de la imagen, azul oscuro) y de la corteza adrenal de la que surgió (arriba a la derecha de la imagen, rosa / azul claro). La médula suprarrenal benigna está presente (mitad derecha de la imagen, gris/azul). Tinción H&E. | ||
| Especialidad | oncología | |
El carcinoma adrenocortical (CAC, carcinoma suprarrenal cortical, cáncer de la corteza suprarrenal, etc.) es un cáncer agresivo que se origina en la corteza (tejido productor de hormonas esteroides) de la glándula suprarrenal. El carcinoma adrenocortical es un tumor poco frecuente, con una incidencia de 1-2 por millón de habitantes anualmente. El carcinoma adrenocortical tiene una distribución bimodal por edad, con casos que se agrupan en niños menores de 5 años y en adultos de 30 a 40 años. El carcinoma adrenocortical es notable por los muchos síndromes hormonales que pueden ocurrir en pacientes con tumores productores de hormonas esteroides ("funcionales"), incluidos el síndrome de Cushing, el síndrome de Conn, la virilización y la feminización. El carcinoma adrenocortical a menudo ha invadido tejidos cercanos o hecho metástasis a órganos distantes en el momento del diagnóstico, y la tasa de supervivencia general a 5 años es de solo 20-35%. La línea celular H295R que produce esteroides, sensible a la angiotensina II y ampliamente utilizada se aisló originalmente de un tumor diagnosticado como carcinoma adrenocortical.[1][2]
Señales y síntomas
[editar]El carcinoma adrenocortical puede presentarse de manera diferente en niños y adultos. La mayoría de los tumores en los niños son funcionales, y la virilización es con mucho el síntoma de presentación más común, seguido del síndrome de Cushing y la pubertad precoz.[3] Entre los adultos que presentan síndromes hormonales, el síndrome de Cushing solo es más común, seguido de Cushing y virilización mixtos (glucocorticoides y sobreproducción de andrógenos). La feminización y el síndrome de Conn (exceso de mineralocorticoides) ocurren en menos del 10% de los casos. En raras ocasiones, se ha informado de hipersecreción de catecolaminas similares a los feocromocitomas en cánceres de la corteza suprarrenal.[4] Los tumores no funcionales (alrededor del 40%, las autoridades varían) generalmente se presentan con dolor abdominal o de flanco, varicocele y trombosis de la vena renal,[5] o pueden ser asintomáticos y detectarse incidentalmente</ref>
Todos los pacientes con sospecha de carcinoma adrenocortical deben evaluarse cuidadosamente para detectar signos y síntomas de síndromes hormonales. Para el síndrome de Cushing (exceso de glucocorticoides) estos incluyen aumento de peso, pérdida de masa muscular, líneas moradas en el abdomen, una "joroba de búfalo" grasosa en el cuello, una cara "lunar" y una piel frágil y adelgazada. El virilismo (exceso de andrógenos) es más evidente en las mujeres y puede producir exceso de vello facial y corporal, acné, agrandamiento del clítoris, engrosamiento de la voz, engrosamiento de los rasgos faciales, interrupción de la menstruación. El síndrome de Conn (exceso de mineralcorticoides) está marcado por presión arterial alta que puede causar dolor de cabeza e hipocalemia (bajo nivel de potasio sérico, que a su vez puede producir debilidad muscular, confusión y palpitaciones) baja actividad de renina en plasma y aldosterona alta en suero. La feminización (exceso de estrógeno) se observa más fácilmente en los hombres, e incluye aumento de senos, disminución de la libido e impotencia.[6]
Fisiopatología
[editar]El principal factor etiológico del cáncer de la corteza suprarrenal es desconocido. Las familias con síndrome de Li-Fraumeni, causadas por una mutación de inactivación hereditaria en TP53, tienen un mayor riesgo. Se ha demostrado que varios genes son mutantes recurrentes, incluidos TP53, CTNNB1, MEN1, PRKAR1A, RPL22 y DAXX.[7][8] El gen TERT de la telomerasa a menudo se amplifica, mientras que ZNRF3y CDKN2Aa menudo se eliminan homocigóticamente.[8] Los genes h19, factor de crecimiento similar a la insulina II (IGF-II), p57kip2 son importantes para el crecimiento y el desarrollo del feto. Están ubicados en el cromosoma 11p. La expresión del gen h19 se reduce notablemente tanto en carcinomas corticosuprarrenales no funcionales como en funcionales, especialmente en tumores que producen cortisol y aldosterona. También hay una pérdida de actividad del producto del gen p57kip2 en adenomas virilizantes y carcinomas corticosuprarrenales. Por el contrario, la expresión del gen IGF-II ha demostrado ser alta en carcinomas corticosuprarrenales. Finalmente, la expresión del gen c-myc es relativamente alta en neoplasmas y, a menudo, está relacionada con un mal pronóstico.[9]
Los tumores adrenocorticales bilaterales son menos comunes que los unilaterales. La mayoría de los tumores bilaterales se pueden distinguir según el tamaño y el aspecto de los nódulos: enfermedad adrenocortical nodular pigmentada primaria que puede ser esporádica o formar parte del complejo de Carney y la hiperplasia suprarrenal macro nodular bilateral primaria.
Diagnosis
[editar]Hallazgos de laboratorio
[editar]Los síndromes hormonales deben confirmarse con pruebas de laboratorio. Los hallazgos de laboratorio en el síndrome de Cushing incluyen aumento de la glucosa sérica (azúcar en la sangre) y aumento del cortisol en la orina. El virilismo suprarrenal se confirma por el hallazgo de un exceso de androstenediona sérica y dehidroepiandrosterona. Los hallazgos en el síndrome de Conn incluyen potasio sérico bajo, actividad de renina plasmática baja y aldosterona sérica alta. La feminización se confirma con el hallazgo de exceso de estrógenos séricos.
Radiología
[editar]Los estudios radiológicos del abdomen, como las tomografías computarizadas y las imágenes de resonancia magnética son útiles para identificar el sitio del tumor, diferenciarlo de otras enfermedades, como el adenoma adrenocortical y determinar la extensión de la invasión del tumor a los órganos y tejidos circundantes. Las tomografías computarizadas del tórax y las exploraciones óseas se realizan rutinariamente para buscar metástasis en los pulmones y los huesos, respectivamente. Estos estudios son fundamentales para determinar si el tumor puede extirparse quirúrgicamente o no, la única cura potencial en este momento.
Patología
[editar]

Los tumores suprarrenales a menudo no se biopsian antes de la cirugía, por lo que el diagnóstico se confirma al examinar la muestra quirúrgica por un patólogo. En general, los carcinomas adrenocorticales a menudo son grandes, con una superficie de corte de color canela y áreas de hemorragia y necrosis. En el examen microscópico, el tumor generalmente muestra láminas de células atípicas con cierta semejanza con las células de la corteza suprarrenal normal. La presencia de invasión y actividad mitótica ayuda a diferenciar cánceres pequeños de adenomas adrenocorticales. Hay varias variantes relativamente raras de carcinoma corticoadrenal:
- Carcinoma suprarrenal cortical oncocítico
- Carcinoma corticosuprarrenal mixoide
- Carcinosarcoma
- Carcinoma adrenocortical adenoescamoso
- Carcinoma cortical suprarrenal de células claras
Diagnosis diferencial
[editar]La diagnosis diferencial incluye:[cita requerida]
- Adrenocortical Adenoma
- Carcinoma renal
- Feocromocitoma
- Hepatocarcinoma
Tratamiento
[editar]El único tratamiento curativo es la extirpación quirúrgica completa del tumor, que puede realizarse incluso en el caso de invasión en vasos sanguíneos grandes, como la vena renal o la vena cava inferior. La tasa de supervivencia a 5 años después de una cirugía exitosa es del 50-60%, pero desafortunadamente, un gran porcentaje de pacientes no son candidatos para la cirugía. La radioterapia y la ablación por radiofrecuencia pueden usarse para la paliación en pacientes que no son candidatos quirúrgicos
Los regímenes de quimioterapia generalmente incluyen el medicamento mitotano, un inhibidor de la síntesis de esteroides que es tóxico para las células de la corteza suprarrenal,[10] así como los medicamentos citotóxicos estándar. Un análisis retrospectivo mostró un beneficio de supervivencia para el mitotano además de la cirugía en comparación con la cirugía sola.</ref>
Los dos regímenes más comunes son cisplatino, doxorrubicina, etopósido + mitotano y estreptozotocina + mitotano. Se desconoce qué régimen es mejor. Investigadores del Hospital Universitario de Uppsala han iniciado una colaboración entre especialistas en cáncer de la corteza suprarrenal en Europa, EE. UU. Y Australia, para llevar a cabo el primer ensayo aleatorizado controlado en cáncer de la corteza suprarrenal (estudio FIRM-ACT),[11] comparando estos dos regímenes.
Pronóstico
[editar]El CAC, en general, tiene un mal pronóstico y es diferente a la mayoría de los tumores de la corteza suprarrenal, que son benignos (adenomas) y solo ocasionalmente causan el síndrome de Cushing. La supervivencia libre de enfermedad a cinco años para una resección completa de un CAC en estadio I-III es aproximadamente del 30%
Los factores pronósticos más importantes son la edad del paciente y la etapa del tumor. Factores de mal pronóstico: actividad mitótica, invasión venosa, peso de 50 g +; diámetro de 6.5 cm +, índice de etiquetado Ki-67 / MIB1 de 4% +, p53 +.[cita requerida]
Referencias
[editar]- ↑ Wang T, Rainey WE (marzo de 2012). «Human adrenocortical carcinoma cell lines». Molecular and Cellular Endocrinology 351 (1): 58-65. PMC 3288152. PMID 21924324. doi:10.1016/j.mce.2011.08.041.
- ↑ Gazdar AF, Oie HK, Shackleton CH, Chen TR, Triche TJ, Myers CE, Chrousos GP, Brennan MF, Stein CA, La Rocca RV (septiembre de 1990). «Establishment and characterization of a human adrenocortical carcinoma cell line that expresses multiple pathways of steroid biosynthesis». Cancer Research 50 (17): 5488-96. PMID 2386954.
- ↑ DeVita, Vincent T.; Hellman, Samuel; Rosenberg, Steven A., eds. (2005). Cancer: principles & practice of oncology. Philadelphia: Lippincott-Raven. ISBN 978-0-7817-4865-0.
- ↑ Cote, Richard; Suster, Saul; Weiss, Lawrence (2002). Weidner, Noel, ed. Modern Surgical Pathology (2 Volume Set). London: W B Saunders. ISBN 0-7216-7253-1.
- ↑ Cheungpasitporn W, Horne JM, Howarth CB (agosto de 2011). «Adrenocortical carcinoma presenting as varicocele and renal vein thrombosis: a case report». Journal of Medical Case Reports 5: 337. PMC 3160386. PMID 21806824. doi:10.1186/1752-1947-5-337.
- ↑ Kasper DL, Braunwald E, Fauci AS, Hauser SL, Longo DL, Jameson JL. Harrison's Principles of Internal Medicine. New York: McGraw-Hill, 2005. ISBN 0-07-139140-1
- ↑ Zheng S, Cherniack AD, Dewal N, Moffitt RA, Danilova L, Murray BA, Lerario AM, Else T, Knijnenburg TA, Ciriello G, Kim S, Assie G, Morozova O, Akbani R, Shih J, Hoadley KA, Choueiri TK, Waldmann J, Mete O, Robertson AG, Wu HT, Raphael BJ, Shao L, Meyerson M, Demeure MJ, Beuschlein F, Gill AJ, Sidhu SB, Almeida MQ, Fragoso MC, Cope LM, Kebebew E, Habra MA, Whitsett TG, Bussey KJ, Rainey WE, Asa SL, Bertherat J, Fassnacht M, Wheeler DA, Hammer GD, Giordano TJ, Verhaak RG (mayo de 2016). «Comprehensive Pan-Genomic Characterization of Adrenocortical Carcinoma». Cancer Cell 29 (5): 723-736. PMC 4864952. PMID 27165744. doi:10.1016/j.ccell.2016.04.002.
- ↑ a b Assié G, Letouzé E, Fassnacht M, Jouinot A, Luscap W, Barreau O, Omeiri H, Rodriguez S, Perlemoine K, René-Corail F, Elarouci N, Sbiera S, Kroiss M, Allolio B, Waldmann J, Quinkler M, Mannelli M, Mantero F, Papathomas T, De Krijger R, Tabarin A, Kerlan V, Baudin E, Tissier F, Dousset B, Groussin L, Amar L, Clauser E, Bertagna X, Ragazzon B, Beuschlein F, Libé R, de Reyniès A, Bertherat J (junio de 2014). «Integrated genomic characterization of adrenocortical carcinoma». Nature Genetics 46 (6): 607-12. PMID 24747642. doi:10.1038/ng.2953.
- ↑ Kufe D (2000). Benedict RC, Holland JF, ed. Cancer medicine (5th edición). Hamilton, Ont: B.C. Decker. ISBN 1-55009-113-1. OCLC 156944448.
- ↑ Brunton, Laurence L.; Lazo, John S.; Parker, Keith L., eds. (2006). Goodman & Gilman's The Pharmacological Basis of Therapeutics, 11th Edition. United States of America: The McGraw-Hill Companies, Inc. ISBN 0-07-142280-3.
- ↑ «Copia archivada». Archivado desde el original el 6 de julio de 2011. Consultado el 2 de septiembre de 2018.
