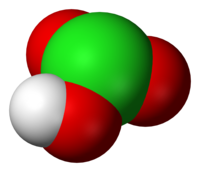
Ácido clórico
  | ||
 | ||
| Nombre IUPAC | ||
| Ácido trioxoclórico (V) | ||
| General | ||
| Otros nombres | Trioxoclorato (V) de hidrógeno | |
| Fórmula molecular | HClO3 | |
| Identificadores | ||
| Número CAS | 7790-93-4[1] | |
| Número RTECS | CN9750000 | |
| ChEBI | 17322 | |
| ChEMBL | CHEMBL1161633 | |
| ChemSpider | 18513 | |
| DrugBank | 14150 | |
| PubChem | 19654 | |
| UNII | Z0V9L75H3K | |
| KEGG | C01485 | |
| Propiedades físicas | ||
| Apariencia | Solución incolora | |
| Densidad | 1000 kg/m³; 1 g/cm³ | |
| Masa molar | 84.45914 g mol−1 g/mol | |
| Punto de fusión | 253,15 K (−20 °C) | |
| Punto de ebullición | 313,15 K (40 °C) | |
| Propiedades químicas | ||
| Acidez | ca. −1 pKa | |
| Solubilidad en agua | >40 g/100 ml (20 °C), soluble | |
| Peligrosidad | ||
| NFPA 704 |
1
3
2
OX
| |
| Riesgos | ||
| Riesgos principales | Oxidante | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Ácido clórico, HClO3, es un oxácido de cloro, y el precursor formal de sales de clorato. Se trata de un ácido fuerte (pKa ≈ −1) y agente oxidante.
Es elaborado por la reacción de ácido sulfúrico con clorato de bario, donde la formación de sulfato de bario insoluble hace salir de la fase acuosa, por precipitación, los iones sulfato y bario (II):
- Ba(ClO3)2 + H2SO4 → 2HClO3 + BaSO4
Otro método es el calentamiento de ácido hipocloroso, obteniéndose así ácido clórico y cloruro de hidrógeno:
- 3HClO → HClO3 + 2 HClHClO
Es estable en solución acuosa en frío hasta una concentración de aproximadamente 30%, y la solución de hasta un 40% puede ser preparado por evaporación a presión reducida. Por encima de estas concentraciones, y en el calentamiento, las soluciones de ácido clórico se descomponen para dar una variedad de productos, por ejemplo:
- 8HClO3 → 4HClO4 + 2H2O + 2Cl2 + 3 O2
- 3HClO3 → HClO4 + H2O + 2 ClO2
La descomposición es controlada por factores cinéticos: de hecho, el ácido clorhídrico no es termodinámicamente estables con respecto a la desproporción.
Véase también[editar]
Bibliografía[editar]
- Greenwood, Norman N.; Earnshaw, A. Chemistry of the Elements (2nd ed.). Oxford: Butterworth-Heinemann. ISBN 0-7506-3365-4.
- King, R. B. (1994). Encyclopedia of Inorganic Chemistry, Vol. 2. Chichester: Wiley. p. 658. ISBN 0-471-93620-0.
Referencias[editar]
Enlaces externos[editar]
- Esta obra contiene una traducción derivada de «Chloric acid» de Wikipedia en inglés, publicada por sus editores bajo la Licencia de documentación libre de GNU y la Licencia Creative Commons Atribución-CompartirIgual 4.0 Internacional.

