Ectasia vascular antral gástrica
| Ectasia vascular antral gástrica | ||
|---|---|---|
 Imagen de endoscopia de la ectasia vascular antral gástrica vista como un patrón radial alrededor del píloro antes (arriba) y después (abajo) del tratamiento con coagulación con plasma de argón. | ||
| Especialidad | gastroenterología | |
| Síntomas | Sangrado en el estómago y los intestinos, edema, vasos sanguíneos dilatados | |
La ectasia vascular antral gástrica (GAVE) es una causa poco frecuente de hemorragia digestiva crónica o anemia ferropénica.[1][2] La afección se asocia con vasos sanguíneos pequeños dilatados en el antro pilórico, que es una parte distal del estómago.[1] Los vasos dilatados dan como resultado sangrado intestinal.[3] También se le llama estómago de sandía porque las áreas largas y rojas que están presentes en el estómago pueden parecerse a las marcas de la sandía.[1][2][3][4]
La enfermedad se descubrió por primera vez en 1952[5] y se publicó en la literatura en 1953.[6] enfermedad de la sandía fue diagnosticada por primera vez por Wheeler et al. en 1979, y descrita definitivamente en cuatro pacientes vivos por Jabbari et al. sólo en 1984.[7] A partir de 2011, la causa y la patogénesis aún no se conocen.[8][9] Sin embargo, hay varias hipótesis que compiten entre sí en cuanto a las diversas causas.[4]
Signos y síntomas[editar]
La mayoría de los pacientes que finalmente son diagnosticados con estómago de sandía acuden al médico quejándose de anemia y pérdida de sangre.[10] A veces, un paciente puede acudir al médico porque nota sangre en las heces, ya sea melena (heces negras y alquitranadas) y/o hematoquecia (heces rojas con sangre).[10]
Causa[editar]
La literatura, desde 1953 hasta 2010, cita a menudo que se desconoce la causa de la ectasia vascular antral gástrica.[4][11][10] La conexión causal entre cirrosis y GAVE no ha sido probada.[11] En algunos casos se ha sospechado una enfermedad del tejido conectivo.[10]
La autoinmunidad puede tener algo que ver con esto,[12] ya que el 25% de todos los pacientes con esclerosis que tenían un determinado marcador anti-ARN tienen GAVE.[13] Se sospecha que la autoinmunidad al ARN es una causa o un marcador desde al menos 1996.[12] Los niveles de gastrina pueden indicar una conexión hormonal.[11]
Enfermedades asociadas[editar]
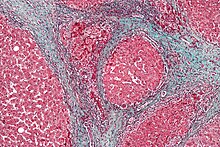
GAVE está asociada con una serie de afecciones, que incluyen hipertensión portal, insuficiencia renal crónica y enfermedades vasculares del colágeno.[2][14][15]
El estómago de sandía también ocurre particularmente con la esclerodermia, y especialmente el subtipo conocido como esclerosis sistémica. Un 5,7% de las personas con esclerosis tienen GAVE, y el 25% de todos los pacientes con esclerosis que tenían un determinado marcador anti-ARN polimerasa tienen GAVE.
La mayoría de los pacientes con GAVE padecen cirrosis hepática, enfermedades autoinmunes, insuficiencia renal crónica y trasplante de médula ósea. Las presentaciones iniciales típicas van desde una hemorragia oculta que provoca una anemia ferropénica crónica dependiente de transfusiones hasta una hemorragia gastrointestinal aguda grave.Masae Komiyama, et al., 2010.
La apariencia endoscópica de GAVE es similar a la gastropatía hipertensiva portal, pero no es la misma enfermedad y puede coincidir con la cirrosis hepática.[2][11][16][17] El 30% de todos los pacientes tienen cirrosis asociada con GAVE.[11]
El síndrome de Sjögren se ha asociado con al menos un paciente.[18]
El primer caso de páncreas ectópico asociado con el estómago de sandía se notificó en 2010.[4]
Los pacientes con GAVE pueden tener niveles elevados de gastrina.[11]
El Centro de Información sobre Enfermedades Raras y Genéticas (GARD) afirma que la anemia perniciosa es una de las afecciones asociadas a los GAVE,[19] y un estudio independiente mostró que más de tres cuartas partes de los pacientes del estudio con GAVE tenían algún tipo de deficiencia de vitamina B12, incluida la afección asociada a la anemia perniciosa[20]
La permeabilidad intestinal y la diverticulitis pueden ocurrir en algunos pacientes con GAVE.
Patogénesis[editar]
La GAVE se caracteriza por capilares dilatados en la lámina propia con trombos de fibrina. El principal diagnóstico diferencial histomorfológico es la hipertensión portal, que a menudo se manifiesta a partir de los hallazgos clínicos.
Las investigaciones realizadas en 2010 han demostrado que los anticuerpos anti- ARN polimerasa III pueden utilizarse como marcador de riesgo de GAVE en pacientes con esclerosis sistémica.[13]
Diagnóstico[editar]

La GAVE suele diagnosticarse de forma definitiva mediante una biopsia endoscópica .[10][11][14][21] Las rayas de sandía reveladoras aparecen durante la endoscopia.[10]
La exploración quirúrgica del abdomen puede ser necesaria para diagnosticar algunos casos, especialmente si el hígado u otros órganos están involucrados.[4]
Diagnóstico diferencial[editar]
La GAVE produce hemorragia intestinal similar a las úlceras duodenales e hipertensión portal.[3][11] El sangrado puede resultar en anemia.[11][10] A menudo se pasa por alto, pero puede ser más común en pacientes de edad avanzada.[3][10] Se ha visto en una paciente de sexo femenino de 26 años de edad.[11]
El estómago en sandía tiene una etiología diferente y tiene un diagnóstico diferencial con la hipertensión portal.[11][16] De hecho, la cirrosis y la hipertensión portal pueden pasar desapercibidas en un paciente con GAVE.[11] El diagnóstico diferencial es importante porque los tratamientos son diferentes.[3][11][10][14]
Tratamiento[editar]
Tratamientos tradicionales[editar]
La GAVE se trata comúnmente por medio de un endoscopio, incluida la coagulación con plasma de argón y electrocauterio.[11][10][22] Dado que la endoscopia con fotocoagulación con argón es "generalmente efectiva", la cirugía "generalmente no es necesaria".[10] La terapia de coagulación es bien tolerada pero "tiende a inducir supuración y sangrado".[10] La "endoscopia con ablación térmica" es el tratamiento médico preferido debido a sus bajos efectos secundarios y baja mortalidad, pero "rara vez es curativa".[11] El tratamiento de la GAVE puede clasificarse en endoscópico, quirúrgico y farmacológico. El tratamiento quirúrgico es definitivo, pero rara vez se realiza hoy en día con la variedad de opciones de tratamiento disponibles. Algunas de las modalidades comentadas se han utilizado en pacientes con GAVE con otra enfermedad subyacente. El tratamiento sintomático incluye la administración de suplementos de hierro y la transfusión de sangre para los casos con anemia grave, los inhibidores de la bomba de protones pueden mejorar la gastritis crónica de fondo y las erosiones diminutas que suelen coexistir en los informes de las biopsias.
Medicamentos[editar]
Se han probado otros tratamientos médicos e incluyen terapia de estrógeno y progesterona,[22] Los corticosteroides son efectivos, pero están "limitados por sus efectos secundarios ".[10]
Tratamiento de condiciones comórbidas[editar]
El procedimiento de derivación portosistémica intrahepática transyugular (TIPS o TIPSS) se utiliza para tratar la hipertensión portal cuando ésta está presente como afección asociada. Desgraciadamente, el TIPSS, que se ha utilizado para condiciones similares, puede causar o exacerbar la encefalopatía hepática.[23][24] La encefalopatía relacionada con el TIPSS se produce en alrededor del 30% de los casos, siendo el riesgo mayor en aquellos con episodios previos de encefalopatía, mayor edad, sexo femenino y enfermedad hepática por causas distintas al alcohol. El paciente, junto con su médico y su familia, debe sopesar la reducción de la hemorragia causada por el DPIT con el importante riesgo de encefalopatía.[25][26][27] En un metaestudio de 22 estudios se ha demostrado que varias derivaciones son un tratamiento eficaz para reducir la hemorragia por várices, pero ninguno ha demostrado una ventaja en la supervivencia.[28]
Si hay cirrosis hepática que ha progresado a insuficiencia hepática, se puede recetar lactulosa para la encefalopatía hepática, especialmente para la encefalopatía tipo C con diabetes.[29] Además, "los antibióticos como la neomicina, el metronidazol y la rifaximina " se pueden usar de manera efectiva para tratar la encefalopatía al eliminar las bacterias productoras de nitrógeno del intestino.[29]
La paracentesis, un procedimiento médico que implica el drenaje con aguja del líquido de una cavidad corporal,[30] se puede usar para extraer líquido de la cavidad peritoneal en el abdomen en tales casos.[31] Este procedimiento utiliza una aguja grande, similar a la amniocentesis más conocida.
Cirugía[editar]
La cirugía, consistente en la escisión de una parte de la parte inferior del estómago, también llamada antrectomía,[32][33] es otra opción. La antrectomía es "la resección, o extirpación quirúrgica, de una parte del estómago conocida como antro".[34] La cirugía laparoscópica es posible en algunos casos, y a partir de 2003, era un "enfoque novedoso para tratar el estómago de sandía"[35]
Un tratamiento que se usa a veces es la ligadura con banda endoscópica.[36]
En 2010, un equipo de cirujanos japoneses realizó una " ablación endoscópica novedosa de ectasia vascular antral gástrica".[14] El procedimiento experimental resultó "sin complicaciones".[14]
La recaída es posible, incluso después del tratamiento con coagulación con plasma de argón y progesterona.[22]
La antrectomía u otra cirugía se usa como último recurso para la GAVE.[2][11][10][14][16][17]
Epidemiología[editar]
La edad promedio de diagnóstico de GAVE es de 73 años para las mujeres,[3][10] y 68 para los hombres.[2] A las mujeres se les diagnostica aproximadamente el doble de ectasia vascular antral gástrica que a los hombres.[2][10] El 71 % de todos los casos de GAVE se diagnostican en mujeres.[3][10] Se ha encontrado que los pacientes en la treintena pueden tener GAVE.[11] Se vuelve más común en mujeres de ochenta años, llegando al 4% de todas estas afecciones gastrointestinales.[14]
El 5,7 % de todos los pacientes con esclerosis (y el 25 % de los que tenían un determinado marcador anti-ARN) tienen GAVE.[13]
Referencias[editar]
- ↑ a b c Suit, PF; Petras, RE; Bauer, TW; Petrini Jr, JL (1987). «Gastric antral vascular ectasia. A histologic and morphometric study of "the watermelon stomach"». The American Journal of Surgical Pathology 11 (10): 750-7. PMID 3499091. doi:10.1097/00000478-198710000-00002.
- ↑ a b c d e f g Surgery Encyclopedia website page on Antrectomy. Accessed September 29, 2010.
- ↑ a b c d e f g Nguyen, Hien; Le, Connie; Nguyen, Hanh (2009). «Gastric antral vascular ectasia (watermelon stomach)-an enigmatic and often-overlooked cause of gastrointestinal bleeding in the elderly». The Permanente Journal 13 (4): 46-9. PMC 2911825. PMID 20740102. doi:10.7812/TPP/09-055.
- ↑ a b c d e Yildiz, Baris; Sokmensuer, Cenk; Kaynaroglu, Volkan (2010). «Chronic anemia due to watermelon stomach». Annals of Saudi Medicine 30 (2): 156-8. PMC 2855069. PMID 20220268. doi:10.4103/0256-4947.60524.
- ↑ Surgery Encyclopedia website page on Antrectomy. Accessed September 29, 2010.
- ↑ Rider, JA; Klotz, AP; Kirsner, JB (1953). «Gastritis with veno-capillary ectasia as a source of massive gastric hemorrhage». Gastroenterology 24 (1): 118-23. PMID 13052170. doi:10.1016/S0016-5085(53)80070-3.
- ↑ Yildiz, Baris; Sokmensuer, Cenk; Kaynaroglu, Volkan (2010). «Chronic anemia due to watermelon stomach». Annals of Saudi Medicine 30 (2): 156-8. PMC 2855069. PMID 20220268. doi:10.4103/0256-4947.60524.
- ↑ Yildiz, Baris; Sokmensuer, Cenk; Kaynaroglu, Volkan (2010). «Chronic anemia due to watermelon stomach». Annals of Saudi Medicine 30 (2): 156-8. PMC 2855069. PMID 20220268. doi:10.4103/0256-4947.60524.
- ↑ Tuveri, Massimiliano; Borsezio, Valentina; Gabbas, Antonio; Mura, Guendalina (2007). «Gastric antral vascular ectasia—an unusual cause of gastric outlet obstruction: report of a case». Surgery Today 37 (6): 503-5. PMID 17522771. S2CID 25727751. doi:10.1007/s00595-006-3430-3.
- ↑ a b c d e f g h i j k l m n ñ o p Rosenfeld, G; Enns, R (2009). «Argon photocoagulation in the treatment of gastric antral vascular ectasia and radiation proctitis». Canadian Journal of Gastroenterology 23 (12): 801-4. PMC 2805515. PMID 20011731. doi:10.1155/2009/374138.
- ↑ a b c d e f g h i j k l m n ñ o p Tuveri, Massimiliano; Borsezio, Valentina; Gabbas, Antonio; Mura, Guendalina (2007). «Gastric antral vascular ectasia—an unusual cause of gastric outlet obstruction: report of a case». Surgery Today 37 (6): 503-5. PMID 17522771. doi:10.1007/s00595-006-3430-3.
- ↑ a b Valdez, BC; Henning, D; Busch, RK; Woods, K; Flores-Rozas, H; Hurwitz, J; Perlaky, L; Busch, H (1996). «A nucleolar RNA helicase recognized by autoimmune antibodies from a patient with watermelon stomach disease». Nucleic Acids Research 24 (7): 1220-4. PMC 145780. PMID 8614622. doi:10.1093/nar/24.7.1220.
- ↑ a b c Ceribelli, A; Cavazzana, I; Airò, P; Franceschini, F (2010). «Anti-RNA polymerase III antibodies as a risk marker for early gastric antral vascular ectasia (GAVE) in systemic sclerosis». The Journal of Rheumatology 37 (7): 1544. PMID 20595295. doi:10.3899/jrheum.100124.
- ↑ a b c d e f g Komiyama, Masae; Fu, K; Morimoto, T; Konuma, H; Yamagata, T; Izumi, Y; Miyazaki, A; Watanabe, S (2010). «A novel endoscopic ablation of gastric antral vascular ectasia». World Journal of Gastrointestinal Endoscopy 2 (8): 298-300. PMC 2999147. PMID 21160630. doi:10.4253/wjge.v2.i8.298.
- ↑ El-Gendy, Hala; Shohdy, Kyrillus S.; Maghraby, Gehad G.; Abadeer, Kerolos; Mahmoud, Moustafa (1 de febrero de 2017). «Gastric antral vascular ectasia in systemic sclerosis: Where do we stand?». International Journal of Rheumatic Diseases (en inglés) 20 (12): 2133-2139. ISSN 1756-185X. PMID 28217887. doi:10.1111/1756-185X.13047.
- ↑ a b c Spahr, L; Villeneuve, J-P; Dufresne, M-P; Tasse, D; Bui, B; Willems, B; Fenyves, D; Pomier-Layrargues, G (1999). «Gastric antral vascular ectasia in cirrhotic patients: absence of relation with portal hypertension». Gut 44 (5): 739-42. PMC 1727493. PMID 10205216. doi:10.1136/gut.44.5.739.
- ↑ a b Spahr, L; Villeneuve, JP; Dufresne, MP; Tassé, D; Bui, B; Willems, B; Fenyves, D; Pomier-Layrargues, G (1999). «Gastric antral vascular ectasia in cirrhotic patients: absence of relation with portal hypertension». Gut 44 (5): 739-42. PMC 1727493. PMID 10205216. doi:10.1136/gut.44.5.739.
- ↑ Krstić, M; Alempijević, T; Andrejević, S; Zlatanović, M; Damjanov, N; Ivanović, B; Jovanović, I; Tarabar, D et al. (2010). «Watermelon stomach in a patient with primary Sjögren's syndrome». Vojnosanitetski Pregled. Military-medical and Pharmaceutical Review 67 (3): 256-8. PMID 20361704. doi:10.2298/VSP1003256K.
- ↑ "Watermelon Stomach" Archivado el 1 de enero de 2012 en Wayback Machine.Genetic and Rare Diseases Information Center (GARD), National Institution of Health.
- ↑ "Watermelon Stomach and Radiiation Proctopathy CCS Publishing, August 1, 2011
- ↑ Gilliam, John H.; Geisinger, Kim R.; Wu, Wallace C.; Weidner, Noel; Richter, Joel E. (1989). «Endoscopic biopsy is diagnostic in gastric antral vascular ectasia». Digestive Diseases and Sciences 34 (6): 885-8. PMID 2721320. doi:10.1007/BF01540274.
- ↑ a b c Shibukawa, G; Irisawa, A; Sakamoto, N; Takagi, T; Wakatsuki, T; Imamura, H; Takahashi, Y; Sato, A et al. (2007). «Gastric antral vascular ectasia (GAVE) associated with systemic sclerosis: relapse after endoscopic treatment by argon plasma coagulation». Internal Medicine (Tokyo, Japan) 46 (6): 279-83. PMID 17379994. doi:10.2169/internalmedicine.46.6203.
- ↑ Khan S, Tudur Smith C, Williamson P, Sutton R (2006), «Portosystemic shunts versus endoscopic therapy for variceal rebleeding in patients with cirrhosis», The Cochrane Database of Systematic Reviews (4): CD000553, PMC 7045742, PMID 17054131, doi:10.1002/14651858.CD000553.pub2.
- ↑ Saab S, Nieto JM, Lewis SK, Runyon BA (2006), «TIPS versus paracentesis for cirrhotic patients with refractory ascites», The Cochrane Database of Systematic Reviews 2010 (4): CD004889, PMC 8855742, PMID 17054221, doi:10.1002/14651858.CD004889.pub2.
- ↑ Khan S, Tudur Smith C, Williamson P, Sutton R (2006), «Portosystemic shunts versus endoscopic therapy for variceal rebleeding in patients with cirrhosis», The Cochrane Database of Systematic Reviews (4): CD000553, PMC 7045742, PMID 17054131, doi:10.1002/14651858.CD000553.pub2.
- ↑ Saab S, Nieto JM, Lewis SK, Runyon BA (2006), «TIPS versus paracentesis for cirrhotic patients with refractory ascites», The Cochrane Database of Systematic Reviews 2010 (4): CD004889, PMC 8855742, PMID 17054221, doi:10.1002/14651858.CD004889.pub2.
- ↑ Sundaram V, Shaikh OS (July 2009). «Hepatic encephalopathy: pathophysiology and emerging therapies». Med. Clin. North Am. 93 (4): 819-36, vii. PMID 19577116. doi:10.1016/j.mcna.2009.03.009.
- ↑ «Portosystemic shunts versus endoscopic therapy for variceal rebleeding in patients with cirrhosis», The Cochrane Database of Systematic Reviews (4), 2006: CD000553, PMC 7045742, PMID 17054131, doi:10.1002/14651858.CD000553.pub2.
- ↑ a b «Hepatic encephalopathy: pathophysiology and emerging therapies». Med. Clin. North Am. 93 (4): 819-36, vii. July 2009. PMID 19577116. doi:10.1016/j.mcna.2009.03.009.
- ↑ paracentesis en el Diccionario Médico de Dorland
- ↑ «TIPS versus paracentesis for cirrhotic patients with refractory ascites», The Cochrane Database of Systematic Reviews 2010 (4), 2006: CD004889, PMC 8855742, PMID 17054221, doi:10.1002/14651858.CD004889.pub2.
- ↑ Tuveri, Massimiliano; Borsezio, Valentina; Gabbas, Antonio; Mura, Guendalina (2007). «Gastric antral vascular ectasia—an unusual cause of gastric outlet obstruction: report of a case». Surgery Today 37 (6): 503-5. PMID 17522771. S2CID 25727751. doi:10.1007/s00595-006-3430-3.
- ↑ Spahr, L; Villeneuve, JP; Dufresne, MP; Tassé, D; Bui, B; Willems, B; Fenyves, D; Pomier-Layrargues, G (1999). «Gastric antral vascular ectasia in cirrhotic patients: absence of relation with portal hypertension». Gut 44 (5): 739-42. PMC 1727493. PMID 10205216. doi:10.1136/gut.44.5.739.
- ↑ Surgery Encyclopedia website page on Antrectomy. Accessed September 29, 2010.
- ↑ Sherman, V; Klassen, DR; Feldman, LS; Jabbari, M; Marcus, V; Fried, GM (2003). «Laparoscopic antrectomy: a novel approach to treating watermelon stomach». Journal of the American College of Surgeons 197 (5): 864-7. PMID 14585429. doi:10.1016/S1072-7515(03)00600-8.
- ↑ Wells, C; Harrison, M; Gurudu, S; Crowell, M; Byrne, T; Depetris, G; Sharma, V (2008). «Treatment of gastric antral vascular ectasia (watermelon stomach) with endoscopic band ligation». Gastrointestinal Endoscopy 68 (2): 231-6. PMID 18533150. doi:10.1016/j.gie.2008.02.021.
Otras lecturas[editar]
- Thonhofer, R; Siegel, C; Trummer, M; Gugl, A (2010). «Clinical images: Gastric antral vascular ectasia in systemic sclerosis». Arthritis and Rheumatism 62 (1): 290. PMID 20039398. doi:10.1002/art.27185.
